基于近紅外光的腹部出血檢測系統的開發*
王紅珂,張言,錢誠,薛莉,劉玉冰,李韙韜
(南京航空航天大學自動化學院生物醫學工程系,南京211100)
1 引 言
腹部閉合性損傷以及由此導致的腹部出血是一種在平時和戰場環境下常見的急性疾病。患者死亡的主要原因是腹腔內部大量出血而造成的失血性休克[1]。腹部閉合性損傷及腹腔出血大多由于損傷部位隱蔽、發病急速、患者行動不便、診斷需要時間等原因,往往診斷困難、誤診率高。因此,臨床上急需一種簡單、方便并能準確、快速的診斷方法。其中腹腔診斷性穿刺術是臨床上一種常用的診斷方法,其簡單易行、準確率高。但腹腔穿刺術并不適合所有患者,有一定的適應證和禁忌證[2]。B超對實質性臟器損傷的診斷具有明顯的優勢并能夠對損傷部位、程度、范圍進行判斷,具有方便、快速、無創的特點,但對胰腺損傷的檢測靈敏度較低[3]。CT對閉合性損傷的定性和診斷的準確性可達90%以上,其準確性優于超聲檢查[4]。但是,在CT診斷的過程中容易產生呼吸偽影,且在費用上要比其它檢測手段昂貴許多[5]。腹腔鏡探查術具有創傷小、安全、準確的優點,還可以避免不必要的開腹手術,但對腹腔內有較大出血和腸道脹氣嚴重的患者并不適用[6]。目前,腹部閉合性損傷的臨床診斷主要以 CT和超聲聯合檢查為主[7]。但是,上述診斷方法都無法實現在野戰和災難環境下實時、快速、準確、無創地檢測腹部創傷。
現代近紅外光譜技術(near infrared spectroscopy,NIRS)是一項新的無損檢測技術,它可以對物體進行快速、準確、無創地檢測。近紅外光對物體的穿透力強,可以對生物體進行無損非侵入檢測,已成為近年來臨床醫學診斷和生物組織研究的熱點之一[8-9]。由于生物組織的不同成分對近紅外光具有不同的吸收和散射特性,因此,近紅外光譜可以區分不同組織成分和其相關變化[10]。臨床上,NIRS在腹部的無創檢測及相關實驗研究還處于探索或評估階段。但是隨著計算機技術、光學技術、光譜技術和電子技術的不斷發展,NIRS技術將更加完善,其在無損監測人體組織和血液代謝中將具有更加廣闊的前景。NIRS技術作為一種檢測方法,可以對物體內部的信息進行實時、無創的檢測,并可以通過分析獲得的復雜光譜就能得到被測物體內部的相關信息。
本研究采用近紅外光作為檢測手段,設計并開發出了一套針對腹部出血的無創檢測系統。通過建立的腹部出血實驗模型,對紅光和近紅外光在腹部組織的傳輸規律進行了研究。研究結果為腹部損傷及出血的無創檢測找到了一種新的方法。
2 近紅外光檢測系統
2.1 檢測原理
光子與生物組織的相互作用主要包括生物組織對光子的吸收和散射作用。在近紅外波長范圍內,其相互作用主要表現為散射作用,因為生物組織中水的成分占有很大比例。水的吸收譜主要在300 nm以下和1 000 nm以上的波長范圍內,而血紅蛋白和黑色素僅對400~650 nm的可見光有強烈的吸收[11-13]。由于生物組織對近紅外光具有低吸收、高散射的特性,因此,近紅外光譜區的光對生物組織有較好的穿透能力,其穿透深度可達數個厘米。通過測量生物組織的光學特性參數,便可得到生物組織深層的生理信息[14]。
通常,將波長范圍在700~900 nm稱為“光學窗口”。此波長范圍內,隨著波長的逐漸增加,氧合血紅蛋白、還原血紅蛋白對光的吸收逐漸減弱,而當波長大于900 nm時水的吸收大大增加。因此,可以選擇波長在“光學窗口”范圍內的近紅外光作為檢測光源。利用血液中的血紅蛋白和體液(主要成分是水)對光子的不同吸收,便可檢測損傷腹部的出血情況。另一方面,近紅外光譜技術還具有安全可靠、連續實時及無損的特點,可以應用于對腹部的檢測。
2.2 檢測系統設計方案
檢測系統主要由探頭、檢測裝置、數據采集卡和計算機等組成,見圖1。系統工作時,檢測裝置控制光源的時序和發光頻率,光源發出的光子照射在待測樣品上,經過組織對光子的吸收和散射等作用,一部分光子被探測器檢測并傳輸到檢測裝置的輸入通道。然后,信號經過放大、濾波等處理后送至數據采集卡,經過數據采集卡的A/D轉換后送至計算機。上位機采用Labview進行編程,編寫了數據采集與控制的用戶界面和程序,主要實現了采集數據的波形顯示、保存和實時分析。
檢測裝置是整個系統的重要組成部分,主要包括:輸入通道、輸出通道、光源驅動模塊、鎖相放大模塊、MCU(microprocessor control unit,MCU)控制模塊和信號處理模塊等。其中輸入和輸出通道主要用于完成采集信號的傳輸;光源驅動模塊實現光源的驅動;MCU是整個檢測裝置的核心;信號處理模塊主要實現信號的放大和去噪聲。
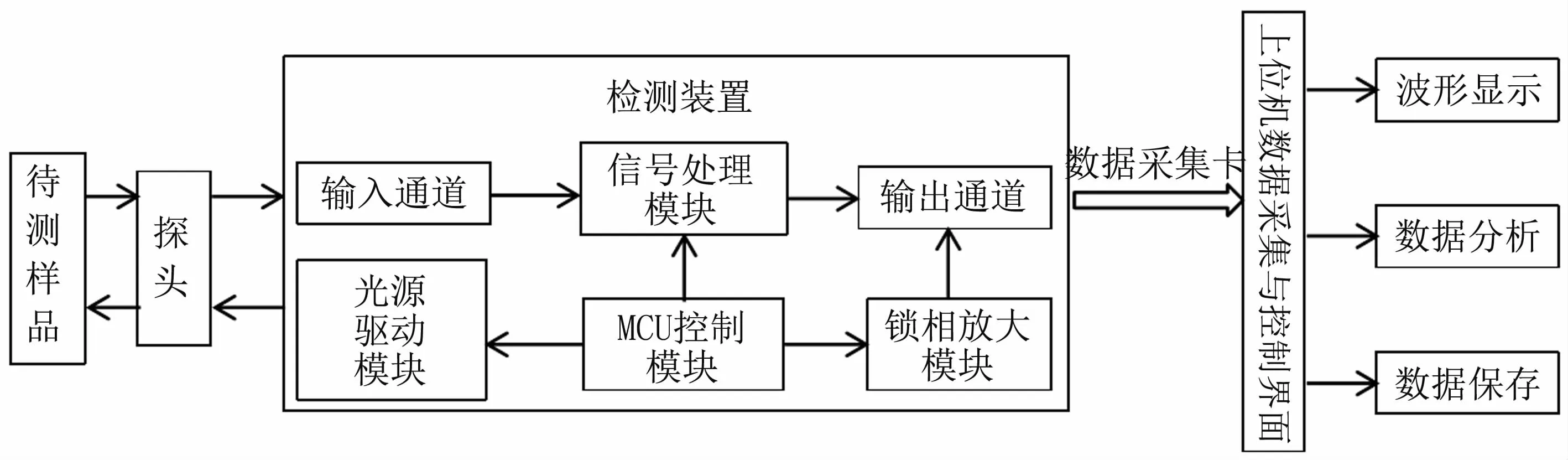
圖1 檢測系統結構示意圖Fig 1 Schematic of the detection system
2.3 探頭
探頭主要包括1個光源和兩個探測器,見圖2。光源采用日本epitex公司生產的型號為L760/850-04A的雙波長發光二極管,其發光波長分別為760 nm和850 nm,工作電流為80 mA。探測器采用美國B-B公司生產的OPT101型光電探測器。光源和兩個探測器的中心間距分別為2.1 cm和3.1 cm。同時,為了減少外界背景光對探測器的影響,整個探頭用一個黑色的柔性橡膠作為基底,并在上面嵌入1個雙波長發光二極管和2個光電探測器。
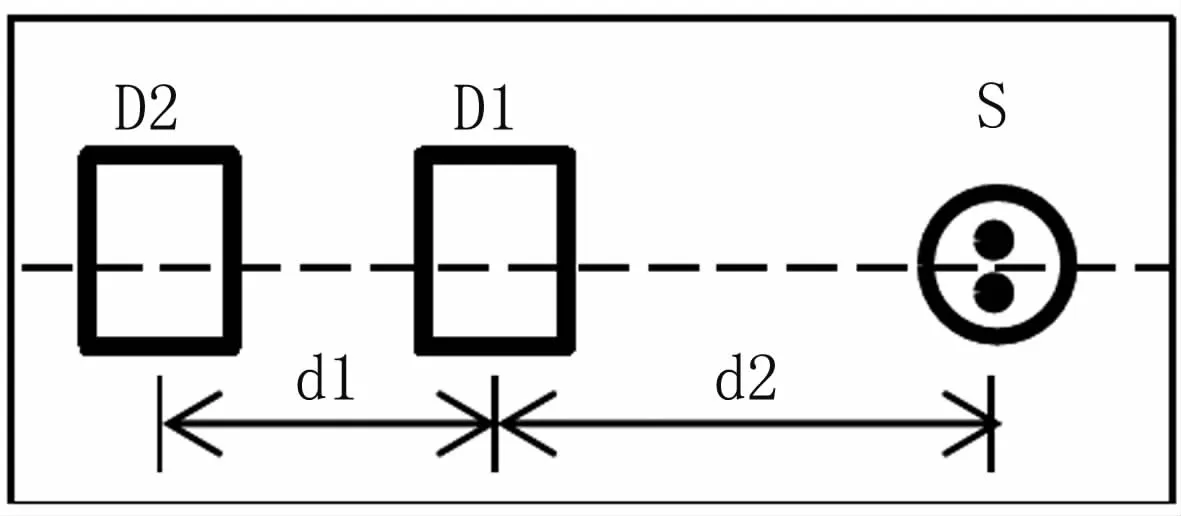
圖2 探頭結構示意圖Fig 2 Diagram of the detector structure
2.4 光源驅動模塊
為保證從腹部組織漫反射出來的光強信號的穩定性,系統采用恒流源驅動方式來驅動激勵光源。該恒流源驅動電路主要由電源基準芯片MAX6126、電子模擬開關芯片MAX4066,采樣電阻和其它元器件構成。光源驅動時,電壓基準芯片實時采集采樣電阻兩端的電壓,同時將采集電壓信號反饋到電壓基準芯片內部,然后根據采樣電壓值調節輸出電壓。采樣電阻的阻值由所需要的驅動電流的大小和電壓基準芯片的輸出電壓來確定。光源的驅動電流可以通過采樣電阻值來改變。
2.5 鎖相放大模塊
由于所要檢測的是微弱光強信號且信號中常常混有噪聲,因此,系統采用鎖相放大電路來去除噪聲。鎖相放大電路不僅具有很高的檢測靈敏度而且信號處理比較簡單,常用來檢測微弱信號。如圖3所示,鎖相放大模塊主要包括帶通濾波器、鎖相放大器和低通濾波器三個部分。在本檢測系統中,調制輸入信號的頻率為20 Hz,并在鎖相放大器前加入帶通濾波器從而實現對輸入信號的濾波,參考信號由微控制器提供。信號經鎖相放大后通過一個低通濾波器來實現信號的整流與濾波。
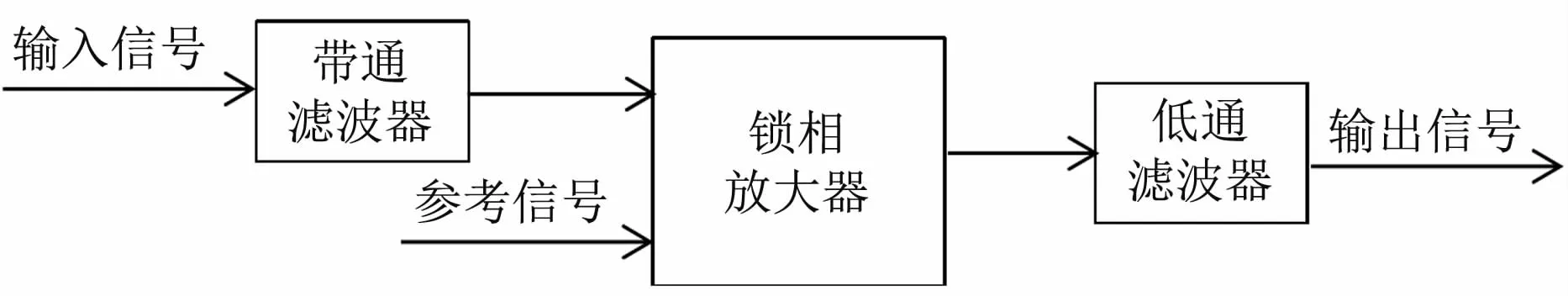
圖3 鎖相放大模塊結構圖Fig 3 Diagram of the lock-in am p lifier modules
2.6 數據采集卡與軟件設計
數據采集卡采用美國NI公司生產的型號為PCI6221板卡。該采集卡分辨率為16位,最高采集速度為250 k/s,具有16路輸入通道,可以滿足系統的采集需求。檢測系統的控制和信號采集程序采用Labview編程。數據采集卡將采集到的信號經過A/D轉換后送至上位機進行保存和顯示。信號采集系統的控制面板(見圖4)主要包括采樣頻率、采樣數、采集通道的設置,波形顯示和數據存儲路徑選擇。在實時信號采集時,首先需要設置數據采集卡的相關參數,然后進行實時采集和波形顯示。圖5為采集系統的程序框圖,可以通過數據采集卡自帶的軟件包,也可以通過采集面板來觀察采集信號的波形。
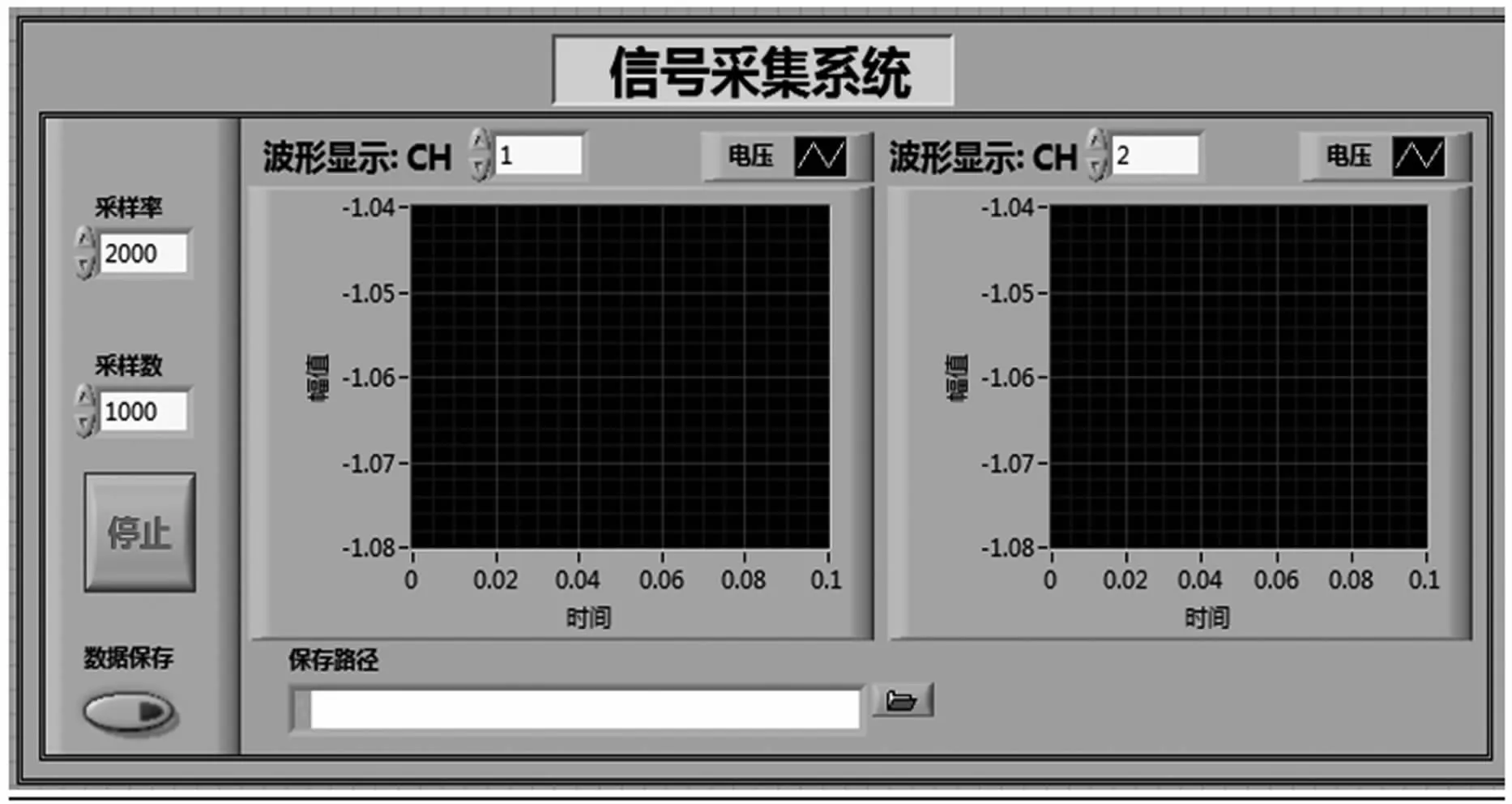
圖4 信號采集系統控制面板Fig 4 Signal acquisition system control panel
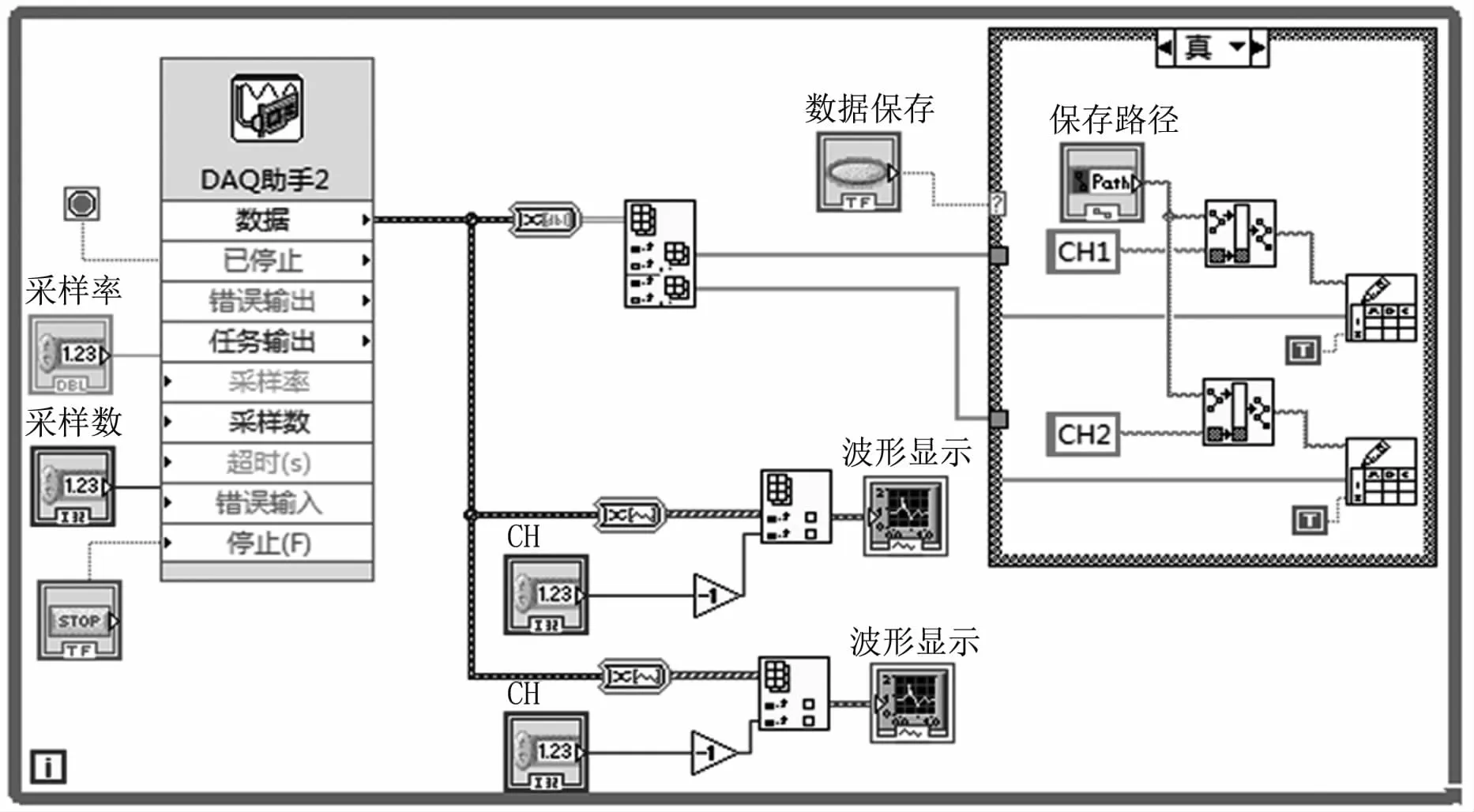
圖5 采集系統程序框圖Fig 5 Program chart of the signal acquisition system
3 實驗及結果分析
3.1 腹部出血模型構建
人體的腹部結構主要由皮膚、皮下組織、腹肌、腹膜外脂肪和腹膜等組成。由于人體腹部結構比較復雜,所以在實驗時需要建立適當的組織模型。在本實驗中,腹部組織用新鮮的雞脯肉來模擬,用Phantom模型來模擬正常腹部和腹部出血時的兩種不同情況,通過改變雞肉的厚度來探究光子在腹部組織中的檢測深度和傳播規律。圖6為模型實驗裝置的示意圖。
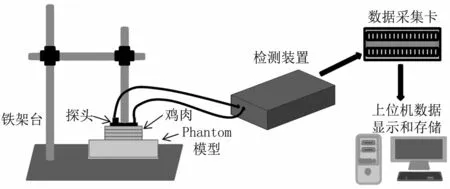
圖6 模型實驗裝置示意圖Fig 6 The schematic of the experiment device
實驗Phantom模型配置步驟如下:(1)分別量取100 ml和150 ml水倒入燒杯中并將其編號為a和b;(2)將水加熱至沸騰后向沸水中加入15 g凝膠并充分攪拌均勻;(3)溶液溫度降至50℃后,向編號為a和b的燒杯中分別加入50 m l牛奶和0.1 m l墨汁并再次充分攪拌均勻;(4)將冷卻后的混合物放入冰箱中,待液體凝固則模型配置完成。兩個模型的整體厚度均為3cm,編號為a和b的模型分別作為實驗模型1和實驗模型2。
模型配好后,利用一臺雙光源、雙檢測通道的檢測生物組織光學特性的ISSOXImeter系統測得模型1的光學參數為:μa=0.0359,μs=14.4648;模型2的光學參數為:μa=0.2079,μs=-20.2259,其中μa和μs分別為組織的吸收系數和散射系數,單位為1/cm。模型2的散射系數小于零,可以認為它是一個吸收體。
3.2 實驗方法和步驟
用新鮮的雞脯肉模擬腹部組織,配置的Phantom模型1和模型2分別模擬正常腹部和有出血的損傷腹部。當光照射到腹部組織時,光子經過腹部組織的吸收和散射作用,一部分光子被探頭檢測到。通過分析這些攜帶腹部組織信息的光強信號便可初步判斷腹部的出血情況。
實驗時,首先按照要求連接好檢測系統,并進行調試;調試完成后將新鮮的雞脯肉切成半徑為4 cm,厚度依次為 0.5、1、1.5、2、2.5、3、3.5 cm的圓片;將Phantom模型放在實驗臺上并在模型上面放置雞脯肉;將探頭用鐵架臺固定,調整高度使其緊貼在雞肉表面;觀察輸出信號波形并保存。將探頭放置在雞脯肉表面的不同位置,重復上述步驟三次。
3.3 實驗結果及分析
當用850 nm的光作為激勵源,雞肉厚度依次從0.5 cm到3.5 cm變化時,探測器D1所檢測到的光強曲線見圖7(a)。Phantom 1和Phantom 2分別表示正常腹部和損傷有積血的腹部所檢測到的光強曲線。圖7(b)表示二者的差值曲線。從圖中可以看出:隨著雞肉厚度的增加,正常腹部的光強信號呈現出一條不規則的曲線,并在一定的幅值范圍內波動;損傷腹部的檢測光強信號隨著雞肉厚度的增加,信號值逐漸增加,且當雞肉厚度大于2.5 cm后,光強幅值則幾乎不隨厚度的變化而變化。因此,正常腹部檢測到的光強信號是一條幅值波動的但均值一定的曲線;損傷有出血的腹部,由于血液對光子的吸收,其檢測到的光強信號隨腹部組織厚度的增加而增大。當雞肉厚度大于2.5 cm時,檢測光強將不再隨厚度的變化而變化。可以說明,此檢測裝置在850 nm光的腹部檢測中,其最大檢測深度為2.5 cm。當厚度大于2.5 cm時,腹腔內部的積血不再對入射光子有明顯的吸收作用。
圖8(a)表示用760 nm的光作為激勵源,雞肉厚度依次從0.5 cm到3.5 cm變化時,探測器D1所檢測到的光強曲線。圖8(b)表示二者差值的變化曲線。從圖7(b)和圖8(b)可以看出:在此檢測裝置中,波長為760 nm和850 nm的光在腹部的最大檢測深度均為2.5 cm,760 nm光的檢測線性度明顯好于850 nm。
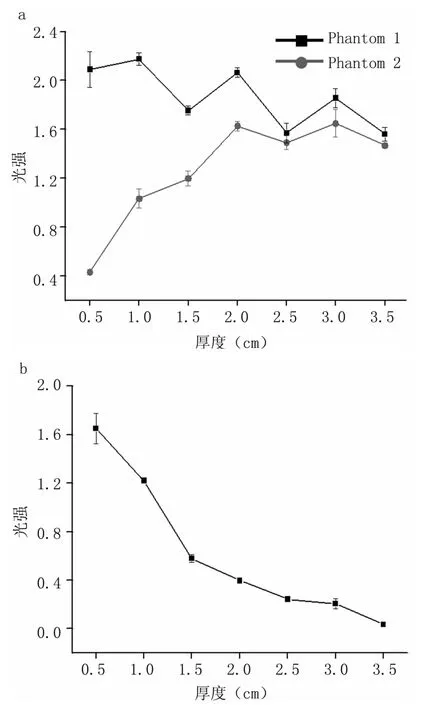
圖7 波長為850 nm光的檢測光強曲線Fig 7 The detected light intensity curve of the light with a wavelength of 850 nm
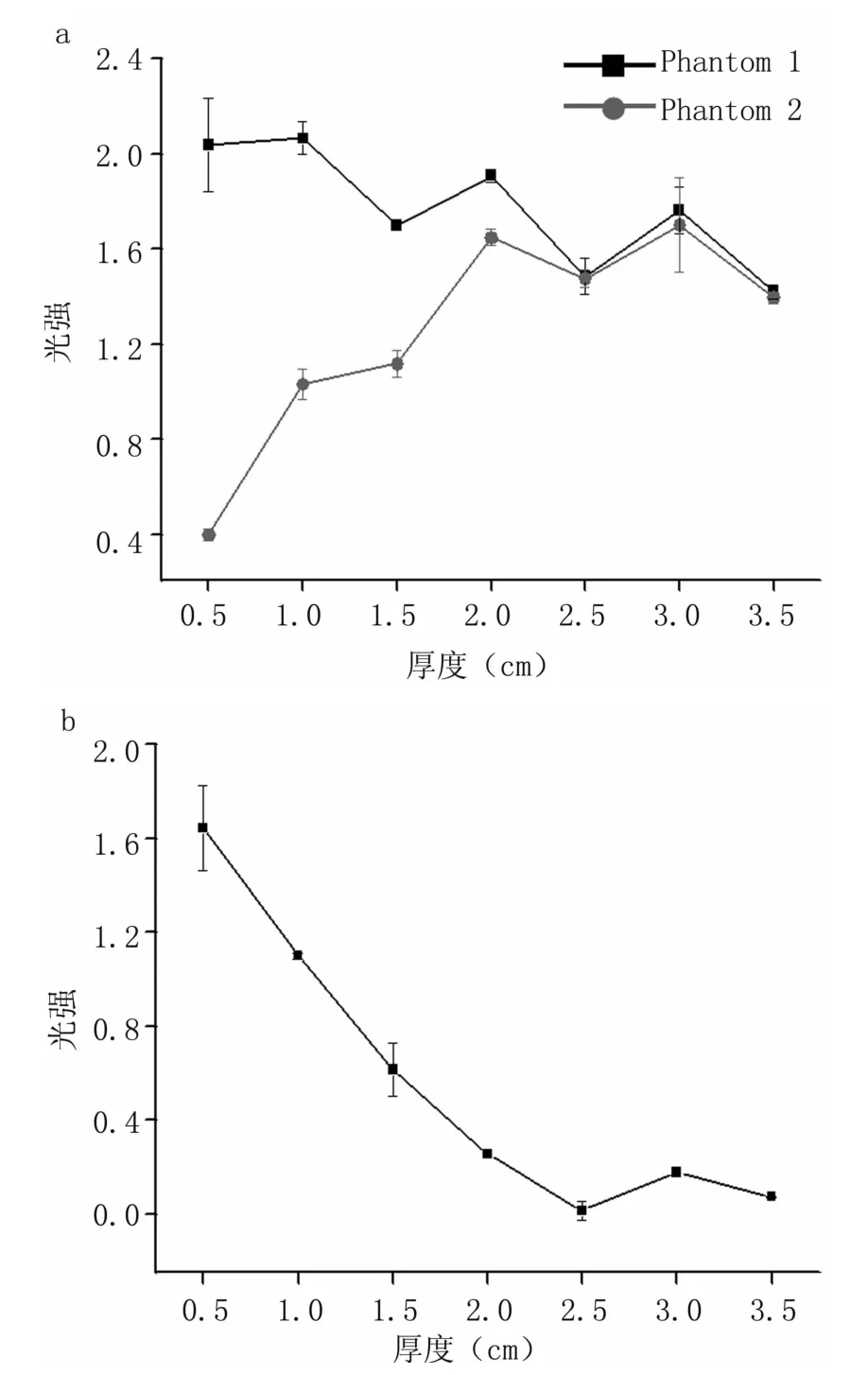
圖8 波長為760 nm光的檢測光強曲線Fig 8 The detected light intensity curve of the light with a wavelength of 760 nm
4 結論與討論
腹部出血模型實驗結果表明:此基于近紅外光技術的檢測系統可以明顯區分出正常腹部和損傷有出血的腹部;用760 nm和850 nm波長的光作為激勵光源時,其檢測的最大深度均為2.5 cm,760 nm光的檢測線性度要好于850 nm。
但是人體的腹部組織比較復雜,出血部位通常比較隱蔽。因此,在腹部損傷及出血檢測時,還需要做進一步的改進和優化。一方面,通過改進探頭來提高檢測靈敏度和分辨率。可以:(1)適當范圍內,采用大功率的激光二極管作為檢測光源;(2)采用更為靈敏的雪崩二極管作為探測器;(3)采用多光源、多檢測器的檢測方案;另一方面,采用其他檢測手段輔助檢測。首先,采用B超初步判定出血的大致位置,然后利用近紅外光技術進行精確定位,并確定出血位置、程度和出血范圍。

