磷酸三丁酯和磷酸二丁酯與Pu(Ⅳ)配合物的密度泛函研究
呂洪彬,左 臣,晏太紅
中國原子能科學研究院 放射化學研究所,北京 102413
?
磷酸三丁酯和磷酸二丁酯與Pu(Ⅳ)配合物的密度泛函研究
呂洪彬,左臣,晏太紅
中國原子能科學研究院 放射化學研究所,北京102413
采用B3LYP密度泛函方法,Pu(Ⅳ)和其他原子分別采用相對論有效原子實勢(RECP)和6-311 g(d,p)全電子基組,研究了Pu(NO3)4TBP2和Pu(NO3)2DBP2的幾何結構、熱力學參數(shù)及紫外可見光譜。幾何結構計算結果表明,由于配體空間位阻的影響,Pu與DBP的鍵長更短,自然布居分析(NPA)結果也表明,Pu與DBP之間的電荷轉移更多,因此二者之間相互作用更強。熱力學分析顯示,Pu(NO3)4TBP2與HDBP發(fā)生配體交換的反應自由能為-178.9 kJ/mol,說明DBP與Pu之間的相互作用更強。Pu(NO3)4TBP2的紫外吸收光譜主要來源于硝酸根到Pu的f軌道的躍遷,TBP貢獻不大;而Pu(NO3)2DBP2的躍遷同時來源于硝酸根和DBP到Pu的f軌道的配體-金屬電荷轉移躍遷(LMCT)。
钚;磷酸三丁酯(TBP);磷酸二丁酯(HDBP);密度泛函理論
利用磷酸三丁酯(TBP)作為萃取劑的普雷克斯(PUREX)流程是核燃料后處理中最為成熟的技術。在萃取過程中TBP和稀釋劑都會在輻射條件下發(fā)生輻解,產(chǎn)生包括磷酸二丁酯(HDBP)在內(nèi)的輻解產(chǎn)物[1-2]。在實驗和工廠運行中存在Pu(Ⅳ)不能被充分反萃的現(xiàn)象,而有機相中TBP的輻解產(chǎn)物(HDBP)與Pu(Ⅳ)的結合被認為是使其無法被充分反萃的重要因素之一[3]。對TBP和HDBP與Pu(Ⅳ)的配合物結構和性質(zhì)的研究將會有助于萃取過程的機理研究和Pu(Ⅳ)回收率的提高。已有文獻[4-6]在實驗上對Pu(Ⅳ)和TBP、HDBP形成的配合物組成、平衡常數(shù)等性質(zhì)進行了研究,但由于Pu的毒性與放射性,對其結構的研究比較少。對钚配合物的理論研究既是相對匱乏的實驗數(shù)據(jù)的補充,還能夠加深對钚配合物的認識。近年來,采用B3LYP、PBE0等泛函的密度泛函理論(DFT)方法被應用于錒系元素配合物的結構、性質(zhì)研究及核燃料后處理流程相關的研究中[7-10]。相對論效應、溶劑效應等因素的引入使得理論計算的結果精確度明顯提高。本工作擬在已有實驗基礎上,采取DFT方法對Pu(Ⅳ)和TBP、HDBP形成的配合物結構進行研究,并對其熱力學參數(shù)進行計算,同時對其紫外光譜進行考察和分析,這些結果將有助于對有機相中TBP和HDBP的Pu(Ⅳ)配位性質(zhì)的理解,同時為工藝改進提供理論基礎。
1 方法和基組
所有的計算均采用密度泛函理論,利用Gaussian 09軟件包[11],選取B3LYP雜化泛函進行不考慮自旋-軌道耦合的標量相對論計算。對钚原子的計算考慮相對論效應,對內(nèi)層電子采用相對論有效原子實勢(RECP),對Pu(Ⅳ)配合物采用五重態(tài)自旋態(tài),對U(Ⅳ)配合物采取單重態(tài)自旋態(tài)。對钚原子采用相對論有效原子實勢基組,在進行結構計算時,對钚原子選取德國斯圖加特大學ECP78MWB_SEG 基組進行計算[12],這個基組包含78個中心電子和16個價電子,在進行自由能及紫外光譜計算時,采取德國斯圖加特大學ECP60MWB_SEG 基組,這個基組包含60個中心電子和34個價電子。本次計算中沒有考慮自旋-軌道耦合效應。對其他原子采取6-311g(d,p)全電子基組[13],有研究結果表明,采用B3LYP/RECP/6-311g(d,p)的理論計算方法對錒系元素及其與有機配體形成的配合物進行計算得到的結果是可靠的[9]。所有的結構優(yōu)化都是在氣相環(huán)境中,采用B3LYP/RECP/6-311g(d,p)的理論計算方法進行的。在優(yōu)化結構的基礎上,采用相同的方法對振動頻率進行計算,在氣象環(huán)境中得到配合物的自由能以及零點能。采用Multiwfn程序對自然原子電荷和Mayer軌道鍵級進行分析。在氣相環(huán)境優(yōu)化結構的基礎上,利用似導體屏蔽模型得到有機溶劑環(huán)境下的自由能以及零點能。利用含時-密度泛函方法(TD-DFT)對其紫外光譜進行模擬同時對紫外峰對應的躍遷進行了分析。為節(jié)省計算量,將TBP及HDBP中的丁基替換為甲基。去質(zhì)子化的HDBP用DBP表示。
2 計算結果
2.1Pu(NO3)4TBP2和Pu(NO3)2DBP2的幾何構型
依據(jù)文獻[4]中钚的TBP和DBP配合物組成,優(yōu)化得到了氣相環(huán)境中Pu(NO3)4TBP2和Pu(NO3)2DBP2兩種化合物的結構,示于圖1。

Pu(NO3)4TBP2和Pu(NO3)2DBP2的結構參數(shù)與自然布居分析(NPA)結果列入表1。NPA分析顯示,Pu(NO3)4TBP2中Pu電荷為1.863,Pu(NO3)2DBP2中Pu電荷為1.601,說明DBP與Pu原子之間電荷轉移更多,這導致了DBP與Pu的結合能比TBP與Pu的結合能更大。計算表明,去離子化的HDBP中的配位氧原子電荷(-1.116)比TBP中的配位氧原子電荷(-1.074)更多,說明DBP中氧原子的配位能力比TBP中氧原子的配位能力更強。
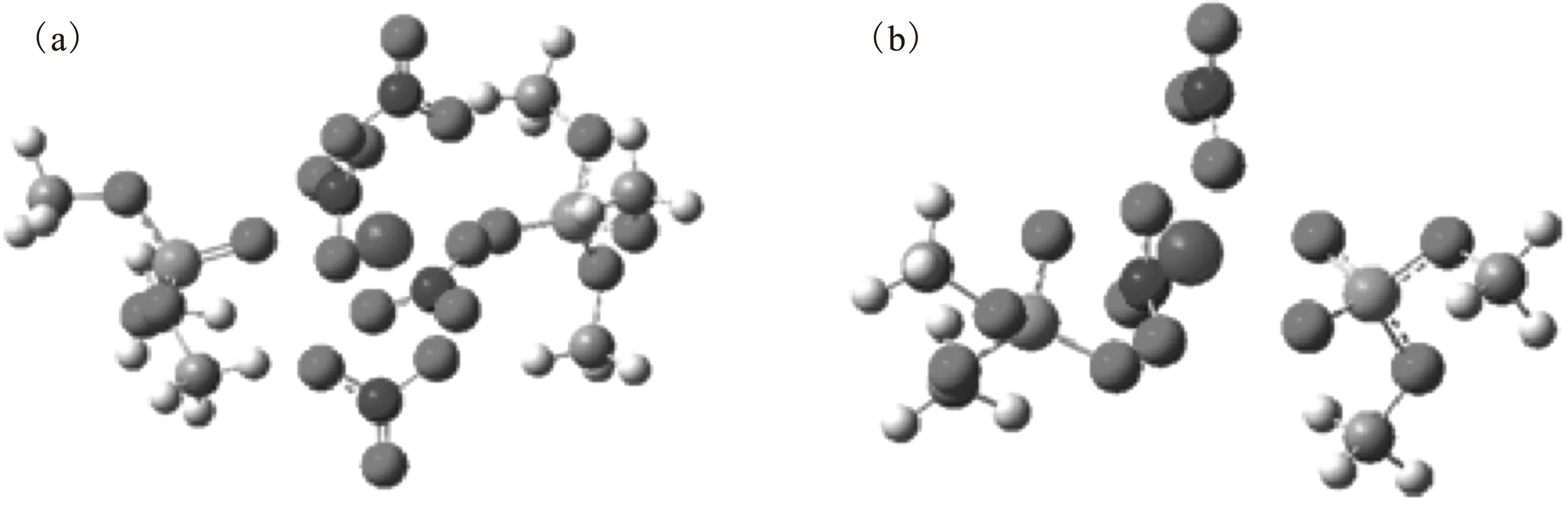
淺藍色代表Pu,紅色代表O,藍色代表N,橙色代表P,灰色代表C,白色代表H圖1 Pu(NO3)4TBP2(a)和Pu(NO3)2DBP2(b)的結構Fig.1 Optimized structure of Pu(NO3)4TBP2(a) and Pu(NO3)2DBP2(b)
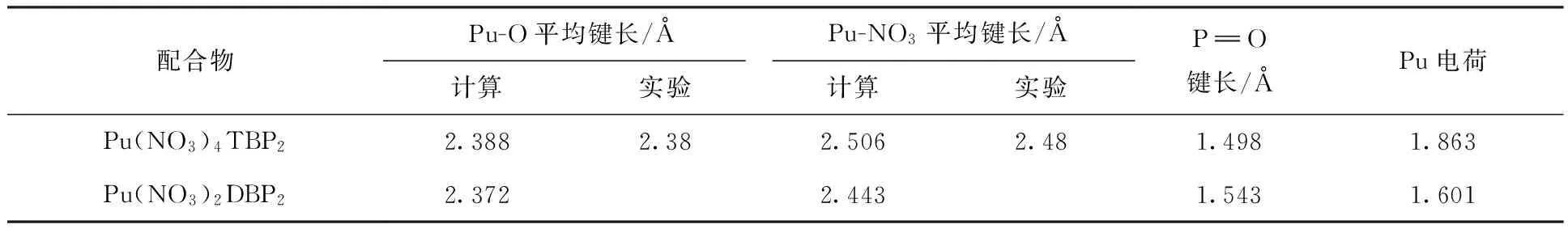
表1 Pu(NO3)4TBP2和Pu(NO3)2DBP2的結構參數(shù)與NPA分析結果Table 1 Structure parameters and NPA analyze results of Pu(NO3)4TBP2 and Pu(NO3)2DBP2
對配合物中Pu-O的Mayer鍵級進行了分析[15],Mayer鍵級越高,化學鍵的共價成分就越多。在Pu(NO3)4TBP2中Pu-OTBP的Mayer鍵級為0.28左右,Pu-ONO3的鍵級為0.27~0.43,在Pu(NO3)2DBP2中Pu-ODBP的Mayer鍵級為0.52~0.55,Pu-ONO3的鍵級為0.40~0.51,這些結果說明Pu與O之間有一定的共價成分。Pu-OTBP的Mayer鍵級比Pu-OTBP的鍵級高,說明二者之間的共價成分更多,因此,Pu與DBP的相互作用更強。Pu(NO3)2DBP2中Pu-ONO3的鍵級比Pu(NO3)4TBP2中Pu-ONO3的鍵級更高,說明Pu(NO3)2DBP2中Pu-ONO3的作用更強,這主要是由于空阻原因導致Pu(NO3)2DBP2中Pu-ONO3的距離更短,使得二者相互作用更強。與自由Pu(NO3)4中Pu-ONO3的鍵級(0.49~0.54)相比,TBP和DBP與Pu配位后,Pu-ONO3的鍵級都有減少,Pu(NO3)4TBP2中減少的更加明顯。
2.2Pu(NO3)4TBP2和Pu(NO3)2DBP2的熱力學性質(zhì)研究
實驗結果表明,在有機相環(huán)境中,DBP與Pu(Ⅳ)配合物的穩(wěn)定常數(shù)比TBP與Pu(Ⅳ)的穩(wěn)定常數(shù)大,說明DBP與Pu(Ⅳ)的相互作用更強。為了研究TBP和DBP對Pu(Ⅳ)的熱力學選擇性,首先在氣相條件下對反應(1)的熱力學參數(shù)進行了計算,結果列入表2。由表2可知:ΔH=20.36 kJ/mol;ΔS=44.40 J/K,說明該反應是熵驅動的反應。配體交換過程是配體解離,新配體再重新配位的過程。配體解離導致熵增,配體配位導致熵減,反應過程中伴隨著TBP和DBP交換的過程有兩個硝酸根從配合物中解離下來,因此導致整個反應的熵增加。雖然反應熵值為正值,但是由于焓變的正值較大,所以計算得到的反應自由能ΔG=7.13 kJ/mol,因此在這種條件下,配位反應難以發(fā)生。
Pu(NO3)2DBP2+2TBPHNO3
(1)
ΔG=ΔG(Pu (NO3)2DBP2)+
2ΔG(TBPHNO3)-ΔG(Pu(NO3)4TBP2)-
2ΔG(HDBP)
(2)
雖然氣相計算結果表明,TBP與Pu(Ⅳ)的結合能力更強,為使計算結果與實際狀態(tài)更加接近,因此在考慮溶劑情況下進行了計算。因為Pu萃取實驗的有機相通常為煤油或正十二烷,因此采用正己烷作為模擬溶劑模型,計算結果列入表2。由表2可知:與在氣相條件中計算結果不同,在溶劑條件下計算得到反應(1)的ΔH=-154.97kJ/mol,在溶劑條件下反應焓變轉為負;ΔS=80.27J/K,在溶劑條件下熵變增大,更有利于反應的進行,由此計算得到的反應自由能ΔG=-178.89kJ/mol,在液相中反應轉變?yōu)闊崃W有利的反應。熱力學計算結果說明,DBP能夠和Pu(NO3)4TBP2配位,說明與TBP相比,DBP與Pu(Ⅳ)的配位能力更強。
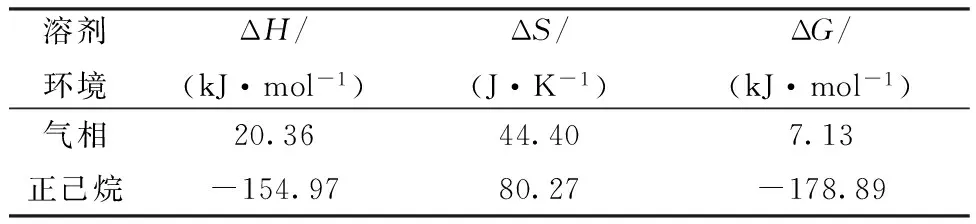
表2 利用B3LYP/6-311G(d,p) 計算得到的反應(1)的熱力學參數(shù)Table 2 Calculated thermodynamic parameters of reaction (1) by B3LYP/6-311G(d,p) methods
2.3Pu(NO3)4TBP2和Pu(NO3)2DBP2吸收光譜的理論研究
利用TD-DFT方法對氣相中Pu(NO3)4TBP2和Pu(NO3)2DBP2的紫外光譜進行了模擬,分子軌道示于圖2、3。Pu(NO3)4TBP2的吸收峰主要為377、407、581、607 nm,分別對應HOMO-2到LUMO+2、HOMO-3到LUMO、HOMO-2到LUMO和HOMO-1到LUMO的躍遷。由圖2可知,Pu(NO3)4TBP2的HOMO-3、HOMO-2、HOMO-1和HOMO軌道其主要由硝酸根中的N、O原子的p軌道構成,LUMO軌道主要由Pu原子f軌道組成,因此其紫外光譜主要對應于硝酸根中的N、O原子的p軌道到Pu原子f軌道的配體-金屬電荷轉移躍遷(LMCT),TBP分子的軌道對紫外光譜躍遷貢獻不大。

圖2 氣相中Pu(NO3)4TBP2的分子軌道Fig.2 Molecular orbitals of Pu(NO3)4TBP2 in gas phase
Pu(NO3)2DBP2的吸收峰主要在405、420、432、487、513、612、630 nm,分別對應于HOMO-4到LUMO+2、HOMO-2/HOMO-1到LUMO+2、HOMO-6到LUMO/HOMO-3到LUMO+1、HOMO-2/HOMO-4到LUMO+1、HOMO到LUMO+1、HOMO到LUMO的躍遷。由圖3可知,HOMO-6、HOMO-4、HOMO-3、HOMO-1主要由DBP中原子軌道組成,HOMO-2和HOMO主要由硝酸根中原子軌道組成,LUMO、LUMO+1和LUMO+2主要由Pu的f軌道組成,因此405、420、32 nm處吸收峰主要對應于DBP到Pu的配體-金屬電荷轉移躍遷(LMCT),487 nm吸收峰由DBP到Pu的LMCT和硝酸根到钚的LMCT混合而成,513、612、630 nm則主要是硝酸根到钚的LMCT。

圖3 氣相中Pu(NO3)2DBP2的分子軌道Fig.3 Molecular orbitals of Pu(NO3)2DBP2 in gas phase
3 結 論
利用B3LYP密度泛函理論方法,采用Gaussian 09程序和相對論贗勢基組,對Pu(NO3)4TBP2和Pu(NO3)2DBP2兩種化合物進行了結構優(yōu)化。結果表明:Pu(NO3)4TBP2的優(yōu)化結構與實驗結果相吻合,Pu(NO3)2DBP2的優(yōu)化結構中,Pu與DBP和硝酸根的鍵長都比Pu(NO3)4TBP2中Pu與TBP和硝酸根的鍵長要短,相互作用更強。在優(yōu)化結構基礎上進行NPA分析,發(fā)現(xiàn)在Pu(NO3)2DBP2中,DBP到Pu的電荷轉移比Pu(NO3)4TBP2中TBP與Pu的電荷轉移更多,且DBP與Pu之間的Mayer鍵級比TBP與Pu的鍵級更大。利用TD-DFT方法對紫外可見光譜進行了模擬并對吸收峰所對應的軌道躍遷進行了分析。對紫外光譜的比較可以發(fā)現(xiàn),Pu(NO3)2DBP2在400~430 nm處的紫外吸收峰更強,這一部分主要對應于DBP到Pu的LMCT躍遷,而在Pu(NO3)4TBP2中,TBP分子則對紫外吸收貢獻較少。
[1]Mincher B J, Elias G, Martin L R, et al. Radiation chemistry and the nuclear fuel cycle[J]. J Radioanal Nucl Chem, 2009, 282(2): 645-649.
[2]Bellido A V, Rubenich M N. Influence of the diluents on the radiolytic degradation of TBP in TBP, 30% (V/V)-diluent-HNO3systems[J]. Radiochim Acta, 1984, 36: 61-64.
[3]Mincher B J, Mezyk S P. Radiation chemical effects on radiochemistry: a review of examples important to nuclear power[J]. Radiochim Acta, 2009, 97(9): 519-534.
[4]May I, Taylor R J, Wallwork A L, et al. The influence of dibutylphosphate on actinide extraction by 30% tributylphosphate[J]. Radiochim Acta, 2000, 88(5/2000): 283-290.
[5]Sokhina L P, Solovkin A S, Teterin E G, et al. Dibutylphosphates of tetravalent plutonium, zirconium and thorium, formed in solutions of tri-n-butyl phosphate (TBP)[J]. Radiokhimiva, 1978, 20(1): 28-31.
[6]Sulka M, Cantrel L, Vallet V. Theoretical study of plutonium(Ⅳ) complexes formed within the PUREX process: a proposal of a plutonium surrogate in fire conditions[J]. J Phys Chem A, 2014, 118(43): 10073-10080.
[7]王東琪,van Gunsteren W F.錒系計算化學進展[J].化學進展,2011,23(7):1566-1581.
[8]Steele H, Taylor R J. A theoretical study of the inner-sphere disproportionation reaction mechanism of the pentavalent actinyl ions[J]. Inorg Chem, 2007, 46(16): 6311-6318.
[9]Xiao C L, Wu Q Y, Wang C Z, et al. Quantum chemistry study of uranium(Ⅵ), neptunium(Ⅴ), and plutonium(Ⅳ,Ⅵ) complexes with preorganized tetradentate phenanthrolineamide ligands[J]. Inorg Chem, 2014, 53(20): 10846-10853.
[11]Frisch M J,Trucks G W,Schlegel H B,et al. Gaussian 09, Revision A.1[R]. U S A: Gaussian, Inc. Wallingford, CT, 2009.
[12]Kuchile W, Dolg M, Stoll H, et al. Energy-adjusted pseudopotentials for the actinides. parameter sets and test calculations for thorium and thorium molecules[J]. J Chem Phys, 1994, 100: 7535-7542.
[13]Dithchfield R, Hehre W J, Pople J A. Self-consistent molecular orbital methods extended gaussian-type basis for molecular-orbital studies of organic molecules[J]. J Chem Phys, 1971, 54: 724-728.
[14]Den Auwer C, Revel R, Charbonnel M C, et al. Actinide coordination sphere in various U, Np and Pu nitrato coordination complexes[J]. J Synchrotron Radiat, 1999, 6: 101-104.
[15]Lu T, Chen F W. Multiwfn: a multifunctional wavefunction analyzer[J]. J Comput Chem, 2012, 33(5): 580-592.
Density Functional Theoretical Analysis of Complexes of Tributylphosphate and Dibutylphosphate of Pu(Ⅳ)
LU Hong-bin, ZUO Chen, YAN Tai-hong
China Institute of Atomic Energy, P. O. Box 275(26), Beijing 102413, China
The geometry, thermodynamic selectivity and UV-vis spectra of Pu(NO3)4TBP2and Pu(NO3)2DBP2in the gas phase were investigated by using B3LYP density functional theory method with the RECP basis for Pu and 6-311 g(d,p) basis for other atoms. The structure optimization results show the bond length between Pu and DBP is shorter than the length between Pu and TBP for the steric hinder of the ligands, and NPA charge analysis shows more electron trasnfer between DBP and Pu ion indicating the stronger coordination ability of DBP. The free energy of ligand exchange between Pu(NO3)4TBP2and HDBP was -178.9 kJ/mol, indicating the higher coordination affinity between DBP and Pu. The UV-vis absorption spectra of Pu(NO3)4TBP2in the gas phase were pmainly from nitrate to f orbital of Pu, TBP ligand made few contribution, yet the absorption spectrum of Pu(NO3)2DBP2were both from nitrate to f orbital of Pu and the ligand-to-metal charge transfer between DBP and Pu.
plutonium; TBP; HDBP; density functional theory
2016-03-03;
2016-09-07
O634.12
A
0253-9950(2016)05-0282-06
10.7538/hhx.2016.38.05.0282

