B與S共摻雜銳鈦礦相TiO2的制備與性能研究*
楊 榮,靳映霞,高洪林,柳清菊
(云南大學 云南省微納材料與技術重點實驗室,昆明 650091)
?
B與S共摻雜銳鈦礦相TiO2的制備與性能研究*
楊 榮,靳映霞,高洪林,柳清菊
(云南大學 云南省微納材料與技術重點實驗室,昆明 650091)
以鈦酸四丁酯、硫脲和硼酸為原料,采用溶膠-水熱法制備了B-S-TiO2光催化劑。通過TG-DTA、XRD、FT-IR、UV-Vis、PL等手段對樣品進行表征和分析,研究了不同熱處理溫度對共摻雜B-S-TiO2光催化劑晶體特性的影響。以亞甲基藍(MB)作為目標降解物,研究了不同熱處理溫度下系列樣品在可見光激發下的光催化性能。結果表明,B和S的共摻可以抑制樣品由銳鈦礦相向金紅石相的轉變,限制晶粒的生長,拓寬TiO2的光譜響應范圍至可見光區,減小了光生電子-空穴對的復合幾率。當n(B)∶n(TiO2)=1∶25,n(S)∶n(TiO2)=1∶50,熱處理溫度為450 ℃時,B-S-TiO2樣品在發光范圍為可見光的普通日光燈下5 h內對亞甲基藍的降解率達92.52%,顯著高于同等實驗條件下P25的降解率(60.74%)。
TiO2;共摻雜;可見光;光催化
0 引 言
TiO2因其具有光催化活性高、化學穩定性好、氧化還原性強、清潔無毒和成本低等優點作為光催化劑被用于降解有機物以來,其禁帶寬度寬和光生載流子壽命短的缺點凸顯[1],嚴重制約了TiO2的應用。因此研究人員致力于尋找有效可行的方法以減小TiO2的禁帶寬度,并提高其對可見光的吸收[2]。在眾多改性TiO2的方法中,離子摻雜改性因性能相對穩定、改性效果好而受到廣泛關注[3]。
研究人員利用第一性原理研究發現離子摻雜可影響TiO2的電子結構,并且有效改善TiO2的光催化性能[4]。實驗也證明非金屬離子的摻雜在避免TiO2晶格被破壞的同時能從窄化禁帶寬度[5]、提供雜化能級[6]和引入氧缺陷[7]3個方面提高TiO2光催化性能,并且不會影響其在紫外光區的催化活性。眾多摻雜改性非金屬中,N摻雜通過N-2p軌道與TiO2價帶頂的O-2p軌道雜化,使得TiO2的價帶上移,能有效將TiO2的光吸收帶邊紅移至可見光區[8-9]。C摻雜主要是在TiO2的禁帶中引入雜質能級,起到減小禁帶寬度的作用[10]。S離子可以以不同的價態(S2-,S4+和S6+)進入TiO2體系形成不同的鍵合形式,且S陽離子和S陰離子進入TiO2對其可見光吸收的影響機理不同,因此S離子的摻雜相對而言比較復雜[11]。通常制備TiO2工藝中環境條件不同會導致S以不同價態形式進入,早期的理論計算顯示S陽離子的摻雜能有效窄化TiO2的禁帶寬度[12],而后期理論計算顯示S的摻雜使S-3p軌道在TiO2的價帶頂部形成的雜質態可能是導致吸收邊界紅移的原因[13]。B摻雜與S摻雜相似,B離子可以以陰離子、陽離子或間隙位置的形式進入TiO2[14-15]。而研究人員對B離子以不同位置替換(B替換O,B替換Ti或間隙)所形成的機理出現爭論[16-17]。有文章認為,B替換O或者B替換Ti的方式實現摻雜,都會因為B-2p軌道與Ti-3d軌道形成耦合效應,在TiO2的導帶底引入雜質態,使摻雜的催化劑的導帶底下移[18]。
所以,不同非金屬離子的摻雜,由于各物質自身物理化學性質的差異,導致對TiO2產生影響的機理不同。我們期望找到一種能對可見光響應、且有效提高光生載流子分離的方法。根據本課題組的理論計算[19]可知, B與S共摻后使得TiO2的能帶整體下移,費米能級由原來的價帶附近移動至導帶附近,而B-2p軌道、S-3p軌道、Ti-3d軌道和O-2p軌道雜化導致價帶寬化,使得TiO2的禁帶寬度變窄,將有利于TiO2光催化性能的提高。基于此,本文通過實驗研究,獲得具有良好的可見光響應的B-S-TiO2光催化劑的制備工藝。
本文采用溶膠-水熱法制備了B-S-TiO2光催化劑,通過TG-DTA、XRD、FT-IR、UV-Vis及PL分析,研究了熱處理溫度對B-S-TiO2光催化性能的影響。
1 實 驗
1.1 B-S-TiO2光催化劑的制備
在60 ℃水浴攪拌條件下,將3 mL自制水解抑制劑加入到75 mL蒸餾水中形成溶液A,充分混合后將5 mL鈦酸四丁酯緩慢加入溶液A中,利用稀硝酸調節溶液的pH值到2~3得到溶液B。稱取一定量的SC(NH2)2和H3BO3加入溶液B中,持續攪拌直至形成透明的淡黃色溶膠。將溶膠靜置陳化12 h后倒入高壓反應釜中,擰緊,放入烘箱中保溫一定時間,冷卻、干燥、熱處理、研磨后得到B-S-TiO2光催化劑。本實驗中,B和S的摻雜量固定為n(B)∶n(Ti)=1∶25,n(S)∶n(Ti)=1∶50。
1.2 光催化劑的表征分析
用德國NETZSCH STA 409 PG/PC型熱重分析儀分析 B-S-TiO2催化劑的反應中間體的晶型轉變溫度;以TTRⅢ型轉靶X射線衍射儀對所得樣品進行物相分析,CuKα靶,管電壓為40 kV,管電流為150 mA,掃描速度為1°/min,掃描范圍為10~90 ℃;以FTS-40型FT-IR光譜儀分析樣品的紅外光譜;以UV-4100型分光光度計測定樣品的紫外-可見漫反射光譜;以FL4500型熒光分光光度計測定樣品的熒光光譜。
1.3 光催化活性研究
實驗以亞甲基藍(MB) 作為目標降解物,取0.2 g所制備的粉體樣品與50 mL的10 mg/L的MB溶液通過磁力攪拌進行混合,黑暗條件下攪拌0.5 h,達到吸附-脫附平衡后取樣,取4 mL溶液,再將混合溶液置于功率為30 W的普通日光燈下進行光催化反應,每隔1 h取樣一次,每次取樣量為4 mL,將所取樣品在離心機中以3 500 r/min離心40 min,取上清液,后用722N型分光光度計測定MB溶液在波長664 nm 處的吸光度值。根據朗伯-比爾定律,溶液的吸光度與濃度成正比,因此可用吸光度代替濃度計算降解率,以此為MB溶液的降解率。利用以下公式計算出MB溶液的降解率η
其中,A0為樣品達到吸附-脫附平衡后MB溶液的初始吸光度;At為反應經過時間t后MB溶液的吸光度。
2 結果與討論
2.1 差熱分析
將未燒結的B-S-TiO2前驅物粉末于空氣氣氛中進行TG-DTA分析,升溫速率10 ℃/min,結果如圖1所示。樣品溫度測試范圍是25~800 ℃,經歷了4個失重過程,其中25~146 ℃為①階段失重3.494%(質量分數),146~275 ℃為②階段失重2.658%(質量分數),275~611 ℃為③階段有2.926%(質量分數)的失重,611~800 ℃為④階段失重1.104%(質量分數)。4個不同的失重階段表明摻雜TiO2由于溫度升高而產生的脫水、脫酯、中間產物分解和摻入的B和S脫出TiO2晶格的過程。階段①伴隨明顯放熱的快速失重過程可歸因于樣品中水分的脫失。此后,在135和170 ℃分別出現弱的放熱和吸熱峰并伴隨少量的失重,這說明該階段可能發生著緩慢有機物分解[20];與純TiO2類似,在130~600 ℃區間內樣品的失重達到5.5%,這是因為樣品中殘留有機物的裂解和中間產物的分解造成的[21- 22]。對于純TiO2,370 ℃開始即出現較緩和的放熱,表明此時已經開始出現了TiO2由銳鈦礦相向金紅石相的轉變。而B-S共摻雜后,TiO2相變的熱吸收溫度提高到了399 ℃,說明B-S共摻雜抑制了TiO2的相變。此外,在249.5 ℃出現了一個較明顯的放熱,這可能是由于B和S與TiO2間形成化合鍵。值得注意的是,共摻雜樣品在600 ℃后存在1.1%(質量分數)的失重,這說明摻雜的B和S不夠穩定,在高溫下能從晶格中逸出形成B2O3或者SO2。另一方面,摻雜樣品的相變完成溫度比純TiO2的低,且吸熱峰強度更弱,表明B和S的析出降低了TiO2的相變溫度和相變所需能量,促進相變。
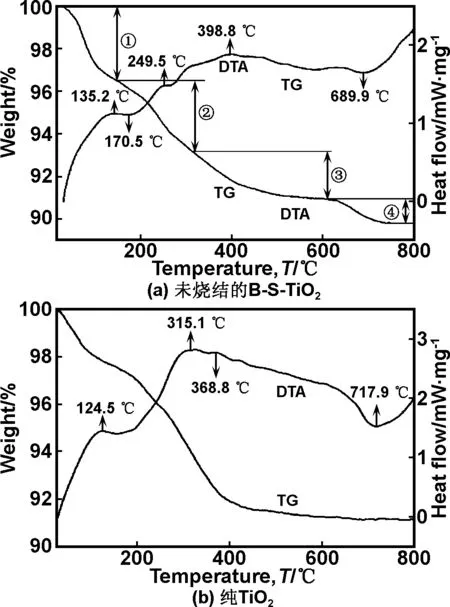
圖1 未燒結的B-S-TiO2和純TiO2樣品的差熱-熱重分析圖
2.2 XRD分析
圖2為制備的B-S-TiO2經不同溫度熱處理后的XRD圖譜以及450 ℃熱處理的純TiO2的XRD圖譜。從圖2中可以看出除400 ℃制備樣品為單一銳鈦礦相,其它樣品均為銳鈦礦相與金紅石相并存。因摻雜樣品中B和S的含量很少,在圖譜中沒有發現B和S的特征衍射峰。
不同溫度下B-S-TiO2系列樣品中,400~550 ℃,晶粒生長速度緩慢,晶相轉變速度更慢,可能是因為TiO2晶格內和晶界上B和S的存在,阻礙了晶體向外界的質量和能量的傳輸,因此會產生類似于“釘扎現象”阻礙 TiO2顆粒的生長[23]。當溫度升高至600 ℃時,分布在晶格內的B2O3和SO2獲得足夠的能量脫離TiO2晶格,抑制作用明顯減弱,晶粒尺寸迅速長大,相變速度提高,650 ℃時,已經有85%銳鈦礦相轉變為金紅石相。
從圖1中可以看出,經450 ℃熱處理的純TiO2中金紅石相含量明顯多于450 ℃熱處理的B-S-TiO2樣品。說明B和S共摻雜對TiO2晶相轉變有一定的抑制作用。

圖2 不同溫度熱處理的B-S-TiO2及450 ℃熱處理的純TiO2樣品的 XRD 譜圖
表1為根據 Quantitative公式和Scherrer公式計算的不同溫度下B-S-TiO2系列樣品和450 ℃熱處理的純TiO2樣品的平均晶粒尺寸和晶胞參數表。通過計算可知,經 450 ℃熱處理后 B-S-TiO2的平均晶粒尺寸為10.49 nm,而相同條件下制備的純TiO2的平均晶粒尺寸為15.79 nm,說明在相同的熱處理溫度下,B和S共摻雜可以抑制 TiO2晶粒的長大。表1數據顯示,所有摻雜樣品在c軸方向均出現壓縮現象。

表1 不同溫度熱處理的B-S-TiO2及450 ℃熱處理的純TiO2樣品的晶格常數及平均晶粒尺寸
B離子半徑為0.088 nm,S離子半徑為0.104 nm,與Ti(離子半徑0.1448 nm)和O(離子半徑0.074 nm)相比,只有B和S替換Ti位進入晶格才有可能出現壓縮的現象。根據楊[24]和Finazzi[25]的理論計算,我們推測摻雜的B是以間隙形式進入TiO2晶胞。至于S離子,根據本課題組的計算[19],結合實際退火實驗條件為富氧條件,我們推測S是以S4+形式進入TiO2晶格。由于S—O的鍵長比Ti—O鍵長短,因此產生壓縮。從銳鈦礦相晶格參數來看,a軸變化不大,c軸為逐漸從壓縮狀態變為接近標準銳鈦礦相TiO2的參數值,這說明隨著溫度的增加,晶胞在逐漸膨脹,晶粒尺寸也隨著熱處理溫度的增加而長大,逐漸轉變為高溫穩定相金紅石相。
2.3 紅外光譜
圖3為450 ℃下熱處理的B-S-TiO2、S-TiO2、B-TiO2以及純TiO2的FT-IR光譜圖。對比圖3的四條曲線發現,S-TiO2曲線中振動峰在相應位置能與B-S-TiO2曲線的振動峰吻合,說明S單摻雜TiO2時所形成的離子形式與共摻所形成的離子形式一致。四條曲線中1 000 cm-1以下的吸收峰均為TiO2晶體和表面Ti—O鍵伸縮振動和彎曲振動引起的,是TiO2晶體的特征振動峰。3 390 cm-1附近的吸收峰是由表面羥基O—H的伸縮振動引起的,與TiO2表面吸附水有關[26],2 354 cm-1處的吸收峰為TiO2的特征吸收峰,1 640 cm-1處的吸收峰為TiO2表面的物理吸附水的彎曲振動峰,TiO2表面吸附水的—OH在光照下可捕獲h+生成具有高氧化能力的羥基自由基·OH,有利于光催化反應的進行[26]。S-TiO2和B-S-TiO2樣品在1 038和1 133 cm-1處有吸收峰,1 133 cm-1處的吸收峰對應于物理吸附SO2,而1 038 cm-1處的吸收峰是由Ti—O—S鍵的振動引起的[27],這也驗證了晶格分析中S以陽離子的形式進入TiO2晶格的猜測是正確的。B-TiO2和B-S-TiO2樣品存在不同的吸收峰。B-TiO2曲線中在1 390和1 330 cm-1左右位置形成的吸收峰在文獻[29]中所提為Ti-O-B振動峰。而B-S-TiO2樣品曲線顯示為1 403和1 201 cm-1存在吸收峰,其中1 201 cm-1為B2O3上形成的B—O鍵彎曲振動峰[28],而1 403 cm-1為Ti-O-B振動峰[29]。B-TiO2和B-S-TiO2樣品FT-IR曲線中Ti-O-B吸收峰位的變化說明B-S的共摻會使B逸出TiO2,形成B2O3。

圖3 B-S-TiO2,B-TiO2,S-TiO2以及純TiO2的FT-IR光譜圖
圖4為經過不同溫度熱處理的B-S-TiO2樣品的FT-IR光譜圖。隨著熱處理溫度的升高,從圖4可以看出,所有特征峰強度均減弱,1 403 cm-1處的Ti-O-B振動峰逐漸減弱,進入TiO2晶格的硼離子獲得能量,逸出TiO2晶格,而1 201 cm-1處的B2O3的B—O鍵彎曲振動峰逐漸消失,說明隨著熱處理溫度的升高,摻入TiO2晶格的硼離子逐漸減少,不足以形成B2O3。隨著熱處理溫度的升高,1 128 cm-1處的物理吸附SO2特征峰也逐漸消失,而1 038 cm-1處的Ti—O—S鍵的振動吸收峰也逐漸消失, 當燒結溫度為600 ℃時,摻入TiO2晶格的物理吸附SO2和陽離子摻雜S4+獲得足夠多的能量逸出晶格,晶格缺陷急劇減少,摻雜離子的抑制作用顯著降低,晶體自修復生長,平均晶粒尺寸迅速增大。
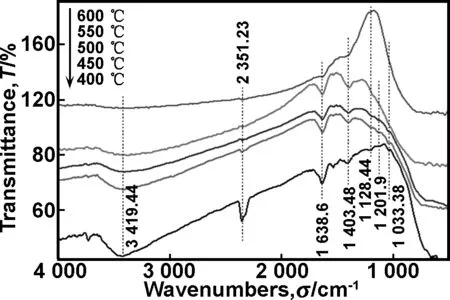
圖4 不同溫度熱處理的B-S-TiO2樣品的FT-IR光譜圖
2.4 紫外-可見漫反射光譜
圖5為經過不同溫度熱處理后的B-S-TiO2樣品及P25的UV-Vis光譜圖。從圖5中可以看出,共摻雜后的樣品與P25相比,在可見光區都有明顯吸收,而且吸收帶邊均發生了一定程度的紅移。隨著熱處理溫度的增加,樣品吸收帶邊紅移程度先保持不變后增加,熱處理溫度為650 ℃時,樣品的吸收帶邊紅移程度最大,較P25紅移約35 nm,因為其金紅石含量最多;熱處理溫度為450 ℃時,樣品在可見光區的吸收最強。根據本課題組的理論計算[19],B和S共摻雜后,使TiO2光催化劑的S-3p軌道、B-2p軌道和O-2p軌道雜化,使價帶寬化上移,禁帶寬度減小,有利于實現TiO2光催化劑對可見光的吸收,說明摻雜能夠有效拓寬TiO2光催化劑對可見光的響應范圍。
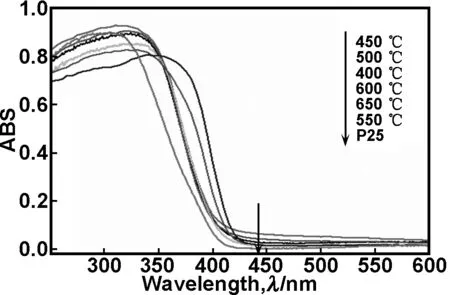
圖5 不同溫度熱處理的B-S-TiO2樣品及P25的UV-Vis光譜圖
2.5 熒光光譜分析
圖6為經過不同溫度熱處理的B-S-TiO2樣品及P25的PL譜圖。從圖6中可看出B-S-TiO2樣品與P25的PL光譜線型和特征峰位置基本一樣,表明B和S的共摻雜沒有引起新的發光現象。隨著溫度的升高,熒光強度先降低后增強,這是由于隨著熱處理溫度的升高,樣品中出現外部為金紅石薄層而內部為銳鈦礦型的包覆結構,金紅石相與銳鈦礦相費米能級不同,在兩相界面間能產生Schottky勢壘,可促進電子及空穴的轉移、分離并遷移到催化劑的表面[31];而當溫度較高時,摻雜進入TiO2晶格的物質可能會逸出晶格,而且金紅石相含量顯著增加,導致晶體缺陷減少,空位增加,空位有可能成為光生載流子的復合中心,不利于光生載流子的傳輸。晶粒也明顯長大,電子、空穴向表面遷移的路程加長,其復合幾率增加。450 ℃熱處理樣品的熒光強度最低,說明該溫度下B和S共摻能更有效抑制光生電子-空穴對的復合。

圖6 P25和不同溫度熱處理的B-S-TiO2樣品的PL譜圖
2.6 光催化性能
圖7為經過不同溫度熱處理制備的B-S-TiO2樣品及P25對亞甲基藍(MB)的光催化降解效果圖。
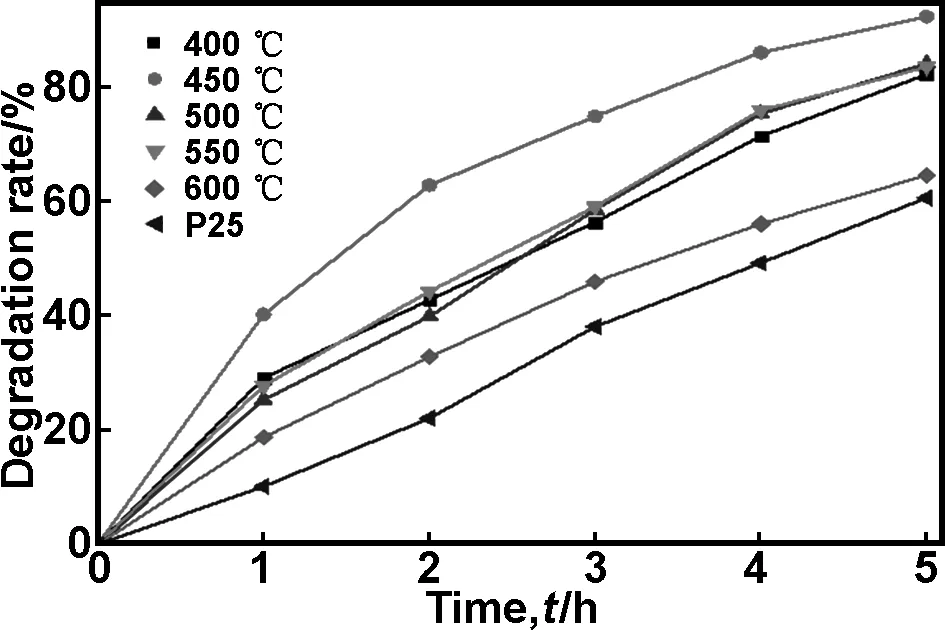
圖7 不同溫度熱處理的B-S-TiO2樣品對MB的光降解曲線
從圖7中可以看出450 ℃熱處理的樣品在普通日光燈下5h 內對 MB 的降解率達到92.52%, 明顯高于 P25(同等實驗條件下60.74%) 及同等條件下制備的其它樣品對 MB 的降解率,由XRD分析可知450 ℃熱處理的樣品平均晶粒尺寸小,比表面積大,光生載流子擴散至催化劑表面的路程短,電子與空穴復合幾率較小,電荷分離效果較好,能夠有更多的光生載流子遷移至催化劑表面參與氧化還原反應,所以催化活性最高。當溫度達到600 ℃時,晶粒尺寸明顯增大,比表面積急劇減小,表面吸附的羥基數量減少,使得光催化活性降低。
3 結 論
通過溶膠-水熱法制備了B-S-TiO2光催化劑。研究發現,B和S分別以陽離子B3+和S4+的形式間隙存在于TiO2晶格中。B和S的共摻雜阻止了TiO2晶相轉變,同時有效抑制了TiO2晶粒的長大。B和S的共摻雜能夠減小TiO2的禁帶寬度,降低光生電子-空穴對的復合,使TiO2吸收光譜帶邊紅移至可見光區,提高了TiO2的光催化活性。當n(B)∶n(TiO2)=1∶25,n(S)∶n(TiO2)=1∶50,450 ℃焙燒4 h實驗條件下樣品的光催化性能最佳,在普通日光燈下5 h內對MB的降解率為92.52%,明顯高于在同等實驗條件下P25對MB的降解率(60.74%)。
[1] Zhang D. Enhanced photocatalytic activity for titanium dioxide by co-modification with copper and iron[J]. Transition Metal Chemistry, 2010, 35(8):933-938.
[2] Kumar S G, Devi L G. Review on modified TiO2photocatalysis under UV/visible light: selected results and related mechanisms on interfacial charge carrier transfer dynamics[J]. The Journal of Physical Chemistry A, 2011, 115(46): 13211-13241.
[3] Yang K, Dai Y, Huang B. Review of the structural stability, electronic and magnetic properties of nonmetal-doped TiO2from first-principles calculations[J]. arXiv Preprint arXiv:1202.5651, 2012.
[4] Zhao Zongyan, Liu Qingju, Zhu Zhongqi, et al. Effects of S doping on electronic structures and photocatalytic properties of anatase TiO2[J]. Acta Physica Sinica-Chinese Edition, 2008,57(6): 3760-3768.
趙宗彥, 柳清菊, 朱忠其, 等. S摻雜對銳鈦礦相TiO2電子結構與光催化性能的影響[J]. 物理學報, 2008,57(6): 3760-3768.
[5] Im J S, Yun S M, Lee Y S. Investigation of multielemental catalysts based on decreasing the band gap of titania for enhanced visible light photocatalysis[J]. Journal of Colloid and Interface Science, 2009, 336(1): 183-188.
[6] Yaghoubi H, Li Z, Chen Y, et al. Toward a visible light-driven photocatalyst: the effect of midgap-states-induced energy gap of undoped TiO2nanoparticles[J]. ACS Catalysis, 2014, 5(1): 327-335.
[7] Ma J, Wu H, Liu Y, et al. Photocatalytic removal of NOxover visible light responsive oxygen-deficient TiO2[J]. The Journal of Physical Chemistry C, 2014, 118(14): 7434-7441.
[8] Livraghi S, Paganini M C, Giamello E, et al. Origin of photoactivity of nitrogen-doped titanium dioxide under visible light[J]. J Am Chem Soc, 2006, 128 (49):15666-15671.
[9] Yang G D, Jiang Z, Shi H H, et al. Preparation of highly visible-light active N-doped TiO2photocatalyst[J]. Journal of Materials Chemistry, 2010, 20(25):5301-5309.
[10] Dong F, Guo S, Wang H Q, et al. Enhancement of the visible light photocatalytic activity of C-doped TiO2nano materials prepared by a green synthetic approach[J]. The Journal of Physical Chemistry C, 2011, 115(27):13285-13292.
[11] Ohno T, Akiyoshi M, Umebayashi T, et al. Preparation of S-doped TiO2photocatalysts and their photocatalytic activities under visible light[J]. Applied Catalysis A: General, 2004, 265(1):115-121.
[12] Sathish M, Sankaran M, Viswanathan B, et al. DFT studies on anionic hetero atom (N or/and S) substitution in TiO2[J]. Indian Journal of Chemistry Section A, 2007, 46(6): 895.
[13] Tian F H, Liu C B. DFT description on electronic structure and optical absorption properties of anionic S-doped anatase TiO2[J]. The Journal of Physical Chemistry B, 2006, 110(36):17866-17871.
[14] Zaleska A, Grabowska E, Sobczak J W, et al. Photocatalytic activity of boron-modified TiO2under visible light: the effect of boron content, calcination temperature and TiO2matrix[J]. Applied Catalysis B: Environmental, 2009, 89(3):469-475.
[15] Chen D M, Yang D, Wang Q, et al. Effects of boron doping on photocatalytic activity and microstructure of titanium dioxide nanoparticles[J]. Industrial and Engineering Chemistry Research, 2006, 45(12):4110-4116.
[16] Finazzi E, Di Valentin C, Pacchioni G. Boron-doped anatase TiO2: pure and hybrid DFT calculations[J]. The Journal of Physical Chemistry C, 2008, 113(1):220-228.
[17] Chen D M, Yang D, Wang Q, et al. Effects of boron doping on photocatalytic activity and microstructure of titanium dioxide nanoparticles[J]. Industrial and Engineering Chemistry Research, 2006, 45(12):4110-4116.
[18] Yang K, Dai Y, Huang B. Origin of the photoactivity in boron-doped anatase and rutile TiO2calculated from first principles[J]. Physical Review B, 2007, 76(19):195201.
[19] Liu Q L, Zhao Z Y, Liu Q J. Synergistic effects of nonmetal co-doping with sulfur in anatase TiO2: a DFT+U study[J]. Physical Chemistry Chemical Physics, 2015(17):3426-3434.
[20] Na Wei, Zhu Zhongqi, Zhang Jin, et al. Study on properties of the anatase nano-TiO2sol [J]. Journal of Functional Materials, 2007, 37(11):1822-1824.
納 薇, 朱忠其, 張 謹,等. 銳鈦礦型納米TiO2溶膠的性能研究[J]. 功能材料, 2007, 37(11):1822-1824.
[21] Wu Y, Xing M, Zhang J, et al. Effective visible light-active boron and carbon modified TiO2photocatalyst for degradation of organic pollutant[J]. Applied Catalysis B: Environmental, 2010, 97(1):182-189.
[22] Wang X, Blackford M, Prince K, et al. Preparation of boron-doped porous titania networks containing gold nanoparticles with enhanced visible-light photocatalytic activity [J]. ACS Applied Materials & Interfaces, 2012, 4(1):476-482.
[23] Wu Jing, Gao Pan, Zhu Zhongqi, et al. Preparation and properties of praseodymium and nitrogen co-doped nano-titanium dioxide photocatalyst[J]. The Chinese Journal of Nonferrous Metals, 2015, 21(6):1480-1484.
吳 晶, 高 攀, 朱忠其, 等. 鐠和氮共摻雜納米TiO2光催化劑的制備與性能[J]. 中國有色金屬學報, 2015, 21(6):1480-1484.
[24] Yang K, Dai Y, Huang B. Origin of the photoactivity in boron-doped anatase and rutile TiO2calculated from first principles[J]. Physical Review B, 2007, 76(19):195201.
[25] Finazzi E, Di Valentin C, Pacchioni G. Boron-doped anatase TiO2: pure and hybrid DFT calculations[J]. The Journal of Physical Chemistry C, 2008, 113(1):220-228.
[26] Wei F Y, Ni L S, Cui P. Preparation and characterization of N-S-codoped TiO2photocatalyst and its photocatalytic activity[J]. Journal of Hazardous Materials, 2008, 156(1):135-140.
[27] Yang G D, Yan Z F, Xiao T C. Low-temperature solvothermal synthesis of visible-light-responsive S-doped TiO2nanocrystal[J]. Applied Surface Science, 2012, 258(8):4016-4022.
[28] Alejandro A, Maria J S, Clara J, et al. Evaluation of sol-gel TiO2photocatalysts modified with carbon or boron compounds and crystallized in nitrogen or air atmospheres[J]. Chemical Engineering Journal, 2015, 277:11-20.
[29] Chen D M, Yang D, Wang Q, et al. Effects of boron doping on photocatalytic activity and microstructure of titanium dioxide nanoparticles[J]. Industrial & Engineering Chemistry Research, 2006, 45(12):4110-4116.
[30] Gao Wei, Wu Fengqing, Luo Zhen, et al. Studies on the relationship between the crystal form of TiO2and its photocatalyzing degradation efficiency[J]. Chemical Journal of Chinese Uuniversity, 2001, 22(4):660-662.
高 偉, 吳鳳清, 羅 臻, 等. TiO2晶型與光催化活性關系的研究[J]. 高等學校化學學報, 2001, 22(4):660-662.
Study on preparation and properties of TiO2codoped with Boron and Sulfur
YANG Rong, JIN Yingxia, GAO Honglin, LIU Qingju
(Yunnan Key Laboratory for Micro/Nano Materials & Technology, Yunnan University,Kunming 650091, China)
B-S-TiO2photocatalysts were synthesized by sol-hydrothermal method using tetrabutyl titanate, thiourea and boric acid as precursors and characterized by TG-DTA, XRD, FT-IR, UV-Vis and PL methods. The influences of different heat treated temperatures on properties were studied. The photocatalytic activity of B-S-TiO2photocatalysts was investigated by measuring the degradation rate of methylene-blue (MB) under visible light irradiation. The results show that B, S codoping can not only inhabit the phase transition of anatase to rutile, restrain the growth of the grain but also broaden the absorption region to visible light and inhibit the recombination of the photo-generated electrons and holes. The photocatalytic activity of the sample with molar ratio ofn(B)∶n(TiO2)=1∶25,n(S)∶n(TiO2)=1∶50 and calcinated temperature of 450 ℃ was the best under the irradiation of fluorescent light, it was 92.52% within 5 hours and significantly higher than that of Degussa P25(60.74%) under the same experimental conditions.
TiO2; codoping; visible light; photocatalytic
1001-9731(2016)10-10142-06
國家高技術研究發展計劃(863計劃)資助項目(2015AA034601);國家自然科學基金資助項目(51262030)
2015-11-10
2016-06-14 通訊作者:柳清菊,E-mail: qjliu@ynu.edu.cn
楊 榮 (1991-),女,在讀碩士,師承柳淸菊教授,從事TiO2光催化材料研究。
TQ426.2
A
10.3969/j.issn.1001-9731.2016.10.026

