碳鋼陽極氧化制備氧化鐵納米管陣列薄膜及其形成機理*
鄧洪達, 曹獻龍,唐 笑
(重慶科技學院 冶金與材料工程學院,重慶 401331)
?
碳鋼陽極氧化制備氧化鐵納米管陣列薄膜及其形成機理*
鄧洪達, 曹獻龍,唐 笑
(重慶科技學院 冶金與材料工程學院,重慶 401331)
采用陽極氧化法在含氟的乙二醇溶液中以低碳鋼為基體制備出高度有序排列的納米管陣列結構氧化鐵薄膜,并采用SEM分析制備工藝參數對薄膜形貌和尺寸的影響;采用XRD和XPS對熱處理前后薄膜表征。結果表明陽極氧化電壓和氟離子濃度是影響薄膜形貌和納米管尺寸最重要因素,在30~60 V陽極氧化電壓和0.03~0.1 mol/L NH4F范圍內可以制備出管狀結構的薄膜,且隨陽極氧化電壓升高,管徑增加;隨氟離子含量提高,管徑增加。溫度只是影響管狀結構生長速度。經過500 ℃氬氣氣氛熱處理后非晶態薄膜轉化為主要由赤鐵礦和少量磁鐵礦構成的晶態薄膜。最后提出了納米管形成機理。
赤鐵礦;納米管陣列結構;陽極氧化;氟離子
0 引 言
材料表面納米化是一種在金屬表面形成一層與基體的機械、物理和化學性能不同的納米表層的技術。基于納米材料獨特的結構和性能,材料表面納米化處理可以明顯提高材料的疲勞強度、抗蝕性和耐磨性或其它特種性能[1]。為了增強碳鋼的性能,如耐蝕性[2]、超疏水性[3]、耐摩擦磨損性[4-5],鋼鐵表面需覆蓋一層納米涂層。為了獲得這些涂層,目前選擇不同方法制備,如熱噴涂[6]、等離子噴涂[7]、機械合金化[8]、超音速激光沉積[9]或無氣噴涂[10]。與其它方法不同,陽極氧化可以在碳鋼表面制備出一維排列有序的納米孔結構赤鐵礦薄膜[11],且該赤鐵礦薄膜具有明顯的半導體性質,已將其應用于光電化學分解水產氫。在所有一維納米結構(納米棒[12]、納米孔[13]和納米管[14])中,納米管陣列結構是目前解決赤鐵礦電子-空穴復合率高,導電率低問題有效辦法之一。該結構的管壁薄,縮短空穴從內部遷移到達薄膜/介質表面距離,極大減少電子-空穴復合可能性[15-16];同時高度排列有序納米管直接生長在導電基底上,不需要額外的電流收集器,降低薄膜與基底之間的Schottky類型接觸電阻,加速電子轉移速度[17-18];納米管內外都能接收光子,改進管的光吸收和傳播[6],因此這樣獨特結構明顯改善赤鐵礦的電學和光學物理性質。
目前常選擇純鐵陽極氧化方法在純鐵表面制備納米管陣列結構赤鐵礦薄膜,如Mohapatra S. K.等[15]最早報道在純鐵基底上制備超薄高度排列有序納米管陣列薄膜,并發現納米管結構的電荷傳遞速度是納米顆粒的40~50倍。由于高度排列有序納米管陣列結構赤鐵礦優異的光電性質,現已經被應用到水分解[14-15,17, 19-20]、光催化[19,21]、光陰極保護[22]和鋰離子電池[18,23]領域。雖然純鐵表面能夠制備出高度排列有序納米管陣列結構薄膜,但目前報道碳鋼表面只能制備出非納米結構氧化膜[24]或納米孔結構氧化膜[11,25],尚未有報道碳鋼表面制備出高度排列有序納米管陣列結構薄膜的制備工藝和形成機理。本文選擇低碳鋼作為研究對象,采用陽極氧化法制備納米管陣列膜,研究制備工藝參數(陽極氧化電壓、時間、氟離子濃度和溫度)對納米管形貌和尺寸影響。利用FI-SEM對納米管陣列結構薄膜的形貌表征;利用X射線能譜儀(XPS)和小角度掠射X射線衍射儀(XRD)對薄膜的成分和晶型表征。結合陽極氧化過程監測電流密度-時間曲線探討納米管生長機制。
1 實 驗
1.1 薄膜制備
選用低碳鋼的化學成分為C 0.05%,Si 0.01%,Mn 0.25%,P 0.015%,Al 0.054%,N 0.0049%。將低碳鋼加工為1 cm×1 cm×0.4 cm尺寸試樣,并采用環氧樹脂封裝,試樣暴露面積為1 cm2。采用水砂紙逐級打磨至2000號,并選用0.3 μm Al2O3拋光;水沖洗后分別在無水乙醇、水和無水乙醇中超聲處理10 min,并用氮氣吹干。采用陽極氧化法在碳鋼制備氧化鐵納米管陣列薄膜,工作電極(低碳鋼)和對電極(Ti-Pt)之間保持4 cm距離,監測電流密度隨時間變化曲線。電解液采用含0.01~0.1 mol/L NH4F和0.3%(體積分數)H2O的乙二醇混合溶液。陽極氧化結束后,取出工作電極,分別在去離子水、無水乙醇浸泡5 s,氮氣吹干,置于80 ℃馬弗爐中烘干12 h(除去薄膜中水分和殘留有機溶劑),最后置于500 ℃純氬氣氣氛中熱處理4 h。
1.2 樣品表征
采用場發射掃描電子顯微鏡(Nova NanoSEM 430)表征薄膜的形貌和納米管尺寸。采用XPS (ESCA Lab 220XL, Thermo VG-Scientific) 和XRD (PW3040, Philips)對薄膜成分和晶型表征。
2 結果與討論
2.1 制備工藝參數對薄膜結構影響
圖1為碳鋼在不同陽極氧化電壓條件下在含0.1 mol/L NH4F乙二醇混合溶液(0.3%H2O)中經過5 min陽極氧化后制得薄膜。當陽極氧化電壓為30 V時,薄膜上分布著孔徑不均勻的納米管,管的內徑約40 nm,管外壁不明顯,膜表面不平整(圖1(a))。當氧化電位提高到40 V時,薄膜上分布著孔徑較為均勻的納米管,管的內徑約55 nm,管壁厚度約為30 nm,管壁之間界線不明顯,膜表面較為平整(圖1(b))。當氧化電位提高到50 V時,薄膜上納米管孔徑均勻,管的內徑約56 nm,管壁厚度約為30 nm,薄膜表面平整,薄膜上納米管分布均勻(圖1(c))。當氧化電位進一步提高到60 V時,薄膜上分布著孔徑均勻納米管,管的內徑約60 nm,管壁厚度約為30 nm,納米管之間間隔距離擴大,部分納米管倒伏(圖1(d))。由此可看出,隨著陽極氧化電壓提高,納米管孔徑增大,壁厚增加,但電位超過50 V后,納米管孔徑和壁厚變化小。

圖1 碳鋼在不同陽極氧化電壓條件下納米管陣列薄膜的SEM譜圖
圖2(a)為碳鋼在40V條件下在含0.1 mol/L NH4F乙二醇混合溶液(0.3%H2O)中經過10 min陽極氧化后制得氧化鐵納米管陣列膜。與圖1(b)相比,隨著時間延長,納米管內徑和管壁變化小,但納米管之間間隙更為明顯,同時膜表面平整度下降。圖2(b)為碳鋼在50 V條件下在含0.1 mol/L NH4F乙二醇混合溶液(3.0%(體積分數)H2O)中經過2 min陽極氧化后制得氧化鐵納米管陣列膜。結合圖2(b)與圖1(c)可看出,陽極氧化時間延長,納米管內徑和壁厚變化小,納米管之間間隙更為明顯,膜平整度也下降。比較圖2(a)和(b)可看出,為了獲得納米管尺寸分布均勻的納米管陣列結構薄膜,當施加低陽極氧化電壓低時,則氧化時間需延長;反之施加陽極氧化電壓高時,則氧化時間縮短。
圖3為碳鋼在50 V條件下在不同NH4F含量的乙二醇混合溶液(3.0%(體積分數)H2O)中經過5 min陽極氧化后制備氧化鐵納米管陣列膜。當氟離子含量為0.01 mol/L時,氧化鐵薄膜表面由一層致密膜構成,且表面分布著不同尺寸的顆粒,沒有發現納米管(圖3(a));當氟離子含量提高到0.03 mol/L時,薄膜表面出現納米管,但納米管尺寸不均勻(圖3(b));當氟離子含量達到0.05 mol/L時,薄膜表面出現明顯的納米管,但納米管尺寸不均勻,管的內徑約20~40 nm,管壁厚度約為25~35 nm(圖3(c));當氟離子含量為0.07 mol/L時,薄膜表面出現明顯的納米管,納米管尺寸均勻,管的內徑約40 nm,管壁厚度約為25 nm(圖3(d))。結合圖1(c)可看出,當氟離子濃度達到和超過0.03 mol/L時,氧化鐵薄膜表面出現納米管,隨氟離子含量提高,納米管內徑增加,且管尺寸分布均勻。

圖2 碳鋼在不同陽極氧化電壓和氧化時間條件下納米管陣列薄膜

圖3 碳鋼在不同氟含量乙二醇溶液中納米管陣列膜形貌
此外還考察了溫度(室溫-50 ℃)對薄膜影響,結果表明,改變溫度只影響其納米管形成速率,對膜的形貌影響不明顯。
2.2 納米管形成機理
明碳鋼陽極氧化過程中納米管狀結構形成機理,選擇碳鋼在含0.1 mol/LNH4F的乙二醇溶液(3.0%(體積分數) H2O)中60 V電壓下陽極氧化過程的電流密度-時間曲線作為代表分析納米管形成機理。在兩極間施加一定電位后,電流密度從最高值瞬間急劇下降,然后緩慢上升,直到最后出現電流密度平臺。根據電流密度-時間曲線特點,可以將陽極氧化制備納米管陣列膜過程劃分為4個階段(圖4):初級氧化薄膜生成、孔引發、納米管形成和納米管生長。在陽極電壓作用下,鐵與水作用,在鐵/溶液界面上形成氧化鐵鈍化膜,極溶解速度急劇下降(圖4(A區))[15]。在高的電壓作用下,配合物(如F-)朝正極方向電遷移,當氟離子與氧化鐵鈍化膜接觸后,氧化鐵膜發生化學溶解反應,則在鈍化膜上隨機分布孔蝕核[15],引發孔蝕核下金屬再次溶解,陽極溶解速度增加(圖4(B區))。隨著氟離子與氧化鐵化學溶解反應繼續進行,鈍化膜上形成有序納米孔,則有更多氟離子進入納米孔,致使孔徑和孔深增大;在電場作用下氧化膜中納米孔內存在電場,氟離子優先沿納米孔徑向遷移到孔邊緣附近,在孔邊緣處濃縮,形成氫氟酸[14],則孔邊緣附近HF蝕刻水合氧化鐵,形成納米管;由于氟離子的化學溶解速度慢于氧化膜生長速度,氧化膜繼續增厚,陽極溶解速度緩慢下降(圖4(C區))。當納米孔在氧化膜生長和化學溶解速度共同競爭到達動態平衡,則在鈍化膜上形成直立納米管陣列,則陽極溶解速度維持穩定(圖4(D區))。
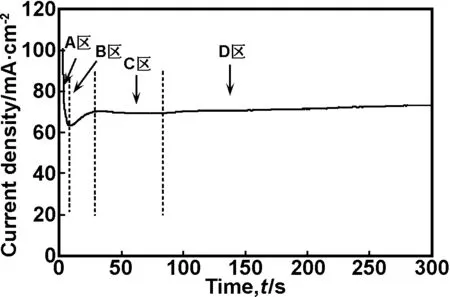
圖4 碳鋼在含0.1 mol/L NH4F和3.0%(體積分數)H2O的乙二醇溶液中不同陽極氧化時間電流密度隨時間變化(Vbia=60 V)
納米管陣列薄膜形成過程受氧化膜生長和氧化膜刻蝕速率控制,而氧化膜生長和氧化膜化學刻蝕速率與陽極氧化工藝密切相關,如氟離子含量和陽極氧化電壓。當陽極氧化電位提高,更多金屬被溶解進入金屬-溶解界面層,初級氧化膜形成速度加快,為氟離子化學刻蝕提供更多場所,納米管分布更為均勻(圖1(d)。當陽極氧化電位低時,化學刻蝕速率快于氧化膜形成速率,則出現納米管分布不均勻,膜不平整(圖1(a)),或甚至無膜。當溶液中氟離子含量增加時,更多的氟離子參與化學蝕刻氧化膜,則裸露出更多金屬基底面積,增加金屬溶解速率,納米管分布均勻(圖3(d))。當氟離子濃度低時,氟離子化學刻蝕能力低,不能產生納米管(圖3(a));當氟離子濃度超過0.03 mol/L時,氧化膜上產生納米管(圖3(b))。
2.3 納米管陣列結構薄膜表征
圖5為碳鋼在含0.1 mol/L NH4F和3.0%(體積分數)H2O的乙二醇溶液中50 V陽極氧化電壓條件下陽極氧化5 min制備的納米管陣列結構薄膜熱處理前后XPS圖譜。由圖5(a)可知,熱處理前薄膜表面除了含有Fe及O元素之外,還含有C和少量的F元素,其中C和F元素來自于溶液殘留。但經過500 ℃熱處理后,薄膜表面氟離子吸收峰消失(圖5(a)),薄膜表面只含Fe、O和C元素。在Fe元素的窄帶上(圖5(b)),經過熱處理前后在約718 eV處出現三價鐵的副峰,其中薄膜熱處理后的三價鐵副峰更為明顯,表明熱處理后薄膜出現三價氧化鐵[26]。圖6為碳鋼在含0.1 mol/L NH4F和3.0%(體積分數)H2O的乙二醇溶液中50 V陽極氧化電壓條件下陽極氧化5 min制備的納米管陣列結構薄膜熱處理前后的X射線角掠射圖。從圖6可看出,熱處理前薄膜的衍射峰主要為碳鋼基底Fe的衍射峰,薄膜呈非晶態; 熱處理后薄膜的衍射峰為薄膜的赤鐵礦和磁鐵礦的衍射峰,表面薄膜主要由赤鐵礦和少量磁鐵礦構成。

圖5 熱處理前后薄膜的X射線光電子能譜
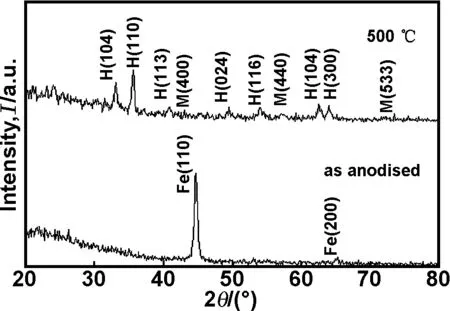
圖6 熱處理前后薄膜的X射線衍射
3 結 論
在含氟離子和3.0%(體積分數) 水的乙二醇溶液中采用陽極氧化法在低碳鋼表面可以制備出赤鐵礦納米管陣列結構薄膜。納米管陣列薄膜形成過程受氧化膜生長和氧化膜刻蝕速率控制。在30~60 V陽極氧化電壓范圍內和在0.03~0.1 mol/L NH4F濃度范圍內可以制備出管狀結構的氧化鐵薄膜,且隨陽極氧化電壓升高,管徑增加;隨氟離子含量提高,管徑增加。溫度只是影響管狀結構的生長速度。熱處理后非晶態薄膜轉化為主要由赤鐵礦和少量磁鐵礦構成的晶態薄膜。
[1] Gao Jiacheng, Wang Qiang, Gao Zhengyuan. Research progress in metallic surface nanocrystallization induced by surface mechanical attrition treatment [J]. Journal of Functional Materials, 2010, 41(5): 741-745.
高家誠, 王 強, 高正源.機械研磨金屬表面納米化的研究進展[J]. 功能材料,2010, 41(5):741-745.
[2] Kang T H, Bagkar Nitin C, Jung Y S, et al. Development of inorganic and organic hybrid nanocoating based on carbon nanotubes for corrosion resistance [J]. Journal of Nanoscience and Nanotechnology, 2014, 14 (10):7824-7829.
[3] Sethi S, Dhinojwala A. Superhydrophobic conductive carbon nanotube coatings for steel [J]. Langmuir, 2009, 25 (8), 4311-4313.
[4] Wang Z B, Tao N R, Li S, et al. Effect of surface nanocrystallization on friction and wear properties in low carbon steel [J]. Materials Science and Engineering: A, 2003, 352 (1-2): 144-149.
[5] Wang Z B, Lu J, Lu K. Wear and corrosion properties of a low carbon steel processed by means of SMAT followed by lower temperature chromizing treatment [J]. Surface and Coatings Technology, 2006, 201 (6): 2796-2801.
[6] Basak A K, Celis J P, Ponthiaux P, et al. Effect of nanostructuring and Al alloying on corrosion behaviour of thermal sprayed WC-Co coatings [J]. Materials Science and Engineering: A, 2012, 558: 377-385.
[7] Fernandes F, Ramalho A, Loureiro A, et al. Influence of nanostructured ZrO2additions on the wear resistance of Ni-based alloy coatings deposited by APS process [J]. Wear, 2013, 303 (1-2): 591-601
[8] Mohammadnezhad M, Shamanian M, Enayati M H, et al. Formation of nanostructured NiAl coating on carbon steel by using mechanical alloying [J]. Applied Surface Science, 263: 730-736.
[9] Lupoi R, Cockburn A, Bryan C, et al. Hardfacing steel with nanostructured coatings of Stellite-6 by supersonic laser deposition [J]. Light: Science & Applications, 2012, 1: 1-6.
[10] Bagherzadeh M R,Daneshvar A. Novel water-based nanosiloxane epoxy coating for corrosion protection of carbon steel [J]. Surface and Coatings Technology, 2012, 206 (8-9): 2057-2063.
[11] Rangaraju R R, Raja K S, Panday A, et al. Low-cost photoelectrocatalyst based on a nanoporous oxide layer of low-carbon steel [J]. Journal of Physics D: Applied Physics, 2010, 43: 445301-445308.
[12] Chang C Y, Wang C H, Tseng C J, et al. Self-oriented iron oxide nanorod array thin film for photoelectrochemical hydrogen production [J]. International Journal of Hydrogen Energy, 2012, 37(18):13616-13622.
[13] Prakasam H E, Varghese O K, Paulose M, et al. Synthesis and photoelectrochemical properties of nanoporous iron (Ⅲ) oxide by potentiostatic anodization [J]. Nanotechnology, 2006, 17:4285.
[14] Rangaraju R R, Raja K S, Panday A, et al. An investigation on room temperature synthesis of vertically oriented arrays of iron oxide nanotubes by anodization of iron [J]. Electrochimica Acta, 2010, 55:785-793.
[15] Mohapatra S K, John S E, Banerjee S, et al. Water Photooxidation by smooth and ultrathin α-Fe2O3nanotube arrays [J]. Chemistry of Materials, 2009, 21, 3048-3055.
[16] Mao A, Shin K, Kim J K, et al. Controlled synthesis of vertically aligned hematite on conducting substrate for photoelectrochemical cells: nanorods versus nanotubes [J]. Applied Materials & Interface, 2011, 3: 1852-1858.
[17] Rangaraju R R, Panday A, Raja K S, et al. Nanostructured anodic iron oxide film as photoanode for water oxidation [J]. Journal of Physics D: Applied Physics, 2009, 42: 135303.
[18] Xie K Y, Li J, Lai Y Q, et al. Highly ordered iron oxide nanotube arrays as electrodes for electrochemical energy storage [J]. Electrochemistry Communications, 2011, 13: 657-660.
[19] Zhang Z H, Hossain M F, Takahashi T. Self-assembled hematite (α-Fe2O3) nanotube arrays for photoelectrocatalytic degradation of azo dye under simulated solar light irradiation [J]. Applied Catalysis B: Environmental, 2010, 95: 423-429.
[20] La Tempa T J, Feng X J, Paulose M, et al. Temperature-dependent growth of self-assembled hematite (α-Fe2O3) nanotube arrays: rapid electrochemical synthesis and photoelectrochemical properties [J]. Journal of Physical Chemistry C, 2009, 113: 16293-16298.
[21] Jang J W, Park J W. Iron oxide nanotube layer fabricated with electrostatic anodization for heterogeneous Fenton like reaction [J]. Journal of Hazardous Materials, 2014, 273: 1-6.
[22] Deng H D, Huang M C, Weng W H, et al. Photocathodic protection of iron oxide nanotube arrays fabricated on carbon steel [J]. Surface & Coatings Technology, 2015, 266: 183-187.
[23] Pervez S A, Kim D, Farooq U, et al. Comparative electrochemical analysis of crystalline and amorphous anodized iron oxide nanotube layers as negative electrode for LIB [J]. ACS Applied Materials & Interfaces, 2014, 6: 11219-1122.
[24] Burleigh T D, Dotson T C, Dotson K T, et al. Anodizing steel in KOH and NaOH solutions [J]. Journal of the Electrochemical Society, 2007, 154 (10): C579-C586.
[25] Konno Y, Yang S, Tuji E, et al. Formation of self-organized nanoporous anodic films on carbon Steel [J]. ECS Transations, 2013, 50(37): 183-190.
[26] Hong J P, Lee S B, Jung Y W, et al. Room temperature formation of half-metallic Fe3O4thin films for the application of spintronic devices [J]. Applied Physics Letters, 2003, 83: 1590-1592.Fabrication and formation mechanism of iron oxide nanotubes arrays on carbon steel by anodization
DENG Hongda,CAO Xianlong, TANG Xiao
(School of Metallurgical and Materials Engineering, Chongqing University of Science and Technology,Chongqing 401331, China)
Thin films consisting of highly self-organized nanotube arrays were fabricated on carbon steel substrate in an aqueous ethylene glycol solution containing fluoride by anodization. It has been investigated by SEM that several synthesis parameters, such as anodizing voltage, anodizing time, concentration of fluoride ion and temperature affected on the morphology of the film comprising nanotube arrays and tube size. XRD and XPS techniques have been used to characterize the nanotube arrays film. Results show that anodization voltage and concentration of fluoride ion are the key factors to effect on the morphology of the film and tube size. The nanotube structured film forms between 30 and 60 V, and in the range of 0.03 and 0.1 mol/L NH4F. The average pore diameter of the tubes increases with the increases of the anodization voltage and concentration of fluoride ion. Temperature only has an influence on the rate of tube formation of flim. Amorphous film transforms into the crystallized film composed of predominant hematite phase and minor magnetite phase. Finally, the possible growth of nanotube arrays was also proposed.
hematite; nanotube arrays strucuture; anodizing; fluoride ion
1001-9731(2016)10-10168-05
重慶市自然科學基金資助項目(cstc2012jjA50022,CSTC2015JCYJA50003);重慶科技學院重點項目培育基金資助項目(CK2016Z09,CK2014Z22);重慶市教委科學技術研究資助項目(KJ1401314,KJ1401310);院士專家工作站合作資助項目(CKYS2014Z03);重慶市南川區科技計劃資助項目(CX201407)
2015-10-19
2016-05-12 通訊作者:鄧洪達,E-mail: dhd7730@163.com
鄧洪達 (1977-),男,四川南部人,副教授,博士. 從事氧化物薄膜光電性質利用研究。
TB332
A
10.3969/j.issn.1001-9731.2016.10.031

