HPLC法測定他米巴羅汀片的溶出度
陳麗姣,楊冬霞,趙艷霞(1.山東理工職業學院,山東濟寧 7067;.山東創新藥物研發有限公司,濟南50101;3.山東省醫學科學院研究生教育中心,濟南 5006)
HPLC法測定他米巴羅汀片的溶出度
陳麗姣1*,楊冬霞2,趙艷霞3#(1.山東理工職業學院,山東濟寧 272067;2.山東創新藥物研發有限公司,濟南250101;3.山東省醫學科學院研究生教育中心,濟南 250062)
目的:建立測定他米巴羅汀片溶出度的方法。方法:采用高效液相色譜法。色譜柱為Diamonsil C18,流動相為甲醇-水-冰乙酸(85∶15∶1,V/V/V),流速為1.0 ml/min,檢測波長為235 nm,柱溫為25℃,進樣量為20 μl。溶出度測定采用槳法,以pH6.8磷酸鹽緩沖液為溶出介質,溶出介質體積為900 ml,轉速為50 r/min,60 min取樣。結果:他米巴羅汀檢測質量濃度線性范圍為0.801~2.804 μg/ml(r=0.999 6);精密度、穩定性、重復性試驗的RSD<3%;回收率分別為99.58%~100.90%(RSD=0.25%,n=9);3批樣品的溶出度測定結果分別為98.25%、96.54%、92.38%(n=6)。結論:該方法簡便、準確,靈敏度高,專屬性強,適用于他米巴羅汀片的溶出度測定。
高效液相色譜法;他米巴羅汀片;溶出度
急性早幼粒細胞白血病(APL)是一種特殊類型急性髓系白血病,病程發展迅速,死亡率高[1]。APL患者存在染色體t(15;17)易位,該易位導致分別定位于染色體15q22和17q21的病變蛋白與維A酸受體(RAR)α嵌合,形成PML-RARα融合基因[2-4]。他米巴羅汀(Tamibarotene)化學名為4-[(5,6,7,8-四氫-5,5,8,8-四甲基-2-萘基)甲酰]苯甲酸,它是一個新的RARα促進劑,對復發或難治性急性前骨髓細胞性白血病(即APL)具有顯著的分化誘導能力,從而可產生治療作用。其片劑由日本新藥株式會社研制開發,于2005年在日本首次上市(商品名:Amnolake,規格:2 mg)[5-6],該藥口服后吸收迅速、療效確切、副作用小[7]。目前,其仿制藥我國有幾家研發單位正在申報臨床,國內市場空間巨大。為了保障藥品質量和用藥安全,筆者參照2015年版《中國藥典》(四部)“溶出度與釋放度測定法”[8]和《普通口服固體制劑溶出度試驗技術指導原則》[9]中的相關要求,采用高效液相色譜法(HPLC)建立了國產他米巴羅汀片的溶出度測定方法。
1 材料
1.1 儀器
600E-2487型HPLC儀,包括600E多溶劑輸送系統(有梯度控制器的高壓輸液泵)、在線脫氣機、Rheodyne 7725i手動進樣閥、2487雙通道紫外檢測器等(美國Waters公司);ZRS-8G型智能溶出試驗儀(天津市天大天發科技有限公司);AX105DR型電子分析天平(瑞士Mettler-Toledo公司)。
1.2 藥品與試劑
他米巴羅汀片(濟南康和醫藥科技有限公司,批號:20130401、20130402、20130403,規格:2 mg);他米巴羅汀對照品(濟南康和醫藥科技有限公司,批號:20130301S,純度:99.9%);甲醇為色譜純,其他試劑均為分析純,水為重蒸水。
2 方法與結果
2.1 色譜條件[10]
色譜柱:Diamonsil C18(250 mm×4.6 mm,5 μm);流動相:甲醇-水-冰乙酸(85∶15∶1,V/V/V);流速:1.0 ml/min;檢測波長:235 nm;柱溫:25℃;進樣量:20 μl。
2.2 溶液的制備
2.2.1 對照品溶液 取對照品適量,精密稱定,加甲醇10 ml使溶解,用溶出介質pH6.8磷酸鹽緩沖液(取0.2 mol/L磷酸二氫鉀溶液250 ml,加0.2 mol/L氫氧化鈉溶液118 ml,用水稀釋至1 000 ml,搖勻,即得)稀釋制成每1 ml中約含2 μg的溶液,作為對照品溶液。
2.2.2 供試品溶液 取樣品適量,采用2015年版《中國藥典》(四部)“溶出度與釋放度測定法”第二法(槳法),以pH6.8磷酸鹽緩沖液為溶出介質,溶出介質體積為900 ml,轉速為50 r/min,溫度為(37±0.5)℃,依法操作,于60 min時取溶出液10 ml,經0.45 μm微孔濾膜濾過,取續濾液作為供試品溶液。
2.3 濾膜吸附試驗
取按“2.2.1”項下方法制備的對照品溶液適量,作為濾過前溶液;取上述濾過前溶液適量,用0.45 μm微孔濾膜濾過,取續濾液作為濾過后溶液。分別取濾過前、后溶液適量,按“2.1”項下色譜條件進樣測定,記錄峰面積并計算含量,以濾過前含量為100%,計算濾膜吸附量。結果表明,0.45 μm微孔濾膜對他米巴羅汀的吸附量<2.0%,符合規定[9]。
2.4 專屬性試驗
取“2.2”項下對照品溶液、供試品溶液和溶出介質各20 μl,分別按“2.1”項下色譜條件進樣測定,記錄色譜,詳見圖1。結果表明,供試品和對照品色譜中主峰的保留時間一致;各成分峰基線分離良好,且其他成分對主成分測定無干擾。
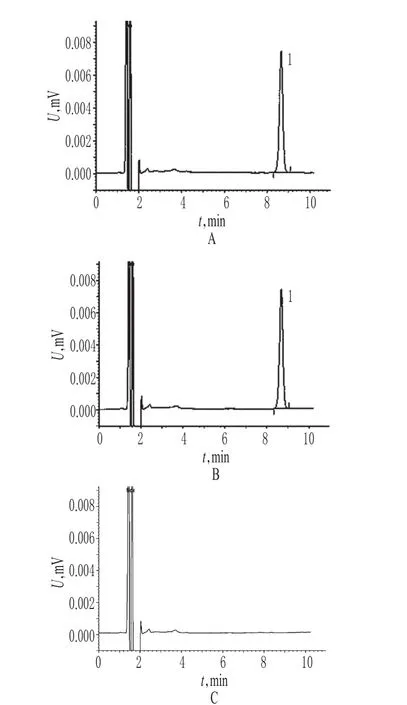
圖1 高效液相色譜圖A.對照品;B.供試品;C.溶出介質;1.他米巴羅汀Fig 1 HPLC chromatogramsA.reference substance;B.test sample;C.dissolution medium;1.tamibarotene
2.5 線性關系考察
取對照品約10 mg,精密稱定,置于100 ml量瓶中,加甲醇10 ml使溶解,以溶出介質pH6.8磷酸鹽緩沖液稀釋至刻度,搖勻,精密量取10 ml,置于50 ml量瓶中,用pH6.8磷酸鹽緩沖液稀釋至刻度,搖勻,作為貯備液。精密量取上述貯備液2、3、4、5、6、7 ml,分別置于50 ml量瓶中,加pH6.8磷酸鹽緩沖液稀釋至刻度,配制成質量濃度分別為0.8~2.8 μg/ml的系列對照品溶液,分別按“2.1”項下色譜條件進樣測定,記錄峰面積。以他米巴羅汀質量濃度(x,μg/ml)為橫坐標、峰面積(y)為縱坐標進行線性回歸,得回歸方程為y=101 023x-1 924.4(r=0.999 6)。結果表明,他米巴羅汀檢測質量濃度線性范圍為0.801~2.804 μg/ml。
2.6 精密度試驗
2.6.1 儀器精密度 取“2.2.1”項下對照品溶液適量,按“2.1”項下色譜條件連續進樣測定6次,記錄峰面積。結果,他米巴羅汀峰面積的RSD=0.25%(n=6),表明儀器精密度良好。2.6.2 中間精密度 取同一批樣品(批號:20130401)6片,由不同人員分別按“2.2.2”項下方法制備供試品溶液,各6份,分別在不同儀器上(Waters 600型和Waters 2695型HPLC儀)按“2.1”項下色譜條件進樣測定并計算溶出度。結果,他米巴羅汀片的平均溶出度分別為98.42%、97.25%,RSD分別為2.06%、2.14%(n=6),表明本方法的中間精密度良好。
2.7 穩定性試驗
取“2.2.2”項下供試品溶液(批號:20130401)適量,分別于室溫下放置0、1、2、4、6、8 h時,按“2.1”項下色譜條件進樣測定,記錄峰面積。結果,他米巴羅汀峰面積的RSD=0.37%(n=6),表明供試品溶液在室溫下放置8 h內穩定性良好。
2.8 重復性試驗
精密稱取同一批樣品(批號:20130401)適量,按“2.2.2”項下方法制備供試品溶液,共6份,再按“2.1”項下色譜條件進樣測定,記錄峰面積。結果,他米巴羅汀峰面積的RSD=0.74%(n=6),表明本方法重復性良好。
2.9 回收率試驗
取對照品約12、16、20 mg,每種質量各3份,置于不同的100 ml量瓶中,再分別按樣品處方比例混合輔料,加甲醇10 ml使溶解,加溶出介質pH6.8磷酸鹽緩沖液稀釋至刻度,搖勻,濾過,分別精密量取續濾液1 ml,置于100 ml量瓶中,加pH6.8磷酸鹽緩沖液稀釋至刻度,搖勻,分別按“2.1”項下色譜條件進樣測定,記錄峰面積并按外標法計算回收率,結果見表1。
2.10 溶出度均一性試驗
取批號20130401的樣品6片,各按“2.2.2”項下方法進行溶出度試驗,分別在5、15、30、45、60 min時取溶出液10 ml(同時補充溶出介質10 ml),濾過,取續濾液適量,按“2.1”項下色譜條件進樣測定,記錄峰面積并按外標法計算他米巴羅汀在各時間點的累積溶出度(詳見表2),并繪制溶出曲線(詳見圖2)。結果,6片樣品溶出曲線趨勢基本相同,在各時間點的累積溶出度的RSD均<2%,表明樣品同一批次內的溶出度均一性良好。

表1 回收率試驗結果(n=9)Tab 1 Results of recovery test(n=9)
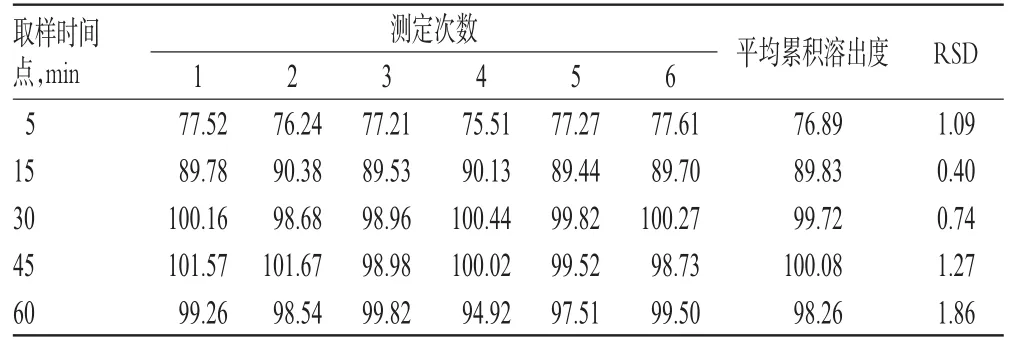
表2 各時間點的累積溶出度測定結果(%)Tab 2 Determination results of cumulative dissolution at each time point(%)
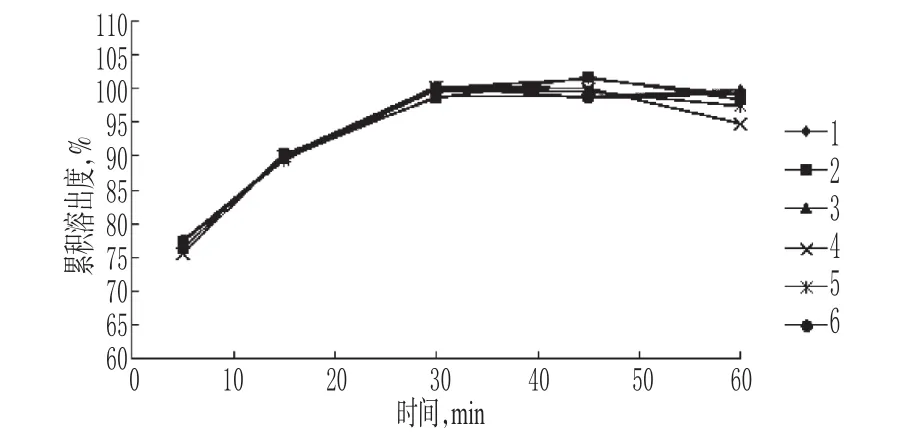
圖2 溶出曲線Fig 2 Dissolution curves
2.11 樣品溶出度測定
取3批樣品各6片,分別按“2.2.2”項下方法制備供試品溶液,再按“2.1”項下色譜條件進樣測定,按外標法以峰面積計算每片的溶出度及平均值(要求均≥標示量的75%),結果見表3。
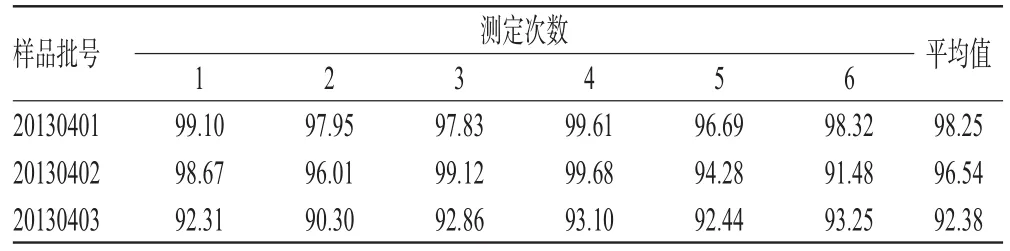
表3 樣品溶出度測定結果(n=6,%)Tab 3 Determination results of dissolution of samples(n= 6,%)
3 討論
3.1 溶出介質體積的選擇
根據《普通口服固體制劑溶出度試驗技術指導原則》[9]的要求,口服固體制劑溶出度測定溶出介質體積一般采用900 ml或1 000 ml,方可符合漏槽條件,并能滿足溶出度測定方法的要求。考慮到樣品規格為2 mg,規格較小,為了提高靈敏度,筆者參考相關文獻[10],選用900 ml作為本試驗溶出介質的體積。
3.2 溶出介質的選擇
口服固體制劑溶出度測定所用溶出介質一般采用水、0.1 mol/L鹽酸溶液(pH1.0)、pH4.5乙酸鹽緩沖液和pH6.8磷酸鹽緩沖液等。本試驗前期曾分別選用以上4種溶出介質進行預試驗(其他試驗條件不變),結果發現,他米巴羅汀在0.1 mol/L鹽酸溶液(pH1.0)和pH4.5乙酸鹽緩沖液介質中60 min時的溶出度均比較低,而在水和pH6.8磷酸鹽緩沖液介質中45~60 min時的溶出度比較高;進一步分析發現在水介質中的溶出曲線未出現拐點,而在pH6.8磷酸鹽緩沖液中溶出曲線有明顯的拐點。故本試驗最終選擇了與文獻[10]方法一致的溶出介質pH6.8磷酸鹽緩沖液。
3.3 轉速的選擇
本試驗前期還對溶出度試驗的轉速進行了考察。通過比較發現以50 r/min作為轉速,溶出速率已較快。在水、pH6.8磷酸鹽緩沖液中5 min時溶出度均>60%,15 min時均>80%,即50 r/min的轉速可以滿足本品溶出度測定要求。
3.4 測定方法的選擇
當他米巴羅汀片溶于900 ml的pH6.8磷酸鹽緩沖液中時,主成分質量濃度約為2.2 μg/ml,值非常低,在紫外條件下的吸收度<0.1,會顯著影響檢測結果的準確性。故本試驗最終選擇了更為靈敏的HPLC法進行測定。
綜上所述,本方法簡便、準確,靈敏度高,專屬性強,適用于他米巴羅汀片的溶出度測定。
[1]劉春燕.急性早幼粒細胞白血病的“克星”:全反式維甲酸[J].開卷有益:求醫問藥,2007(3):10.
[2] Ohnishi K.PML-RARalpha inhibitors(ATRA,tamibaroten,arsenic troxide)for acute promyelocytic leukemia[J]. Int J Clin Oncol,2007,12(5):313.
[3]王杰松,陳志哲.急性早幼粒細胞白血病的治療現狀[J].醫學綜述,2007,13(11):838.
[4]楊立平.他米巴羅汀藥理學研究進展[J].中華臨床醫學雜志,2008,9(7):57.
[5]Takeuchi M.Clinical experience with a new synthetic retinoid,tamibarotene(Am-80)for relapsed or refractory acute promyelocytic leukemia[J].Gan To Kagalcu Ryoho,2006,33(3):401.
[6]Davies SL,Castaner J,Capdevila LG.Tamibarotene[J]. Drugs Future,2005,30(7):688.
[7]賴樹清,須媚.急性早幼粒細胞性白血病治療藥:他米巴羅汀:tamibarotene[J].世界臨床藥物,2007,28(4):252.
[8]國家藥典委員會.中華人民共和國藥典:四部[S].2015年版.北京:中國醫藥科技出版社,2015:121-124.
[9]國家食品藥品監督管理局.普通口服固體制劑溶出度試驗技術指導原則[S].2009.
[10] 東光薬品工業(株).アムノレイク錠2mgに関する資料,新薬の承認に関する情報[EB/OL].(2005-06)[2013-06].http://www.info.pmda.go.jp/shinyaku/P200500 012/left.html.
(編輯:周 箐)
Dissolution Determination of Tamibarotene Tablet by HPLC
CHEN Lijiao1,YANG Dongxia2,ZHAO Yanxia3(1.Shandong Polytechnic College,Shandong Jining 272067,China;2.Shandong Chuangxin Pharmaceutical Research and Development Co.Ltd.,Jinan 250101,China;3.Graduate Education Center,Shandong Academy of Medical Sciences,Jinan 250062,China)
OBJECTIVE:To establish a method for the dissolution determination of Tamibarotene tablet.METHODS:HPLC was performed on the column of Diamonsil C18with mobile phase of methanol-water-acetic acid(85∶15∶1,V/V/V)at a flow rate of 1.0 ml/min,detection wavelength was 235 nm,column temperature was 25℃,and injection volume was 20 μl.The paddle method was used to determine the dissolution,using pH6.8 phosphate buffer dissolution as medium,medium volume was 900 ml,the rotating speed was 50 r/min,taking samples after 60 min.RESULTS:The linear range of tamibarotene was 0.801-2.804 μg/ml(r= 0.999 6);RSDs of precision,stability and reproducibility tests were lower than 3%;recovery was 99.58%-100.90%(RSD= 0.25%,n=9);the accumulative dissolution rate of 3 batches of samples was 98.25%,96.54%,92.38%(n=6).CONCLUSIONS:The method simple,accurate with high sensitivity and specificity,and suitable for the dissolution determination of Tamibarotene tablet.
HPLC;Tamibarotene tablet;Dissolution
R927
A
1001-0408(2016)30-4304-03
2015-12-02
2016-09-17)
*講師,碩士研究生。研究方向:儀器分析。電話:0537-3617622。E-mail:hahachenlijiao@126.com
#通信作者:副研究員,碩士。研究方向:藥物分析。電話:0531-58672115。E-mail:mls_zhaoyx@ujn.edu.cn
DOI 10.6039/j.issn.1001-0408.2016.30.42

