含鈾有機廢液中微量鈾的回收
郭倚天 陳慶德 沈興海 鄒樂西 李英秋
?
含鈾有機廢液中微量鈾的回收
郭倚天1陳慶德1,?沈興海1,?鄒樂西2李英秋2
1. 北京大學化學與分子工程學院, 放射化學與輻射化學重點學科實驗室, 北京分子科學國家實驗室, 北京 100871; 2. 中國工程物理研究院, 綿陽 621900; ? 通信作者, E-mail: qdchen@pku.edu.cn (陳慶德), xshen@pku.edu.cn (沈興海)
針對含微量鈾的有機廢液中鈾難以回收的難題, 選擇 Na2CO3水溶液對有機相中的鈾進行反萃, 得到堿性含鈾水溶液,并應用偕胺肟基吸附材料進行富集。考察了碳酸鹽對有機相中鈾的反萃過程中反萃動力學、碳酸鈉濃度以及相比的影響,探究吸附過程中振蕩速率、吸附材料使用量、溶液中 CO32-濃度等參數的影響,研究了偕胺肟基吸附材料的重復利用性。在此基礎上, 提出了從有機廢液中高效富集與回收微量鈾的 流程。
偕胺肟; 三碳酸鈾酰銨; 吸附; 有機廢液; 反萃
鈾是核工業中重要的核材料, 在鈾材料的使用和研究過程中, 鈾的分離和富集是一項重要工作。國內一些涉核單位在多年鈾材料的分析研究工作中, 積累了大量含鈾和磷酸三丁酯(TBP)的有機廢液。因其鈾含量低且來源和組成比較復雜, 目前還沒有經濟適用的處理技術, 一直處于集中存放等待處理的狀態。此類易燃的有機放射性廢液的大量存放, 給存放地的環境帶來很大的安全隱患。因此, 有必要開展相關研究, 建立相應的流程, 以實現含鈾有機廢液處理、處置的目的。
有機相萃取鈾, 一般采用的反萃劑分為酸類與碳酸鹽類兩種[1–4]。酸類反萃劑在有機相中鈾濃度較高時適用。對于鈾濃度較低的有機相, 通常采用碳酸鹽類反萃劑, 但是往往需要大量的碳酸鹽水溶液來反萃, 得到低濃度的含鈾水溶液。若用酸化處理, 一方面要消耗大量的酸, 導致廢物量增加; 另一方面, 大量酸的加入會進一步降低鈾的濃度, 使其回收過程更加繁瑣。
對于弱堿性水溶液中低濃度鈾的回收, 文獻報道主要集中在海水提鈾方面。海水的 pH 為7.5~8.5,極低濃度的鈾(3.3 μg/L)主要以[UO2(CO3)3]4-形式存在[5]。大量文獻報道偕胺肟基吸附材料能有效地從海水中富集鈾酰離子[6–10], 是一類具有很好應用前景的用于海水提鈾的吸附材料。日本高崎研究所的實驗結果表明 30 天內鈾的平均回收率為 0.5 g/kg, 240 天的海試實驗總計回收 1 kg 黃餅[11]。在碳酸鹽水溶液反萃有機相得到的堿性含鈾稀水溶液中, 鈾主要以[UO2(CO3)2]2-和[UO2(CO3)3]4-形式存在, 與海水中鈾的形態基本一致。雖然反萃水相相對比較簡單, 但 CO32-的濃度更高, 與偕胺肟基競爭配位UO22+的情況更嚴重。因此, 開展偕胺肟基吸附材料回收有機廢液中微量鈾的研究并建立相應的流程很有意義, 可為尋求高效經濟地處理含鈾放射性有機廢液的方法提供理論依據和技術支持。
1 實驗材料與方法
1.1 實驗試劑
硝酸鈾酰(UO2(NO3)2· 6H2O, G.R., Chemapol, 捷克斯洛伐克)、碳酸鈾酰銨((NH4)4[UO2(CO3)3], 根據文獻[12]制備)、碳酸鈉(Na2CO3, A.R., 北京化工廠)、磷酸三丁酯((C4H9O)3PO, A.R., 國藥集團化學試劑北京有限公司)、十二烷(C12H26, A.R., 沃凱化成工業上海有限公司)、硫酸亞鐵銨((NH4)2Fe(SO4)2·6H2O, A.R., 天津市天河化學試劑廠)和鹽酸羥胺(NH2OH·HCl, A.R., 西隴化工股份有限公司)直接使用。丙烯酸(CH2=CHCOOH, A.R.)和丙烯腈(CH2=CHCN, A.R.)購自北京益利精細化學品有限公司, 使用前經減壓蒸餾提純。丙烯酰胺(CH2=CHCONH2, A.R.)購自北京化學試劑公司, 使用前經重結晶提純。聚丙烯(20 目)粉料由北京化工研究院提供, 使用前用丙酮在索氏提取器中抽提 24 小時除去雜質, 真空干燥備用。除特別說明外, 其余試劑均為分析純。實驗用水為超純水。
1.2 實驗儀器
元素分析在元素分析儀Vario EL (Elementar Analysensysteme GmbH, 德國)上測定。電感耦合等離子體原子發射光譜儀(ICP-AES, Leeman, 美國) 用于測量鈾的濃度。鈾的檢測限為0.05 mg/L。
1.3 偕胺肟基吸附材料的制備
偕胺肟基吸附材料的制備經歷預輻射接枝共聚和偕胺肟化兩個過程(如圖 1), 具體過程及表征參見文獻[13-14]。所制備的中間產物聚丙烯-丙烯腈/丙烯酸(PP--AN/AA)和聚丙烯-丙烯腈/丙烯酰胺(PP--AN/AAm)的表征結果如表 1 所示。在最終產物聚丙烯-偕胺肟/丙烯酸(PP--AO/AA)和聚丙烯-偕胺肟/丙烯酰胺(PP--AO/AAm)中, 偕胺肟基的密度分別為2.21和2.55 mmol/g。
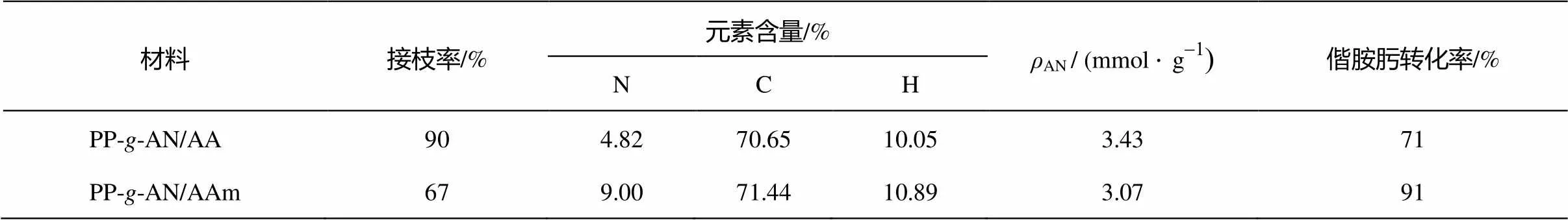
表1 PP-g-AN/AA和PP-g-AN/AAm的表征結果
1.4 碳酸鈉溶液反萃模擬含鈾有機廢液
將一定質量的 UO2(NO3)2·6H2O 溶于 30%的TBP-十二烷溶液中配成模擬含鈾有機廢液, 其中鈾的濃度為5mg/L。控制相比(有機相體積與水相體積之比),將有機相和一定濃度的 Na2CO3溶液加入離心管中, 在恒溫振蕩箱中 25oC 下振蕩。反萃完成后, 經 8000 r/min 離心分相, 取下層水相, 用ICP-AES測定其中鈾的濃度。
鈾的萃取率(%)可用式(1)求得:
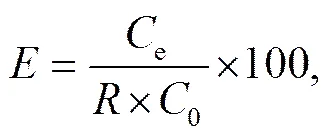
0為有機相中鈾的初始濃度(mg/L);e為萃取完成后水相中鈾的濃度(mg/L);為相比。
1.5 偕胺肟基吸附材料在模擬反萃水相中對鈾的吸附實驗
稱取已知質量的吸附材料, 與一定體積的鈾濃度為 20~120 mg/L 的 NH4[UO2(CO3)3]溶液(Na2CO3濃度為 3 mmol/L 作為穩定劑, 模擬反萃水相)在25oC 進行振蕩吸附。用 ICP-AES 測量吸附后溶液中剩余鈾的濃度。
吸附材料的吸附量(mg/g)可用式(2)計算:
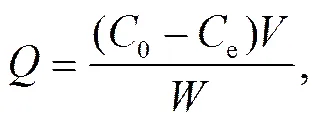
鈾的吸附效率(%)可用式(3)求得:
(3)
其中,0為吸附液的初始鈾濃度(mg/L);e為吸附后上層清液的剩余鈾濃度(mg/L);為吸附液的體積(L);為吸附材料的質量(g)。
2 結果與討論
2.1 反萃動力學
水相對有機相中鈾的反萃效率隨時間的變化如圖 2 所示。可以看出, 振蕩 5 分鐘即可達到 100%的反萃效率, 隨著振蕩時間的增加, 反萃效率略有下降, 1 小時后反萃效率可維持在 91%左右。這有可能是空氣中 CO2影響的緣故。為保證后續實驗的重復性, 反萃平衡時間選擇為1小時。
2.2 碳酸鈉溶液的濃度對反萃的影響
使用Na2CO3溶液對含鈾有機廢液進行反萃后, UO22+會進入堿性水相溶液中, 與水相中的 CO32-形成 UO2(CO3)22-和 UO2(CO3)34-等形式的陰離子配合物。如果溶液中存在的 CO32-濃度較高, 在使用偕胺肟基吸附材料對反萃水相中的鈾進行富集過程中, CO32-勢必會與偕胺肟基競爭配位 UO22+而影響吸附量; 如果水相中的 CO32-濃度太低,則會影響UO22+在溶液中的穩定性, 導致鈾以氫氧化物的形式沉淀下來。因此, 考察碳酸鈉溶液濃度對反萃的影響是很有必要的。
水相對有機相中鈾的反萃效率隨 Na2CO3溶液濃度的變化如圖 3 所示。當 Na2CO3溶液濃度為 0時(即選擇純水對含鈾有機相進行反萃), 反萃效率僅為 40%; 當 Na2CO3溶液濃度在較低范圍(0.1~0.5 mmol/L, 即水相中 Na2CO3與有機相中 UO22+的摩爾比小于 10)時, Na2CO3溶液對 TBP-十二烷溶液中 UO22+反萃效率小于90%; 當 Na2CO3溶液在較高濃度范圍(1~5 mmol/L, 即水相中 Na2CO3與有機相中 UO22+的摩爾比大于20)時, Na2CO3溶液對TBP-十二烷溶液中 UO22+的反萃效率恒定在90%以上。在實驗所用的 Na2CO3濃度范圍內, 并無鈾的氫氧化物沉淀生成, 可能的原因是有機相中鈾濃度為 5 mg/L, 經低濃度 Na2CO3溶液反萃后, 水相中鈾的濃度更低, 不足以沉淀下來。因此, 為保證較高的反萃效率且水相中 CO32-濃度不會影響偕胺肟基吸附材料的吸附性能, 優化反萃實驗條件為相比為 2, 水相中 Na2CO3與有機相中 UO22+的摩爾比大于20。
2.3 相比對反萃的影響
有機廢液中殘余的鈾的濃度很低, 不利于后續環節中使用偕胺肟基吸附材料進行鈾的回收。可以通過小體積的 Na2CO3溶液對大體積的有機相進行反萃, 使得水相中鈾的濃度得到提升。因此, 我們考察相比對反萃的影響。
水相對有機相中鈾的反萃效率隨相比的變化如圖 4 所示。隨著相比由 2 增加到 8,Na2CO3溶液對TBP-十二烷溶液中 UO22+的反萃效率恒定在 90%左右, 這就說明當相比為 8 時, 經 Na2CO3溶液反萃即可將有機相中低濃度的鈾富集 7 倍以上。因此, 對有機廢液中微量鈾的回收流程可選擇合適的反萃相比, 將鈾進行反萃濃縮, 更有利于實現偕胺肟基吸附材料回收水相中鈾的目標。
2.4 多級萃取
為了進一步降低有機廢液中鈾的含量, 控制相比為8, 有機相鈾濃度為5 mg/L, Na2CO3濃度為16 mmol/L, 進行三級反萃實驗。結果發現, 通過兩級反萃, 有機相中 99%以上的鈾進入 Na2CO3溶液中;第三級反萃時,水相中鈾的濃度已經低于儀器檢測限。因此,含鈾有機廢液經 Na2CO3溶液兩級反萃后,有機相中鈾濃度低于0.05 mg/L, 即可用常規方法進行處理。
2.5 振蕩速率對吸附過程的影響
振蕩速率對偕胺肟基吸附材料吸附性能的影響如圖 5 所示, 由于吸附屬于一種傳質過程, 如果振蕩速率為 0 (即靜態吸附), 則不利于 UO22+向吸附材料表面擴散; 而振蕩速率的快慢不會影響吸附材料的吸附性能。因此, 在保證同樣的吸附平衡時間的條件下, 可以選擇低振蕩速率進行吸附實驗。
2.6 吸附動力學及吸附容量
圖6為時間對偕胺肟基吸附材料吸附模擬反萃水相中鈾的影響。可以看出, 吸附材料的吸附量先隨時間增大, 之后上升緩慢, 逐漸達到平衡。對于PP--AO/AA吸附材料, 12小時逐漸達到吸附平衡; 對于PP--AO/AAm吸附材料, 8小時逐漸達到吸附平衡。為了便于對比, 后續的吸附實驗的平衡吸附時間均為12小時。
圖 7 為鈾的初始濃度對偕胺肟基吸附材料吸附容量的影響。可以看出, 在研究濃度范圍內, 吸附材料的吸附量隨濃度0的增大而升高, 逐漸達到一個平臺, 即達到飽和吸附。PP--AO/AA 和PP--AO/AAm 這兩種吸附材料在模擬反萃水相中對鈾的最大吸附容量分別為18.74和4.89 mg/g。
2.7 碳酸鈉溶液的濃度對吸附的影響
因為回收有機廢液中的微量鈾需用 Na2CO3溶液進行反萃, 所以考察水相中 CO32-濃度對偕胺肟基吸附材料吸附效果的影響是非常必要的。借此可以找到用于反萃含鈾有機廢液的 Na2CO3溶液合適的濃度范圍, 并為吸附材料的選擇提供依據。圖 8為 Na2CO3溶液濃度的改變對吸附材料在模擬反萃水相中對鈾吸附性能的影響。可以看出, 盡管 PP--AO/AA 吸附材料對鈾的吸附性能比 PP--AO/ AAm吸附材料好很多, 但是隨著溶液中CO32-濃度上升, 大量 CO32-會抑制羧基與 UO22+的配位, 使其對鈾的吸附效率迅速下降。當[CO32-] = 9 mmol/L時, PP--AO/AA 吸附材料的吸附效率下降了 95%; 隨著 CO32-濃度繼續增大,該材料不再吸附鈾。而對于 PP--AO/AAm 吸附材料, 在實驗研究的CO32-濃度范圍內對鈾的吸附效率穩定在25 %左右。因此, PP--AO/AAm吸附材料更適用于在更寬的CO32-濃度范圍內對鈾進行回收。
結合反萃部分實驗數據, 最終確定吸附實驗條件: 若反萃環節控制水相中 Na2CO3與有機相中UO22+的摩爾比大于 30, 可選用 PP--AO/AAm 吸附材料對水相中的鈾進行富集; 如果反萃環節控制水相中 Na2CO3與有機相中的摩爾比在 20~ 30, 吸附環節選用 PP--AO/AA 吸附材料富集水相中的鈾亦可達到較好效果。
2.8 吸附材料使用量對吸附的影響
由于水相中 CO32-與 UO22+的摩爾比在10~90范圍內,PP--AO/AAm 吸附材料對 UO22+的吸附效率穩定在25%左右,可通過增加其使用量來達到 90%以上鈾的吸附效率。作為對照, 我們還考察了 PP--AO/AA 吸附材料用量對吸附效率的影響。圖 9為不同質量的吸附材料在模擬反萃水相中對鈾的吸附效率及吸附量的變化。可以看出, 增大這兩種吸附材料的質量, 在模擬反萃水相中對鈾的吸附效率逐漸上升, 而吸附量逐漸下降。對于 PP--AO/AAm吸附材料, 當吸附材料質量與模擬反萃水相體積之比大于 12 時, 對鈾的吸附效率可達 90%以上; 對于 PP--AO/AA 吸附材料, 隨著吸附材料的使用量增加, 羧酸根的存在導致水相出現鈾水解產生的沉淀(溶液中無緩沖溶液穩定碳酸鈾酰)。因此, 在反萃水相中鈾的回收環節應選擇 PP--AO/AAm 吸附材料, 控制吸附材料質量與水相之比大于 12, 可達到90%以上的吸附效率。
2.9 吸附材料重復利用性
對于 200 mg PP--AO/AAm 吸附材料, 在 10 mL模擬反萃水相中吸附UO22+后, 用1 mL濃度為1 mol/L 的 HCl 溶液經過 2 小時浸泡, 可以洗脫85%左右的 UO22+, 富集因子為 13.6±0.3。將洗脫后的吸附材料用NaHCO3溶液浸泡至中性, 洗凈干燥后繼續用于從模擬反萃水相中吸附 UO22+, 在吸附與解吸循環中考察 PP--AO/AAm 吸附材料的重復利用性。
圖 10 描述 PP--AO/AAm吸附材料在 5 次循環使用中對鈾的吸附效率和洗脫效率。在5次循環使用后, PP--AO/AAm吸附材料對鈾的吸附效率保持在 90%以上, 并略有增大。這可能是由部分酰胺基團在 1 mol/L 的 HCl 溶液中發生水解造成, 但洗脫效率始終保持在 80%左右。結果表明, PP--AO/AAm吸附材料有較好的重復利用性。
基于以上實驗數據, 設計含鈾有機廢液中微量鈾的富集與回收流程(圖11)。
3 結論
本文設計了含鈾有機廢液中微量鈾的富集與回收流程, 并初步優化了相關實驗參數。
1) 使用 Na2CO3溶液對含鈾有機廢液中微量鈾進行反萃, 控制相比為 8, 水相中 Na2CO3與有機相中 UO22+的摩爾比大于 20, 可在保證水相不出現鈾氫氧化物沉淀的前提下達到 90%以上的反萃效率, 并將有機相中 5 mg/L 的鈾富集至 37 mg/L 左右, 且水相中 CO32-濃度幾乎不影響后續 PP--AO/ AAm對鈾的回收。經過 Na2CO3溶液的兩級萃取可進一步將鈾的反萃效率提高到99%。
2) 篩選出PP--AO/AAm吸附材料用于模擬反萃水相中的鈾的富集。當PP--AO/AAm吸附材料的質量與反萃水相體積比大于12時, 振蕩8小時即可達到90%以上的鈾的吸附效率。含殘余鈾的吸附母液中仍含有大量CO32-,可作為反萃水相循環使用。由于偕胺肟基吸附材料吸附鈾達到平衡的時間較長, 不利于生產實踐操作。可以考慮制備以偕胺肟基改性的填料或者研制新型用于預富集鈾的吸附材料, 開展柱層析分離和富集, 以期取得更快、更好的分離效果。
3) PP--AO/AAm 吸附材料在濃度為 1 mol/L的HCl溶液中浸泡2小時, 可以達到80%的洗脫效率, 富集因子為 13.6±0.3, 經 NaHCO3處理后可以循環使用。
參考文獻
[1]Li C B, Zuo C, Yan T H, et al. Study on the technology of U-Pu Co-stripping process for reproce-ssing spent fuel of fast reactor. Radiochim Acta, 2014, 102(12): 1075–1081
[2]Wei M, Liu X G, Chen J. Agents and processes design for transuranium elements back extraction in TRPO process. J Radioanal Nucl Chem, 2012, 291(3): 717–723
[3]Birkett J E, Carrott M J, Fox O D, et al. Recent developments in the purex process for nuclear fuel reprocessing: complexant based stripping for uranium/ plutonium separation. Chimia, 2005, 59(12): 898–904
[4]郭一飛, 焦榮洲, 梁俊福, 等. TRPO流程中U的反萃Ⅰ. 反萃劑的選擇. 核化學與放射化學, 1999, 22(1): 22–28
[5]Annual Report 2011 [R]. International Atomic Energy Agency: Vienna, 2012
[6]Egawa H, Nakayama M, Nonaka T, et al. Recovery of uranium from seawater 5. preparation and properties of the macroreticular chelating resins containing amidoxime and other functional-groups. J Appl Polym Sci, 1987, 34(4): 1557–1575
[7]Kawai T, Saito K, Sugita K, et al. Comparison of amidoxime adsorbents prepared by cografting metha-crylic acid and 2-hydroxyethyl methacrylate with acrylonitrile onto polyethylene. Ind Eng Chem Res, 2000, 39(8): 2910–2915
[8]Rao L. Recent international R&D activities in the extraction of uranium from seawater [R]. Lawrence Berkeley National Laboratory. Berkeley, CA, 2011
[9]Kim J, Tsouris C, Mayes R T, et al. Recovery of Uranium from Seawater: a review of current status and future research needs. Sep Sci Technol, 2013, 48(3): 367–387
[10]Yue Y F, Mayes R T, Kim J, et al. Seawater uranium sorbents: preparation from a mesoporous copolymer initiator by atom-transfer radical polymerization. Angew Chem-Int Edit, 2013, 52(50): 13458–13462
[11]饒林峰. 輻射接枝技術的應用: 日本海水提鈾研究的進展及現狀. 同位素, 2012, 25(3): 129–139
[12]吳克明. 碳酸鈾酰銨的溶解度. 原子能科學技術, 1961, 3(3): 148–156
[13]Kabay N, Katakai A, Sugo T, et al. Preparation of fibrous adsorbents containing amidoxime groups by radiation-induced grafting and application to uranium recovery from sea-water. J Appl Polym Sci, 1993, 49(4): 599–607
[14]Lin W P, Lu Y, Zeng H M. Studies of the preparation, structure, and properties of an acrylic chelating fiber containing amidoxime groups. J Appl Polym Sci, 1993, 47(1): 45–52
Recovery of Trace Uranium in Organic Waste Liquid
GUO Yitian1, CHEN Qingde1,?, SHEN Xinghai1,?, ZOU Lexi2, LI Yingqiu2
1. Beijing National Laboratory for Molecular Sciences (BNLMS), Fundamental Science on Radiochemistry and Radiation Chemistry Laboratory, College of Chemistry and Molecular Engineering, Peking University, Beijing 100871; 2. China Academy of Engineering Physics, Mianyang 621900; ? Corresponding authors, E-mail: qdchen@pku.edu.cn (CHEN Qingde); xshen@pku.edu.cn (SHEN Xinghai)
Considering the difficulty to recover trace uranium in organic phase, Na2CO3aqueous solution was used to strip uranium, then the amidoxime adsorbents were chosen to enrich uranyl in the aqueous phase. In the stripping part, the kinetics of stripping, the effects of the concentration of Na2CO3and phase ratio on the stripping efficiency were investigated. Then, in the adsorption part, the effects of shaking rate, the mass of adsorbents and the concentration of Na2CO3were studied. After the validation of the recyclable performance of the amidoxime adsorbents, a process for recovering trace uranium in organic waste liquid was proposed.
amidoxime; (NH4)4[UO2(CO3)3]; adsorption; organic waste liquid; stripping
10.13209/j.0479-8023.2016.117
O69
國家自然科學基金(91226112, 20871009)資助
2015-05-25;
2015-06-11;
網絡出版日期: 2016-11-07

