老年男性糖代謝異常患者骨代謝標志物探析
郭南京 李 津 陳慶福 朱雨霏
老年男性糖代謝異常患者骨代謝標志物探析
郭南京 李 津 陳慶福 朱雨霏
目的 通過對我科住院的120例老年男性糖代謝異常患者骨代謝標志物水平的檢測,分析探討此類患者骨代謝標志物的變化。方法收集2013年1月~2016年6月我科收治的年齡≥60歲男性2型糖尿病和糖調節(jié)受損患者各60例,另選取60例年齡≥60歲男性糖代謝正常者作為對照組,分別檢測β-膠原特殊系列(CTX)、骨鈣素(BGP)、總I型膠原氨基端延長肽(TPINP)、全段甲狀腺旁腺激素(IPT)、25-羥基維生素D3[25-(OH)VD3]、硫酸去氫表雄酮(DHS)、睪酮(TSTO)、血鈣(Ca)、血磷(P)、血堿性磷酸酶(ALP)的濃度。結果 三組之間血鈣、磷、堿性磷酸酶、DHS及TSTO含量的差異無統(tǒng)計學意義。與對照組相比,糖代謝異常組患者的CTX、BGP、TPINP、IPT及25-(OH)VD3含量均降低(P<0.05)。結論 測定血清中的CTX、BGP、TPINP、IPT及25-(OH)VD3可在一定程度上了解老年男性糖代謝異常患者體內骨代謝情況,有利于對骨質疏松癥的早期防治提供理論依據。
老年男性;2型糖尿病;糖調節(jié)受損;骨代謝標志物
隨著社會的進步、人類生活水平的提高,人類壽命逐漸延長,我國已經步入老齡化社會,是世界上60歲以上老齡人口數量最多的國家,多達1.73億。老年性骨質疏松癥嚴重威脅老年人身心健康,已逐漸成為突出的社會公共衛(wèi)生問題[1]。骨質疏松癥(OP,Osteoporosis)是一種以骨量減少、骨微結構破壞為病理特征的全身性、代謝性骨骼系統(tǒng)疾病,導致骨脆性增加,骨強度下降,極易發(fā)生骨折。流行病學顯示,我國50歲以上人群中骨質疏松癥男女患病率分別為14.4%和20.7%[1]。骨折是骨質疏松癥最嚴重的后果,老年男性骨質疏松癥患者更易發(fā)生骨折,其死亡率及致殘率高于女性。糖尿病是一種慢性代謝性疾病,由于高血糖、胰島素抵抗、胰島素樣生長因子缺乏及糖尿病慢性并發(fā)癥等多種因素的作用,糖尿病人群并發(fā)骨質疏松癥的發(fā)病率高于普通人群,骨折危險性也升高[2-3]。骨代謝標志物能夠早期反映骨代謝改變,及時反映骨轉換率,可應用于預測骨折風險、評價骨代謝狀態(tài)及抗骨質疏松質量療效評價等。但老年男性糖代謝異常與骨代謝標志物的關系,尚不明確。為研究老年男性糖代謝異常患者骨代謝標志物的變化,筆者對2型糖尿病、糖調節(jié)受損及糖代謝正常的老年男性患者進行比較研究,探索此類患者骨代謝標志物的改變,為臨床防治老年男性糖代謝異常患者骨質疏松提供理論依據。
1 研究對象與方法
1.1研究對象
選取2013年1月~2016年6月在我院保健病房住院的年齡≥60歲男性糖代謝異常患者,其中2型糖尿病60例(DM組),年齡60~94歲,平均(81.42±8.26)歲;糖調節(jié)受損(IGR,Impaired Glucose Regulation)60例(IGR組),年齡61~95歲,平均(83.52±8.48)歲,另選取同年齡段老年男性糖代謝正常者60例作為對照組,年齡60~95歲,平均(83.7±7.18)歲。糖代謝異常診斷參照世界衛(wèi)生組織(WHO)1999年標準:空腹血糖≥7.0 mmol/L或口服葡萄糖耐量試驗(OGTT)2 h血糖≥11.1 mmol/L,診斷為糖尿病;空腹血糖6.1~7.0 mmol/L為空腹血糖受損(IFG,Impaired Fasting Glucose);OGTT 2 h血糖7.8~11.1 mmol/L為糖耐量減低(IGT,Impaired Glucose Tolerance)。后兩者統(tǒng)稱為糖調節(jié)受損。
排除標準:(1)1型糖尿病及其他特殊類型糖尿病;(2)甲亢、甲減及甲旁亢等內分泌代謝性疾病;(3)風濕、類風濕等結締組織病;(4)6個月內有骨折、成骨不全、骨髓纖維化、骨腫瘤、多發(fā)性骨髓瘤等;(5)嚴重肝腎功能衰竭、胃腸道切除術、營養(yǎng)不良及其它惡性腫瘤患者;(6)6個月內使用甲狀腺激素、糖皮質激素、降鈣素、維生素D類似物、鈣劑及抗癲癇藥物等影響骨代謝水平的藥物。
1.2方法
所有受試者均于清晨空腹8 h后抽取靜脈血,利用雅培Aeroset全自動生化分析儀測定生化指標血鈣(Ca)、血磷(P)、血堿性磷酸酶(ALP)水平。應用羅氏Cobase e 601電化學發(fā)光全自動免疫分析系統(tǒng)測定β-膠原特殊系列(CTX)、骨鈣素(BGP)、總1型膠原氨基端延長肽(TPINP)、全段甲狀腺旁腺激素(IPT)、25-羥基維生素D3[25-(OH)VD3]、硫酸去氫表雄酮(DHS)、睪酮(TSTO)水平。
1.3統(tǒng)計學方法
2 結果
2.1年齡及生化指標
三組之間年齡、血鈣、磷及堿性磷酸酶水平差異均無統(tǒng)計學意義。見表1。
2.2骨代謝標志物
2型糖尿病及糖調節(jié)受損組患者的CTX、BGP、TPINP、IPT及25-(OH)VD3含量均低于對照組(P<0.05);而DHS和TSTO水平高于對照組,但差異無統(tǒng)計學意義(P>0.05)。見表2。
3 討論
骨質疏松癥是一種以骨量低下,骨微結構破壞,骨脆性增加,導致易發(fā)生骨折為特征的全身性骨病。骨質疏松性骨折是骨質疏松癥最嚴重的后果,導致病殘率和死亡率的增加。雙能X線吸收骨密度儀(DEXA,Dual Energy X Ray Absorptiometry)檢測骨礦密度(BMD,Bone Mass Density)被認為是診斷OP的金標準[1],但骨礦密度并不能全面反映骨強度,一方面檢測部位骨質增生、硬化或異位骨化等可能導致測量結果產生偏差,另一方面骨微結構損傷蓄積、骨代謝改變及骨基質等變化能夠導致骨強度下降,從而發(fā)生OP[4]。再者,骨密度需要相對長時間改變,大量骨丟失時才能檢測到變化,而骨代謝指標能夠更加敏感反映骨代謝動態(tài)變化水平。因此,檢測血清骨代謝標志物能夠在一定程度上早期預測骨強度及OP。本研究選擇老年男性2型糖尿病和糖調節(jié)受損人群,結果表明糖代謝異常組骨代謝指標CTX、BGP、TPINP、 IPT及25-(OH)VD3 較糖代謝正常組降低。
大量研究顯示,1型糖尿病患者骨密度下降和骨折風險性增加,相關機制相對明確[5-6],而2型糖尿病的骨密度變化仍存在爭議,但大多數研究認為2型糖尿病患者的骨密度無變化或增加,并且骨折風險同樣是增高的[2,6]。一般認為2型糖尿病骨折風險性增加可能與其并發(fā)癥如神經病變、視網膜病變、血管病變、低血糖或體位性低血壓等引起的跌倒相關,或者與其服用藥物如噻唑烷二酮類有關,但前者已被證實兩者無因果關系[7]。骨代謝或骨轉換是機體成骨細胞生成新骨和破骨細胞對舊骨進行吸收的過程,通常情況下,骨形成和骨吸收隨時間變化而改變,兩者形成動態(tài)平衡,維持骨的相對穩(wěn)態(tài)[8]。在平衡被打破情況下,骨形成不足或骨吸收大于骨形成時,則導致骨質疏松的發(fā)生。吳少英等[9]測定了50例老年男性2型糖尿病合并骨質疏松患者的骨代謝指標,結果顯示相對于對照組,觀察組患者甲狀旁腺激素和尿中脫氧吡啶啉的濃度升高,血清骨鈣素含量降低,提示觀察組患者骨形成能力降低,骨吸收功能亢進。馮纓纓等[10]同樣觀察老年男性2型糖尿病合并骨質疏松患者骨形成和骨吸收生化指標,顯示OP組的骨形成指標(BAP、BGP、PINP)含量低于非OP組,而骨吸收指標(CTX)水平高于非OP組。闞全娥等[11]觀察了116例絕經后2型糖尿病患者的骨代謝標志物,結果顯示骨質疏松組較骨量正常組骨鈣素及TPINP水平降低,CTX升高。而本研究顯示,2型糖尿病及糖調節(jié)受損組的CTX、BGP、TPINP、IPT及25-(OH)VD3含量均低于對照組(P<0.05),與其他國內外研究相一致[12-13],提示糖代謝異常患者的骨轉換能力低下或受抑制。雖然骨轉換能力降低能夠減少骨量丟失,但是同時也使得骨結構微損傷不能得到及時修復,導致骨質量下降和骨折風險性增加[12]。
綜上所述,本研究表明老年男性糖代謝異常患者骨轉換能力低下,可能導致其骨質量下降和骨折風險增加,通過檢測血清中CTX、BGP、TPINP、IPT及25-(OH)VD3的含量,可在一定程度上了解其體內骨代謝情況,有利于對骨質疏松癥的早期診治提供理論依據。
表1 三組之間年齡及生化指標比較()
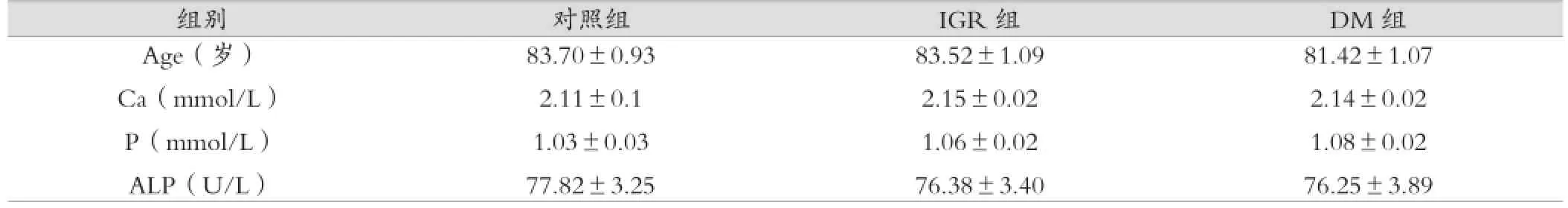
表1 三組之間年齡及生化指標比較()
組別 對照組 IGR組 DM組Age(歲)Ca(mmol/L)P(mmol/L)ALP(U/L)83.70±0.93 2.11±0.1 1.03±0.03 77.82±3.25 83.52±1.09 2.15±0.02 1.06±0.02 76.38±3.40 81.42±1.07 2.14±0.02 1.08±0.02 76.25±3.89
表2 三組之間骨代謝標志物比較()
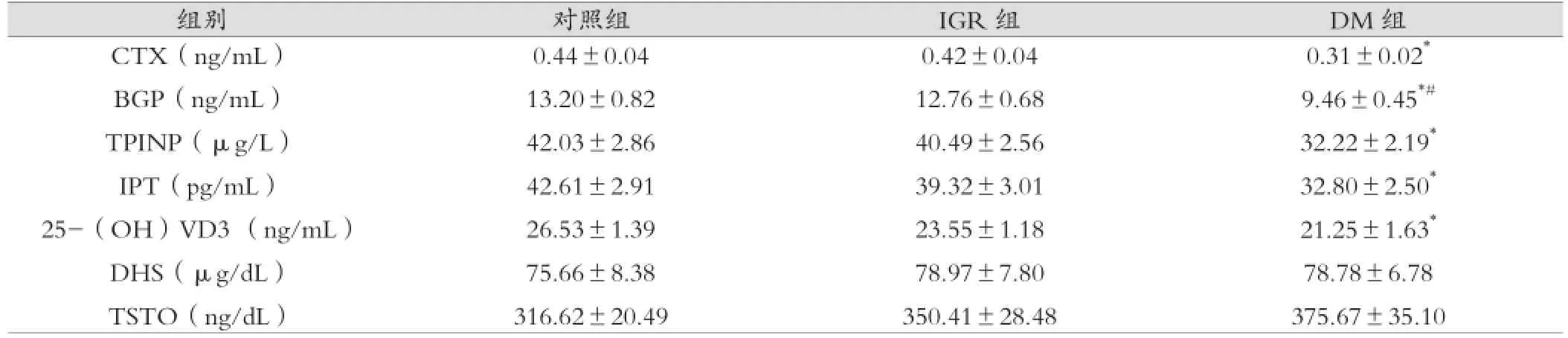
表2 三組之間骨代謝標志物比較()
注:*與對照組比較P<0.05;#與IGR組比較P<0.05
0.31±0.02*9.46±0.45*#32.22±2.19*32.80±2.50*21.25±1.63*78.78±6.78 375.67±35.10組別 對照組 IGR組 DM組CTX(ng/mL)BGP(ng/mL)TPINP(μg/L)IPT(pg/mL)25-(OH)VD3 (ng/mL)DHS(μg/dL)TSTO(ng/dL)0.44±0.04 13.20±0.82 42.03±2.86 42.61±2.91 26.53±1.39 75.66±8.38 316.62±20.49 0.42±0.04 12.76±0.68 40.49±2.56 39.32±3.01 23.55±1.18 78.97±7.80 350.41±28.48
[1] 中華醫(yī)學會骨質疏松和骨礦鹽疾病分會. 原發(fā)性骨質疏松癥診治指南(2011年)[J]. 中華骨質疏松和骨礦鹽疾病雜志,2011,4(1): 2-17.
[2] Lipscombe LL,Jamal SA,Booth GL,et al. The risk of hip fractures in older individuals with diabetes: a population-based study[J]. Diabetes Care,2007,30(4): 835-841.
[3] 胡玲萍,吳雪華. 老年男性2型糖尿病并發(fā)骨質疏松相關危險因素研究現狀[J]. 中國臨床保健雜志,2014,17(1): 107-109.
[4] 陳偉,張紅梅,張靜,等. 骨質疏松癥骨生化指標檢測分析[J].醫(yī)學綜述,2016,22(14): 2846-2848,2852.
[5] Hough FS,Pierroz DD,Cooper C,et al. MECHANISMS IN ENDOCRINOLOGY: Mechanisms and evaluation of bone fragility in type 1 diabetes mellitus[J]. Eur J Endocrinol,2016,174(4): R127-R138.
[6] Vestergaard P. Discrepancies in bone mineral density and fracture risk in patients with type 1 and type 2 diabetes--a meta-analysis[J]. Osteoporos Int,2007,18(4): 427-444.
[7] Shu A,Yin MT,Stein E,et al. Bone structure and turnover in type 2 diabetes mellitus[J]. Osteoporos Int,2012,23(2):635-641.
[8] Ljunggren O,Bolinder J,Johansson L,et al. Dapagliflozin has no effect on markers of bone formation and resorption or bone mineral density in patients with inadequately controlled type 2 diabetes mellitus on metformin[J]. Diabetes Obes Metab,2012,14(11):990-999.
[9] 吳少英,張銘,李瑋,等. 老年男性2型糖尿病合并骨質疏松患者骨代謝生化指標探析[J]. 臨床合理用藥雜志,2015,8(20): 7-8.
[10] 馮纓纓,鐘遠,金俊. 老年男性2型糖尿病合并骨質疏松癥患者骨代謝生化指標分析[J]. 實用老年醫(yī)學,2011,25(6):510-512.
[11] 闞全娥,楊慧慧. 絕經后2型糖尿病患者骨密度與骨代謝標志物的相關分析[J]. 中華老年醫(yī)學雜志,2013,32(11):1206-1208.
[12] Jiajue R,Jiang Y,Wang O,et al. Suppressed bone turnover was associated with increased osteoporotic fracture risks in non-obese postmenopausal Chinese women with type 2 diabetes mellitus[J]. Osteoporos Int,2014,25(8): 1999-2005.
[13] Yamamoto M,Yamaguchi T,Nawata K,et al. Decreased PTH levels accompanied by low bone formation are associated with vertebral fractures in postmenopausal women with type 2 diabetes[J]. J Clin Endocrinol Metab,2012,97(4): 1277-1284.
Bone Turnover Markers of the Aged Male Patients With Abnormal Glucose Metabolism
GUO Nanjing LI Jin CHEN Qingfu ZHU Yufei Department of Cadre Sanitarian,First Affiliated Hospital of Xiamen University,Xiamen Fujian 361003,China
Objective To investigate the bone turnover markers of 120 aged male patients with abnormal glucose metabolism,who were hospitalized in our department. Methods Sixty cases of aged male patients with type 2 diabetes mellitus and impaired glucose regulation were selected as observation group,and 60 cases of aged male patients with normal glucose metabolism were selected as control group in our department from January 2013 to June 2016. Serum bone turnover makers such as type I collagen carboxy-terminal peptide(CTX),bone glaprotein(BGP),total type I collagen amino-terminal extension of peptides(TPINP),intact parathyroid hormone(IPT),25-hydroxyvitamin D3[25-(OH)VD3],dehydroepiandrosterone sulfate(DHS),testosterone (TSTO),blood calcium(Ca),phosphorus(P)and blood alkaline phosphatase(ALP)were measured.Results There were no significant differences in calcium,phosphorus,ALP,DHS and TSTO among the three groups. The levels of serum CTX,BGP,TPINP and 25-(OH)VD3 in observation groups were lower than those in control group(P<0.05). Conclusion The determination of serum CTX,BGP,TPINP,IPT and 25-(OH)VD3 may contribute to understand the bone metabolism contion of patients with abnormal glucose metabolism,and it can be regarded as the prevention and treatment index of osteoporosis.
Aged men,Type 2 diabetes mellitus,Impaired glucose regulation,Bone turnover markers
R587
A
1674-9316(2016)21-0019-03
10.3969/j.issn.1674-9316.2016.21.012
福建省衛(wèi)生廳青年科研課題(編號:2013-2-87)
廈門大學附屬第一醫(yī)院保健病房,福建 廈門 361003
郭南京,E-mail:drnjguo@126.com

