轉谷氨酰胺酶及其在魚糜制品加工中的應用
張夢玲,張晉,熊善柏,趙思明,劉茹,*
(1.華中農業大學食品科技學院,湖北武漢430070;2.國家大宗淡水魚加工技術研發分中心,湖北武漢430070)
轉谷氨酰胺酶及其在魚糜制品加工中的應用
張夢玲1,2,張晉1,2,熊善柏1,2,趙思明1,2,劉茹1,2,*
(1.華中農業大學食品科技學院,湖北武漢430070;2.國家大宗淡水魚加工技術研發分中心,湖北武漢430070)
通過比較分析魚內源性轉谷氨酰胺酶(Fish endogenous transglutaminase,FTGase)和微生物來源的轉谷氨酰胺酶(Microbial transglutaminase,MTGase)的性質和作用機理的異同。在此基礎上探討影響轉谷氨酰胺酶(Transglutaminase,TGase)作用的因素(熱處理方式、酶活促進劑、酶活抑制劑)及在魚糜制品加工中的應用(改善凝膠特性、提高營養價值、提高持水性),并對TGase在今后的研究方向進行了展望,以期為TGase在魚糜制品加工中的開發利用提供參考。
轉谷氨酰胺酶;魚糜;凝膠;影響因素;應用
轉谷氨酰胺酶(Transglutaminase,TGase)可催化酰基轉移反應,促進蛋白質分子間或分子內的共價交聯[1],提高蛋白質熱穩定性[2]及膠凝性質[3]。早在20世紀50年代,就有學者從動物組織中提取分離出TGase,1989年日本味之素公司將動物性來源的TGase投放市場,1992年Ando發現鏈霉菌屬中的其他一些菌株也能產生TGase,并對發酵過程進行了優化,使得該酶的產量有了大幅度提高,從而為食品工業利用此酶創造了條件。
魚糜凝膠性能是衡量其品質的一個重要指標,為改善其凝膠性能,常添加磷酸鹽、非肌肉蛋白、淀粉、親水膠體等。然而磷酸鹽過量攝入會降低鈣的吸收,導致人體骨骼組織中鈣的流失[4]。非肌肉蛋白中,谷朊粉會使凝膠變得硬而脆,降低凝膠彈性[5];大豆分離蛋白易導致魚糜制品白度下降而偏黃[6]。添加淀粉的魚糜制品在常溫下較黏,冷藏后變得又硬又脆,缺乏柔韌感[7];黃原膠雖能提高魚糜嫩度和白度,但不能改善凝膠特性;結冷膠易與高價金屬離子結合,導致魚糜顏色偏暗[8];當pH值小于7.0,魔芋膠需要與碳酸鈉、氫氧化鈉、碳酸鉀、氫氧化鉀等聯合使用,否則不能發生脫乙酰基反應,不利于凝膠的形成[9]。而TGase能改善上述添加物在魚糜制品加工中的局限,以其獨特的優勢在魚糜制品中應用的越來越廣泛。
1 魚糜制品加工中常見TGase的種類和性質
魚內源性轉谷氨酰胺酶(Fish endogenous transglutaminase,FTGase)和微生物來源的轉谷氨酰胺酶(MTGase)是魚糜制品加工中常見的兩種TGase,其來源不同,性質存在很大的差異。FTGase普遍存在于魚的肝臟、肌肉、魚卵等中(見表1)。其分子量一般在66 kDa~95 kDa,活性中心均包含一個Cys-His-Asp或者Cys-His-Asn的三分子序列[10]。在酰胺轉移反應過程中,FTGase活性中心的半胱氨酸的硫醇與谷氨酸殘基形成硫代硫酯中間體,然后酰胺基團轉移到賴氨酸殘基上[11]。具有催化活性的半胱氨酸位于兩個色氨酸橋接形成的疏水性通道中,谷氨酸從疏水性通道的一端接近活性半胱氨酸,賴氨酸從另一端靠近催化活性半胱氨酸并形成穩定的反應四面體,保持在疏水性通道中形成異肽交聯鍵[12]。隨著ε-(γ-Gln)-Lys異肽交聯鍵的形成,疏水性通道打開形成一個連續性的凹槽以釋放形成的產物[13]。FTGase在未被激活狀態下,“色氨酸橋”阻止反應底物進入疏水性通道,當與Ca2+綁定后,發生形變,結構顯著擴展[14-15],打開控制底物與活性中心接觸的兩個疏水性色氨酸殘基,其活力才能被激活[16],故FTGase需要Ca2+激活。另外,FTGase含量少,提純工藝復雜,生產成本高,因此很少提純后用于工業生產,主要通過調節工藝條件激活FTGase來提高魚糜的凝膠性能[17]。
MTGase為球狀單體蛋白,分子量為23kDa~45kDa,多數為40 kDa左右,約為FTGase的一半。其二級結構含22%α-螺旋和33.1%β-折疊,存在兩個糖基化位點(-Thr-Xxx-Asn-),具有高度的親水性,在蛋白質分子的邊緣有一個很深的裂縫,酶活中心的Cys殘基位于裂縫的底部。這種位置安排即使沒有Ca2+條件下,MTGase也可充分接觸溶劑,催化底物快速反應[28-29]。TGase作用的良好底物如肌漿蛋白易被Ca2+沉淀,MTGase不需要Ca2+激活的特性使其在食品加工中具有更顯著的優勢[30]。并且MTGase屬于胞外酶,易于分離純化,還具有較高的熱穩定性和抗凍能力,40℃處理10min后活性無顯著性變化,即使在50℃處理10min后仍有74%的殘余酶活性[29];在-20℃下保存數月酶活僅損失10%,并且經過純化處理后穩定性更強,其適宜的pH值為6.0~7.0[30]。與FTGase相比,MTGase底物特異性低,對Ca2+無依賴性,催化活力、親水性和熱穩定性都較強,pH范圍廣[29],且其來源廣、生產成本低[31],這些性質決定了MTGase在食品工業中的廣泛應用,目前MTGase主要來源于輪枝鏈霉菌[28]。
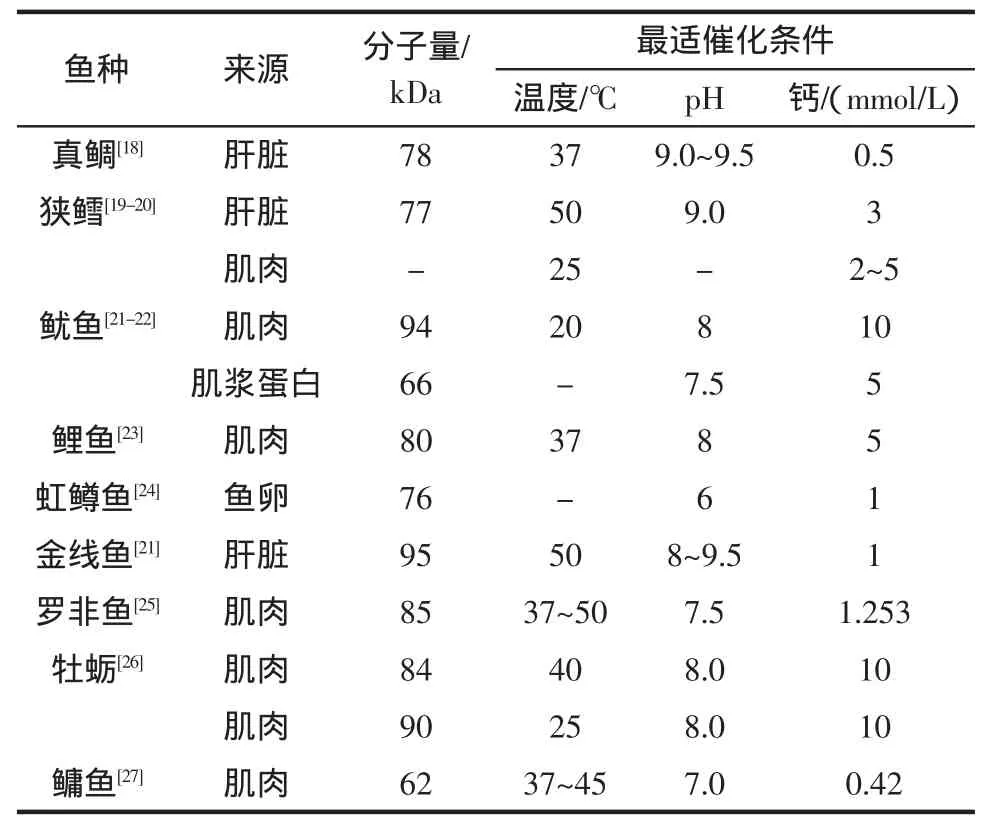
表1 不同魚種來源的的轉谷氨酸酰胺酶的性能Table1 TGase properties from different fish species
2 TGase作用機理
TGase是一種轉酰胺酶,在催化反應中肽鏈上谷氨酰殘基的γ-酰氨基是酰基供體,而酰基受體可以為賴氨酸的ε-氨基、伯胺和水3類(見表2),據此可將反應歸為3類:(1)蛋白質交聯反應。當底物中存在Lys殘基時,TGase催化Gln殘基的γ-羧酰胺基與Lys殘基的ε-氨基反應,生成ε-(γ-Gln)-Lys異型肽鍵,使蛋白質發生分子內或分子間交聯反應,改善魚糜制品的凝膠強度和持水性[2]。(2)酰基轉移反應。當底物中不存在Lys殘基,但存在伯氨基時,TGase催化Gln殘基的γ-羧酰胺基轉移到伯氨基的R基團上,發生酰基轉移反應[32]。利用該反應可以使蛋白質連接一些限制性氨基酸,從而提高食物蛋白質的營養價值。(3)脫酰基反應。當底物中既沒有Lys殘基,也沒有伯氨基時,TGase催化Gln殘基的γ-羧酰胺基與水反應,脫去酰胺基生成谷氨酸殘基。該反應可以改變蛋白質的等電點、溶解度等[29-30],并且因為生成谷氨酸殘基,還可起到改善魚糜制品風味的作用[33-34]。雖然3種催化反應同時進行,但以蛋白質交聯反應速率遠遠大于酰基轉移和脫酰基反應速率[2],故TGase催化反應以蛋白質交聯反應為主,這一性質有利于魚糜形成熱穩定性不可逆凝膠。
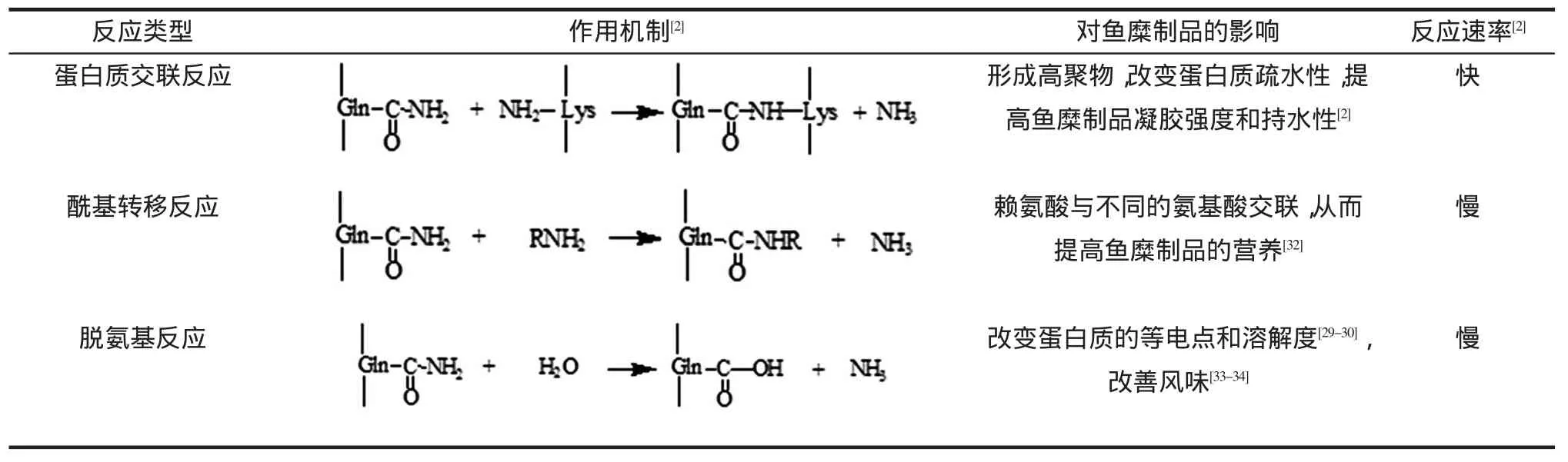
表2 TGase催化反應及其對魚糜制品功能特性的影響Table2 Reactions catalysed by TGaseand itsm echanism sof action inm odifying the functionalpropertiesof surim iproductions
3 影響TGase作用效果因素
3.1 熱處理方式
TGase的作用效果不僅與作用溫度有關,還受底物蛋白分子的展開程度的影響。一般而言,TGase在37℃~40℃下活力高,短時間(1 h)凝膠化處理就可獲得高程度的異肽交聯[34]。與此同時,肌球蛋白對溫度比較敏感,低溫下肌球蛋白分子構象也會發生變化。因此適當延長中低溫凝膠化時間(0 h~8 h),肌球蛋白分子逐漸伸展,TGase與底物蛋白的作用位點增加,可提高TGase共價交聯的程度[35]。
3.2 TGase活性促進劑
Ca2+對FTGase具有很好的激活作用,而對MTGase影響較小。在魚糜制品加工中常添加的鈣鹽有乳酸鈣、檸檬酸鈣、硫酸鈣、酪蛋白酸鈣、CaCl2等[36]。對于阿拉斯加鱈魚來說,添加0.05%醋酸鈣或CaCl2即可獲得最佳的凝膠性能,而對于溶解度較差的乳酸鈣則需0.1%的添加量,說明鈣鹽溶解性越好對魚糜凝膠的增強效果越顯著[36]。隨后不少學者選用溶解度較好的CaCl2,研究離子態鈣對魚糜及魚蛋白凝膠性能的影響,發現10mmol/kg~20mmol/kg的CaCl2可激活FTGase,催化MHC之間的共價交聯,但當CaCl2濃度達到50mmol/kg時會增大其空間位阻,導致MHC交聯受阻,抑制凝膠形成[37]。鈣鹽對魚糜凝膠性能的增強作用也會因魚種而異,對于阿拉斯加鱈魚來說,添加0.1%乳酸鈣其凝膠特性最佳,而對于太平洋鱈魚而言,則需添加0.2%乳酸鈣[38]。綜上分析可知,目前對于鈣鹽及其復合物對FTGase的影響主要是從離子態鈣的影響角度來分析的。魚骨等新型天然鈣源的開發,對副產物的高效利用和減少環境的污染具有重要意義。魚骨鈣大多以羥基磷灰石存在且與膠原蛋白有機結合,溶出量甚微。目前主要以酸水解法[39]、酶水解法[40]、高壓處理[41]促進魚骨中鈣的溶出。團隊前期研究發現對魚骨進行微粒化處理也是促進鈣釋放的手段之一[42]。當魚骨粒徑為微米級時,不僅不能改善魚糜的凝膠性能,反而阻礙魚肉蛋白網絡的形成[43]。當魚骨粒徑將至納米尺寸時,魚骨鈣可激活FTGase,進而改善魚糜的凝膠性能[44]。進一步探究發現,與CaCl2相比,納米魚骨中僅有少部分鈣是以離子態的形式存在,對FTGase的激活效果相對較弱,但其對魚糜凝膠性能的提高效果卻優于CaCl2[45],推測存在如下兩個方面的原因:(1)微粒化魚骨的小尺寸效應,特別是當魚骨粒度降至納米級別時,由于尺寸區域而展現出不同于宏觀材料的理化性質;(2)魚骨鈣賦存形態的轉化,在加熱過程中,微粒化魚骨可能存在著鈣的游離態與結合態之間的轉化平衡。
此外,二硫蘇糖醇(DTT)、半胱氨酸、亞硫酸鹽,可以改變蛋白質空間結構,使其更利于TGase催化交聯[46],β-巰基乙醇也可以增加TGase酶活,然而,β-巰基乙醇有劇毒,僅用于機理研究。
3.3 TGase活性抑制劑
金屬離子中Zn2+、Cu2+、Pb2+對TGase有很強的抑制作用,而Ni2+、Co2+、Fe2+可中度抑制TGase活性[29],這些金屬離子因不同程度地束縛了半胱氨酸的硫醇基團而降低TGase的活性[47]。N-甲基順丁烯亞胺(NEM)、NH4Cl(AC)、乙二胺四乙酸(EDTA)對TGase活性也具有抑制作用,NEM阻斷TGase活性中心Cys殘基上的活性巰基,AC能通過提高NH4+濃度直接抑制TGase催化的酰基轉移反應。EDTA通過兩種機制抑制TGase活性:(1)作為巰基烷化劑,能與TGase活性位置的巰基反應使之烷化,進而降低酶活,(2)通過螯合Ca2+降低FTGase活性,該機制對MTGase無影響[46]。劉海梅等[48]研究認為以上3種抑制劑對鰱魚糜凝膠形成的抑制效果依次是AC﹥NEM﹥EDTA,說明阻斷酰基轉移反應的進行比降低TGase活性更能有效抑制肌球蛋白重鏈(MHC)的交聯反應。對于海水魚而言,抑制效果順序相反,依次是EDTA﹥NEM﹥AC[49],說明抑制劑對于不同來源的魚種抑制效果存在差異,從側面證明了TGase是魚糜凝膠化過程中起作用的關鍵酶。
4 TGase在魚糜制品加工中的應用
4.1 改善魚糜制品的凝膠特性
大部分魚種體內FTGase含量不高,且具有水溶性,水中漂洗可部分去除,在最終的魚糜制品中僅有44%FTGase保存下來[33],在加工中,可通過激活或抑制FTGase來調節魚糜的凝膠性能。魚糜凝膠通常采用的兩段式加熱,其凝膠化過程主要就是為了使FTGase充分交聯而提高魚糜的凝膠性能[44]。而檸檬酸、EDTA、多聚磷酸鹽等的添加會螯合鈣離子而抑制凝膠的形成,降低魚糜的凝膠性能[50]。為進一步提高魚糜的凝膠性能,可適量添加MTGase,例如,添加MTGase后再凝膠化,可顯著提高魚糜的破斷強度、凹陷深度、凝膠強度和彈性[51]。MTGase還可用于碎魚肉的重組織化,催化肌球蛋白重鏈交聯反應,增加魚糜的凝膠強度[52]。MTGase添加量過大時,魚肉分子表面的作用位點與MTGase接觸機會多,會很快被交聯形成致密的牢固的三維結構,進而阻礙了MTGase進入蛋白質內部,導致魚糜凝膠強度的下降[47,53]。所以,在使用MTGase時,必須注意適量添加。
與此同時,酪蛋白、明膠等含有大量Lys殘基和Gln殘基的蛋白質可為魚肌球蛋白與TGase的共價交聯提供Lys-和Gln-基團。因此,魚糜制品生產加工中,常加入酪蛋白、明膠等添加劑與魚糜復合使用,促進TGase交聯程度。Na+、K+、Mg2+、Mn2+和Ba2+等離子適量使用可顯著提高魚糜的凝膠性能,其中,0.3mol/L~0.5 mol/L的NaCl促進肌原纖維蛋白溶出,提高與TGase作用的底物濃度,同樣可促進交聯[54]。
4.2 提高魚糜制品的營養價值
TGase通過催化蛋白質分子間或分子內的交聯反應將限制性氨基酸(如谷氨酸,賴氨酸)連接到魚糜蛋白質上,防止美拉德反應對氨基酸的破壞[47];同時,ε-(γ-Gln)-Lys異型肽鍵可被腎臟、小腸刷狀緣細胞及血液中的γ-谷氨環化轉移酶分解為賴氨酸和谷氨酸[29,55],可在體內正常代謝,從而提高魚糜及其制品的營養價值。與此同時,酪蛋白與魚糜的復配使用不僅可以促進TGase的交聯程度、提高魚糜的凝膠強度(見4.1),也可提高魚糜制品的營養價值。
4.3 增強魚糜制品的持水能力
持水性是評價魚糜制品品質的重要指標[56],當MTGase添加量為0~450U/kg時,魚糜凝膠持水性隨MTGase添加量的增加而上升,添加300U/kgMTGase可使其持水性從88%提高到92%[57],這是因為MTGase可使蛋白質分子間形成異型肽鍵及致密的交聯網絡,進而束縛包埋水分子,提高魚糜凝膠的持水性[2]。繼續增加TGase的添加量并不會提高魚糜凝膠的持水性,過量反而造成持水性下降,這是因為(1)底物濃度一定后,酶促反應達到一定程度后趨于平緩[57],(2)蛋白質與蛋白質之間的相互作用增強,蛋白質與水之間的相互作用減弱[58]。
5 展望
隨著對TGase性能研究的深入,TGase在魚糜制品中的應用仍在不斷擴大,今后對于TGase的研究在如下幾個方面尚需進一步加強:(1)開發以魚骨為代表的天然低價優質鈣源,探討其與化學合成鈣對FTGase激活效果及其對凝膠品質影響的異同,為副產物的高效利用提供思路。且化學合成鈣大多數具有苦味,大量添加會產生不愉快的口感,天然鈣源能否突破這一局限也是未來研究的方向。(2)FTGase易溶于水,漂洗過程中存在大量損失,因此如何減少漂洗過程中FTGase的損失,并提高FTGase的作用效果將具有重要意義。(3)風味釋放是近年來食品領域研究的熱點,研究TGase如何誘導蛋白凝膠網絡的形成,以及凝膠交聯網絡與魚糜風味釋放的聯系,將具有廣闊的前景。
[1] Pimchanok K,Soottawat B,Kongkarn K.Properties of surimigel as influenced by fish gelatin and microbial transglutaminase[J].Food Bioscience,2013,3(1):39-47
[2]Gaspar A LC,deGóes-FavoniSP.Action ofmicrobial transglutaminase (MTGase)in themodification of food proteins:A review[J]. Food Chemistry,2015,171:315-322
[3] Chaijan M,PanpipatW.Gel-forming ability ofmackerel(Rastrel-liger branchysoma)protein isolate asaffected bymicrobial transglutaminase[J].Walailak Journal of Science and Technology(WJST), 2010,7(1):41-49
[4]董若琰,王錫昌,劉源,等.近紅外光譜技術快速無損測定帶魚糜及其制品中磷酸鹽含量[J].光譜學與光譜分析,2013,33(6):1542-1546
[5] 周愛梅,曾慶孝,劉欣,等.兩種蛋白類添加劑對鳙魚魚糜凝膠特性的改良[J].華南理工大學學報(自然科學版),2005,33(4):87-91
[6] 張海均,程仲毅,賈冬英,等.轉谷氨酰胺酶聚合改性大豆分離蛋白的功能特性研究[J].食品科技,2013,38(2):233-236
[7] 李丹辰,陳麗嬌,梁鵬,等.木薯淀粉與木薯變性淀粉魚糜加工性質的影響[J].中國糧油學報,2014,29(8):60-64
[8]陸劍鋒,邵明栓,林琳,等.結冷膠和超高壓對魚糜凝膠性質的影響[J].農業工程學報,2011,27(11):372-377
[9] 劉海梅,鮑軍軍,張莉,等.親水性膠體對鰱魚糜凝膠特性的影響[J].魯東大學學報(自然科學版),2011,27(1):51-54
[10]Liu CH,Chang CC,Chiu Y C,etal.Identification and cloningof a transglutaminase from giant freshwater prawn,Macrobrachium rosenbergii,and its transcription during pathogen infection and moulting[J].Fish&Shellfish Immunology,2011,31(6):871-880
[11]Kenniston JA,Conley G P,Sexton D J,etal.A homogeneous fluorescence anisotropy assay formeasuring transglutaminase 2 activity [J].AnalyticalBiochemistry,2013,436(1):13-15
[12]PinkasDM,Strop P,Brunger A T,etal.Transglutaminase 2 undergoesa large conformational change upon activation[J].PLOSBiology,2007,5(12):e327
[13]Nemes Z,Petrovski G,Csosz E,et al.Structure-function relationships of transglutaminases-a contemporary view[J].Transglutaminases:Family ofEnzymeswith Diverse Functions,2005,38:19-36
[14]Di Venere A,Rossi A,De Matteis F,et al.Opposite effects of Ca2+and GTP binding on tissue transglutaminase tertiary structure[J]. JournalofBiologicalChemistry,2000,275(6):3915-3921
[15]MarianiP,CarsughiF,SpinozziF,etal.Ligand-induced conformational changes in tissue transglutaminase:Monte Carlo analysis of small-angle scattering data[J].Biophysical Journal,2000,78(6): 3240-3251
[16]Ahvazi B,Kim H C,Kee SH,etal.Three-dimensional structure of the human transglutaminase 3 enzyme:binding of calcium ions changesstructure for activation[J].The EMBO Journal,2002,21(9): 2055-2067
[17]Hemung BORN,Yongsawatdigul J.Partial purification and characterization of transglutaminase from threadfin bream(Nemipterus sp.)liver[J].Journalof Food Biochemistry,2008,32(2):182-200
[18]Yasueda H,Kumazawa Y,MotokiM.Purification and characterization of a tissue-type transglutaminase from red sea bream(Pagrus major)[J].Bioscience,Biotechnology,and Biochemistry,1994,58 (11):2041-2045
[19]Kumazawa Y,NakanishiK,Yasueda H,etal.Purification and Characterization of Transglutaminase from Walleye Pollack Liver[J]. FisheriesScience,1996,62(6):959-964
[20]Wan J,Kimura I,SatakeM,etal.Effectofcalcium ion concentration on the gelling properties and transglutaminase activity of walleye pollack surimipaste[J].Fisheries Science,1994,60:107-113
[21]Hemung BO,Yongsawadigul J.Partialpurification and characterization transglutaminases from Threadfin Bream (nemipterussp.)liver [J].Journalof Food Biochemistry,2008,32:182-200
[22]Piyadhammaviboon P,Yongsawatdigul J.Protein cross-linkingability of sarcoplasmic proteins extracted from Threadfin bream[J]. LWT-Food Scienceand Technology,2009,42:37-43
[23]Binsi PK,Shamasundar BA.Purification and characterisation of transglutaminases from four fish species:Effect of added transglutaminase on the viscoelastic behaviour of fish mince.Food Chemistry,2012,132:1922-1929
[24]Ha CR,Iuchi I.Purification and partial characterization of 76 kDa transglutaminase in the egg envelope (chorion)of rainbow trout, Oncorhynchusmykiss[J].JournalofBiochemistry,1997,122(5):947-954
[25]Worratao A,Yongsawatdigul J.Purification and characterization of transglutaminase from tropical tilapia (Oreochromis niloticus)[J]. Food Chemistry,2005,93(4):651-658
[26]Kumazawa Y,Sano K,Seguro K,etal.Purification and characterization of transglutaminase from Japanese oyster(Crassostrea gigas)[J]. JournalofAgriculturaland Food Chemistry,1997,45(3):604-610
[27]婁忠緯.鳙魚中轉谷氨酰胺酶性質的研究及其對魚糜凝膠化的影響[D].杭州:浙江工商大學,2015:1-2
[28]Kashiwagi T,Yokoyama K,Ishikawa K,et al.Crystal Structure of Microbial Transglutaminase from Streptoverticillium mobaraense[J]. JournalofBiologicalChemistry,2002,277(46):44252-44260
[29]Yokoyama K,Nio N,Kikuchi Y.Properties and applications ofmicrobial transglutaminase[J].Applied Microbiology and Biotechnology,2004,64(4):447-454
[30]劉心偉,呂加平,范貴生.微生物轉谷氨酰胺酶在食品工業中的研究進展[J].內蒙古農業大學學報(自然科學版),2005,26(4):54-57
[31]MotokiM,Seguro K.Transglutaminase and its use for food processing[J].Trends in Food Science&Technology,1998,9(5):204-210
[32]MotokiM,Kumazawa Y.Recent Research Trends in Transglutaminase Technology for Food Processing[J].Food Scienceand Technology Research,2000,6(3):151-160
[33]Yongsawatdigul J,Worratao A,Park JW.Effect of endogenous transglutaminase on threadfin bream surimi gelation[J].Journal of Food Science,2002,67(9):3258-3263
[34]Kamath G G,Lanier TC,Foegeding E A,et al.Nondisulfide covalentcross-linkingofmyosin heavy chain in“setting”of Alaska pollock and Atlantic croaker surimi[J].Journal of Food Biochemistry, 1992,16(3):151-172
[35]Kaneda I,Aonuma K,Funatsu Y,etal.Effectof setting temperature on themechanicalpropertiesofsurimigels[J].Journalof Biorheology,2014,28(1):11-15
[36]郭秀瑾,尤娟,于錦河,等.碳酸鈣與外源蛋白復配物對含有MTGase的魚糜凝膠特性的促進作用[J].食品安全質量檢測學報, 2015,6(6):2063-2070
[37]劉海梅,熊善柏,謝筆鈞.鈣離子對白鰱魚糜熱誘導凝膠化的影響[J].食品科學,2006,27(8):87-90
[38]Lee NG,Park JW.Calcium compounds to improvegel functionality ofPacificwhitingand Alaskapollock surimi[J].Journalof Food Science,1998,63:969-974
[39]赫美,許鑫,楊春瑜.食醋對魚骨中鈣溶出的影響[J].現代食品科技,2011,27(1):87-89
[40]常佳駒.白鰱魚骨酶解濃湯的制備及其生理活性的研究[D].合肥:合肥工業大學,2014:4-5
[41]周亞軍,隋思瑤,黃卉,等.高壓脈沖電場輔助提取魚骨鈣工藝優化[J].農業工程學報,2012(23):265-270
[42]Yin T,Park JW.Texturaland rheologicalpropertiesof Pacific whiting surimiasaffected by nano-scaled fish boneand heating rates[J]. Food Chemistry,2015,180:42-47
[43]李俊杰,熊善柏,曾俊,等.鰱魚魚漿對魚糜凝膠品質的影響[J].食品科學,2013,34(1):53-56
[44]Yin T,Park JW.Effects of nano-scaled fish bone on the gelation properties of Alaska pollock surimi[J].Food Chemistry,2014,150: 463-468
[45]尹濤.納米魚骨的制備,特性表征及其對魚糜膠凝影響的機制研究[D].武漢:華中農業大學,2015:75-77
[46]孫靜靜,羅自生,吳翔,等.草魚中內源性轉谷氨酰胺酶特性的研究[J].中國食品學報,2012,12(9):67-72
[47]劉香海,劉璘.TG酶性質及在肉類重組產品中的應用[J].中國食品添加劑,2012(2):149-154
[48]劉海梅,熊善柏,張麗.TGase抑制劑對鰱魚糜熱誘導凝膠形成的影響[J].食品科學,2008,29(12):124-127
[49]Benjakul S,Visessanguan W,Pecharat S.Suwari gel properties as affected by transglutaminaseactivator and inhibitors[J].Food Chemistry,2004,85(1):91-99
[50]ChanaratS,Benjakul S.Comparative study on protein cross-linking and gel enhancing effect of microbial transglutaminase on surimi from differentfish[J].Journalof the Science of Food and Agriculture, 2012,92(4):844-852
[51]賈丹,劉茹,劉明菲,等.轉谷氨酰胺酶對鳙魚糜熱誘導膠凝特性的影響[J].食品科學,2013,34(9):37-41
[52]溫慧芳,趙利,袁美蘭,等.魚肉重組制品研究進展[J].中國釀造, 2014,33(3):13-16
[53]賀江航,呂峰,黃金燕.TG催化魚肉蛋白共價交聯作用研究[J].徐州工程學院學報(自然科學版),2012,27(2):50-56
[54]夏文水,羅永康,熊善柏,等.大宗淡水魚貯運保鮮及加工技術[M].北京:中國農業出版社,2014:88-89
[55]黃志良,寧正祥.轉谷氨酰胺酶對乳蛋白質的改性作用[J].食品工業科技,2002,23(3):77-79
[56]Liu R,Zhao SM,Xie B J,etal.Contribution ofprotein conformation and intermolecular bonds to fish and pork gelation properties[J]. Food Hydrocolloids,2011,25(5):898-906
[57]莊瑋婧,謝三都.轉谷氨酰胺酶對鰱魚魚丸品質特性的影響[J].中國農學通報,2010,26(24):89-94
[58]Martelo-VidalM J,Fernández-No IC,Guerra-Rodríguez E,etal. Obtaining reduced-salt restructured white tuna(Thunnus alalunga) mediated bymicrobial transglutaminase[J].LWT-Food Science and Technology,2016,65:341-348
Transglutam inase and Its App lication in Processing of Surim i Product
ZHANGMeng-ling1,2,ZHANG Jin1,2,XIONGShan-bai1,2,ZHAOSi-ming1,2,LIURu1,2,*
(1.Collegeof Food Scienceand Technology,Huazhong AgriculturalUniversity,Wuhan 430070,Hubei,China;2.NationalResearch and DevelopmentBranch Center forConventional Freshwater Fish Processing,Wuhan 430070,Hubei,China)
Thispapersummarized the propertiesand actionmechanism of fish endogenousandmicrobial transglutaminase,then italso discussed its influencing factors(heating,activorsand inhibitorsof transglutaminase)and applications(modificationsofgelproperties,nutritionalvalue and waterholding capacity).Finally,its future development tendencieswere proposed,so as to provide reference on application of transglutaminase in surimiproductprocessing.
transglutaminase(TGase);surimi;gel;influencing factors;application
10.3969/j.issn.1005-6521.2016.24.046
2016-03-14
國家自然科學基金面上項目(31471686);現代農業產業技術體系建設專項(CARS-46-23)
張夢玲(1991—),女(漢),碩士研究生,研究方向:水產品加工及貯藏工程。
*通信作者:劉茹,副教授,博士,研究方向:水產品加工及貯藏工程。

