銅試劑在有機合成中的應用研究進展
鄭紹軍,楊丹丹,劉 靜,朱 瑞,王 瑜,高玉華*(1.江蘇科技大學 a.環境與化學工程學院;b.海洋裝備研究院,江蘇 鎮江 212003)
·綜合評述·
銅試劑在有機合成中的應用研究進展
鄭紹軍1a,1b*,楊丹丹1a,劉 靜1a,朱 瑞1a,王 瑜1a,高玉華1a*(1.江蘇科技大學 a.環境與化學工程學院;b.海洋裝備研究院,江蘇 鎮江 212003)
銅試劑催化的偶聯反應是直接構建碳-碳鍵最有效的方法之一。本文綜述了銅試劑催化的偶聯反應構筑六種碳-碳鍵的方法;重點闡述了銅試劑催化構筑C(SP2)—C(SP2)的研究進展,含分子間偶聯和分子內偶聯。參考文獻44篇。
銅試劑;有機合成;天然產物;碳-碳偶聯;綜述
1901年,Ullmann[1]首次報道了銅試劑參與的反應,加熱銅粉和鄰位溴代硝基苯,銅轉化成溴化銅,而溴代硝基苯轉化成2,2-二硝基聯苯(Scheme 1)。

Scheme 1
1903年,Ullmann[2]又報道了苯胺和 2-氯苯甲酸在銅催化下生成 2-苯氨基苯甲酸(Scheme 2)。Ullmann還發現,在銅和氫氧化鉀共同作用下,苯酚和溴代苯發生反應,生成了二苯醚(Scheme 2~3)。

Scheme 2
1906年,Goldbery[3]報道了在銅和碳酸鉀的作用下,2-氨基苯甲酸和溴代苯反應,生成了 2-苯氨基苯甲酸(Scheme 4)。同年還報道了在銅粉的催化作用下,生成酰胺化合物的反應(Scheme 5)。
前期的研究工作為現代銅試劑的迅速發展奠定了堅實的基礎,特別是 Ullmann 反應。在相同鹵代芳烴相互偶聯時用 Ullmann 反應可以得到令人滿意的對稱聯苯化合物,但是當偶聯反應發生在兩種不同的鹵代芳烴分子(Ar1X和Ar2X)之間時,會形成三種產物(Ar1—Ar1,Ar2—Ar2,Ar1—Ar2)。為解決這個問題,科研工作者采用了另一種方法,即先通過金屬-鹵素交換反應,也就是將一種鹵代芳烴 Ar1X 轉化為相應的芳基金屬試劑如銅試劑 Ar1Cu,隨后再使其與另一鹵代芳烴分子 Ar2X 低溫偶聯,得到單一偶聯產物 Ar1—Ar2。該方法條件溫和,而且當鹵代芳烴的兩個鄰位均有取代基時亦可偶聯,克服了 Ullmann 反應的缺陷,大量的實例證實其非常適合于不對稱聯苯衍生物的合成。

Scheme 3

Scheme 4

Scheme 5
近 20 年,銅試劑的研究取得了很大的進展,新興的銅催化體系,使得反應條件變的更加溫和,產率明顯提高[4-6]。本文依據碳-碳鍵的構筑類型闡述通過銅試劑構筑碳-碳鍵的方法及其在全合成中的應用。
1 銅試劑催化構筑C(SP3)—C(SP3)健
2004年,Falck等[7]報道了以THF為溶劑,在 CuCN 的作用下,于 50 ℃ 完成了碳-碳鍵的形成,最終得到了具有生物活性的 11(R),12(R),15(S)-THETA,產率高達89%(Scheme 6)。
2008年,Li等[8]描述了以Cu(OTf)2為催化劑,完成了1,3-二酮與端基烯的選擇性偶聯反應(Scheme 7)。發現溶劑對該反應影響很大,通過大量實驗篩選,最終確定在二惡烷或液體的[bmim]PF6中反應效果最佳,產率85%。
2015年,許課題組[9]以CuI為催化劑,實現了對甲苯磺酰腙與β-酮酸酯的芐基化反應(Scheme 8)。該反應條件溫和、底物適用范圍廣、產率高(87%),為β-酮酸酯的芐基化提供了一種新的方法。

Scheme 6

Scheme 7

Scheme 8
2 銅試劑催化構筑C(SP3)—C(SP2)鍵
近代化學家研究表明,均相催化劑如 Cu(OAc)2、CuI或CuBr代替青銅,NaH代替甲醇鈉或氫氧化鈉[10-11],大大提高了反應的活性和產率,使得銅試劑在合成中得到更廣泛的應用(Scheme 9)。在鹵化亞銅(CuI、CuBr和CuCl)或其他更容易溶解的銅試劑(CuCl/TMEDA[6]CuBr/HMPA[7],Li2CuCl4[8],CuBr/LiBr/PhSLi)催化下,芳香環鹵代烴,烯丙基鹵代烴和乙烯基鹵代烴形成鎂的格氏試劑后[12-14],可與有機鹵代烴在室溫下反應,生成偶聯產物(Scheme 10)。
2002年,Hennessy等[15]發現,在配體的輔助下,銅試劑催化的反應可在較低溫度下和低沸點溶劑如THF中進行,產率也很高(Scheme 11)。
其余部分銅催化體系也適合此類反應,例如:CuI/DMEDA[16]體系作為分子內偶聯反應的催化試劑,以85%的產率順利得到了預期的產物(Scheme 12)。
2009年,Mino等[17]報道在5 mol%CuI和腙的共同作用下,以甲苯作為溶劑,在90 ℃下反應24 h完成了碘苯41與丙二酸二乙酯25的偶聯反應(Scheme 13)。
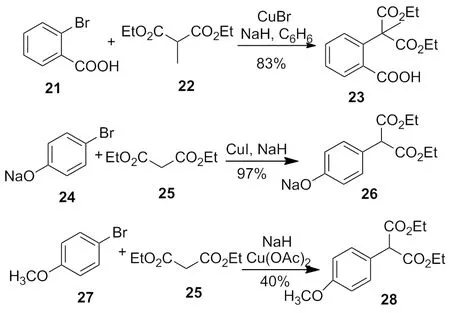
Scheme 9

Scheme 10
2012 年,Huang等[18)報道了以一價銅的烯醇混合物為催化體系,通過烯醇三價銅鹽的中間體,最終完成了化合物43與化合物44的偶聯反應(Scheme 14)。
3 銅試劑催化構筑C(SP3)—C(SP)鍵
2006年,Montel等[19]報道了在1,3-二甲基咪唑酮(DMI)中,10%的CuI為催化劑,很好的構建了新的C(SP3)—C(SP)鍵,產率達到 60%~90% (Scheme 15)。

Scheme 11

Scheme 12

Scheme 13
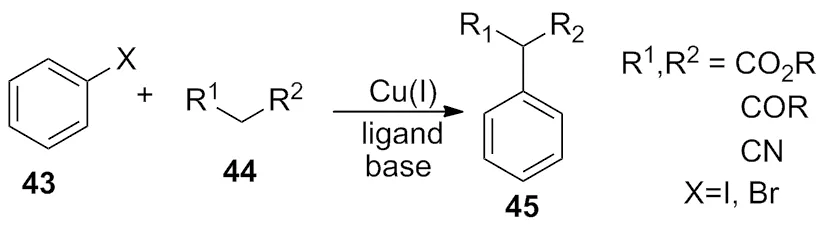
Scheme 14

Scheme 15
4 銅試劑催化構筑C(SP2)—C(SP2)鍵
4.1 銅試劑催化構筑芳基碳-碳鍵
聯苯結構是某些天然產物的重要組成部分,也是藥理活性的重要單元。按照聯苯的構建方式將芳基碳-碳鍵偶聯分為分子間偶聯和分子內偶聯。
(1) 分子間偶聯
a.對稱的分子間偶聯
聯苯經典的合成方法是Ullmann反應,高溫條件下,缺電子的芳香鹵代化合物和銅一起加熱,發生分子間的偶聯反應,芳香鹵代物上的硝基、羧基等吸電子基團,可以加速反應的進行。
2003年,Mulrooney等[20]利用1,5二氮順十氫化萘銅催化劑完成了一系列天然產物的全合成,如化合物51和化合物(R)Niaerone的合成(Scheme 16)。
2003年,Molander等[21]在異五味子素的全合
成中,利用Ullmann 反應,在DMF中回流反應18 h合成了關鍵反應中間體4,4′,5,5′,6,6′-六甲氧基-[1,1′-二苯]-2,2′-二醛(Scheme 17)。
2005年,Surry等[22]報道了在-20 ℃條件下,將芳香鹵代烴和格氏試劑異丙基溴化鎂溶解在THF中,通過導管將上述反應液導入至含有CuBr·SMe2的另一個反應瓶中,然后加入氧化劑57,室溫反應1 h,合成碳-碳鍵偶聯的系列化合物(Scheme 18)。
2009 年,Chen等[23]小組研究了在二價銅鹽和碘的共同作用下,通過碳-氫活化,合成了一系列對稱的偶聯化合物,大部分官能團適用該體系(Scheme 19)。
2010年,Martinek等[24]報道了在催化量Cu(I)OCOR 的參與下,在DMF中,于50 ℃反應合成了對稱的偶聯產物(Scheme 20)。

Scheme 16

Scheme 17

Scheme 18

Scheme 19

Scheme 20
b.不對稱的分子間偶聯
2011年,Peng課題組[25]報道了利用銅試劑催化的Mizoroki-Heck偶聯反應(Scheme 21)。該反應不需要配體作為輔助,但是溶劑和堿對反應影響很大,通過大量篩選發現,10 mol%Cu2O為催化劑,在DMF溶劑中,TMAB為堿是最佳的反應條件。利用分子間偶聯方法構建聯苯軸的主要難題是:進行交叉偶聯反應時,如果缺乏區域選擇性,會生成復雜的產物,而且對空間位阻要求很高。理論上,這些難題可以通過分子內偶聯反應來解決。
2012年,Aves課題組[26]報道了在-40 ℃下,把芳香鹵代烴和叔丁基鋰溶解于THF,于-20 ℃下,通過導管將上述反應液導入到含有CuBr·SMe2的另一個反應瓶中,緊接著加入氧化劑57,于室溫反應30 min,合成碳-碳偶聯化合物(Scheme 22)。
(2) 分子內偶聯
2000年,Piers等[27]研究CuCl 在無水DMF 中,于室溫反應,成功合成了偶聯化合物,產率較為理想(Scheme 23)。
2004 年,Yamada等[28]和Ikeda等[29]報道了Ullmann類型的反應,利用CuCl2與胺組成的催化體系,完成了天然產物合成中關鍵一步的偶聯反應,并最終合成了天然產物1,9-亞壬柯里拉京(Scheme 24)。
2007年,Hosokawa[30]報道了利用CuTC催化體系,在NMP溶液中,以80%的產率完成了關鍵步驟的偶聯反應(Scheme 25)。


EntryCatalystBaseSolventYield/%1CuIEt3NDMF192CuBrEt3NDMF213CuClEt3NDMF794Cu2OEt3NDMF855CuBr2Et3NDMF56Cu(OTf)2Et3NDMF787CuCl2Et3NDMF538Cu(OAc)2Et3NDMF359Cu2OK2CO3DMF85
Scheme 21

Scheme 22

Scheme 23

Scheme 24

Scheme 25
4.2 銅試劑催化構筑烷基C(SP2)—C(SP2)鍵
2001 年,Cuzzupe等[31]報道了(±)-Reveromycin B的全合成,利用CuTC與Pd2(dba)3聯合催化,順利得到偶聯化合物(Scheme 26)。
5 銅試劑催化構筑C(SP2)—C(SP)鍵
2000年,Nandi小組[32]報道了在銅和鈀試劑共同作用下,完成了碘苯41和化合物79的偶聯反應(Scheme 27)。
2005年,Hoshi等[33]利用Suzuki和Sonogashira類型的反應,在溫和的條件下,Cu(acac)2作為催化劑,高效高立體選擇性的合成了1-arylalk-3-en-1-ynes(83),大部分官能團不受該體系的影響(Scheme 28)。

Scheme 26
2006年,Yu等[34]報道了Sonogashira類型的偶聯反應,催化體系是CuI與氮氮二甲基甘氨酸混合物,高效完成了86的全合成(Scheme 29)。
2011年,Yuan等[35]報道了納米CuO催化的Sonogashira反應(Scheme 30),高效的促使端基炔和鹵代烴發生偶聯反應。
2011年,Zhu小組[36]報道了在碘化亞銅的作用下,使乙烯基鹵化烴與端基炔化合物發生偶聯反應。該反應的顯著優點是,雙鍵的構型在反應前后保持不變,具有很大的應用價值(Scheme 31)。
2012年,Zhou[37]小組開發了一種新的合成反應體系,即在 PdCl2(PPh3)2(5%)/CuI,THF 和TEA的條件下,合成了一系列的對稱偶聯分子(Scheme 32)。此反應催化體系大大的提高了合成Bis(arylethynyl)benzene的產率 。
2012年,Shang小組[38]利用二價銅鹽活化芳基碳-氫鍵,或一價銅插入到碳-碘鍵中間,形成三價銅中間體,與端基炔化合物反應,生成偶聯化合物(Scheme 33)。
6 銅試劑催化構筑C(SP)—C(SP)鍵
2009年,Nador等[39]報道了在沒有鈀、配體、氧化劑存在條件下,利用準備好的納米級銅為催化劑合成了對稱的1,3二炔化合物(Scheme 34)。當炔為脂肪鏈端基炔時,以碳酸鈉為堿,產率較高,并且只需要催化量的銅試劑。

Scheme 27

Scheme 28

Scheme 29

Scheme 30


Scheme 31

Scheme 32

Scheme 33

Scheme 34

Scheme 35

Scheme 36

Scheme 37

Scheme 38

Scheme 39
2010年,Wang小組[40]利用二價銅鹽為催化劑,在沒有溶劑的條件下,將末端炔基偶聯成1,3二炔化合物(Scheme 35),該反應不僅適用于對稱分子的合成,還可以合成不對稱的二炔化合物,并且催化劑可以重復使用。
2011年,Zhang等[41]描述了在碘化亞銅和配體TMEDA共同作用下,空氣為氧化劑,室溫下發生偶聯反應,生成對稱的化合物(Scheme 36)。
2011年,Jia等[42]在研究端基炔對稱偶聯形成1,3二炔化合物的過程中,在沒有配體存在的條件下,利用碘化亞銅為催化劑,NaOAc為堿,依然用空氣為氧化劑,高產率的完成了偶聯反應,并且沒有副產物產生(Scheme 37)。
2011年,Kusuda[43]小組報道了利用氯化亞銅完成了Glaser類型的反應,以Solkane 365 mfc 為載體,得到了偶聯化合物(Scheme 38)。
2015年,楊振平等[44]報道了端炔烴的二聚偶聯反應是合成含有共軛碳-碳叁鍵化合物的一個重要方法。在CuI的催化下,以催化量的N-甲基咪唑為堿,在偶氮二甲酸二乙酯(DEAD)的協助下,各種不同的芳香族和脂肪族端炔都能順利的發生二聚Glaser偶聯反應(Scheme 39)。考察了不同銅催化劑和溶劑對該反應的影響。反應具有收率高、操作簡單、條件溫和等優點。
7 結論
主要依據構筑碳-碳鍵的類型進行分類,總結了典型的銅試劑構筑碳-碳鍵的方法及其在全合成中的應用,包含經典的Ullmann反應、Stille反應和本小組開發的新方法等。由于銅試劑具有價格低廉、對環境友好、后處理簡單等優點,使其在天然產物合成和藥物先導化合物的結構優化等方面的應用價值很高,隨著有機化學的不斷發展,必將有越來越多的銅試劑及其新的合成方法被開發出來,這將大大豐富有機化學的內容。
[1] Ullmann F.Ueber synthesen in der biphenylreihe.Bielecki J Ber Dtsch Chem Ges[J].1901,34:2174-2185.
[2] Ullmann F.Ueber symmetrische biphenylderivate.Over symmetrical Diphenyl derivative[J].Liebigs Ann Chem.1904,332:38-81.
[3] Goldberg I D.Ueber phenylirungen bei gegenwart von kupfer als katalysator[J].B Chem Ges.1906,39:1691-1692.
[4] Strieter E R,Blackmond D G,Buchwald S L.The role of chelating diamine ligands in the goldberg reaction:A kinetic study on the copper-catalyzed amidation of aryl iodides[J].J Amer Chem Soc,2005,127:4120-4121.
[5] Ouali A,Taillefer M,Spindler J F,etal.Precatalysts involved in copper-catalyzed arylations of nucleophiles[J].Organometallics,2006,26:65-74.
[6] Zhang S L,Liu L,Fu Y,etal.Theoretical study on copper(I)-catalyzed cross-coupling between aryl halides and amides[J].Organometallics,2007,26:4546-4554.
[7] Falck J R,Barma D,Mohapatra S,etal.Asymmetric synthesis of the stereoisomers of 11,12,15(S)-trihydroxyeicosa-5(Z),8(Z),13(E)-trienoic acid,a potent endothelium-derived vasodilator[J].Bioorg Med Chem Lett,2004,14:4987-4990.
[8] Li Y,Yu Z,Wu S.Efficient copper(II)-catalyzed addition of activated methylene compounds to alkenes[J].J Org Chem,2008,73:5647-5650.
[9] 許愷,沈沖,盛衛堅,等.銅催化β-酮酸酯的芐基化反應[J].有機化學,2015,35:633-637.
[10] McKillop A,Rao D P.Copper-catalysed condensation ofβ-Dicarbonyl compounds with 2-Bromobenzaldoximes:A simple,one-step synthesis of 3-hydroxyisoquinolineN-Oxides[J].Synthesis,1977:760,761-765.
[11] McKillop A,Rao D P.Copper-catalysed direct arylation ofα-substitutedβ-dicarbonyl compounds with 2-bromobenzoic acid[J].Synthesis,1977:759,760-763.
[12] Vyvyan J R,Holst C L,Johnson A J,etal.Total synthesis of gibbilimbols A-D[J].J Org Chem,2002,67:2263-2265.
[13] Shimizu R,Yoneda E,Fuchikami T.Copper catalyzed grignard cross-coupling reaction withβ-perfluoroalkyl-substituted alkyl halides[J].Tetrahedron Lett,1996,37:5557-5560.
[14] Johnson D K,Ciavarri J P,Ishmael F T,etal.A novel copper (i) mediated,symmetrical coupling procedure for alkyl,aryl,benzyl,and thiophenyl dihalides[J].Tetrahedron Lett,1995,36:8565-8568.
[15] Hennessy E J,Buchwald S L.A general and mild copper-catalyzed arylation of diethyl malonate[J].Org Lett,2002,4:269-272.
[16] Fang Y,Li C.O-Arylation versus C-arylation:Copper-catalyzed intramolecular coupling of aryl Bromides with 1,3-dicarbonyls[J].J Org Chem,2006,71:6427-6431.
[17] Mino T,Yagishita F,Shibuya M.Copper(I)-catalyzed C-C and C-O coupling reactions using hydrazone ligands[J].Synlett,2009:2457-2460.
[18] Huang Z,Hartwig J F.Copper(I) enolate complexes inα-arylation reactions:Synthesis,reactivity,and mechanism[J].Angew Chem Int Ed,2012,51:1028-1032.
[19] Montel F,Beaudegnies R,Kessabi J,etal.New method based on 1-(trimethysilyl)alk-1-yne to prepare 1,4-skipped diynes[J].Org Lett,2006,8:1905-1908.
[20] Mulrooney C A,Li X,DiVirgilio E S,etal.General approach for the synthesis of chiral perylenequinones via catalytic enantioselective oxidative biaryl coupling[J].J Amer Chem Soc,2003,125:6856-6857.
[21] Molander G A,George K M,Monovich L G.Total synthesis of (+)-isoschizandrin utilizing a samarium(II) iodide-Promoted 8-Endo Ketyl-Olefin cyclization[J].J Org Chem,2003,68:9533-9540.
[22] Surry D S,Su X,Fox D J,etal.Synthesis of medium-ring and iodinated biaryl compounds by organocuprate oxidation[J].Angew Chem Int Ed,2005,44:1870-1873.
[23] Chen X,Dobereiner G,Hao X S,etal.Cu(II)-mediated oxidative dimerization of 2-phenylpyridine derivatives[J].Tetrahedron,2009,65:3085-3089.
[24] Martinek M,Korf M,Srogl J.Ascorbate mediated copper catalyzed reductive cross-coupling of disulfides with aryl iodides[J].Chem Commun,2010,46:4387-4389.
[25] Peng Y,Chen J,Ding J,etal.Ligand-free copper-catalyzed arylation of olefins by the Mizoroki-Heck reaction[J].Synthesis,2011,2:213-216.
[26] Aves S J,O'Connell K M G,Pike K G,etal.Synthesis of highly substituted symmetrical 1,3-dienes via organocuprate oxidation[J].Synlett,2012:298,300.
[27] Piers E,Yee J G K,Gladstone P L.CuCl-mediated intramolecular oxidative coupling of aryl- and alkenyltrimethylstannane functions[J].Org Lett,2000,2:481-484.
[28] Yamada H,Nagao K,Dokei K,etal.Total synthesis of (-)-corilagin[J].J Amer Chem Soc,2008,130:7566-7567.
[29] Ikeda Y,Nagao K,Tanigakiuchi K,etal.The first construction of a 3,6-bridged ellagitannin skeleton with 1C4/B glucose core;synthesis of nonamethylcorilagin[J].Tetrahedron Lett,2004,45:487-489.
[30] Hosokawa S,Fumiyama H,Fukuda H,etal.The first total synthesis and structural determination of TMC-66[J].Tetrahedron Lett,2007,48:7305-7308.
[31] Cuzzupe A N,Hutton C A,Lilly M J,etal.Total synthesis of the epidermal growth factor inhibitor (-)-reveromycin B[J].J Org Chem,2001,66:2382-2393.
[32] Nandi B,Kundu N G.Heteroannulation through copper catalysis:A novel cyclization leading to a highly regio-and stereoselective synthesis of 2-substituted benzothiazolines[J].Org Lett,2000,2:235-238.
[33] Hoshi M,Nakayabu H,Shirakawa K.Stereoselective syntheses of (E)- and (Z)-1-arylalk-3-en-1-ynes and (E,E)-,(Z,E)-,(E,Z)-,and (Z,Z)-alka-1,5-dien-3-ynes via a one-pot multicomponent coupling reaction[J].Synthesis,2005:1991-2007.
[34] Yu S,Liu F,Ma D A.Flexible route to immunosuppressive agent FR252921.Asymmetric total synthesis of its (13R,14R,19R)-isomer[J].Tetrahedron Lett,2006,47:9155-9157.
[35] Yuan Y,Zhu H,Zhao D,etal.Ligand-free copper oxide nanoparticle-catalyzed sonogashira coupling reaction[J].Synthesis,2011:1792-1798.
[36] Zhu Y,Li T,Qu X,etal.Copper(I)-catalyzed synthesis of 1,3-enynes via coupling between vinyl halides and alkynes or domino coupling of vinyl halides[J].Org Biomol Chem,2011,9:7309-7312.
[37] Zhou Z L,Zhao L,Zhang S,etal.Facile synthesis of functionalized bis(arylethynyl)benzene derivatives via sila-Sonogashira reaction[J].Synth Commun,2012,42:1622-1631.
[38] Shang J,Wang W M,Wang W M.Synthesis,crystal structure,invitroacetohydroxyacid synthase inhibition,in vivo herbicidal activity,and 3D-QSAR of new asymmetric aryl Disulfides[J].J Agric Food Chem.2012,60:8286-8293.
[39] Nador F,Fortunato L,Moglie Y,etal.A simple one-pot procedure for the direct homocoupling of terminal alkynes promoted by copper nanoparticles[J].Synthesis,2009:4027-4031.
[40] Wang D,Li J,Li N,etal.An efficient approach to homocoupling of terminal alkynes.Solvent-free synthesis of 1,3-diynes using catalytic Cu(II) and base[J].Green Chem,2010,12:45-48.
[41] Zhang S,Liu X,Wang T.An efficient copper-catalyzed homocoupling of terminal alkynes to give symmetrical 1,4-disubstituted 1,3-diynes[J].Adv Synth Catal,2011,353:1463-1466.
[42] Jia X,Yin K,Li C,etal.Copper-catalyzed oxidative alkyne homocoupling without palladium,ligands and bases[J].Green Chem,2011,13:2175-2178.
[43] Kusuda A,Xu X H,Wang X,etal.Organic reaction in solkane 365 mfc:Homocoupling reaction of terminal alkynes[J].Green Chem,2011,13:843-846.
[44] 楊振平,王兵南,許孝良,等.CuI/DEAD促進的端炔的二聚偶聯反應[J].有機化學,2015:207-211.
Research Progress on the Application of Copper Reagents in Organic Synthesis
ZHENG Shao-jun1a,1b*,YANG Dan-dan1a,LIU Jing1a, ZHU Rui1a,WANG Yu1a,GAO Yu-Hua1a*
(a.School of Environmental and Chemical Engineering;b.Marine Equipment and Technology Institute, 1.Jiangsu University of Scince and Technology,Zhenjiang 212003,China)
The copper reagent-catalyzed coupling reaction is one of the most effective way to construct the carbonk-carbon bond.Six kinds of C—C bond coupling catalyzed by copper were reviewed with 44 references.The progress of C(SP2)—C(SP2) coupling,including intermolecular C—C bond coupling and intramolecular coupling C—C bond coupling,were described in detail.
copper reagent;organic synthesis;nature product;C—C bond coupling;review
2016-08-15
國家自然科學基金資助項目(21502073);江蘇省自然科學基金資助項目(BK20150465);江蘇高校(高技術船舶)協同創新中心及江蘇科技大學海洋裝備研究院資助項目(HZ2016012)
鄭紹軍(1980-),男,漢族,江蘇連云港人,博士,主要從事天然產物全合成研究。 E-mail:sz281cam@just.edu.cn
高玉華,副教授,Tel.0511-85605150,E-mail:gaoyuhua1964@163.com
O621.3
DOI:10.15952/j.cnki.cjsc.1005-1511.2016.12.16208

