超聲造影評估胰腺癌周圍血管受侵程度及可切除性的應用價值
劉 站, 唐少珊
(中國醫科大學附屬盛京醫院 超聲科, 沈陽 110004 )
超聲造影評估胰腺癌周圍血管受侵程度及可切除性的應用價值
劉 站, 唐少珊
(中國醫科大學附屬盛京醫院 超聲科, 沈陽 110004 )
目的 應用超聲造影(CEUS)觀察胰腺癌侵犯周圍血管情況,探討術前CEUS評估胰腺癌可切除性的價值。方法 回顧性分析2012年12月-2014年10月在中國醫科大學附屬盛京醫院就診的經手術探查或術后病理證實為胰腺癌的患者25例,術前均行CEUS檢查。觀察病灶與胰周大血管的關系,評估受侵犯程度,同時進行評分,與術中探查及術后病理結果進行對比,分別計算胰周大血管受侵率、術前CEUS評估胰周血管受侵程度的敏感性、特異性,CEUS評估胰腺癌可切除性的敏感性、特異性、陽性預測值、陰性預測值、總符合率及約登指數。結果 術前CEUS診斷血管受侵42條,術中所見血管受侵41條;術前CEUS評估可切除者17例,術中探查判定可切除15例,CEUS評估胰腺癌可切除的敏感性為93.3%,特異性為70.0%,總符合率為84.0%,假陽性率為30.0%,假陰性率為6.7%,陽性預測值為82.4%,陰性預測值為87.5%,約登指數為0.633。結論 CEUS評估胰腺癌周圍大血管受侵程度與術中判斷相比具有較高的敏感性和特異性,CEUS評估胰腺癌可切除性與術中判斷對比,具有較高的敏感性、特異性及符合率,能較為準確的評估胰腺癌對胰周大血管的浸潤程度,為術前評價胰腺癌的可切除性提供了一種新方法。
胰腺腫瘤; 胰腺切除術; 超聲造影
胰腺癌患者病死率在惡性腫瘤中排第七位,且呈快速上升趨勢[1]。目前手術切除為公認的治療胰腺癌首選方法[2],但其術后病死率及并發癥發生率均很高,因此術前準確評估胰腺癌的可切除性顯得尤為重要,從而減少盲目無效的手術探查對患者的傷害[3-4]。當胰腺癌未發生肝臟明顯轉移或淋巴結轉移時,它的可切除性主要取決于其對胰周大血管的侵犯程度。近年來超聲造影(contrast-enhanced ultrasound,CEUS)技術在胰腺占位性病變的定性診斷方面得到了廣泛應用。本研究應用CEUS對胰腺癌患者進行術前評估,評價胰腺癌對周圍血管浸潤情況,并與術中探查及術后病理結果進行比較,探討術前CEUS評估胰腺癌可切除性的價值。
1 資料與方法
1.1 研究對象 回顧性分析2012年12月-2014年10月本院收治的經手術探查或術后病理證實為胰腺癌患者的臨床資料。所有患者術前均行CEUS檢查,并簽署知情同意書。
1.2 儀器與方法 應用Philips IU22和Toshiba Aplio500彩色多普勒超聲診斷儀,使用寬頻凸陣探頭,中心頻率為3.5 MHz,機械指數為0.06~0.15,內置實時造影匹配成像技術(real time gray-scale contrast tuned imaging technology,CnTI),造影劑為SonoVue(意大利Bracco公司)。由同一醫師對所有患者術前先行常規超聲檢查觀察病灶的部位、大小、回聲、邊界及血流情況,重點觀察并記錄病灶與門靜脈(portal vein,PV)、腸系膜上靜脈(superior mesenteric vein,SMV)、脾靜脈(splenic vein,SPV)、肝動脈(hepatic artery,HA)、腸系膜上動脈(superior mesenteric artery, SMA)、脾動脈(splenic artery,SPA)、腹腔動脈(celiac artery,CA)根部等胰周大血管的關系,同時進行評分。選擇最佳切面,固定探頭,啟用CnTI模式,造影過程中儀器參數、增益、機械指數等不變,抽取造影劑2.4 ml,經患者肘前靜脈快速團注,隨后用5 ml生理鹽水沖注,密切觀察病灶的灌注情況及與上述胰周大血管的關系,包括是否接觸、接觸的長度、管腔有無狹窄,并進行評分。在造影延遲相進行肝臟的掃查,觀察轉移情況。操作完成后將圖像刻錄到光盤上保存,記錄全部患者術前CEUS檢查結果、手術探查情況及術后病理結果,并進行對比分析。在評估血管受侵與腫物可切除性時將PV與SMV聯合進行評價。行CEUS檢查前告知所有患者檢查禁忌證及造影過程中可能出現的不良反應。
根據瘤體與周圍血管的關系設定評分標準[5-7]:0分,腫瘤和周圍血管之間有正常組織(包括正常胰腺組織或脂肪組織間隙),血管壁回聲連續、完整無浸潤(圖1a);1分,腫瘤環繞浸潤血管<1/2周或沿血管長軸測定腫瘤和血管的接觸長度<2 cm(圖1b);2分,腫瘤浸潤血管1/2~2/3周或腫瘤與血管的接觸長度>2 cm,并使血管受壓(圖1c);3分,腫瘤完全包繞血管>2/3周或血管壁連續中斷、消失,管腔內可見栓塞形成(圖1d)。
可切除性的評估標準:評分為0~2分者可行手術治療;評分為3分者或多發肝轉移者則不可切除(單獨包裹SPV和SPA除外)。
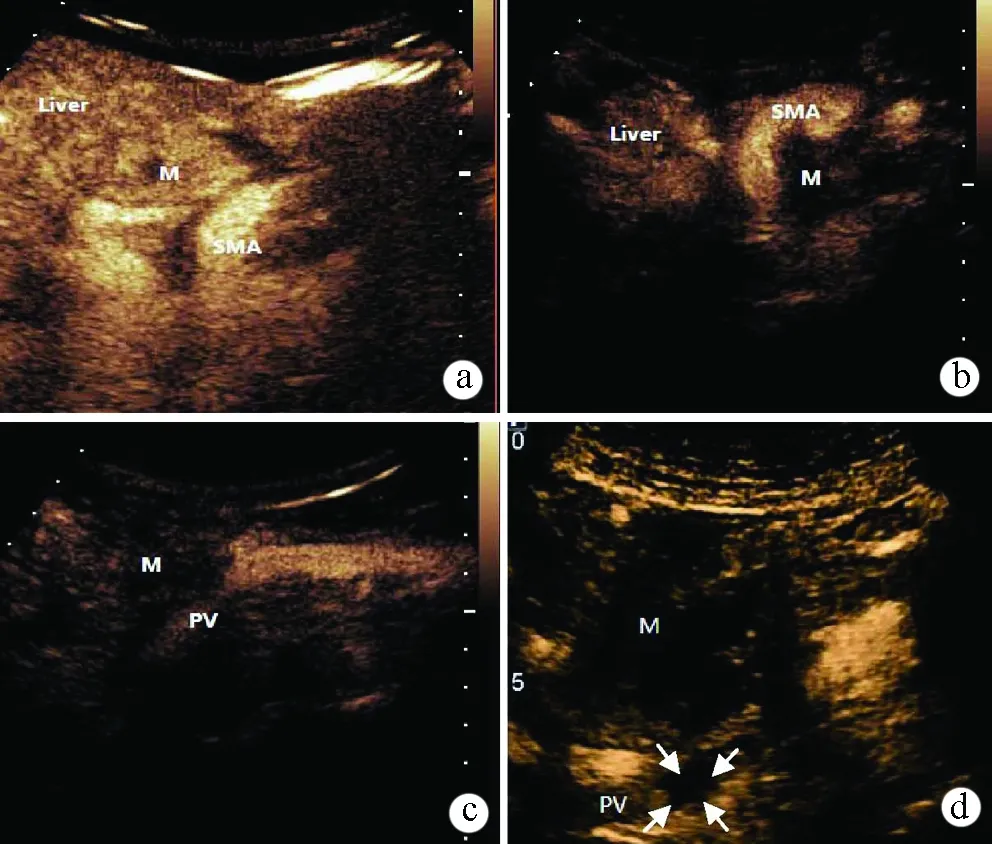
圖1 CEUS檢查結果評分 a:0分,腫物與SMA有正常組織間隙;b:1分,腫物與SMA接觸<2 cm;c:2分,腫物與門靜脈接觸>2 cm,并使血管局部受壓變細;d:3分,門靜脈內可見栓子形成(箭頭所示)。Liver:肝臟;M:腫物
1.3 統計學方法 將術中探查及術后病理結果作為判斷瘤體與胰周大血管的關系及判斷胰腺癌可切除性的金標準,分別計算胰周大血管受侵率、術前CEUS評估胰周血管受侵程度的敏感性、特異性,CEUS評估胰腺癌可切除性的敏感性、特異性、陽性預測值、陰性預測值、總符合率及約登指數。
2 結果
2.1 一般資料 共收集25例患者,其中男13例,女12例,年齡44~65歲,平均(55.8±6.16)歲。18例患者CA19-9升高,其中1例CEA升高;1例患者CEA、CA19-9和CA12-5略高;6例CA19-9正常。
2.2 CEUS評分結果 CEUS評分0分者5例,1分者2例,2分者10例,3分者8例。其中術前CEUS檢查有2例患者于延遲相發現肝臟的轉移灶。
2.3 術前CEUS顯示胰周血管受侵情況 25例患者共42條胰周大血管受侵,其中動脈19條,靜脈23條。CA根部、HA、SPA、SMA、PV、SMV、SPV的受侵率分別為7.1%(3/42)、11.9%(5/42)、16.7%(7/42)、9.5%(4/42)、31.0%(13/42)、11.9%(5/42)、11.9%(5/42)。
2.4 手術情況及病理結果 25例患者中有15 例患者根據手術探查情況實施根治性手術治療,術后病理學結果:胰腺腺癌12例,胰腺導管腺癌1例,胰腺腺鱗癌1例,壺腹部腺癌1例。10例患者根據手術探查情況無法實施根治性手術切除,其中7例實施姑息性手術,3例僅手術探查穿刺活組織檢查。
2.5 CEUS評估胰腺癌侵襲周圍血管的敏感性、特異性 CEUS評估胰腺癌周圍大血管受侵程度與術中判斷相比具有較高的敏感性和特異性(表1)。

表1 CEUS與術中所見評估胰周各大血管受侵結果對比
2.6 CEUS評估胰腺癌可切除性與手術切除結果的一致性比較 術前CEUS評估可切除者17例,術中探查判定可切除15例。CEUS評估胰腺癌可切除性的敏感性為93.3%,特異性為70.0%,總符合率為84.0%,假陽性率為30.0%,假陰性率為6.7%,陽性預測值為82.4%,陰性預測值為87.5%,約登指數為0.633。說明CEUS評估胰腺癌可切除性與術中判斷對比,具有較高的敏感性、特異性及符合率。
3 討論
目前臨床上常用的術前評估的手段主要有增強CT和超聲內鏡(endoscopic ultrasonography, EUS),兩者的敏感性及特異性較高[8-9],但均有其局限性。由于胰腺癌CT檢查多表現為低密度,與周圍正常胰腺組織密度相近,即使增強掃描,對胰腺癌腫瘤大小的估計也存在偏差;此外,增強CT無法進行實時動態觀察。EUS是一種有創性檢查,且無法判斷有無遠處轉移。超聲作為發現胰腺占位性病變的常規檢查,對于評估胰腺癌可切除性方面有一定的準確性[3,5]。超聲造影技術的應用彌補了增強CT和EUS的缺點,通過注射造影劑來增強血液的散射信號強度,提高圖像的對比分辨率,清楚的顯示腫瘤的邊界與周圍血管的關系,其最大優勢在于可以實時動態觀察胰腺腫瘤周圍血管造影增強的全過程,更加直觀地顯示血流灌注狀態以及血管走行、狹窄變形的情況[10-11]。
本研究以術中探查血管受侵情況為金標準, CEUS評估血管受侵的敏感性、特異性較高,與丁維寶[12]報道的相近。由于彩色多普勒易受胃腸道氣體干擾,部分病灶效果不是很滿意,CEUS判斷血管受侵可以彌補彩色多普勒的不足,但CEUS評估SMA受侵的敏感性較低,這可能與SMA位于腹腔干的稍下方,并經胰頭與胰體交界處的后方下行,位置較深,且受腹腔腸氣干擾有關,超聲顯示不是很清晰。其次本研究中有4例胰腺癌患者瘤體位于胰腺鉤突部,由于鉤突與胰頭和胰頸之間夾有SMA,當胰腺鉤突部瘤體較大時可致SMA的顯示率降低。此外本研究的病例數較少,這些都可能是導致CEUS評估SMA受侵的敏感性較低的原因,因此臨床不能忽視CEUS評估SMA的陰性結果,應結合增強CT等其他檢查提高準確性。
應用CEUS評估胰腺癌可切除性,評分為3分或有遠處轉移者為不可切除,因此術前CEUS評估25例患者中17例為可切除,8例為不可切除。術中進行手術探查,15例為可切除,10例為不可切除,其中術前CEUS評估的14例可切除與7例不可切除與術中探查一致,3例假陽性患者中1例為盆腔及大網膜多發轉移而無法實施根治性手術;2例為腫物完全包繞腸系膜上動、靜脈的主干及主要分支起始部而無法實施根治性手術,分析原因可能與腫物位置較深、造影劑在管腔內停留時間較短、觀察受限等有關。此外,本研究中術前CEUS評估假陰性患者1例,術中探查發現雖然腫物侵犯肝動脈及門靜脈,但十二指腸鉗能通過胰頸與門靜脈的間隙,故切除部分肝動脈且與門靜脈分離從而成功切除腫物。分析原因可能是胰腺癌導致胰腺周圍血管的炎癥反應,使周圍脂肪間隙有滲出,圖像顯示模糊,而并非是真正腫瘤侵犯。術前CEUS評估可實施胰腺癌根治性手術切除與術中探查結果相比,符合率較高,具有重要的臨床參考價值。
另外,25例患者中有2例于造影延遲相發現肝臟的轉移灶,但二維圖像上未見明顯異常回聲灶,這2例患者均進行了肝穿刺活組織檢查,病理均證實為肝轉移性腺癌,說明CEUS在發現肝臟轉移灶方面具有明顯優勢。當胰腺癌發生遠處多發轉移時,評估為不可切除,避免了盲目的手術探查。
本研究的局限性在于病例數偏少,選取的病例均為住院患者,尚需大樣本進一步探討和完善。而且由于CEUS僅可以顯示血管腔內血流灌注情況,血管壁的情況顯示欠佳,對結果可能造成一定的影響。另外由于外科手術技術的提高及動、靜脈對于可切除性的標準可能不完全一致,本研究所采用的評估標準可能存在一定的誤差,有待于進一步完善。
[1] Group of Pancreas Surgery, Chinese Society of Surgery, Chinese Medical Association. Guidelines for the management of pancreatic cancer (2014)[J]. J Clin Hepatol, 2014, 30(12): 1240-1245. (in Chinese) 中華醫學會外科學分會胰腺外科學組. 胰腺癌診治指南(2014)[J]. 臨床肝膽病雜志, 2014, 30(12): 1240-1245.
[2] National Comprehensive Cancer Network(NCCN). Clinical practice guideline in oncology. Pancreatic Adenocarcinoma (Version2. 2014)[EB/OL]. https:// www.nccn.org/professionals/hysician-glslf-guidelines.asp.
[3] WANG SC. Preoperative resectability evaluation of pancreatic adenocarcinoma with computer tomographic angio graphy[J]. Chin J Surg Integr Tradit West Med, 2013, 19(5): 502-504. (in Chinese) 王樹成. 血管受侵程度對胰頭癌可切除性影響[J]. 中國中西醫結合外科雜志, 2013, 19(5): 502-504.
[4] YANG YM. Highlights and difficulties in surgical treatment for pancreatic carcinoma[J]. Chin J Dig Surg, 2015, 14(8): 612-614. (in Chinese) 楊尹默. 胰腺癌外科治療的熱點與難點[J]. 中華消化外科雜志, 2015, 14(8): 612-614.
[5] WU CH, LI FH, FANG H, et al. Value of contrast-enhanced ultrasound in evaluating resectability of pancreatic carcinoma[J]. J Shanghai Jiaotong Univ:Med Sci, 2010, 30(10): 1217-1220. (in Chinese) 吳春華, 李鳳華, 方華, 等.超聲造影在胰腺癌可切除性評估中的價值[J]. 上海交通大學學報(醫學版), 2010, 30(10): 1217-1220.
[6] YANG B, XU L, WU ZY, et al. Assessment of resectability of pancreatic head and periampullary tumors by color Doppler flow imaging[J]. Chin J Ultrasonogr, 2000, 9(2): 94-95. (in Chinese) 楊斌, 徐琳, 吳志勇, 等. 彩色多普勒血流顯像在胰頭和壺腹周圍癌可切除性評估中的應用價值[J].中國超聲影像學雜志, 2000, 9(2): 94-95.
[7] LI FS, HUO XL, MA SR, et al. Value of color Doppler ultrasound in evaluating vascular invasion and resectability of pancreatic head carcinoma[J]. J Mod Oncol, 2004, 12(5): 463-464. (in Chinese) 李逢生, 霍興隆, 馬社榮, 等. 彩色多普勒超聲在胰頭癌血管浸潤及切除問題中的應用價值[J]. 現代腫瘤醫學, 2004, 12(5): 463-464.
[8] WANG SC. Advances in radiological research on preoperative staging and resectability evaluation of pancreatic cancer[J]. Chin J Surg Integr Tradit West Med, 2013,19(1): 103-104. (in Chinese) 王樹成. 胰腺癌術前分期及可切除性評估的影像學研究進展[J]. 中國中西醫結合外科雜志, 2013, 19(1): 103-104.
[9] RICHARDSON W, STEFANIDIS D, MITTAL S,et al. Sages guidelines for the use of laparoscopic ultrasound [J]. Surg Endosc, 2010, 24(4): 745-756.
[10] POSTEMA M, GILJA OH. Contrast-enhanced and targeted ultrasound [J]. World J Gastroenterol, 2011, 17(1): 28-41.
[11] ROSSI S, GHITTONI G, RAVETTA V, et al. Contrast-enhanced ultrasonography and spiral computed tomography in the detection and characterization of portal vein thrombosis complicating hepatocellular carcinoma[J]. Eur Radiol, 2008, 18(8): 1749-1756.
[12] DING WB. Advances of resectability evaluation of pancreatic cancer[J]. Clin J Curr Adv Gen Surg, 2005, 8(6): 331-333. (in Chinese) 丁維寶. 胰頭癌可切除性評估研究進展[J].中國現代普通外科進展, 2005, 8(6): 331-333.
引證本文:LIU Z, TANG SS. Value of contrast-enhanced ultrasound in evaluating peripancreatic vascular invasion and resectability of pancreatic cancer[J]. J Clin Hepatol, 2017, 33(1): 126-129. (in Chinese) 劉站, 唐少珊. 超聲造影評估胰腺癌周圍血管受侵程度及可切除性的應用價值[J]. 臨床肝膽病雜志, 2017, 33(1): 126-129.
(本文編輯:朱 晶)
Value of contrast-enhanced ultrasound in evaluating peripancreatic vascular invasion and resectability of pancreatic cancer
LIUZhan,TANGShaoshan.
(DepartmentofUltrasound,ShengjingHospitalofChinaMedicalUniversity,Shenyang110004,China)
Objective To investigate the value of preoperative contrast-enhanced ultrasound (CEUS) in evaluating peripancreatic vascular invasion and resectability of pancreatic cancer. Methods A retrospective analysis was performed for the clinical data of 25 patients with pancreatic cancer confirmed by surgical exploration or postoperative pathological examination, who visited Shengjing Hospital of China Medical University from December 2012 to October 2014, and all the patients underwent CEUS before surgery. The relationship between the lesion and the peripancreatic vessels was observed, the degree of invasion was evaluated, and related scores were measured. These results were compared with the results of intraoperative exploration and postoperative pathological results. The rate of peripancreatic vascular invasion, sensitivity and specificity of preoperative CEUS in evaluating the degree of peripancreatic vascular invasion, and sensitivity, specificity, positive predictive value, negative predictive value, overall coincidence rate, and Youden index of CEUS in evaluating the resectability of pancreatic cancer were calculated. Results Preoperative CEUS showed that 42 vessels were invaded, while intraoperative exploration showed 41 vessels were invaded. A total of 17 patients were considered resectable by CEUS, while 15 patients were considered resectable by intraoperative exploration. In evaluating the resectability of pancreatic cancer, CEUS had a sensitivity of 93.3%, a specificity of 70.0%, an overall coincidence rate of 84.0%, a false positive rate of 30.0%, a false negative rate of 6.7%, a positive predictive value of 82.4%, a negative predictive value of 87.5%, and a Youden index of 0.633. Conclusion Compared with intraoperative exploration, CEUS has higher sensitivity and specificity in evaluating the degree of peripancreatic vascular invasion and higher sensitivity, specificity, and coincidence rate in evaluating the resectability of pancreatic cancer. CEUS can accurately evaluate the degree of peripancreatic vascular invasion and provides a new method for preoperative evaluation of the resectability of pancreatic cancer.
pancreatic neoplasms; pancreatectomy; contrast-enhanced ultrasound
10.3969/j.issn.1001-5256.2017.01.027
2016-11-07;
2016-12-02。
劉站(1988-),女,主要從事腹部超聲診斷方面的研究。
唐少珊,電子信箱:tangss@sj-hospital.org。
R735.9
A
1001-5256(2017)01-0126-04

