糖皮質激素聯合慢作用抗風濕藥治療類風濕關節炎的臨床觀察
李 爽,楊旭玲
糖皮質激素聯合慢作用抗風濕藥治療類風濕關節炎的臨床觀察
李 爽,楊旭玲
目的 觀察小劑量糖皮質激素聯合慢作用抗風濕藥物治療類風濕關節炎的臨床療效。方法 將76例初發類風濕關節炎患者隨機分為小劑量糖皮質激素聯合慢作用抗風濕藥物組(激素聯合治療組,共38例)及慢作用抗風濕藥物治療組(對照組,共38例),兩組均給予慢作用抗風濕藥物,其中激素聯合治療組另給予小劑量糖皮質激素,對照組給予洛索洛芬鈉治療,全部患者在治療前與治療后2、4、12、24周檢測臨床指標、免疫學指標及足跟骨密度值。結果 治療后聯合治療組VAS評分、DAS28評分及ESR、CRP水平與治療前、同期對照組相比,差異均有統計學意義(P<0.05)。治療24周,兩組足跟骨密度值比較差異無統計學意義(P>0.05)。結論 小劑量糖皮質激素聯合慢作用抗風濕藥物可在短期內明顯緩解臨床癥狀,降低炎性指標,且短期內未見增加骨質疏松風險。
糖皮質激素;慢作用抗風濕藥;類風濕關節炎;骨密度
0 引言
類風濕關節炎(Rheumatoid Arthritis,RA)是以侵蝕性、對稱性多關節炎為主要臨床表現的慢性、全身性自身免疫性疾病。其病理基礎為滑膜血管翳的形成,臨床表現為關節軟骨和骨破壞,最終導致關節畸形和功能喪失,是造成人類喪失勞動力和致殘的主要原因之一;同時導致其多臟器受累,是該疾病預后不良甚至死亡的主要原因。在我國,類風濕性關節炎的發病率在0.32%~0.36%。
目前RA患者是否應用糖皮質激素進行治療備受爭議。傳統觀念認為,糖皮質激素不良反應大,不宜治療類風濕關節炎。近10多年來,許多國內外文獻報道小劑量糖皮質激素能有效且安全地控制類風濕關節炎,有減慢類風濕關節炎骨破壞的作用,甚至比現有的慢作用抗風濕藥物(Disease-modifying anti-rheumatic drugs,DMARDs)作用強,可迅速緩解關節癥狀,小劑量運用療效可靠,并且不良反應小[1]。本研究觀察小劑量糖皮質激素聯合慢作用抗風濕藥物治療類風濕關節炎的療效,現將結果報道如下。
1 資料與方法
1.1 一般資料 病例來源均為我院2012年1月至2013年12月門診及住院初診患者,共76例,病史均在1年之內,未經類固醇類激素及免疫抑制劑系統用藥治療,且均符合2010年EULAR對類風濕關節炎評分標準[2],評分≥6分。將76例患者隨機分為2組,聯合治療組 38例,男12例,女26例,年齡32~76歲,平均51歲;對照組38例,男8例,女30例,年齡38~67歲,平均54歲,所有病例均排除其他結締組織病、感染性疾病及重要臟器功能不全等疾病。
1.2 研究方法 聯合治療組給予患者醋酸潑尼松10 mg,晨起1次口服;對照組給予患者洛索洛芬鈉60 mg,2次/d,口服。連續2周。兩組同時給予來氟米特20 mg,1次/d,口服,硫酸羥氯喹0.2 g,2次/d,口服。兩組患者均在治療前和接受治療后2、4、12、24周時進行臨床指標觀察及血清學檢查,并在接受治療前和接受治療后各階段,按照統一測定方法測定右足跟骨密度T值。
1.3 測量指標
1.3.1 臨床觀察指標 對兩組患者治療前后疼痛癥狀通過視覺模擬評分法(Visual analogue scale,VAS)進行評估,記錄關節腫脹數、關節壓痛數,計算疾病活動性(DAS)28評分。參照Prevoo等[3]對周身28個關節的評分,判斷標準為DAS28>5.1表示疾病活動,DAS28<3.2表示疾病活動度低,DAS28<2.6表示疾病緩解。
1.3.2 血清檢測指標 監測血沉(ESR)、超敏C反應蛋白(CRP)、類風濕因子(RF)。
1.3.3 足跟骨密度檢測 治療前后對兩組患者進行骨密度檢查,檢測儀器采用美國HOLOGIC公司的超聲波干式骨密度測定儀(型號Sahara)。檢測標準:T≥-1.5為正常,T>-2.5為骨量下降,T≤-2.5為骨質疏松。
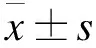
2 結果
2.1 兩組患者臨床指標比較 治療前兩組患者臨床觀察指標、免疫學指標及足跟骨密度值比較差異均無統計學意義(P>0.05)。治療后兩組患者關節腫脹數、關節壓痛數在同一時期比較,聯合治療組優于對照組(P<0.05)。見表1。
2.2 自我疼痛評分(VAS)及DAS28評分 在同一時期聯合治療組均優于對照組,兩組比較差異具有統計學意義(P<0.05)。治療后24周,對照組類風濕關節炎疾病活動度下降;聯合治療組在治療后4周開始逐漸出現疾病活動度下降,治療后12周,疾病緩解。見表1。
2.3 免疫學指標檢測結果 治療前,兩組血清學指標比較差異均無統計學意義(P>0.05)。聯合治療組治療后ESR、CRP與治療前、與同期對照組比較,差異有統計學意義(P<0.05)。足跟骨密度檢測結果:兩組患者治療前足跟骨密度指標比較差異無統計學意義。治療后24周,聯合治療組患者右足跟骨密度與對照組及治療前相比差異無統計學意義(P>0.05)。見表1。
2.4 兩組不良反應發生情況 兩組均未出現明顯的不良反應。

表1 兩組臨床指標、免疫學指標及骨密度值比較
注:與同組治療前比較,*P<0.05;與同期對照組比較,ΔP<0.05
3 討論
類風濕關節炎目前發病機制尚不明確,可能與感染、遺傳、免疫機制異常等因素有關[4-5]。其臨床表現為關節腫脹、關節疼痛,以及在疾病發展過程中出現骨侵蝕、骨破壞、關節畸形,給患者帶來極大的軀體痛苦及精神壓力,生活質量明顯下降,并具有致殘性。在疾病早期,給予系統抗風濕治療對改善預后有重要意義。
近年來,對于活動期類風濕關節炎的早期治療,應用小劑量糖皮質激素聯合慢作用抗風濕藥已被廣泛認可。美國風濕病協會在2002年修訂的類風濕關節炎的治療指南中,將每日10 mg的醋酸潑尼松列為類風濕關節炎的治療方法之一[6]。在活動性類風濕關節炎早期,給予小劑量糖皮質激素,不僅可以高效、快速地減輕患者關節腫脹、疼痛等臨床癥狀,同時因其可進入胞漿,與胞漿內糖皮質激素受體相結合,激活受體,從而抑制相應炎性因子的表達和釋放[7],有效抑制炎性反應。而且,Everdingen等[8-10]分別對不同劑量糖皮質激素進行對比分析,結果提示,小劑量糖皮質激素(≤10 mg/d)對類風濕關節炎的關節損傷與破壞有抑制作用,可明顯減少類風濕關節炎患者受累關節的 X線進展。在我國,因糖皮質激素對糖脂代謝、離子代謝、骨代謝血壓、心腦血管系統及胃腸黏膜不良事件發生的影響等,導致臨床醫師對糖皮質激素的應用采取比較保守的態度。
本研究嘗試應用小劑量糖皮質激素聯合慢作用抗風濕藥物治療后,同一時期,治療組在關節腫脹、壓痛、自我疼痛評分及DAS28評分等方面,均明顯優于同期對照組。類風濕關節炎疾病的發展過程中,因炎癥因子激活破骨細胞,而成骨細胞不能有效代償,導致骨丟失多于骨形成,進而出現受累的關節局部及全身的骨量減少,導致骨質疏松形成[11]。本研究發現,用藥治療24周后,兩組患者足跟骨密度測得值比較差異無統計學意義(P>0.05)。短期應用小劑量糖皮質激素對骨質代謝的影響,與本身疾病進展導致骨質疏松差異無統計學意義。同時本研究顯示,聯合治療組在治療過程中未出現明顯不良反應,考慮可能與口服糖皮質激素劑量較小,口服藥物時間短有關。
在我國,絕大多數RA患者收入不高,無力支付與糖皮質激素聯合DMARDs療效相當但價格比其高幾十倍的生物制劑治療費用[12]。因此,在類風濕關節炎治療早期,給予糖皮質激素聯合慢作用抗風濕藥物,不僅可以快速有效地緩解患者痛苦,降低臨床炎性指標,還能增加患者治療的依從性,改善患者預后,同時降低患者的治療成本,值得臨床推廣。
[1] Strand V,Simon LS.Low dose glucocorticoids in early rheumatoid arthritis[J].Clin Exp Rheumatol,2003,21(5 Suppl 31):S186-S190.
[2] Aletaha D,Neogi T,SIlman A,et al.2010 rheumatoid arthritis classification criteria:an America College of Rhuematology/European League Against Rheumatism collaborative initiative [J].Ann Rheum Dis,2010,62(9):1580-1588.
[3] Prevoo ML,Vant′ Hof MA,Kuper HH,et al.Modified disease activity scores that include twenty-eight-joint counts.Development and validation in a prospective longitudinal study of patients with rheumatoid [J].Arthritis Rhuem,1995,38(1):44-48
[4] 薛麗巾,王秦,羅靜,等.類風濕關節炎患者外周血T淋巴細胞亞群于臨床相關性分析[J].中國醫藥,2011,6(6):692-694.
[5] 劉健,謝秀麗,盛長健,等.老年類風濕關節炎患者蛋白質代謝變化及相關因素分析[J].中國臨床醫學,2010,17(2):278-281.
[6] American College of Rheumatology Subcommittee on Rheumatoid Arthritis Guidelines.Guidelines for the management of rheumatoid arthritis:2002 update[J].Arthritis Rheum,2002,136(11):328-346.
[7] Rainer HS,Rheumatoid arthritis-a neuroendocrine immune disorder:glucocorticoid resistance,relative glucocorticoid deficiency,low-dose glucocorticoid therapy,and insulin resistance[J].Straub Arthritis Res Ther,2014,16(Suppl 2):I1
[8] Van Everdingen AA,Jacobs JW.Siewertsz van RDR.et al.Low-dose prednisone therapy for patients with early active rheumatoid arthritis:clinical efficacy,disease-modifying properties,and side effects[J].Ann Intern Med,2002,136:1-12
[9] Kirwan JR.The effect of glucocorticoids on joint destruction in rheumatoid arthritis[J].N Engl J Med,1995,333:142-146
[10]Wassenberg S,Rau R,Steinfeld P,et al.Very low-dose prednisolone in early rheumatoid arthritis retards radiographic progression over two years:a multicenter,double-blind,placebo-controlled trial[J].Arthritis Rheum,2005,52(11):3371-3380.
[11]Broy SB,Tanner SB.Official Positions for FRAX (R) clinical regarding rheumatoid arthritis from joint official positions development conference of the international society for clinical densitometry and international osteoporosis foundation on FRAX (R) [J].J Clin Densitom, 2011,14(3):184-189.
[12]施桂英.糖皮質激素聯合改變病情抗風濕藥物對早期類風濕關節炎治療作用的再評價[J].中華風濕病學雜志,2013,1(17):1-4.
Clinical observation of glucocorticoid and DMARDs treatment for rheumatoid arthritis
LI Shuang,YANG Xu-ling
(Central Hospital Affiliated to Shenyang Medical College,Shenyang 110024,China)
Objective To explore the efficacy of low-dose glucocorticoid and modifying anti-rheumatic drugs in the treatment of rheumatoid arthritis(RA).Methods Totally 76 cases of RA patients were divided into two groups:low-dose glucocorticoid and DMARDS group (combination therapy group,n=38),DMARs group (control group,n=38).Both groups were given the same DMARDs,and the combination therapy group was also given low-dose glucocorticoid.All the clinical and immunological variables were measured at baseline and 2,4,12 and 24 weeks after treatment.Bone mineral density (BMD) was measured at baseline and 24 weeks after treatment.Results Compared with prior treatment and control group,there was significant difference in VAS scores,DAS 28 scores and the levels of ESR and CRP in combination therapy group (P<0.05).There was no significant difference in bone mineral density between the two groups (P>0.05).Conclusion The treatment of low-dose glucocorticoid and DMARDs is effective in improving the clinical symptoms and immunological variables without the risks of osteoporosis in short time.
Glucocorticoid;Modifying anti-rheumatic drugs;Rheumatoid arthritis;Bone mineral density
2016-09-12
沈陽醫學院附屬中心醫院,沈陽 110024
10.14053/j.cnki.ppcr.201701012

