小麥干熱風抗性鑒定及熱脅迫相關基因TaHSPs的表達分析
李美玲,孫愛清,楊 敏,張杰道,王振林,陳蕾太,陳路路,馬雪麗,尹燕枰
(山東農業大學農學院/作物生物學國家重點實驗室/山東省作物生物學重點實驗室,山東泰安 271018)
小麥干熱風抗性鑒定及熱脅迫相關基因TaHSPs的表達分析
李美玲,孫愛清,楊 敏,張杰道,王振林,陳蕾太,陳路路,馬雪麗,尹燕枰
(山東農業大學農學院/作物生物學國家重點實驗室/山東省作物生物學重點實驗室,山東泰安 271018)
為鑒定黃淮麥區小麥品種干熱風抗性以及不同抗性品種熱激蛋白(TaHSPs)基因的表達差異,以98個小麥品種為試驗材料,于花后10~20 d進行人工模擬干熱風處理,通過測定小麥不同生長時期的葉綠素含量、收獲后的千粒重與籽粒品質,評價不同品種干熱風抗性;對篩選出的干熱風抗性不同的品種在出苗15 d進行熱脅迫處理,通過熒光定量PCR測定熱脅迫0~4.5 h內TaHSPs基因表達量的變化。結果表明,干熱風處理后,供試小麥品種旗葉的葉綠素含量均降低,高抗干熱風品種降幅較小,熱敏感型品種降幅較大;供試小麥品種的千粒重均降低。山農23號等3個品種達到高、中抗干熱風等級,且抗性比較穩定,師欒02-1為熱敏感型品種。干熱風處理后籽粒蛋白質含量升高,總淀粉含量降低,抗干熱風小麥品種總淀粉相對含量降幅較小。不同小麥品種幼苗在熱脅迫0~4.5 h期間,TaHSPs基因表達量均為拋物線趨勢,抗干熱風品種在熱脅迫1 h時 TaHSP16.9基因表達上調幅度大于熱敏感型品種。對于 TaHSP17.8基因,抗干熱風品種在熱脅迫期間,上調表達反應時間均早于熱敏感型品種;在熱脅迫0.5 h時,山農23號、周麥18與泰山9818三個抗干熱風品種基因表達均上調至590倍以上,而師欒02-1與濟南17號的上調幅度在300倍以下。對于 TaHSP23.6基因,山農23號的上調表達峰值遠高于其他品種。對于 TaHSP26.6基因,熱敏感型品種在熱脅迫后期的上調倍數高于抗干熱風品種,師欒02-1與濟南17號兩個熱敏感型品種在熱脅迫4.5 h時上調幅度均在4 000倍以上,而抗干熱風品種山農23號、周麥18與泰山9818上調幅度均在3 000倍以下。
小麥;干熱風;千粒重;抗逆指數;熱激蛋白
干熱風是中國北方麥區的主要氣象災害之一,發生在每年5月中下旬到6月初的高溫少雨天氣,此時正值小麥灌漿期,高溫低濕使得籽粒灌漿期縮短,造成小麥產量、品質嚴重下降。高溫對小麥產量和穗粒數有顯著影響[1],對籽粒蛋白質的影響也明顯高于水分、干旱等其他脅迫對蛋白質的影響[2-3]。高溫主要通過影響小麥淀粉的形成而影響其品質,蛋白質相對含量的提高也與淀粉合成減少有關[4-6]。劉 萍等[4]研究表明,灌漿期溫度超過30 ℃,小麥淀粉的形成受到抑制,且在花后25~27 d受影響程度最大。李永庚等[5]研究表明,灌漿后期高溫會提高小麥蛋白質的含量,主要原因是籽粒淀粉積累減少。
防御干熱風的關鍵在于選用適宜當地播種的抗干熱風品種,因此,鑒定、篩選抗干熱風小麥品種、研究其抗性相關指標具有重要意義。儀小梅等[7]于2011-2013年以旗葉功能期抗逆指數和千粒重抗逆指數為鑒定指標,對黃淮麥區部分小麥品種進行了干熱風抗性鑒定,篩選出一批干熱風抗性好的品種。有研究表明,葉綠素是評價植物抗逆境脅迫、尤其是熱脅迫的一個關鍵性指標[8-10]。Kumar等[11]認為,從分子生物學角度研究小麥抗性,是當前研究小麥抵御高溫危害的趨勢。不同基因型小麥的耐熱性不同,可能與熱激蛋白的表達、轉錄因子以及其他相關基因有關[12]。Miller等[13]研究表明,熱激蛋白可以通過提高植物的光合效率、改變同化物的分配、提高水分和營養成分的利用效率、增強細胞膜穩定性等生理作用提高植物體應對高溫脅迫的能力[14]。在熱激蛋白中,12~45 kD小分子量熱激蛋白種類最豐富,且在植物生長的各個階段都有分布,植物在遭遇高溫時,其表達量會在短時間內異常升高,是植物耐高溫脅迫的關鍵[15-16]。郭秀林等[17]研究表明,耐熱小麥品種受高溫脅迫后會激發更強的抗性基因表達。Lee等[18]發現, EsHSP16.9基因表達量升高可以提高野生黑麥的抗逆性。Abu-Romman[19]研究發現, TdHSP23.5 與 TdHSP26.5基因在高抗性小麥品種中表達量高于低抗品種。上述研究主要涉及高溫對小麥產量和品質或對小麥品種某個熱激蛋白的影響,而在田間模擬干熱風脅迫鑒定小麥品種的干熱風抗性,并利用多個熱抗性不同的品種同時分析多個熱激蛋白表達的報道較少。本研究在儀小梅等[7]研究的基礎上,田間模擬干熱風脅迫,根據傳統指標對黃淮麥區小麥品種干熱風抗性進行鑒定,并利用分子生物學方法研究干熱風抗性不同的多個小麥品種的小分子熱激蛋白基因(TaHSPs)的表達差異,分析小麥干熱風抗性與TaHSPs基因表達的關系,以期為小麥品種的合理布局和灌漿期小麥干熱風抗性鑒定提供參考依據。
1 材料與方法
1.1 試驗材料
供試材料為98個小麥品種,分別于2014、2015兩年進行鑒定,部分品種在兩年內均有鑒定,詳情見表1。
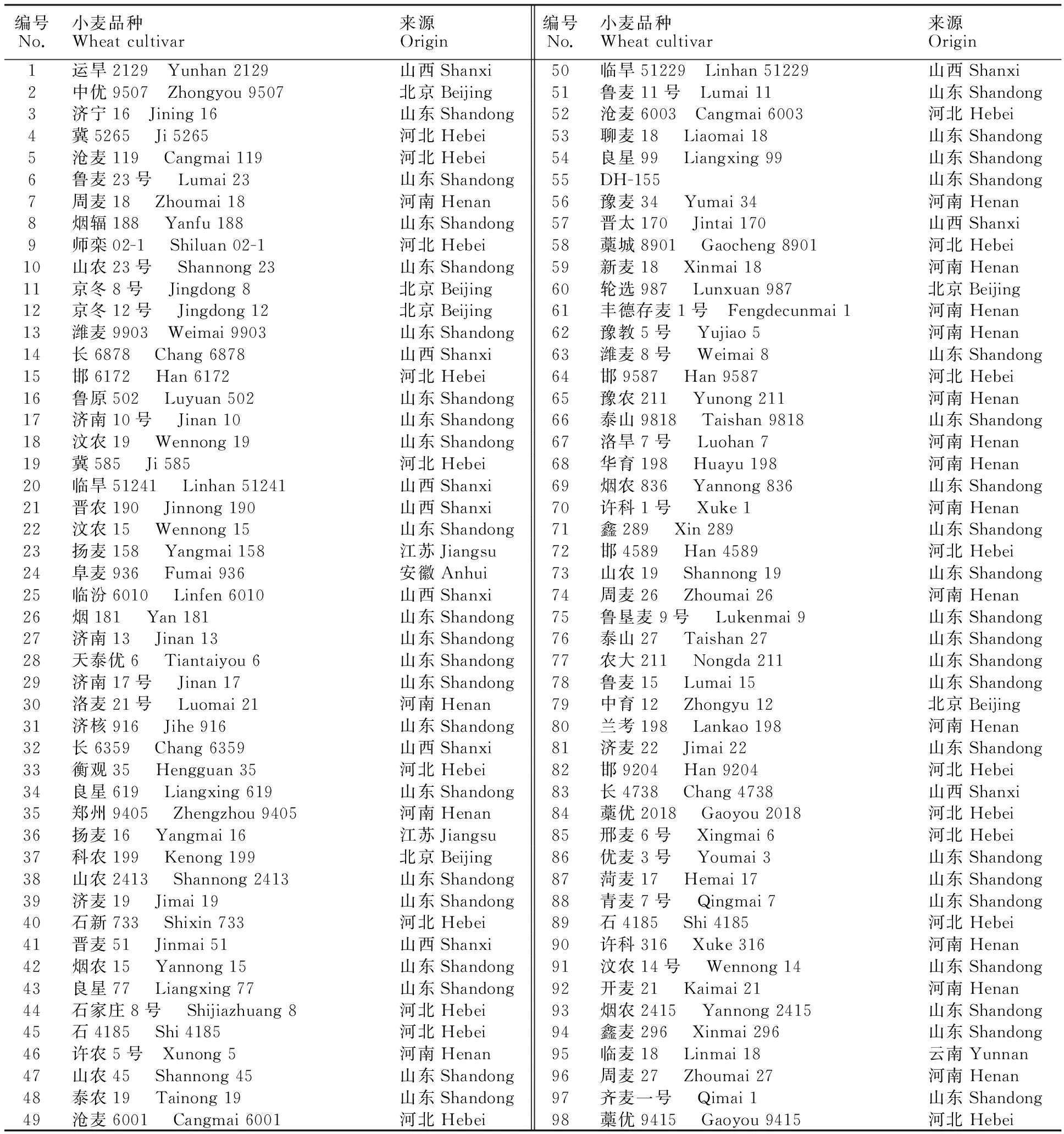
表1 供試小麥品種Table 1 Wheat cultivars tested in this study
1~10:兩年重復鑒定品種;11~60:2014年鑒定品種;61~98:2015年鑒定品種。
1-10:Wheat cultivars with repetitive identification in two years; 11-60:Wheat cultivars identified in 2014; 61-98:Wheat cultivars identified in 2015.
1.2 試驗設計
灌漿期干熱風處理試驗于2013-2014和2014-2015兩個小麥生長季在山東農業大學農學試驗站完成。試驗采用裂區設計,主區為干熱風處理,副區為品種,以正常生長為對照;3次重復。于小麥花后10 d進行人工模擬干熱風處理,處理時間為每天9:00~16:00,通過人工氣候室中智能控溫、控濕系統控制溫、濕度,溫度低于38 ℃系統自動加溫,溫度高于40 ℃時,手動開窗散熱,連續10 d進行模擬干熱風處理。期間采用Davis氣象儀記錄溫、濕度等氣象數據。
在預試驗基礎上,選取小麥品種周麥18、山農23號、濰麥9903、魯麥23號、藁城8901、滄麥6003、師欒02-1及濟南17號用于灌漿期干熱風處理期間葉綠素的測定。
山農23號、周麥18、泰山9818、師欒02-1及濟南17號用于苗期高溫誘導相關基因TaHSPs的表達測定。苗期TaHSPs基因的表達測定于2015年9月18日至2015年10月6日在山東農業大學國家重點實驗室進行。選取飽滿一致的種子,點播于穴盤的基質中,待幼苗在室外長至10 d后,轉移至光照培養箱中繼續培養。光暗比14/10,溫度22/17 ℃,相對濕度為60%,培養5 d后分別置于38 ℃和25 ℃培養箱,分別于處理0、0.5、1.0、1.5、2.5、3.5、4.5 h后剪取小麥葉片于2 mL離心管中,液氮速凍后保存于-80 ℃冰箱中備用。3次重復。
1.3 測定項目與方法
1.3.1 葉綠素和千粒重測定
葉綠素含量測定:在小麥抽穗期選取長勢一致的穗子掛牌標記,每個品種標記20個單莖,利用SPAD 502葉綠素儀測定小麥干熱風處理前、中、后期旗葉的SPAD值。
千粒重測定:選用百粒法測千粒重。
1.3.2 小麥品種抗性評定
采用儀小梅等[7]提出的千粒重抗逆指數評價小麥干熱風抗性,抗逆指數≥100為高抗干熱風品種(HR),90~99之間為中抗干熱風品種(R),80~89之間為低抗干熱風品種(LR),小于80為敏感干熱風品種(S)。
1.3.3 品質性狀的測定
用近紅外谷物分析儀測定不同小麥品種籽粒淀粉、蛋白質含量,3次重復。
1.3.4 基因表達量的測定
采用熒光定量PCR方法測定1.2中于-80 ℃保存小麥葉片的小分子熱激蛋白基因 TaHSP16.9、 TaHSP17.8、 TaHSP23.6、 TaHSP26.6的表達量。擴增體系為20 μL,10 μmol·L-1的上下游引物各0.4 μL,10 μL 2×SYBR,0.4 μL ROX Reference Dye,2 μL稀釋后的cDNA,用ddH2O補足至20 μL。PCR擴增程序:95 ℃預變性30 s;95 ℃變性5 s,60 ℃ 30 s;75 ℃ 34 s,40個循環。RNA的提取按照RNAiso Plus C Takara說明書進行。用紫外分光光度計測量RNA濃度與純度;用1%瓊脂糖凝膠電泳法檢測RNA的完整性。RNA的反轉錄試劑盒(RR047A)與熒光定量試劑盒(RR420A)均購自大連寶生物工程有限公司。所用引物見表2,由北京六合華大基因科技有限公司合成。
1.4 數據分析
用Microsoft Excel 2003進行數據分析與作圖,用DPS v7.05進行差異顯著性分析。

表2 小分子熱激蛋白基因表達分析所用引物Table 2 Primers used in the expression analysis of TaHSPs gene
2 結果與分析
2.1 干熱風對小麥旗葉SPAD值的影響
由圖1可知,小麥灌漿期經干熱風處理后,不同抗性品種旗葉的SPAD值均有不同程度下降,處理前期下降緩慢,后期下降幅度較大;藁城8901、滄麥6003、師欒02-1、濟南17號4個熱敏感型品種葉綠素含量下降幅度較大,在熱脅迫10 d后SPAD值低于周麥18、山農23號、濰麥9903、魯麥23號4個抗干熱風品種。其中,干熱風抗性強的山農23號旗葉的SPAD值大于50,降低幅度最小。

Gaocheng 8901:藁城8901;Cangmai 6003:滄麥6003;Shiluan 02-1:師欒02-1;Jinan 17:濟南17號;Zhoumai 18:周麥18;Shannong 23:山農23號;Weimai 9903:濰麥9903;Lumai 23:魯麥23號。

圖1 8個小麥品種經干熱風處理不同時期后旗葉的葉綠素含量
DH:干熱風處理;CK:對照;HR:高抗干熱風;R:中抗干熱風;LR:低抗干熱風;S:干熱風敏感型。同一品種數據后不同字母表示處理與對照在5%水平下差異顯著。表4至表8同。
DH:Dry-hot wind treatment; CK:Control;TKW:Thousand kernal weight;AITKW:Adversity index of TKW;HR:High resistant to dry-hot wind; R:Resistant to dry-hot wind; LR:Low resistant to dry-hot wind; S:Sensitive to dry-hot wind. Different letters following data of the same variety mean significant difference at 5% level between dry-hot wind stress and CK. The same in table 4-8.
2.2 干熱風對小麥千粒重的影響
由表3、表4可知,98個小麥品種經干熱風處理后,千粒重均有不同程度下降。2014年的運旱2129、京冬8號等4個品種與2015年的山農23號、豐德存麥1號等5個品種經干熱風處理后,千粒重平均下降6 g左右,抗逆指數達到100%以上,屬高抗干熱風品種;2014年的濟寧16、濰麥9903等8個小麥品種與2015年的周麥18、豫農211等8個小麥品種千粒重平均下降7.6 g左右,抗逆指數達到90%以上,屬中抗干熱風品種。2014年的邯6172、魯原502等16個小麥品種與2015年的鑫289、冀5265等13個小麥品種千粒重平均下降8 g左右,抗逆指數大于80%,為低抗干熱風品種。2014年的洛麥21號與濟核916等32個小麥品種與2015年的魯麥15、中育12等22個品種千粒重平均下降10 g以上,抗逆指數均小于80%,為熱敏感型品種,占到供試品種的二分之一。
共10個品種在2014與2015年均有鑒定,其中山農23號、運旱2129與周麥18三個品種在兩年抗性鑒定中的抗逆指數均達到90%以上,抗性比較穩定,屬于抗干熱風品種;冀5265、魯麥23號、滄麥119、濟寧16號與中優9507五個品種在兩年抗性鑒定中,抗性表現不穩定,2014年表現為中抗與高抗干熱風,2015年表現為低抗干熱風;2014年篩選出的熱敏感型小麥品種師欒02-1,在2015年的重復鑒定中,抗逆指數在70%以下,抗性表現仍比較差。

表4 2015年鑒定小麥品種的千粒重及其抗逆指數與抗性等級Table 4 Classification of wheat cultivars in 2015 based on adversity resistance index of 1 000-kernel weight
2.3 干熱風對小麥品質的影響
2.3.1 干熱風對蛋白質含量的影響
表5、表6顯示,98個小麥品種中,除2014年鑒定的中優9507、魯麥23號2個品種和2015年鑒定的山農23號等6個品種,其余品種的蛋白質含量經干熱風處理后均升高。2014年鑒定品種中(表5),蛋白質含量增幅在-1.73%~26.67%之間,其中,中優9507蛋白質含量變化最小,僅比對照降低0.25%,而豫麥34變化幅度最大,在干熱風處理后,蛋白質含量升高26.67%。2015年鑒定品種中(表6),蛋白質含量變化幅度在-11.43%~19.64%之間,其中,滄麥119變化幅度最小,蛋白質相對含量僅比對照高0.64%,而菏麥17變化幅度最大,處理后升高19.64%。
蛋白質含量的增幅與干熱風抗性等級存在一定關系,2014年鑒定的小麥品種中(表5),高抗小麥品種(HR)經干熱風處理后,蛋白質含量增幅均在10%以下,而大部分熱敏感型品種(S)蛋白質含量增幅均15%以上,甚至高于20%。表6顯示,2015年鑒定的小麥品種中,高抗干熱風品種(HR)的蛋白質含量增幅均在10%以下,同樣,大部分的熱敏感型品種(S)蛋白質含量增幅在15%以上。高抗干熱風品種經干熱風處理后蛋白質含量升高幅度顯著低于熱敏感型品種(P<0.05)。對兩年鑒定小麥品種的抗逆指數與蛋白質含量增幅分別進行相關性分析發現,2014年、2015年鑒定品種的相關系數分別為-0.681與-0.659(P≤0.01),均表現為極顯著負相關。

表5 2014年鑒定小麥品種的蛋白質含量Table 5 Protein content of wheat cultivars identified in 2014 %
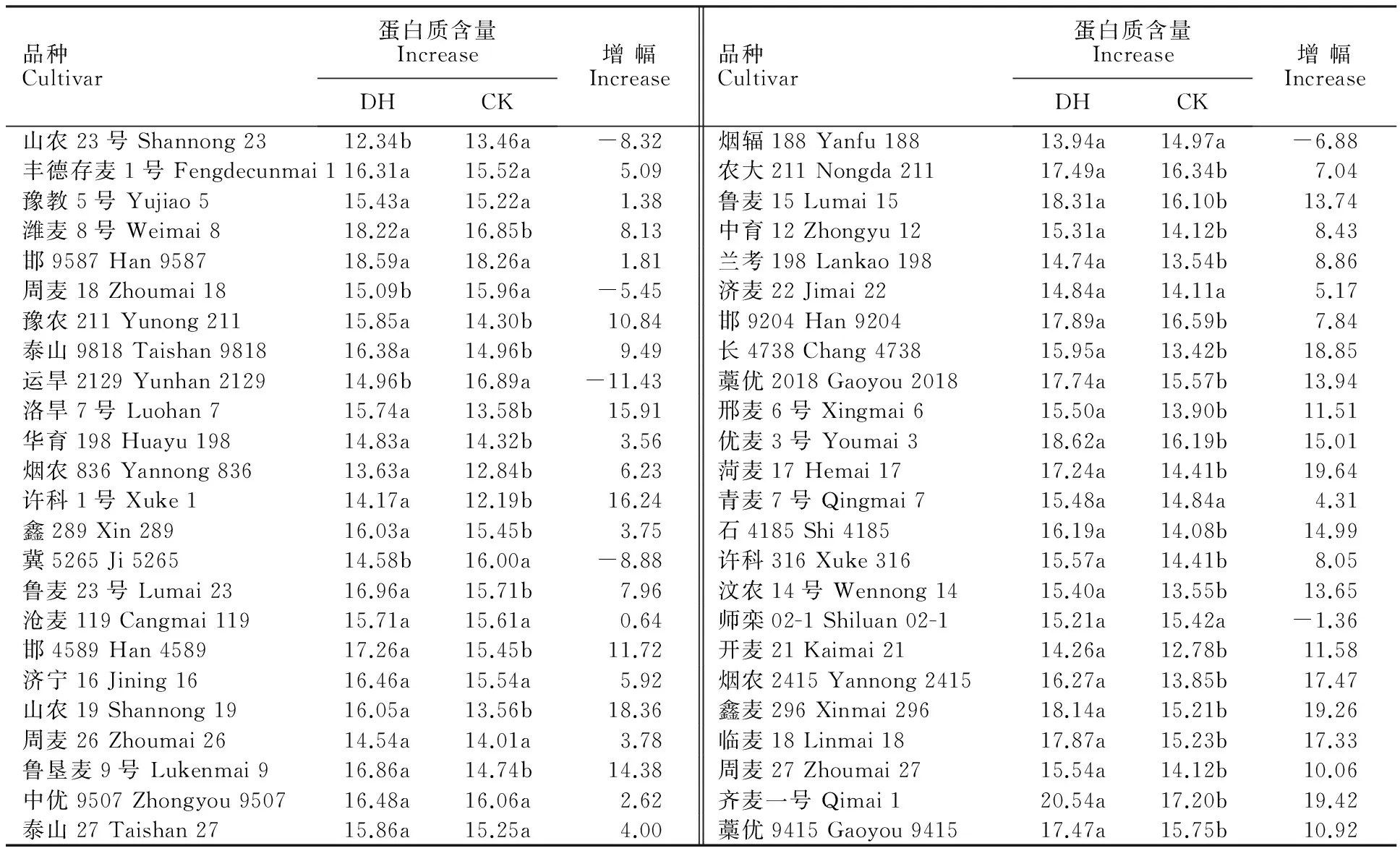
表6 2015年鑒定小麥品種的蛋白質含量Table 6 Protein content of wheat cultivars identified in 2015 %

表7 2014年鑒定小麥品種的淀粉含量Table 7 Starch content of wheat cultivars identified in 2014 %
2.3.2 干熱風對淀粉含量的影響
由表7、表8可知,2014年干熱風處理后,小麥籽粒淀粉含量均降低,降幅在0.01%~4.42%之間,其中,高抗(HR)與中抗(R)干熱風品種淀粉含量降幅在0.01%~1.93%之間,而熱敏感型品種(S)在0.09%~4.42%之間;2015年鑒定小麥品種中,除山農23號等8個品種在干熱風處理后淀粉含量不降反升,其余品種籽粒淀粉含量均降低,降幅為-2.47%~4.41%,其中高抗干熱風品種(HR)的降幅小于2.5%,而大部分熱敏感型品種降幅大于2.5%,豫麥34等品種的降幅高達4%。說明干熱風處理后小麥籽粒淀粉含量的降幅與品種的干熱風抗性關系密切,干熱風抗性越強,干熱風處理后淀粉含量降幅越小。對兩年鑒定小麥品種的抗逆指數與淀粉含量降幅分別進行相關性分析發現,2014年、2015年的相關系數分別為-0.689與-0.651(P≤0.01),均為極顯著負相關。
2.4 高溫誘導對不同抗性小麥品種小分子熱激蛋白基因表達的影響
2.4.1 高溫誘導對 TaHSP16.9基因表達的影響
圖2顯示,5個小麥品種在苗期經高溫38 ℃處理0~4.5 h, TaHSP16.9基因表達水平均迅速上調,泰山9818的上調倍數高達6 000。除周麥18,其余4個品種基因表達上調倍數呈先上升后下降趨勢,在高溫誘導1.5 h時達到峰值,隨后開始下降。在熱脅迫過程中,山農23號、周麥18與泰山9818三個抗干熱風品種的 TaHSP16.9基因表達上調倍數變化幅度較大,而師欒02-1與濟南17號兩個熱敏感型品種的 TaHSP16.9基因表達變化幅度較平緩,不同時間之間差異較小。

表8 2015年鑒定小麥品種的淀粉含量Table 8 Starch content of wheat cultivars identified in 2015 %
2.4.2 高溫誘導對 TaHSP17.8基因表達的影響
圖3顯示,5個干熱風抗性不同的小麥品種在38 ℃高溫誘導過程中, TaHSP17.8基因表達均迅速上調,在0.5~1 h內基因上調至峰值,隨后開始下降,基因表達上調倍數呈先上升后下降趨勢,在2.5 h之后,基因上調倍數均趨于穩定至最低水平。山農23號、周麥18與泰山9818三個抗干熱風品種 TaHSP17.8基因對高溫的反應迅速,熱脅迫0.5 h后,上調倍數分別迅速上升至1 212、1 010與598,而師欒02-1與濟南17號兩個熱敏感型品種 TaHSP17.8基因對高溫反應遲緩,熱脅迫0.5 h時,基因表達僅上調至304與273倍。

SL02-1:師欒02-1;JN17:濟南17;SN23:山農23號;ZM18:周麥18號;TS 9818:泰山9818。下同。
SL02-1:Shiluan 02-1;JN17:Jinan 17;SN23:Shannong 23;ZM18:Zhoumai 18;TS 9818:Taishan 9818.The same in Fig.3-5.
圖2 抗、感干熱風小麥品種熱脅迫不同時間 TaHSP16.9基因的表達差異
Fig.2 Differential expression of TaHSP16.9 in both resistant and susceptible wheat cultivars under high temperature stress

圖3 抗、感干熱風小麥品種熱脅迫不同時間 TaHSP17.8基因的表達差異

圖4 抗、感干熱風小麥品種熱脅迫不同時間 TaHSP23.6基因的表達差異
2.4.3 高溫誘導對 TaHSP23.6基因表達的影響
圖4顯示,5個干熱風抗性不同的小麥品種在高溫38 ℃處理0~4.5 h內, TaHSP23.6基因表達上調倍數呈先上升后下降趨勢,基因表達上調峰值在熱脅迫0.5 h左右出現,隨后開始下降,在熱脅迫2.5 h之后,基因表達上調倍數趨于穩定至最低水平。5個品種中,山農23號基因表達上調峰值最大,接近400倍,其余品種基因表達上調峰值相對較小,均在100倍以下。
2.4.4 高溫誘導對 TaHSP26.6基因表達的影響
圖5顯示,5個干熱風抗性不同的小麥品種在高溫38 ℃處理0~4.5 h內, TaHSP26.6基因表達上調倍數為先上升后下降的趨勢,熱脅迫至1.5~2.5 h出現峰值,較其他小分子熱激蛋白基因出現晚,隨后開始下降。5個品種中,山農23號與周麥18上調表達峰值最大,高至10 000倍以上,師欒02-1上調表達峰值最小,為6 000倍左右;此外,師欒02-1與濟南17號兩個熱敏感型品種在熱脅迫4.5 h時基因表達分別上調至5 829與4 163倍,而山農23號、周麥18與泰山9818三個抗干熱風品種上調幅度分別為1 317、2 896、894倍,可見,抗干熱風品種在處理后期 TaHSP26.6基因上調表達倍數顯著低于熱敏感型品種。

圖5 抗、感干熱風小麥品種熱脅迫不同時間 TaHSP26.6基因的表達差異
3 討 論
3.1 高溫對小麥籽粒品質與千粒重的影響
關于干熱風對小麥品質的影響前人已做了大量研究。小麥在灌漿后期經歷高溫,籽粒蛋白的積累速率加快,淀粉含量降低;蛋白質的積累與淀粉形成是兩個相互獨立又有聯系的過程,灌漿期經歷高溫,籽粒蛋白含量增加是由于淀粉的減少造成的[2,5,20]。儀小梅等[7]研究發現,抗干熱風品種在灌漿后期經干熱風脅迫后,淀粉含量降低幅度小于熱敏感型品種。本研究發現,兩年鑒定的98個小麥品種在灌漿期經歷干熱風后,大部分品種的籽粒蛋白質含量顯著提高,淀粉含量顯著降低,籽粒蛋白質含量升高的主因是籽粒淀粉含量降低。
Hanft等[21]研究表明,環境對籽粒的發育具有重要作用,小麥灌漿期間經歷干熱風,必然會嚴重影響到小麥千粒重。Zhao等[22]研究表明,在灌漿期遭受高溫后,蛋白質含量高的小麥品種千粒重高于蛋白質含量低的小麥品種。本研究表明,不同小麥品種經干熱風處理后,千粒重均下降,降低幅度為4%~30%。根據小麥千粒重抗逆指數鑒定出的小麥抗性與淀粉、蛋白質含量變化有一定關系,即抗性強的品種,其籽粒的淀粉含量下降幅度與蛋白質含量升高幅度也較低。
3.2 高溫對小分子熱激蛋白表達的影響
在熱激蛋白中,12~45 kD小分子量熱激蛋白種類最豐富[23],且其在植物生長的各個階段都有分布。高溫條件下,小分子熱激蛋白會大量合成[12,15-16]。熱激蛋白的積累可以增強植物耐熱性[13]。Xue等[10]對高溫誘導擬南芥中 HSP26基因的研究發現,HSP26熱激蛋白的積累可以增強植物的耐熱性。Zhang等[24]對擬南芥的高溫誘導研究結果表明, HSP21.4基因能在短時間內迅速表達,對抵御外界脅迫有關鍵性作用。Murakami等[25]對水稻中 HSP17.7基因的研究發現,過量表達的 HSP17.7基因,可以提高水稻對高溫脅迫的抵抗能力。Park等[26]對高溫誘導胡蘿卜中 HSP17.7基因表達的研究也表明,高溫會在短時間內提高 HSP17.7基因的表達量。本研究表明,小麥中 TaHSP16.9、 TaHSP17.8、 TaHSP23.6、 TaHSP26.6四個小分子熱激蛋白基因在高溫脅迫下能在短時間內快速大量表達,這與前人研究相一致。此外,本研究還發現,高溫誘導小麥幼苗中,小分子熱激蛋白基因表達在干熱風抗性不同的品種間有差異,抗干熱風品種在高溫誘導期間, TaHSP16.9基因表達上調變化幅度大于熱敏感型品種, TaHSP17.8基因上調表達時間均早于熱敏感型品種,山農23號的 TaHSP23.6基因上調表達峰值遠高于其他品種,熱敏感型品種在熱脅迫后期 TaHSP26.6基因的上調倍數高于抗干熱風品種,這表明TaHSPs基因的熱激反應時間、上調表達幅度、基因表達峰值以及高溫誘導后期基因表達水平的維持在干熱風抗性不同的品種間有差異。因此,還需進一步明確小麥苗期小分子熱激蛋白基因的表達與灌漿期小麥干熱風抗性的關系,以期為干熱風抗性品種的選育提供更有價值的理論依據。
4 結 論
干熱風處理導致干熱風抗性有差異的小麥品種千粒重不同程度下降,在兩年重復鑒定小麥品種中,山農23號等品種抗性等級均達到高、中抗干熱風水平,抗性穩定,而師欒02-1在兩年的鑒定中,均為熱敏感型品種。干熱風處理顯著提高籽粒蛋白質含量,降低籽粒淀粉含量和旗葉葉綠素含量,且抗性高的品種蛋白質含量升高幅度與淀粉及葉綠素含量降低幅度較小。在38 ℃高溫誘導0~4.5 h的小麥幼苗中, TaHSP16.9、TaHSP17.8、)TaHSP23.6與 TaHSP26.6基因迅速大量表達,且不同品種的表達均為拋物線趨勢,但小分子熱激蛋白基因上調表達幅度、基因表達峰值以及高溫誘導后期基因表達水平的維持方面在干熱風抗性不同的品種間有差異。
[1] SHPILER L,BLUM A.Heat tolerance for yield and its components in different wheat cultivars [J].Euphytica,1990,51(3):257.
[2] 趙 輝,荊 奇,戴廷波,等.花后高溫和水分逆境對小麥籽粒蛋白質形成及其關鍵酶活性的影響[J].作物學報,2007,33(12):2021.
ZHAO H,JING Q,DAI Y B,etal.Effects of high temperature during grain filling on key enzymes involved in starch synthesis in two wheat cultivars with different quality types [J].ActaAgronomicaSinica,2007,33(12):2021.
[3] 盧紅芳,王晨陽,郭天財,等.灌漿前期高溫和干旱脅迫對小麥籽粒蛋白質含量和氮代謝關鍵酶活性的影響[J].生態學報,2014,34(13):3612.
LU H F,WANG C Y,GUO T C,etal.Effects of high temperature and dry stress on protein concentration enzyme activities in relation to nitrogen metabolism in wheat grains during the early stage of grain filling [J].ActaEcologicaSinica,2014,34(13):3612
[4] 劉 萍,郭文善,浦漢春,等.灌漿期短暫高溫對小麥淀粉形成的影響[J].作物學報,2006,32(2):182.
LIU P,GUO W S,PU H C,etal.Effects of transient high temperature during grain filling period on starch formation in wheat(TriticumaestivumL.) [J].ActaAgronomicaSinica,2006,32(2):182.
[5] 李永庚,于振文,張秀杰,等.小麥產量與品質對灌漿不同階段高溫脅迫的響應[J].植物生態學報,2005,29(3):461.
LI Y G,YU Z W,ZHANG X J,etal.Response of yield and quality of wheat to heat stress at different grain filling stress [J].ActaPhytoecologicaSinica,2005,29(3):461.
[6] 閆素輝,尹燕枰,李文陽,等.灌漿期高溫對小麥籽粒淀粉的積累、粒度分布及相關酶活性的影響[J].作物學報,2008,34(6):1092.
YAN S H,YIN Y P,LI W Y,etal.Effect of high temperature during gain filling on starch accumulation,starch granule distribution,and activities of related enzymes in wheat [J].ActaAgronomicaSinica,2008,34(6):1092.
[7] 儀小梅,孫愛清,韓曉玉,等.黃淮麥區小麥主推品種(系)干熱風抗性鑒定[J].麥類作物學報,2015,35(2):274.
YI X M,SUN A Q,HAN X Y,etal.Identification of dry-hot wind resistance of major wheat cultivars(strains) in Huanghuai wheat region [J].JournalofTriticeaeCrops,2015,35(2):274.
[8] 張英華,楊佑明,曹 蓮,等.灌漿期高溫對小麥旗葉與非葉器官光合和抗氧化酶活性的影響[J].作物學報,2015,41(1):136.
ZHANG Y H,YANG Y M,CAO L,etal.Effect of high temperature on photosynthetic capability and antioxidant enzyme activity of flag leaf and non-leaf organs in wheat [J].ActaAgronomicaSinica,2015,41(1):136.
[9] RISTIC Z,BUKOVNIK U,PRASAD P V V.Correlation between heat stability of thylakoid membranes and loss of chlorophyll in winter wheat under heat stress [J].CropScience,2007,47(5):2067.
[10] XUE Y,PENG R,XIONG A,etal.Over-expression of heat shock protein gene hsp26 inArabidopsisthalianaenhances heat tolerance [J].BiologiaPlantarum,2010,54(1):105.
[11] KUMAR S,KUMARI P,KUMAR U,etal.Molecular approaches for designing heat tolerant wheat [J].JournalofPlantBiochemistry&Biotechnology,2013,22(4):359.
[12] QIN D D,WU H Y,PENG H R,etal.Heat stress-responsive transcriptome analysis in heat susceptible and tolerant wheat(TriticumaestivumL.) by using wheat genome array [J].BiomedcentralGenomics,2008,9(9):1.
[13] MILLER G,MITTLER R.Could heat shock transcription factors function as hydrogen peroxide sensors in plants [J].AnnalsofBotany,2006,98(2):279.
[14] MOMCILOVIC I,RISTIC Z.Expression of chloroplast protein synthesis elongation factor,EF-Tu,in two lines of maize with contrasting tolerance to heat stress during early stages of plant development[J].JournalofPlantPhysiology,2007,164(1):90.
[15] WAHID A,GELANI S,ASHRAF M,etal.Heat tolerance in plants:An overview[J].Environmental&ExperimentalBotany,2007,61(3):199.
[16] BHARATI P,AMANDEEP K,OM P G,etal.Identification of HSP20 gene family in wheat and barley and their differential expression profiling under heat stress[J].AppliedBiochemistry&Biotechnology,2015,175(5):24276.
[17] 郭秀林,劉子會,趙會嶶,等.熱鍛煉和高溫脅迫下冬小麥熱激蛋白與抗氧化酶基因表達[J].華北農學報,2014(4):13.
GUO X L,LIU Z H,ZHAO H W,etal.Gene expression of heat-shock proteins and antioxidant enzymes under heat acclimation and heat stress in winter wheat [J].ActaAgriculturaeBoreali-Sinica,2014(4):13.
[18] LEE S H,LEE K W,LEE D G,etal.Identification and functional characterization of Siberian wild rye(ElymussibiricusL.) small heat shock protein 16.9 gene( EsHsp16.9) conferring diverse stress tolerance in prokaryotic cells [J].BiotechnologyLetters,2015,37(4):1.
[19] ABU-ROMMAN S.Genotypic response to heat stress in durum wheat and the expression of smallHSPgenes [J].RendicontiLinceiScienzeFisicheENaturali,2016,27(2):261.
[20] 戴廷波,趙 輝,荊 奇,等.灌漿期高溫和水分逆境對冬小麥籽粒蛋白質和淀粉含量的影響[J].生態學報,2016,27(2):261.
DAI Y B,ZHAO H,JING Q,etal.Effects of high temperature and water stress during grain filling on grain protein and starch formation in winter wheat [J].ActaEcologicaSinica,2016,27(2):261..
[21] HANFT J M,JONES R J,STUMME A B.Dry matter accumulation and carbohydrate concentration patterns of field-grown andinvitrocultured maize kernels from the tip and middle ear positions [J].CropScience,1986,26(3):568.
[22] ZHAO H,DAI T,JING Q,etal.Leaf senescence and grain filling affected by post-anthesis high temperatures in two different wheat cultivars [J].PlantGrowthRegulation,2007,51(2):149.
[23] VIERLING E.The roles of heat shock proteins in plants [J].AnnualReviewofPlantBiology,2003,42(1):579.
[24] LU Z,ZHANG Q,GAO Y,etal.Overexpression of heat shock protein gene PfHSP21.4 inArabidopsisthalianaenhances heat tolerance[J].ActaPhysiologiaePlantarum,2014,36(6):1555.
[25] MURAKAMI T,MATSUBA S,FUNATSUKI H,etal.Over-expression of a small heat shock protein, sHSP17.7,confers both heat tolerance and UV-B resistance to rice plants [J].MolecularBreeding,2004,13(2):165.
[26] PARK H,KO E,JANG E,etal.Expression of DcHsp17.7,a small heat shock protein gene in carrot(DaucuscarotaL.) [J].HorticultureEnvironment&Biotechnology,2013,54(2):121.
Identification of Dry-Hot Wind Resistance of Wheat Cultivars and Gene Expression Analysis ofTaHSPsRelated to Heat Stress
LI Meiling,SUN Aiqing,YANG Min,ZHANG Jiedao,WANG Zhenlin,CHEN Leitai,CHEN Lulu,MA Xueli,YIN Yanping
(College of Agronomy,Shandong Agricultural University/State Key Laboratory of Crop Biology/Shandong Key Laboratory of Crop Biology,Tai’an,Shandong 271018,China)
This study aims to identify dry-hot wind resistance of wheat cultivars and analyze expression of heat shock protein genes(TaHSPs) related to heat stress in resistant and susceptible wheat cultivars. Ninety-eight wheat cultivars were used as materials and treated with simulating dry-hot wind from 10 to 20 days after anthesis. Chlorophyll content,grain quality and thousand-kernel weight were tested,and the effects of dry-hot wind resistance of wheat cultivars were studied. The expression ofTaHSPsin 15-day-old seedling of resistant and susceptible wheat cultivars,which were subjected to continuous heat stress at 38 ℃ for 4.5 h,was tested by real-time quantitative PCR. The results showed that the chlorophyll content in flag leaf of wheat cultivars decreased gradually during the treatment of dry-hot wind and decreased much more in susceptible wheat cultivars than in resistant cultivars. Thousand-kernel weight of all cultivars was reduced after dry-hot wind treatment and some cultivars which were identified showed the same resistance to dry-hot wind in two-year replications,such as Shannong 23 showed steady resistance to dry-hot wind,whereas Shiluan 02-1 was sensitive to dry-hot wind in 2-year replications. Protein content was significantly increased while the starch content was significantly decreased. Besides,the percentage of decreased starch content of wheat cultivars with high adversity resistance index (AI) was lower than those with low AI. Expression analysis ofTaHSPsgenes showed, TaHSP16.9, TaHSP17.7, TaHSP23.6 and TaHSP26.6 in wheat seedling were highly expressed and the expression trends ofTaHSPswere first increasing and then decreasing during heat stress at 38 ℃. In addition,the gene expression patterns ofTaHSPswere different between resistant and susceptible wheat cultivars under heat stress at 1 h.For TaHSP16.9,the up-regulated extent of gene expression in resistant wheat cultivars was greater than that in susceptible wheat cultivars. For TaHSP17.8,the up-regulated times of gene expression in resistant wheat cultivars was higher than that in susceptible wheat cultivars under heat stress at 0.5 h. The up-regulated times of gene expression level in Shannong 23 with heat tolerance was higher than 590,whereas the expression level in Shiluan 02-1 with heat sensitivity only reached 300. For TaHSP23.6,the peak of Shannong 23 with heat tolerance was four times higher than those in other cultivars. For TaHSP26.6,the up-regulated times of gene expression in susceptible wheat cultivars were higher than resistant wheat cultivars under heat stress at 4.5 h. The up-regulated times of TaHSP26.6 in heat susceptible cultivars were higher than 4 000,whereas that in heat tolerant cultivars only reached 3 000.
Wheat; Dry-hot wind; 1 000-kernel weight; Adversity resistance index; Heat shock protein
時間:2017-01-16
2016-04-07
2016-05-23
國家公益性行業(農業)科研專項(201203029)
E-mail:limeiling0602@163.com
尹燕枰(E-mail:ypyinsdau@sina.com)
S512.1;S330
A
1009-1041(2017)02-0162-13
網絡出版地址:http://www.cnki.net/kcms/detail/61.1359.S.20170116.1833.006.html

