外源亞精胺對PEG脅迫下燕麥幼苗生長及部分生理特性的影響
吳旭紅,馮晶旻
(1.齊齊哈爾大學生命科學與農林學院,黑龍江齊齊哈爾 161006; 2.齊齊哈爾市衛生監督所,黑龍江齊齊哈爾 161005)
外源亞精胺對PEG脅迫下燕麥幼苗生長及部分生理特性的影響
吳旭紅1,馮晶旻2
(1.齊齊哈爾大學生命科學與農林學院,黑龍江齊齊哈爾 161006; 2.齊齊哈爾市衛生監督所,黑龍江齊齊哈爾 161005)

燕麥幼苗;亞精胺;滲透脅迫;滲透調節物質;抗氧化特性
干旱是全球性影響農業生產和生態環境的焦點問題。據統計,全球耕地中約有43%受到干旱脅迫[1]。我國是全球13個最貧水的國家之一,干旱、半干旱的土地面積約占國土總面積的52.5%[2],尤其是我國北方處于亞洲季風氣候區,旱災的普遍性和持續性都較嚴峻。干旱條件下,由土壤溶液水勢下降導致的滲透脅迫會使活性氧(ROS)過量積累而對植物產生過氧化損傷,進而破壞生物大分子的結構,使其喪失生理功能,嚴重影響植株發育,甚至造成死亡[3]。植物在進化過程中,除對生態逆境在形態上作出加強導管組織發育、加大根冠比等適應性改變外,通過上調抗氧化系統活性和抗氧化劑含量、增加胞內溶質、降低細胞水勢、維持細胞膨壓而進行滲透調節等抵御干旱等逆境脅迫。近年來,有關多胺對植物在逆境下的生理調控作用日益受到關注。
亞精胺(spermidine,Spd)作為多胺(polyamine,PA)中的一種具有強烈生理活性的小分子脂肪族含氮堿,對植物生長發育具有多方面的調節作用。噴施外源Spd可在一定程度上緩解黃瓜[4]、番茄[5]、白三葉[6]等植物的非生物逆境傷害。在逆境下,植物細胞內常會積累大量多胺,能夠對多種生物和非生物逆境作出應答。研究表明,亞精胺合成酶基因轉入后,擬南芥(Arabidopsisthaliana)受體內亞精胺含量顯著增加,耐旱、耐冷、耐鹽等特性顯著增強[7];高鹽脅迫下,外源Spd和精胺(spermine,Spm)通過上調鐵超氧化物歧化酶(Fe-SOD)基因的表達,提高了粗齒冷水花(Ulvafasciata)的抗氧化能力,緩解了鹽脅迫所導致的氧化損傷[8]。Spd和Spm在DNA復制中能與拓補異構酶之間發生交互作用,穩定酶-模板復合物,且在轉錄后修飾、蛋白質合成的后加工過程中參與磷酸化等代謝,從而影響DNA的復制、RNA的轉錄和蛋白質的生物合成[9],在植物的生長發育中介導了胞內離子平衡、酶活調控、細胞分化等多種生理過程。尤其是Spd,除參與植物的性別分化、果實成熟與衰老等過程外,還作為逆境下的直接脅迫保護物質,以其獨特的分子結構,在脅迫信號轉導中直接參與脅迫抗性機制的構建,被認為是植物對逆境響應中的信號調節樞紐。外源多胺已成功被應用于提高植物的抗逆性。外源Spd可通過提高脯氨酸合成代謝關鍵酶活性,促進脯氨酸和可溶性糖的積累,從而提高小麥幼苗的保水性和抗旱能力[10];外源Spd通過抑制NADPH氧化酶活性提高抗氧化酶活力,降低玉米葉片內ROS,提高幼苗的抗旱性[11];外源Spd能促進干旱條件下番茄幼苗的糖類轉換和利用,通過參與番茄生育早期碳水化合物的代謝,促進植株生長發育[5]。
燕麥(AvenanudaL.)是我國種植歷史悠久的糧飼兼用作物,廣泛分布于三北地區和青藏高原等16省(區)。近年來,因其含多種活性營養成分及在控制血脂、降低血糖等方面獨特的食療功效,在種植業結構中的地位和價值日益凸顯。東北、西北及內蒙農牧交錯帶大面積種植的燕麥經常遭受頻發的春旱甚至春夏連旱的威脅,因此通過探索外源調節物對燕麥抵御干旱脅迫的生理機制,提高其避旱和耐旱能力具有重要意義。而目前有關外源Spd對燕麥在干旱脅迫下的生理調控作用及其生化響應研究鮮見報道。本研究通過葉面噴施不同濃度的Spd,研究其對燕麥幼苗生長、ROS的產生和清除、抗氧化體系的生理響應及滲透調節物質含量的影響,以期為Spd在燕麥抗旱栽培中的應用提供理論依據。
1 材料與方法
1.1 材 料
供試燕麥品種為壩莜1號,由齊齊哈爾市畜牧局提供。亞精胺(spermidine,Spd)為Sigma公司產品,先用去離子水配成100 mmol·L-1母液,4 ℃保存,稀釋成相應濃度待用。
1.2 試驗設計
試驗于2015年3-7月在齊齊哈爾大學生化實驗室進行,室內溫度20~25 ℃,自然采光,通風良好。將精選的燕麥種子,先經2% NaClO浸泡消毒15 min,去離子水反復沖洗干凈后催芽。將露白整齊的種子播于細砂經清水浸泡1 h、高溫滅菌(130 ℃,3 h)、定量稱重的花盆中,每盆120粒,播深1.5 cm。每3 d用1/4 Hoagland營養液等量澆灌。待幼苗2葉1心時,每盆定苗約90株。
當幼苗長至3葉1心時,將其隨機分為三組:第一組為CK1組,進行1/2 Hoagland營養液+葉噴蒸餾水處理;第二組為CK2組,進行1/2 Hoagland 營養液+ PEG-6000 200 g·L-1+葉噴蒸餾水處理;第三組為Spd噴施組,進行1/2 Hoagland 營養液+ PEG-6000 200 g·L-1+葉噴不同濃度Spd處理,Spd設0.3、0.6、0.9和1.2 mmol·L-14個濃度水平(分別用T1~T4表示),Spd每天8:30和16:30葉面噴施2次,每次噴施量為每盆10 mL。共形成6個處理,隨機排列,每處理3盆,處理15 d后收獲植株進行相關生理指標測定。
1.3 測定項目和方法
1.3.1幼苗株高、根長、干重、根系活力及相對干物質增長率的測定
每處理輕取20株幼苗,去除根部培養基質,用直尺量取株高和最大根長。之后迅速用蒸餾水洗凈,110 ℃烘箱殺青10 min后轉至75 ℃烘干至衡重,稱干重。根系活力用TTC法測定[12]。耐旱性強弱以抗旱系數表示,抗旱系數=處理生物量/對照生物量[13]。以“處理后20株干重/處理前20株干重”計算幼苗干物質相對增長率[10]。
1.3.2 滲透調節物質含量的測定
脯氨酸、可溶性糖、可溶性蛋白和游離氨基酸含量分別用茚三酮比色法、蒽酮比色法、考馬斯亮藍法和茚三酮顯色法測定[14]。
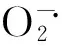
1.3.4 抗氧化劑含量及抗氧化酶活性的測定
采用張志良等[12]的方法測定超氧物歧化酶(SOD)、過氧化物酶(POD)和過氧化氫酶(CAT)活性;抗壞血酸(ASA)含量采用紅菲咯啉(BP)用顯色法測定[15];抗壞血酸過氧化物酶(APX)活性采用抗壞血酸氧化法測定[15];谷胱甘肽(GSH)含量測定采用DTNB顯色法[16];谷胱甘肽還原酶(GR)活性按照NADPH氧化法測定[17]。各生化指標均取頂端全展的功能葉進行測定,3次重復,取平均值。
1.4 統計分析
所有實驗數據用平均值±標準誤表示,用SPSS統計軟件方差分析和Duncan法進行多重比較(P<0.05)。
2 結果與分析
2.1 外源Spd對PEG脅迫下燕麥幼苗生長的影響
PEG脅迫顯著降低了燕麥幼苗株高、根長及干物質積累量(表1)。在PEG脅迫下,各濃度外源Spd處理均不同程度地提高了燕麥幼苗的相對干物質增長率和根系活力,促進了幼苗生長。T1(0.3 mmol·L-1Spd)處理增加了幼苗株高和根干重,但對根的伸長和地上部干物質的積累并無明顯作用。隨著Spd濃度的升高,幼苗生長先增進后減弱,根系活力、抗旱系數及干物質相對增長率也呈相同的變化趨勢。在4個Spd處理中以T3處理的幼苗株高、根長及干物質積累量、根系活力、抗旱系數及干物質相對增長率最高,說明小麥苗期葉面噴施適宜濃度的Spd對干旱脅迫的不利影響有緩解作用。
2.2 外源Spd對PEG脅迫下燕麥幼苗葉片滲透調節物質含量的影響
PEG脅迫造成燕麥葉片脯氨酸(Pro)大量積累,其含量比CK1高2.01倍,同時顯著提高了可溶性糖和游離氨基酸的含量,降低了可溶性蛋白含量(表2)。在PEG脅迫下,Spd低濃度處理(T1)對Pro和可溶性蛋白的積累影響不大,但使可溶性糖和游離氨基酸含量分別提高了26.67%和降低了16.47%。隨Spd濃度的加大,其對Pro和可溶性糖的累積產生明顯促進效應,并進一步降低游離氨基酸含量,尤其以0.9 mmol·L-1Spd處理效果最明顯。
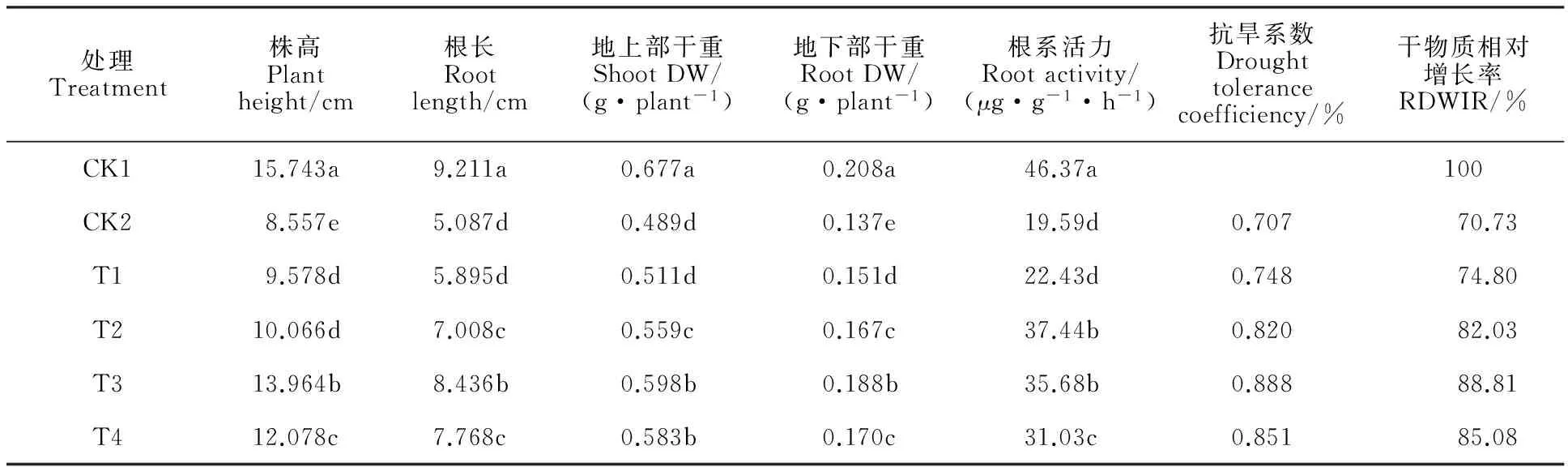
表1 外源亞精胺對PEG脅迫下燕麥幼苗生長的影響Table 1 Effects of exogenous spermidine on the growth of oat seedlings under PEG stress
同一列數據后不同小寫字母表示處理間差異顯著(P<0.05)。下表同。
DW:Dry weight; RDWIR: Relatively increasing rate of DW; Values with different small letters within the same column are significantly different among the treatments at 0.05 level. The same in other tables.

表2 外源Spd對PEG脅迫下燕麥葉片滲透調節物質含量的影響Table 2 Effects of PEG and exogenous Spd on osmoregulation substance contents in leaves of oat seedlings


處理TreatmentO-·2產生速率O-·2productiverate/(μmol·min-1·g-1FW)H2O2含量H2O2content/(μmol·g-1FW)MDA含量MDAcontent/(μg·g-1FW)CK117.08±0.12d4.39±0.08d3.76±0.11dCK213.29±0.30a12.36±0.38a5.89±0.25aT112.87±0.27a11.65±0.19a5.42±0.48aT29.43±0.44b8.71±0.20b4.89±0.57bT38.66±0.17c6.33±0.08c4.28±0.21cT49.28±0.51b6.97±0.63c4.73±0.61b
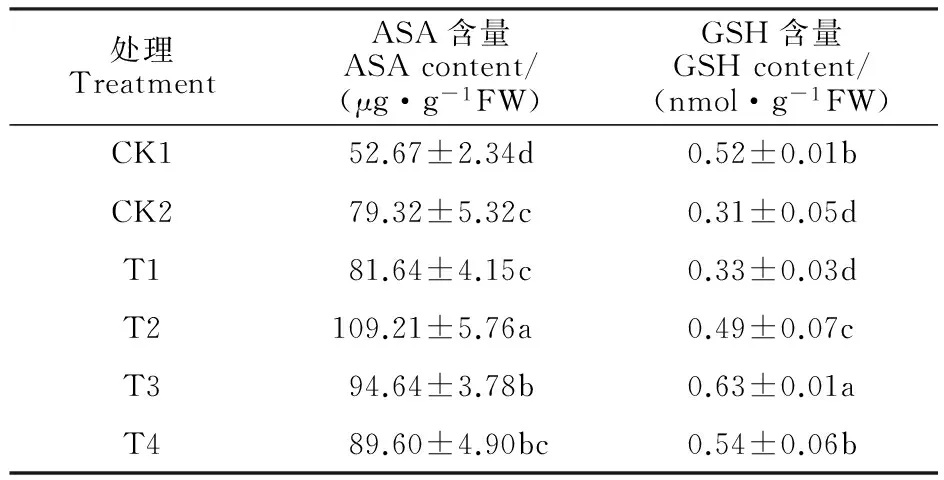
表4 外源Spd對PEG脅迫下燕麥葉片ASA和GSH含量的影響Table 4 Effects of exogenous Spd on contents of ASA and GSH in leaves of oat seedlings under PEG stress
2.4 外源Spd對PEG脅迫下燕麥幼苗葉片ASA和GSH含量的影響
PEG脅迫使燕麥葉片ASA含量激增,導致GSH含量顯著下降。在PEG脅迫下,噴施較低濃度(0.3 mmol·L-1)的Spd后,燕麥葉片ASA和GSH含量未發生明顯變化;進一步增加Spd濃度后,葉片ASA和GSH含量不同程度提高,且分別以0.6和0.9 mmol·L-1Spd處理的效果最佳,較CK2分別增加37.68%和103%,說明適宜濃度的Spd處理可促進燕麥葉片中的ASA-GSH循環(表4)。
2.5 外源Spd對PEG脅迫下燕麥幼苗葉片抗氧化酶活性的影響
PEG脅迫后,燕麥葉片SOD、POD和APX活性均顯著升高,但GR和CAT活性明顯下降(表5)。在PEG脅迫下,與CK2相比,0.3 mmol·L-1Spd處理(T1)的4種酶活性均上升,但只有CAT活性變化顯著;0.6~1.2 mmol·L-1Spd處理(T2~T4)均顯著上調了4種酶活性,其中SOD、CAT和GR活性均以T3處理最高,POD和APX活性分別以T4和T2處理最高。說明適宜濃度的Spd處理可上調燕麥葉片的抗氧化酶活性,有助于增強抗氧化能力。

表5 外源Spd對PEG脅迫下燕麥葉片保護酶活性的影響Table 5 Effects of exogenous Spd on anti-oxidative enzyme activities in oat seedlings under PEG stress
3 討 論
3.1 Spd對PEG脅迫下燕麥幼苗生長的影響
植物的生長源于根系從環境中吸收養分和水分,同時依靠光合碳氮代謝完成器官發育和形態建成。生物積累量是植物對逆境響應的直接體現,也是遭受生理傷害的綜合反映。PEG脅迫下,燕麥幼苗干物重降低,這是因為植株體內ROS過量累積,導致膜結構受損,對光合作用產生抑制,使碳同化產物減少。滲透脅迫會引起生理干旱,導致植株形態建成過程中C/N代謝受阻,尤其是碳架不足,以及滲透調節能耗損失較大,從而抑制了燕麥生長。在本研究中,0.6、0.9 mmol·L-1外源Spd處理明顯緩解了PEG脅迫對燕麥幼苗根系活力的不利影響,有利于根系對營養物質的吸收、轉運、積累和利用;對ROS產生和積累有顯著抑制作用,有助于在PEG脅迫條件下類囊體膜結構的穩定和修復,使葉綠體對光能的吸收和利用能力增強,這可從光合碳同化產物可溶性糖的積累得以印證;由于光合碳代謝為氨基酸的合成提供了碳架和同化力,因此光合能力的改善有利于燕麥葉片氨基酸和可溶性蛋白的積累。非酶抗氧化劑ASA在Spd作用下大量生成,不僅可促進根系的細胞分裂,而且可在ASA氧化酶作用下氧化形成MDHA,進而MDHA通過質膜上的細胞色素b還原和跨膜轉運,促進細胞生長[18]。總體來看,PEG脅迫下0.9 mmol·L-1外源Spd處理對燕麥幼苗生長促進效果最佳。
3.2 Spd對PEG脅迫下燕麥幼苗滲透調節作用的影響
滲透調節是植物為適應脅迫逆境而產生的生理應答。可溶性糖是重要的滲透調節物質;Pro既是滲透調節物質,又是抗氧化劑,因其具有極高的水溶性,因而可以調節細胞的滲透勢并增加蛋白質的水合度,從而維持細胞的正常功能,因此通過外源物質誘導和調控Pro積累可以有效緩解逆境傷害。杜紅陽等[10]報道,滲透脅迫導致小麥葉片Pro合成途徑中的關鍵酶Δ1-吡咯啉-5-羧酸合成酶(P5CS)和Δ1-吡咯啉-5-羧酸還原酶(P5CR)的活性增強,外源Spd處理進一步提高了P5CS和 P5CR活性,由此促進了Pro和可溶性糖的積累,提高了小麥幼苗的保水和抗旱能力。本研究發現,PEG脅迫使燕麥葉片Pro和可溶性糖含量增加,有助于提高原生質的粘度和彈性,增強植株對缺水環境的適應性。0.9、1.2 mmol·L-1Spd葉面處理顯著促進了燕麥葉片可溶性糖的累積,這可能與Spd增強了燕麥在干旱條件下碳水化合物代謝,上調了葡萄糖、果糖及蔗糖合成酶的活性有關[5];Spd誘導下Pro含量的加大會進一步增加了細胞液的濃度和原生質膠體束縛水的含量,最大限度地保持細胞與環境的滲透平衡,維持細胞內環境的穩定,提高細胞的保水能力。推測其可能機制:一方面,外源Spd激活了燕麥在滲透脅迫條件下Pro合成途徑的關鍵酶P5CS和P5CR的活性,促進Pro合成;另一方面,在線粒體中催化Pro降解的脯氨酸脫氫酶(ProDH)和吡咯啉-5-羧酸脫氫酶(P5CDH)的氧化降解過程受到抑制,也導致Pro積累增加,這從杜紅陽等[10]的研究結果中得到了進一步的印證。
植物在發育過程中,不斷需要氨基酸來合成自身組織蛋白和功能性含氮有機物。本試驗中,在PEG脅迫下,可能由于較低的ATP水平誘導了蛋白水解酶活性的提高,蛋白質的水解加劇,使可溶性蛋白含量下降,從而導致游離氨基酸含量升高。這與陳立松等[19 ]對荔枝的研究得出水分脅迫下可溶性蛋白含量的下降是由蛋白水解酶活性的提高而使蛋白質降解所致的結論一致。Spd處理后,燕麥葉片游離氨基酸含量隨處理濃度加大而下降,可溶性蛋白含量則隨Spd處理濃度的加大而升高,并且峰值都出現在0.9 mmol·L-1Spd處理,表明外源Spd通過對過氧化水平的調控,使類囊體膜結構和功能得以修復和穩定,使光合作用同時向碳代謝和氮代謝提供能量和電子,促進了碳素的流動,使可溶性蛋白大幅度增加。其可能的調控機制:首先Spd作為信息分子,在信號轉導過程中,先激活腺苷酸環化酶→cAMP升高→蛋白激酶→磷酸化酶激酶→使非組蛋白磷酸化,與組蛋白相互作用,導致組蛋白與DNA解聚、DNA解旋,從而誘導了逆境蛋白相關基因的高水平表達,增加了蛋白質的合成;其次在蛋白質翻譯后,以多聚陽離子狀態存在的多胺,與胞內某些蛋白質之間因電荷效應發生共價交聯,穩定了蛋白質的結構,減緩了蛋白質的降解,起到了維持細胞內環境穩定的作用[9]。
3.3 Spd對PEG脅迫下燕麥幼苗ROS產生及抗氧化體系的影響
植物體內的抗氧化體系除抗氧化酶外,ASA-GSH循環也是植物體內重要的抗氧化系統。ASA 除可清除(OH-)羥基自由基、淬滅單線態氧外,還可轉化為維生素E。APX是ASA-GSH氧化還原途徑中重要的組分,ASA在APX作用下與H2O2反應,H2O2接受GSH脫氫產生的NADPH的電子還原成H2O,ASA則被氧化為單脫氫抗壞血酸(MDHA)和脫氫抗壞血酸(DHA)。有毒的H2O2通過Halliwell-Asada途徑清除過程中,對還原型GSH的再生具重要意義,其活性高低與ASA含量密切相關[22 ]。APX活性的提高是在干旱逆境下對ROS過量生成的應激反應,標志著ROS清除能力的進一步增強。GR是一種黃素蛋白酶,在NADPH作用下催化氧化型谷胱甘肽(GSSG)還原為GSH,因此其在氧化還原體系中使胞內谷胱甘肽庫保持在還原狀態,從而緩解氧化損傷。試驗結果顯示,滲透脅迫下,可能是脫氫抗壞血酸(DHA)在脫氫抗壞血酸還原酶(DHAR)和單脫氫抗壞血酸還原酶(MDHAR)的作用下,進行逆境應答,大量還原生成ASA而消耗了還原力,因此不能將GSSG還原為GSH,從而使GR活性降低。0.9 mmol·L-1Spd處理,通過降低DHAR活性,提高了GR活性和GSH含量,使ASA-GSH循環的進行有助于抗氧化物質的積累。本研究表明,滲透脅迫降低了葉片GSH含量,說明可能由于逆境脅迫,H2O2等ROS持續積累并被GSH還原,結果導致GSH不斷被氧化為GSSG,從而使之含量下降;PEG脅迫處理燕麥葉片ASA含量的升高是對逆境的一種保護性應答。作為抗氧化劑,ASA和GSH既可通過酶促和非酶促反應清除ROS,還可以通過ASA-GSH循環途徑清除ROS。0.9 mmol·L-1Spd處理顯著提高了滲透脅迫下ASA和GSH水平,且APX活性的上調與ASA含量的增加呈現了高度的同步性。ASA含量的增加又導致GSH含量的升高。
綜上所述,0.9 mmol·L-1外源Spd葉噴處理,可有效降低ROS和MDA生成量,使膜的氧化損傷得以修復,有助于膜結構的穩定,提高了可溶性糖、脯氨酸、游離氨基酸和可溶性蛋白等滲透調節物質的含量,顯著提高了滲透脅迫下燕麥葉片SOD、POD、CAT、APX和GR活性和ASA和GSH等抗氧化劑含量。這說明外源Spd可高效修復燕麥幼苗因滲透脅迫引起的傷害,恢復和維持生理代謝和生化反應的恒穩狀態,從而增強了滲透脅迫下燕麥幼苗的抗氧化脅迫能力,使燕麥幼苗在生理缺水逆境下的生長抑制得以緩解,提高了燕麥幼苗的抗旱性。
[1] 劉建新,王金成,王瑞娟,等.旱鹽交叉脅迫對燕麥幼苗葉片生理特性的影響[J].干旱地區農業研究,2014,32(3):24.
LIU J X,WANG J C,WANG R J,etal.Effects of drought and salinity combined stress on activities of physiol`ical characteristics inAvenanudaseedling leaves [J].AgriculturalResearchintheAridAreas,2014,32(3):24.
[2] 李雪芹,金松恒.干旱脅迫對假儉草氣體交換和葉綠素熒光特性的影響[J].中國農學通報,2010,26(8):170.
LI X Q,JIN S H.Effects of drought stress on gas exchange and chlorophyll fluorescence characteristics inEremochloaophiuroides[J].ChineseAgriculturalScienceBulletin,2010,26(8):170
[3] 單長卷,趙新亮,湯菊香.水楊酸對干旱脅迫下小麥幼苗抗氧化特性的影響[J].麥類作物學報,2014,34(1):91.
SHAN C J,ZHAO X L,TANG J X.Effects of exogenous salicylic acid on antioxidant properties of wheat seedling under drought stress [J].JournalofTriticeaeCrops,2014,34(1):91.
[4] 李 娜,陳 紅,裴孝伯.外源亞精胺對鹽脅迫下黃瓜幼苗耐鹽性的影響[J].熱帶作物學報,2013, 34(7):1359.
LI N,CHEN H,PEI X B.Effects of extraneous spermidine on the salt tolerance in cucumber seedlings under salt stress [J].ChineseJournalofTropicalCrops,2013, 34(7): 1359.
[5] 閆 剛,張春梅,鄒志榮.外源亞精胺對干旱脅迫下番茄幼苗碳水化合物代謝及相關酶活性的影響[J].干旱地區農業研究,2012,30(1):143.
YAN G,ZHANG C M,ZOU Z R.Effects of exogenous spermidine on metabolism of nonstructural carbonhydrate and involved activity of enzymes of tomato seedlings under drought stress [J].AgriculturalresearchintheAridAreas,2012,30(1):143.
[6] 李 州,彭 燕.亞精胺對水分脅迫下白三葉脯氨酸代謝、抗氧化酶活性及其基因表達的影響[J].草業學報,2015,24(4):148.
LI Z,PENG Y.Effects of spermidine on proline metabolism,antioxidant enzyme activity and gene expression in white clover leaves under water stress [J].ActaPrataculturaeSinica,2015,24(4):148.
[7] KASUKABE Y,HE L,NADA K,etal.Over expression of spermidine synthase enhances tolerance to multiple environmental stress and up-regulates the expression of various stress-regulated genes in transgenicArabidopsisthaliana[J].Plant&CellPhysiology,2004,45:712.
[8] SUNG M S,CHOW T J,LEE T M.Polyamine acclimation alleviates hypersalinity-induced oxidative stress in a marine green macroalga,Ulvafasciata,by modulation of antioxidative enzyme gene [J].JournalofPhycology,2011,47(3):538.
[9] 杜紅陽,常云霞,劉懷攀.多胺的作用機理研究進展[J].周口師范學院學報,2010,27(5):88.
DU H Y,CHANG Y X,LIU H P.Study advance of function mechanism of polyamines [J].JournalofZhoukouNormalUniversity,2010,27(5):88.
[10] 杜紅陽,李青芝,楊青華,等.亞精胺對滲透脅迫下小麥幼苗滲透調節物質含量和脯氨酸代謝酶活性的影響[J].麥類作物學報,2014,34(8):1092.
DU H Y,LI Q Z,YANG Q H,etal.Effects of spermidine on the content of osmoregulation substance and activity of proline metabolic enzyme in wheat seedling under osmotic stress [J].JournalofTriticeaeCrops,2014,34(8):1092.
[11] 劉懷攀,胡炳義,劉天學,等.亞精胺對滲透脅迫的玉米幼苗葉片NADPH氧化酶和抗氧化酶活性的影響[J].河南農業大學學報,2007,41(4):363.
LIU H P,HU B Y,LIU T X,etal.Effects of spermidine on the activities of NADPH oxidase and antioxidation enzymes in leaves of maize seedlings under osmotic stress [J].JournalofHenanAgriculturalUniversity,2007,41(4):363.
[12] 張志良,瞿偉菁,李小方.植物生理學實驗指導[M].第四版.北京:高等教育出版社,2009:32,227.
ZHANG Z L,QU W Q,LI X F.Laboratory Guide of Plant Physiology(4rd Ed.) [M].Beijing:Higher Education Press,2009:32,218.
[13] 李國瑞,馬宏亮,胡雯媚,等.西南麥區小麥品種萌發期抗旱性的綜合鑒定及評價[J].麥類作物學報, 2015,35(4):479.
LI G R, MA H L,HU W M,etal.Identification and evaluation of wheat cultivars for drought resistance during germination in southwest area [J].JournalofTriticeaeCrops,2015,35(4):479.
[14] 李合生.植物生理生化實驗原理和技術[M].北京:高等教育出版社,2000:184-195.
LI H S.Physiology and Biochemistry of Plant Experimental Principle and Technology [M].Beijing:Higher Education Press,2000:184-195.
[15] 鄒 琦.植物生理學實驗指導[M].北京:中國農業出版社,2000:172.
ZOU Q.Laboratory Guide of Plant Physiology [M].China Agriculture Press,2000:172.
[16] 黃愛纓,吳珍齡.水稻谷胱甘肽過氧化物酶的測定法[J].西南農業大學學報,1999,21(4):324.
HUANG A Y,WU Z L.Determination of glutathione peroxidase in rice seedlings [J].JournalofSouthwestAgriculturalUniversity,1999,21(4):324.
[17] SCHAEDLE M,BASHAM J A.Chloroplast glutathione reductace [J].PlantPhysiol,1977,59:1011.
[18] 安華明,陳力耕,樊衛國,等.高等植物中維生素C的功能、合成及代謝研究進展[J].植物學通報,2004,21(5):608.
AN H M,CHEN L G,FAN W G,etal.Advances in research on function,biosynthesis and metabolism of ascorbic acid in higher plant [J].ChineseBulletinofBotany,2004,21(5):608.
[19] 陳立松,劉星輝.水分脅迫對荔枝葉片氮和核酸代謝的影響與其抗旱性的關系[J].植物生理學報,1999,25(1):49.
CHEN L S,LIU X H.Effects of water stress on nitrogen and nucleic acid metabolisms in litchi(LitchichinensisSonn.)leaves and their relations to drought-resistance [J].ActaPhytophysiologicaSinica,1999,25(1):49.
[20] WEN X P,BAN Y,INOUE H,etal.Aluminum tolerance in a spermidine synthase-overexpressing transgenic European pear is correlated with the enhanced level of spermidine via alleviating oxidative status [J].EnvironmentalandExperimentalBotany,2009,66:471.
[21] HE L X,BAN Y,INOUE H,etal.Enhancement of spermidine content and antioxidant capacity in transgentic pear shoots overexpressing apple spermidine synthase in response to salinity and hyperosmosis [J].Phytochemistry,2008,69:2133.
[22] 朱為民,丁海東,齊乃敏,等.Cd2+脅迫對番茄幼苗抗壞血酸-谷胱甘肽代謝的影響[J].華北農學報,2005,20(3):50.
ZHU W M,DING H D,QI N M,etal.Effects of Cd2+stress on ascorbate-glutathion cycle metabolism in tomato seedlings [J].ActaAgriculturaeBoreali-sinica,2005,20(3):50.
Effect of Extraneous Spermidine on Growth and some Physiological Characteristics in Oat Seedlings under PEG Stress
WU Xuhong1,FENG Jingmin2
(1.College of Life Sciences,Agriculture and Forestry,Qiqihar University,Qiqihar,Heilongjiang 161006,China;2.Qiqihaer Sanitary Supervision Institute,Qiqihaer,Heilongjiang 161006,China)

Oat seedlings;Spermidine;Osmotic stress;Osmoregulation substance;Antioxidant characteristics
時間:2017-01-03
2016-04-07
2016-05-26
E-mail:wvg25583681129@sina.com
S512.1;S311
A
1009-1041(2017)01-0122-08
網絡出版地址:http://www.cnki.net/kcms/detail/61.1359.S.20170103.1629.034.html

