高效磷酸銀可見光催化劑的制備及脫除 NOx的性能研究
湯春妮,樊 君
(1. 陜西國防工業職業技術學院 化學工程學院,陜西 西安 710302; 2.西北大學化工學院,陜西 西安 710069)
高效磷酸銀可見光催化劑的制備及脫除 NOx的性能研究
湯春妮1,樊 君2
(1. 陜西國防工業職業技術學院 化學工程學院,陜西 西安 710302; 2.西北大學化工學院,陜西 西安 710069)
采用不同沉淀劑 Na3PO4、Na2HPO4、NaH2PO4通過水相沉淀法制備 Ag3PO4產物并考察其可見光催化脫除 NOx的性能。結果表明,不同沉淀劑對 Ag3PO4產物的晶相組成、形貌、光學性能和光催化活性有顯著影響,其中 Na2HPO4制備出的不規則狀純相 Ag3PO4樣品具有更高的光催化脫除 NOx的活性。
磷酸銀;光催化;脫除 NOx
氮氧化物(NOx)是主要的大氣污染物之一,不僅會引起如缺氧癥、肺水腫、神經衰弱和麻痹等身體危害[1],還會產生酸沉降、光化學煙霧、臭氧層破壞、溫室效應、富營養化、PM2.5 和城市灰霆天氣等環境污染[2]。因此,對 NOx的控制技術提出了嚴峻的挑戰。光催化技術脫除 NOx技術具有反應條件溫和、節能、綠色環保等優點,是目前相關研究的重點和熱點。
光催化技術的關鍵是光催化材料,其性能與自身理化性質密切相關,這又很大程度上取決于材料表面微結構,如形貌、顆粒大小、暴露晶面、比表面積等。因此,通過簡單易行的方法制備高效的Ag3PO4光催化劑,是提高其光催化性能的有效手段之一。由于水相直接沉淀法簡單、成本低,因此常被用來制備各種材料。本文主要考察不同磷酸鹽沉淀劑對Ag3PO4產物的結構、理化性質以及光催化脫除NOx性能的影響。
1 實驗部分
1.1 催化劑的制備
采用水相直接沉淀法制備 Ag3PO4產物。室溫下分別將三種 0.15 M 磷酸鹽(Na3PO4、Na2HPO4、NaH2PO4)溶液滴加至 0.05 M AgNO3溶液中。離心分離,洗滌沉淀數次后,真空干燥。不同沉淀劑制備 的 樣 品 被 依 次 標 記 為 Ag3PO4(Na3PO4) 、Ag3PO4(Na2HPO4) 和 Ag3PO4(NaH2PO4)。
1.2 光催化脫除NOx的實驗

圖1 光催化脫除 NOx反應裝置圖Fig.1Equipment ofphotocatalytic removal of NOx 1-NO 標準氣;2-全自動空氣源;3-加濕器;4-氣體混合器;5-流量控制器;6-反應器(石英玻璃,380 cm3);7-光源;8-NO 分析儀;9-NO2分析儀;10-NaOH 洗瓶
光催化脫除NOx實驗在自制的連續流動光催化實驗裝置中進行,如圖1所示。0.1g光催化劑置于反應器底部,光源采用高性能模擬日光氙燈光源(帶λ> 400 nm濾光片),進出口氣體采用NO分析儀和NO2分析儀在線監測。
光催化劑脫除 NOx的催化性能以穩定狀態下NO 轉化率(NO conversion (%))、NO2生成率(NO2formation (%))和 NOx去除率(NOxremoval (%))來評價,見下式:

其中,0NOC 、20NOC 、0NOCx分別為 NO、NO2和 NOx的初始濃度;NOC 、2NOC 和NOCx為光催化時間為 t 時 NO、NO2和 NOx的濃度(其中,

2 表征結果與討論
2.1 XRD 結果分析

圖2 不同 Ag3PO4樣品的 XRD 圖Fig.2 XRDpatterns of different Ag3PO4samples
由圖 2 可知,Ag3PO4(NaH2PO4)和 Ag3PO4(Na2HPO4)的 XRD 譜圖與立方晶型 Ag3PO4的標準卡片JCPDS 06-0505 相吻合,沒有出現其他雜質衍射峰。Ag3PO4(Na3PO4)的 XRD 圖中除了 Ag3PO4的特征衍射峰外,還在 2θ= 32.6°出現了一個弱峰,此峰可歸屬于 Ag2O(JCPDS 41-1104),說明 Ag3PO4(Na3PO4)是 Ag3PO4和 Ag2O 的混晶。出現這種現象的原因是不同磷酸鹽水解(式 4 和 5)后溶液的pH 環境不同,而酸堿度對 Ag3PO4沉淀生成有很大的影響。磷酸鹽會水解產生 OH-, 與pO43-競爭和 Ag+反應。在一定的 OH-濃度下,OH-會和 Ag+反應生成 AgOH,隨即脫水形成 Ag2O。不同磷酸鹽水解產生的 OH-濃度和pO43-濃度見表 1。


表1 不同磷酸鹽的初始pH、OH-和PO43-濃度和AgOH、Ag3PO4離子積Table 1 Initial pH values, OH- and PO43-concentrations,AgOH and Ag3PO4ion products of the precipitating agent
磷酸鹽溶液中pO43-的濃度可用式(6)計算:

Ag3PO4的溶度積常數 Ksp=1.4×10-16,AgOH 的Ksp=2.0×10-8[3,4]。從表 1可知,以 Na3PO4為沉淀劑時,由于初始的pO43-濃度很大,使初始 JAg3PO4>>KspAg3PO4,因此加入 Na3PO4后會快速形成大量的Ag3PO4晶核。 但初始的 OH-濃 度同樣 也很大JAgOH>> KspAgOH,同樣也會形成大量 AgOH 晶核(隨即脫水形成 Ag2O)。OH-會和pO43-一起競爭 Ag+,因此 XRD 圖中出現了 Ag2O 的特征峰。當以Na2HPO4為沉淀劑時,初始 JAg3PO4>> KspAg3PO4,而JAgOH> KspAgOH,因此 Ag3PO4的沉淀速率>>AgOH的沉淀速率,XRD 圖中沒有出現了 Ag2O 的特征峰。當以 NaH2PO4為沉淀劑時,初始 JAgOH< KspAgOH,因此不會有 AgOH 和 Ag2O 產生。初始 JAg3PO4>KspAg3PO4會有 Ag3PO4沉淀產生,但隨著反應的進行,JAg3PO4會逐漸減小,Ag3PO4沉淀將不會再產生,因此 Ag3PO4(NaH2PO4)的收率與 Ag3PO4(Na2HPO4)和Ag3PO4(Na3PO4)相比大大降低。
2.2 SEM結果分析
由圖 3 可以看出,3 種 Ag3PO4顆粒均為無規則狀,Ag3PO4(Na3PO4)粒徑范圍為 0.10~0.26 μm,平均粒 徑 0.16 μm ; Ag3PO4(Na2HPO4)粒 徑 范圍 為0.18~1.01μm,平均粒徑 0.50 μm;Ag3PO4(NaH2PO4)粒徑范圍 1.32~8.10 μm,平均粒徑 5.29 μm。樣品尺 寸出 現 Ag3PO4(Na3PO4)< Ag3PO4(Na2HPO4) <Ag3PO4(NaH2PO4)的原因可能是:
(1)初始 J Ag3PO4(Na3PO4)> J Ag3PO4(Na2HPO4)> JAg3PO4(NaH2PO4),使得 Ag3PO4的成核速率:Na3PO4>Na2HPO4> NaH2PO4,當成核速率較大時往往容易獲得晶粒多而尺寸小的細晶;當成核速率較小時容易獲得晶粒少而尺寸大的粗晶。
(2)當 Na3PO4為沉淀劑時,產生的 Ag2O 包圍在 Ag3PO4晶核周圍阻礙了其生長(Zener 釘扎),因此尺寸最小;當 Na2HPO4為沉淀劑時,雖然 Ag2O沒有被檢測出,但在晶體生長過程中 OH-和pO43-會在 Ag3PO4晶核表面競爭和 Ag+反應,因此尺寸比Ag3PO4(Na3PO4)大;當 NaH2PO4為沉淀劑時,既沒有 Ag2O 的 Zener 釘扎作用,OH-的競爭效應也非常小,因此尺寸最大。

圖3 不同磷酸鹽制備的Ag3PO4樣品的SEM圖:(a)Na3PO4, (b) Na2HPO4和(c) NaH2PO4Fig.3 SEM images of Ag3PO4prepared from (a) Na3PO4, (b) Na2HPO4, and (c) NaH2PO4
2.3 UV-Vis光譜結果分析
樣品 Ag3PO4(NaH2PO4)、Ag3PO4(Na2HPO4)、Ag3PO4(Na3PO4)的顏色分別為鮮黃色、黃綠色和棕黃色。由圖 4 可以看出,Ag3PO4不僅可以吸收太陽光中的紫外光部分,其吸收帶的邊緣已經延伸至可見光。三種樣品均可以吸收小于 530 nm 的光,在450 nm 附近均出現了肩峰,這可能為 Ag3PO4的光生電子從 O 2p 軌道躍遷到 Ag 5s 軌道引起的。Ag3PO4(Na3PO4)在 500 nm 后出現了較強的光吸收是源于黑色 Ag2O 的吸收。
2.4 PL光譜結果分析
從圖 5 中可以看出,Ag3PO4的pL 譜圖具有寬頻吸收特性(400~475 nm),且在 445 nm 處發光最強,這可能是由于簇和簇間的電荷轉移引起的電子-空 穴 對 復 合 導 致 的 , 如 [AgO4]-[PO4]簇 間 和[AgO4]-[AgO4] 簇 間[5]。 由 圖 還 可 看 出 , Ag3PO4(Na3PO4)和 Ag3PO4(NaH2PO4)的熒光強度均比 Ag3PO4(Na2HPO4)大。
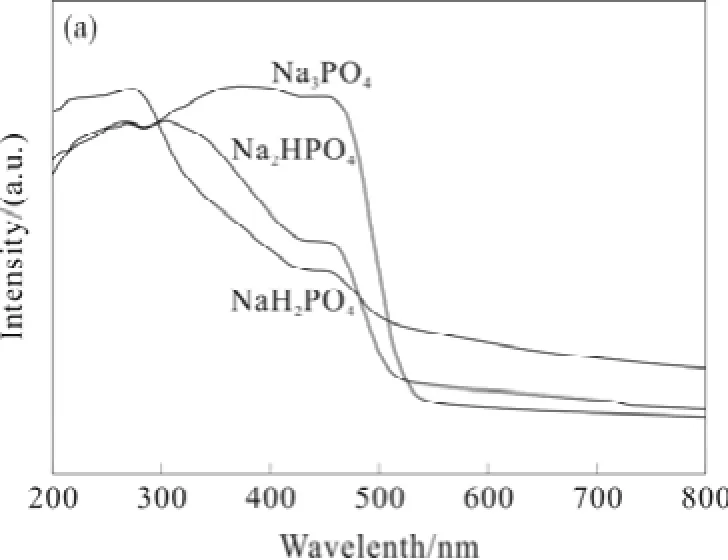
圖4 不同Ag3PO4樣品的UV-Vis 吸收譜圖Fig.4 Absorption spectra of different Ag3PO4samples
當Ag3PO4樣品受到光輻射而被激發形成光生電子和空穴后,在Ag3PO4(Na3PO4)中Ag2O成為載流子對復合中心,而Ag3PO4(NaH2PO4)尺寸較大,載流子在由顆粒內部遷移至表面的途中極易復合,因此Ag3PO4(Na3PO4)和Ag3PO4(NaH2PO4)的光生電子-空穴對的復合幾率比Ag3PO4(Na2HPO4)大。

圖5 不同Ag3PO4樣品的PL圖Fig.5pLpatterns of different Ag3PO4samples
2.5 BET結果分析
由表2可知,不同沉淀劑制備的產物的比表面積 和 孔 容 大 小 為 : Ag3PO4(Na3PO4)> Ag3PO4(Na2HPO4)> Ag3PO4(NaH2PO4)。催化劑的比表面積和孔容大,有利于反應活性位點的增加和反應物的吸附,從而有利于催化反應。

表2 不同Ag3PO4樣品的比表面積Table 2 Specific surface areas of different Ag3PO4samples
3 光催化脫除 NOx實驗結果與討論
由圖 6(a)可知,光催化反應開始后,NO 轉化率和 NO2生成率均迅速上升后二者趨于穩定。

圖6 (a) 不同Ag3PO4樣品在可見光下的NO轉化率和NO2形成率隨時間的變化曲線圖;(b) 樣品轉化NO的動力學特性圖;(c)樣品的NO轉化率、NO2形成率和NOx去除率Fig.6 (a)plots of the NO conversion and NO2formationvsirradiation time on different Ag3PO4samples under visible light irradiation; (b) Reaction rate constants in thepresence of samples; (c)photocatalytic NO conversion, NO2formation and NOxremoval over samples
對第一個 1min 下的實驗數據用擬一級動力學模型進行擬合。由圖 6(b)可知, Ag3PO4(Na3PO4)、Ag3PO4(Na2HPO4)和 Ag3PO4(NaH2PO4)光催化轉化 NO 的表觀動力學常數 k 分別為 0.0627、0.1357和 0.0563 min 。其中 Ag3PO4(Na2HPO4)的 k 是分別是 Ag3PO4(Na3PO4)和 Ag3PO4(NaH2PO4)的 2.16 和 2. 41倍。由圖 6(c)可以看出,Ag3PO4(Na3PO4)、A g3PO4(Na2HPO4)和 Ag3PO4(NaH2PO4)三種催化劑的NO 轉化率分別為 7.8%、15.0%和 6.2%;三種催化劑的 NOx去除率分別為 4.8%、9.2%和 3.5%。Ag3P O4(Na2HPO4)對 NOx光催化去除活性顯著高于 Ag3pO4(Na3PO4)和 Ag3PO4(NaH2PO4)。Ag3PO4(NaH2P O4)的比表面積最小,因此對反應物的吸附少、活性反應位點少,而且光生電子和空穴對的復合幾率大,導致其光催化反應活性最差。雖然 Ag3PO4(Na3PO4)的比表面積最大,但其中含有的 Ag2O 會減小其活性位點,而且光生載流子的復合幾率較大,這些均導致了催化反應活性的降低。
4 結 論
本文利用水相直接沉淀法,以不同的沉淀劑(Na3PO4、Na2HPO4、NaH2PO4)制備出 Ag3PO4產物,用不同表征手段對其晶相組成、形貌、光學性能、比表面積等進行表征,并考察了在可見光下脫除氣相中 NOx的光催化性能。結果表明不同沉淀劑使體系的pH 環境不同,以 Na3PO4制備的樣品為尺寸較小的 Ag3PO4和 Ag2O 的混合產物,以Na2HPO4和NaH2PO4制備的樣品為尺寸較大的純相Ag3PO4。相比于 Na3PO4和 NaH2PO4,以 Na2HPO4制備的無規則狀 Ag3PO4樣品具有更高的光催化活性,可脫除氣相中 9.2%的 NOx。
[1]蘇亞欣, 毛玉如, 徐璋. 燃煤氮氧化物控制排放技術[M]. 北京: 化學工業出版社, 2005: 43-54.
[2]Chuang K. H., Lu C. Y., Wey M. Y., et al. NO removal by activated carbon-supported copper catalystsprepared by impregnation,polyol, and microwave heatedpolyolprocesses[J]. Applied Catalysis A: General, 2011, 397(1-2): 234-240.
[3]Amornpitoksukp., Intarasuwan K., Suwanboon S., et al. Effect ofphosphate salts (Na3PO4, Na2HPO4, and NaH2PO4) on Ag3PO4morphology forphotocatalytic dye degradation under visible light and toxicity of the degraded dyeproducts[J]. Industrial & Engineering Chemistry Research, 2013, 52(49): 17369-17375.
[4]謝東. 溶液酸度與 Ag3PO4沉淀生成及溶解關系的討論[J]. 大學化學, 2011, 26(2): 73-74.
[5]Botelho G., Sczancoski J. C., Andres J, et al. Experimental and t heoretical study on the structure, opticalproperties, and growth of metallic silver nanostructures in Ag3PO4[J]. The Journal ofph ysical Chemistry C, 2015, 119(11): 6293-630.
Preparation of Efficient Silverphosphate Visible Lightphotocatalyst and Its NOxRemovalproperties
TANG Chun-ni1, FAN Jun2
(1. Department of Chemical Engineering, Shaanxi Institute of Technology, Shaanxi Xi’an 710302, China; 2. School of Chemical Engineering,Northwest University, Shaanxi Xi’an 710069, China)
Ag3PO4products wereprepared with differentprecipitation agents (Na3PO4,Na2HPO4,NaH2PO4) through the waterphaseprecipitation method, and NOxremovalperformances ofprepared visible lightphotocatalysts were investigated. The results show that differentprecipitation agents have remarkable effect onpurity, morphology, optical absorptionproperties andphotocatalytic activity ofproducts, and the irregular Ag3PO4prepared with Na2HPO4has the bestphotocatalytic NOxremoval efficiency.
Silverphosphate;photocatalysis; NOxremoval
TQ 032 O 482.3
: A
: 1671-0460(2017)02-0211-04
國家自然科學基金項目(21476183);陜西國防工業職業技術學院研究與開發項目(Gfy 16-36)。
2016-08-28
湯春妮(1985-),女,博士研究生,講師,研究方向:光催化材料開發、光催化反應體系設計以及光催化技術在能源轉換、環境治理和制藥方面的應用研究。E-mail:tcn2007@126.com。

