多級孔ZSM-5分子篩對亞甲基藍的吸附性能
張建民,吳喜勇,李紅璣,2,劉 娟
(1. 西安工程大學 環境與化學工程學院,陜西 西安 710048;2. 西安理工大學 水利水電學院,陜西 西安 710048)
多級孔ZSM-5分子篩對亞甲基藍的吸附性能
張建民1,吳喜勇1,李紅璣1,2,劉 娟1
(1. 西安工程大學 環境與化學工程學院,陜西 西安 710048;2. 西安理工大學 水利水電學院,陜西 西安 710048)
以多級孔ZSM-5分子篩為吸附劑,吸附水中的亞甲基藍(MB),考察了吸附條件對吸附效果的影響,并探討了吸附的熱力學和動力學特征。實驗結果表明:在溶液pH為11、分子篩加入量為800 mg/L、吸附溫度為303.15 K、吸附時間為60 min、初始MB質量濃度為20 mg/L的條件下,該分子篩對MB的吸附率達97%;溶液pH為5~12時,吸附率均達89%以上,說明該分子篩具有寬的pH適應范圍;該分子篩對MB的吸附熱力學符合Langmuir和Freundlich方程,293.15~313.15 K的飽和吸附量達50.51~62.11 mg/g,吸附為吸熱、自發過程;吸附動力學符合擬二級動力學方程。
多級孔ZSM-5分子篩;亞甲基藍;吸附動力學;吸附熱力學
染料廢水主要來源于印染工業廢水和染料生產廢水,其成分復雜、色度高、有機污染物含量高、可生化性差、難降解,屬較難處理工業廢水[1-4]。大多數染料及其代謝中間產物具有毒性和致癌性,其中,亞甲基藍(MB)為水溶性偶氮染料,在水溶液中以正一價季胺鹽離子基團的形式存在[5-6]。目前印染廢水的處理方法中吸附法因能耗低、可有效富集分離污染物而成為研究熱點,但其成本較高,且不能徹底降解污染物[7]。
ZSM-5分子篩是人工合成沸石中重要的吸附催化材料之一,屬于高硅五元環型沸石,熱穩定性、耐酸性及水熱穩定性良好,具有選擇吸附和高效吸附的特性[8-9]。分子篩對MB的吸附實際上是分子篩對水分子吸附飽和之后,解吸水分子,再吸附MB陽離子基團的過程,并于解吸速率與吸附速率相等時達到吸附平衡[10-11]。單一的微孔會限制吸附質在孔道中的傳遞,在微孔ZSM-5分子篩中引入介孔結構,不僅增大了孔道表面積和孔徑,而且提高了物質在孔道內的擴散速率,使吸附質能夠快速地擴散至活化位點,進而提高吸附效率,同時對大分子的有機物也有較好的吸附性能[12]。但對多級孔ZSM-5分子篩吸附性能的研究報道還很少。
本工作以多級孔ZSM-5分子篩為吸附劑,吸附水中的MB,考察了吸附條件對吸附效果的影響,并探討了吸附的熱力學和動力學特征,以期為下一步利用該材料光催化降解有機染料提供一定的理論依據。
1 實驗部分
1.1 試劑和儀器
MB、鹽酸、氫氧化鈉:分析純。
SHZ-88A型往復式恒溫水浴振蕩器:太倉市實驗設備廠;UV757CRT型紫外-可見分光光度計:上海光譜儀器有限公司;AL204型電子天平:瑞士Mettler-Toledo公司。
1.2 實驗方法
采用雙模板法,通過水熱合成制得多級孔ZSM-5分子篩[13]。
取25 mL一定濃度的MB溶液于離心管中,調節溶液pH,加入一定量的多級孔ZSM-5分子篩,一定溫度下于水浴搖床上振蕩一定時間后,離心分離。取上清液,采用紫外-可見分光光度計于664 nm波長處測定其吸光度,進而得到MB的質量濃度。
2 結果與討論
2.1 吸附條件對吸附效果的影響
2.1.1 溶液pH
在分子篩加入量為800 mg/L、吸附溫度為303.15 K、吸附時間為60 min、初始MB質量濃度為20 mg/L的條件下,溶液pH對MB吸附率的影響見圖1。由圖1可見:隨著pH的升高,多級孔ZSM-5分子篩對MB的吸附率先增大后略有減小,pH=11時達最大值97%;pH為5~12時,吸附率均較高,達89%以上,顯示該分子篩的吸附具有寬的pH適應范圍;MB在酸性條件下的吸附率明顯低于堿性條件。這是由于:pH影響著分子篩的活化位點[14],pH較低時,大量的H+占據著吸附位點,阻礙了分子篩與MB分子的結合,導致吸附率降低;而pH較高時,陽離子染料與分子篩的靜電引力作用增大,有利于吸附的進行;繼續增大pH,溶液中OH-濃度升高,分子篩骨架結構中部分Si流失而引起結構塌陷,影響了其吸附能力。因此,選擇溶液pH為11。
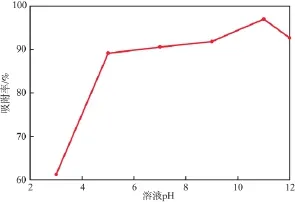
圖1 溶液pH對MB吸附率的影響
2.1.2 分子篩加入量
在溶液pH為11、吸附溫度為303.15 K、吸附時間為60 min、初始MB質量濃度為20 mg/L的條件下,分子篩加入量對MB吸附效果的影響見圖2。
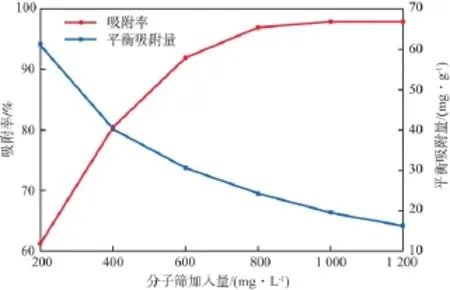
圖2 分子篩加入量對MB吸附效果的影響
由圖2可見:隨著分子篩用量的增加,MB的吸附率不斷增大,而平衡吸附量不斷減小;當分子篩用量為800 mg/L時,吸附率達97%,平衡吸附量為24.3 mg/g;之后,MB吸附率隨分子篩加入量的增加變化很小,而平衡吸附量的降低較為明顯。這是由于:被吸附的溶質的量以及單位質量吸附劑上的吸附活性位是一定的,因此,當吸附劑用量增加時,總的吸附活性位也隨之增加,使得MB的吸附速率加快,同時也導致單位質量吸附劑上的吸附活性位利用率下降,表現為吸附量的下降;繼續增大吸附劑用量,MB的剩余量趨近于零,故吸附效果未見明顯改變[15]。綜合考慮,選擇分子篩加入量為800 mg/L。
2.1.3 吸附溫度
在溶液pH為11、分子篩加入量為800 mg/L、吸附時間為60 min的條件下,分子篩對MB的吸附等溫線見圖3。由圖3可見,隨著溫度的升高,MB的平衡吸附量增大。根據液相吸附中的“溶劑置換”理論[16],升溫加快了MB的遷移速率,同時也加快了分子篩外表面吸附水分子的解吸;另一方面,隨著溫度的升高,溶液的黏度下降,吸附速率增大[17]。因此,升高溫度有利于多級孔ZSM-5分子篩對MB的吸附。
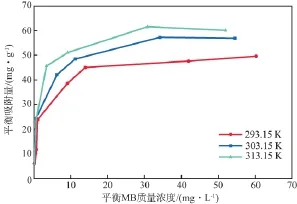
圖3 分子篩對MB的吸附等溫線
2.1.4 吸附時間和初始MB質量濃度
在溶液pH為11、分子篩加入量為800 mg/L、吸附溫度為303.15 K的條件下,吸附時間和初始MB質量濃度對MB吸附效果的影響見圖4。由圖4可見:隨著吸附時間的延長,吸附量增加,之后趨于平緩,瞬時吸附速率逐漸減小;隨著初始MB濃度的增加,平衡吸附量增大,吸附達到平衡的時間也會延長。多級孔ZSM-5分子篩對MB的吸附同時存在著吸附和解吸兩個過程,當吸附時間較短時,吸附速率大于解吸速率,故曲線呈上升趨勢;隨著吸附時間的延長,解吸速率逐漸加快,同時吸附材料表面的活性位點數量降低,吸附推動力逐漸減小,吸附速率逐漸減慢,直至吸附平衡。另一方面,在低濃度時,染料能迅速的占據吸附活性位點,而在較高濃度時,染料需要通過內擴散擴散至吸附劑表面,溶質分子間的空間位阻斥力會減緩吸附進程[18]。
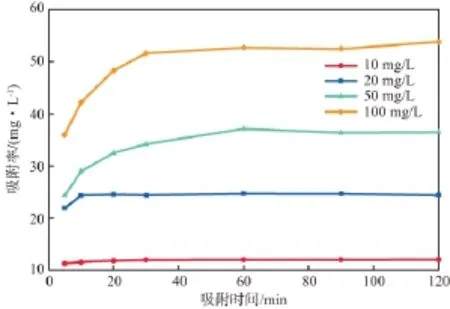
圖4 吸附時間和初始MB質量濃度對MB吸附效果的影響
2.2 吸附熱力學
2.2.1 等溫吸附方程
Langmuir和Freundlich方程是描述固液體系等溫吸附過程的最常用表達式,分別見式(1)和式(2)。

式中:ρe為吸附平衡時的MB質量濃度,mg/L;qe為平衡吸附量,mg/g;qsat為飽和吸附量,mg/ g;b為Langmuir吸附平衡常數,L/mg;n和K為Freundlich吸附特征常數。
采用上述方程對圖3的實驗數據進行擬合,擬合結果見表1。由表1可見:Langmuir和Freundlich方程均能描述多級孔ZSM-5分子篩對MB的吸附行為(相較而言,Langmuir方程更為適合),說明多級孔ZSM-5分子篩對于MB的吸附是多層吸附,提高MB濃度時飽和吸附量會持續增加[19];Langmuir方程的飽和吸附量隨溫度的升高而增大,由293.15 K時的50.51 mg/g增至313.15 K時的62.11 mg/g,表明該吸附過程為吸熱過程。

表1 等溫吸附方程的擬合結果
2.2.2 熱力學參數
根據范特霍夫方程(見式(3)),以lnb對T-1作圖(見圖5),由斜率可求得吸附焓變為14.51×103J/mol,為正值,說明該吸附過程為吸熱過程;由直線的截距可求得吸附熵變為150.16 J/(mol·K),大于0,表明分子篩對MB有很好的親和性,且在吸附過程中MB在吸附界面上是無序和隨機吸附的[20-21]。由ΔH和ΔS可得293.15,303.15,313.15 K下的吸附自由能變分別為-29.51,-31.01,
-32.52 kJ/mol,均為負值,說明吸附過程均為自發進行;且隨溫度升高,ΔG的絕對值變大,說明溫度越高,吸附過程的自發趨勢越大[22]。

式中:ΔH為吸附焓變,J/mol;R為通用氣體常數,8.314 J(/mol·K);T為吸附溫度,K;ΔS為吸附熵變,J(/mol·K)。
2.3 吸附動力學
吸附動力學模型可用Lagergren方程描述,一級反應速率方程反映顆粒內傳質阻力是吸附的限制因素,二級反應速率方程反映吸附的限制因素是吸附機制。分別采用Lagergren擬一級動力學方程(見式(4))和擬二級動力學方程(見式(5))對圖4的實驗數據進行擬合,擬合結果見表2。

圖5 范特霍夫方程的擬合線

式中:t為吸附時間,min;qt為t時刻的吸附量,mg/g;k1為擬一級吸附速率常數,min-1;k2為擬二級吸附速率常數,g(/mg·min)。
由表2可見,擬二級動力學方程對吸附過程的擬合度更高,不同初始MB濃度下的R2均大于0.99。擬二級反應動力學模型包含吸附的外部液膜擴散、表面吸附和顆粒內部擴散等過程[23],能夠更真實的反映MB在多級孔ZSM-5分子篩上的吸附機理。
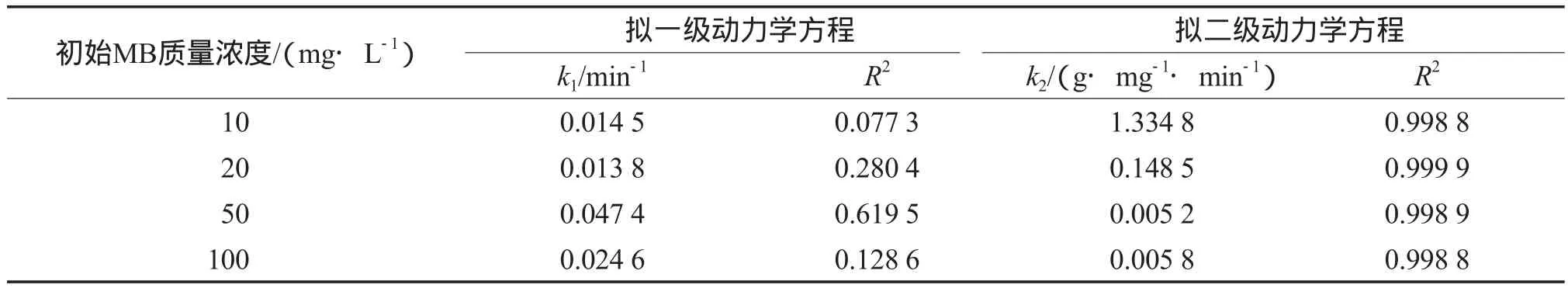
表2 動力學方程的擬合結果
3 結論
a)在溶液pH為11、分子篩加入量為800 mg/L、吸附溫度為303.15 K、吸附時間為60 min、初始MB質量濃度為20 mg/L的條件下,多級孔ZSM-5分子篩對MB的吸附率達97%;溶液pH為5~12時,吸附率均達89%以上,說明該分子篩具有寬的pH適應范圍。
b)多級孔ZSM-5分子篩對MB的吸附熱力學符合Langmuir和Freundlich方程,293.15~313.15 K的飽和吸附量達50.51~62.11 mg/g,吸附為吸熱、自發過程;吸附動力學符合擬二級動力學方程。
[1] Slokr Y M,Majcen Le Marechal A. Methods of decoloration of textile wastewater[J]. Dyes Pigments,1998,37(4):335 - 356.
[2] Liu H,Yang S,Ni Y. Comparison of dye behavior from aspen HYP:Dyes added in the HYP manufacturing process versus dyes added at the papermaking wet end[J]. J Wood Chem Technol,2010,30(2):118 - 128.
[3] Rebane R,Leito I,Yurchenko S,et al. A review of analytical techniques for determination of Sudan Ⅰ-Ⅳdyes in food matrixes[J]. J Chromatogr A,2010,1217(17):2747 - 2757.
[4] 李家珍. 染料、染色工業廢水處理[M]. 北京:化學工業出版社,1997:71 - 74.
[5] 姚超,劉敏,李為民,等. 凹凸棒石/氧化鋅納米復合材料對亞甲基藍的吸附性能[J]. 環境科學學報,2010,30(6):1211 - 1219.
[6] Kumar P S,Ramalingam S,Sathishkumar K. Removal of methylene blue dye from aqueous solution by activated carbon prepared from cashew nut shell as a new low-cost adsorbent[J]. Korean J Chem Eng,2011,28(1):149 - 155.
[7] 王會麗,趙越,馬樂寬,等. 復合改性膨脹石墨的制備及對酸性艷藍染料的吸附[J]. 高等學校化學學報,2016,37(2):335 - 341.
[8] Cheng Jifang,Pei Supeng,Yue Bin,et al. Synthesis and characterization of hollow zeolite microspheres with a mesoporous shell by O/W/O emulsion and vapor-phase transport method[J]. Microporous Mesoporous Mater,2008,115(3):383 - 388.
[9] Zhou Wei,Zhang Shiyu,Hao Xiangying,et al. MFI-type boroaluminosilicate:A comparative study between the direct synthesis and the templating method[J]. J Solid State Chem,2006,179(3):855 - 865.
[10] Hameed B H. Equilibrium and kinetic studies of methyl violet sorption by agricultural waste[J]. J Hazard Mater,2008,154(1/2/3):204 - 212.
[11] Ghosh D,Bhattacharyya K G. Adsorption of methylene blue on kaolinite[J]. Appl Clay Sci,2002,20(6):295 - 300.
[12] Serrano D P,Aguado J,Escola J M,et al. Hierarchical zeolites with enhanced textural and catalytic properties synthesized from organofunctionalized seeds[J]. Chem Mater,2006,18(10):2462 - 2464.
[13] 張建民,吳喜勇,李紅璣,等. 飽和ATP為原料合成多級孔ZSM-5沸石分子篩的制備與表征[J]. 應用化工,2016,45(11):2080 - 2083,2087.
[14] Monash P,Pugazhenthi G. Investigation of equilibrium and equilibrium and kinetic parameters of methylene blue adsorption onto MCM-41[J]. Korean J Chem Eng,2010,27(4):1184 - 1191.
[15] 羅玲玲. 石墨烯基復合介孔材料的制備及其對亞甲基藍的吸附性能研究[D]. 杭州:浙江師范大學,2014.
[16] G?kmen V,Serpen A. Equilibrium and kinetic studies on the adsorption of dark colored compounds from apple juice using adsorbent resin[J]. J Food Eng,2002,53(3):221 - 227.
[17] 彭書傳,王詩生,陳天虎,等. 坡縷石對水中亞甲基藍的吸附動力學[J]. 硅酸鹽學報,2006,34(6):733 - 738.
[18] 古興興. 介孔分子篩MCM-48對水溶液中有機物的吸附性能研究[D]. 杭州:浙江師范大學,2013.
[19] 李瑞月,陳德,李戀卿,等. 不同作物秸稈生物炭對溶液中Pb2+、Cd2+的吸附[J]. 農業環境科學學報,2015,34(5):1001 - 1008.
[20] 徐恩兵,李坤權,朱志強,等. 雙孔介孔碳的合成及其對亞甲基藍的吸附[J]. 環境化學,2015,34(1):137 - 143.
[21] Al-Rashed S M,Al-Gaid A A. Kinetic and thermodynamic studies on the adsorption behavior of Rhodamine B dye on Duolite C-20 resin[J]. J Saudi Chem Soc,2012,16(2):209 - 215.
[22] Arivoli S,Thenkuzhali M. Kinetic,mechanistic,thermodynamic and equilibrium studies on the adsorption of Rhodamine B by acid activated low cost carbon[J]. E-J Chem,2008,5(2):187 - 200.
[23] Chang Minyun,Juang Rueyshin. Adsorption of tannic acid,humic acid and dyes from water using the composite of chitosan and activated clay[J]. J Colloid Interface Sci,2004,278(1):18 - 25.
(編輯 魏京華)
Adsorption of methylene blue on hierarchically porous ZSM-5 molecular sieve
Zhang Jianmin1,Wu Xiyong1,Li Hongji1,2,Liu Juan1
(1. School of Environmental and Chemical Engineering,Xi’an Polytechnic University,Xi’an Shaanxi 710048,China;2. School of Water Resource and Hydropowder,Xi’an University of Technology,X’ian Shaanxi 710048,China)
The hierarchically porous ZSM-5 molecular sieve was used as to adsorb methylene blue(MB)in water. The effects of adsorption conditions on adsorption were investigated,and the adsorption thermodynamics and kinetics characteristics were also discussed. The experimental results show that:Under the conditions of solution pH 11,molecular sieve dosage 800 mg/L,adsorption temperature 303.15 K,adsorption time 60 min and initial MB mass concentration 20 mg/L,the adsorption rate of MB on the molecular sieve is up to 97%;when the solution pH is 5-12,the adsorption rates are all above 89%,which indicates that the molecular sieve has a wide adaptation range of pH;The adsorption thermodynamics of methylene blue on the molecular sieve follows the Langmuir and Freundlich adsorption equation,the adsorption capacity reaches 50.51-62.11 mg/g at 293.15-313.15 K,and the adsorption process is endothermic and spontaneous;The adsorption kinetics fi ts the pseudo-second-order kinetic model.
hierarchically porous ZSM-5 molecular sieve;methylene blue;adsorption thermodynamics;adsorption kinetics
X703.5
A
1006-1878(2017)01-0074-05
10.3969/j.issn.1006-1878.2017.01.013
2016 - 07 - 01;
2016 - 11 - 02。
張建民(1963—),男,陜西省韓城市人,學士,副教授,電話 13991392208,電郵 jm0865@sina.com。聯系人:吳喜勇,電話 18706784989,電郵 1058893607@qq.com。
陜西省教育廳專項科研計劃項目(15JK1327)。

