辛烯基琥珀酸-阿拉伯膠酯的合成工藝及乳化性能
石 燕,李 翠,羅 琦,歐陽佰玲,涂宗財,2,王 輝,黃 濤,張曉榮
(1.南昌大學食品學院,食品科學與技術國家重點實驗室,江西 南昌 330047;2.江西師范大學 功能有機小分子教育部重點實驗室,江西 南昌 330022)
辛烯基琥珀酸-阿拉伯膠酯的合成工藝及乳化性能
石 燕1,李 翠1,羅 琦1,歐陽佰玲1,涂宗財1,2,王 輝1,黃 濤1,張曉榮1
(1.南昌大學食品學院,食品科學與技術國家重點實驗室,江西 南昌 330047;2.江西師范大學 功能有機小分子教育部重點實驗室,江西 南昌 330022)
以阿拉伯膠(gum arabic,GA)和辛烯基琥珀酸酐(octenyl succinic anhydride,OSA)為原料,采用濕法制備辛烯基琥珀酸-阿拉伯膠酯(octenyl succinic acid-GA ester,OS-GA)。通過單因素試驗和響應面分析研究OS-GA的合成工藝,并對其產物乳化性能進行了研究。結果表明:OS-GA合成的較優組合為OSA添加量3.0%(以干基GA計)、GA溶液初始質量濃度40 g/100 mL、反應體系pH 8.85、反應溫度33 ℃、反應時間130 min。在此工藝條件下制備的OS-GA的辛烯基琥珀酸接入量為1.99%,其乳化能力及乳化穩定性均顯著提高。
阿拉伯膠;辛烯基琥珀酸酐;辛烯基琥珀酸-阿拉伯膠酯;響應面分析;乳化性能
阿拉伯膠(gum arabic,GA)主要產自非洲、是一種應用較為廣泛的親水性膠體[1],在食品行業中,常作為乳化穩定劑[2]、微膠囊壁材[3-4]、水溶性膳食纖維[5]等。其中乳化性能是GA的最主要的性能。但由于受到氣候、土壤、樹齡等的影響,不同來源的GA的乳化性能存在一定的差別[6]。且目前,商業化的GA主要來源于金合歡屬的Gemmiferae系和Vulgares系樹種,其中Acacia senegal和Acacia seyal是金合歡屬植物中被用于采集GA最多的兩類樹種[7],雖然來源于兩者的GA的氨基酸組成和糖鏈結構均相似,但由于來源于Acacia seyal的GA的鼠李糖及含氮量低,其乳化性能一般低于Acacia senegal[8-9]。故真正具有商業價值的GA產量非常有限[10-11]。因此如何提高來源于Acacia seyal的GA的乳化性能就顯得非常迫切。
目前,對GA進行改性應用較多的方法為“熟化法”,Al-Assaf[12]和Aoki[13]等通過“熟化”法制備出一種乳化性能較高的新型GA即SUPER GUMTM。但“熟化”過程中常涉及到高溫加熱,可能會造成GA褐變、結塊、焦化最終影響產品質量。而采用酯化法對GA進行改性,使GA分子接入疏水性基團,進一步提高其應用性能已逐漸成為研究的熱點。酯化法操作簡單,產品無異味、無著色。Wang Hao等[14]利用濕法,采用十二烯基琥珀酸酐對GA進行酯化改性研究,發現改性后的GA的乳化性能得到大幅度提高。Sarkar等[15]利用干法,采用辛烯基琥珀酸酐(octenyl succinic anhydride,OSA)對GA進行酯化改性研究,同樣發現改性后的GA的乳化性得到提高,但干法可能存在局部反應劇烈,產品性能不一致的問題。
因此,本實驗以GA和OSA為原料,采用濕法工藝制備辛烯基琥珀酸-阿拉伯膠酯(octenyl succinic acid-GA ester,OS-GA),考察OSA添加量、GA溶液初始質量濃度、反應體系pH值、反應溫度和反應時間對酯化反應的影響,通過響應面分析法研究OS-GA的最佳制備工藝條件,以期制備出高乳化性能的GA改性產品,拓寬GA在食品中的應用范圍。
1 材料與方法
1.1 材料與試劑
GA(Acacia seyal樹種) 法國Nexira有限公司;OSA(優級純) 深圳市思利凱貿易有限公司;月見草油(食品級) 天津寶信國際油脂生物工程有限公司;乙腈、甲醇(均為色譜純) 美國Tedia有限公司;其他化學試劑均為分析純。
1.2 儀器與設備
MDR.P-5型噴霧干燥機 無錫市現代噴霧干燥設備有限公司;D-2000 HSM高效液相色譜儀 日本Hitachi公司;Nicolet Nexus FT-IR傅里葉變換紅外光譜儀美國Thermo Nicolet公司;Nicomp 380ZLS 美國PPS公司;TU-1810紫外分光光度計 北京普析通用儀器有限責任公司。
1.3 方法
1.3.1 OS-GA的制備[16]
稱取一定質量的GA與適量蒸餾水混合,配成一定質量濃度的溶液,用恒溫磁力攪拌器控制反應溫度與攪拌速度,調節溶液pH值為8.00左右,分批加入經乙醇稀釋數倍(V/V)的OSA,控制在一定的時間內加完,反應過程中用氫氧化鈉溶液維持體系pH值,待反應結束后用鹽酸溶液將體系pH值調到6.00左右,最后進行噴霧干燥,冷卻、收集得到OS-GA。
1.3.2 單因素試驗
考察OSA添加量(1.0%、1.5%、2.0%、2.5%、3.0%)、GA溶液初始質量濃度(25、30、35、40、45 g/100 mL)、反應體系pH值(7.50、8.00、8.50、9.00、9.50)、反應溫度(20、30、40、50、60 ℃)、反應時間(0.5、1.0、1.5、2.0、2.5 h)對OS-GA的OS接入量的影響,采用1.3.1節的方法制備OS-GA,以OS接入量值作為評價指標。
1.3.3 響應面試驗設計
根據單因素的試驗結果,利用響應面法,采用Box-Behnken模型,以反應體系pH值(A)、反應溫度(B)、反應時間(C)為響應因素,以OS接入量為響應值設計三因素三水平試驗,如表1所示。
1.3.4 OS接入量的測定[17]
色譜條件:Wa t e r s N o v a-P a k?C18色譜柱(3.9 mm×150 mm,4 μm);流動相:乙腈-超純水(35∶65,V/V);流速1.0 mL/min;進樣量10 μL;紫外檢測器波長200 nm;柱溫25 ℃。
精確稱取OS-GA(m1,0.050 0 g),置于50 mL離心管中。向其中加入1 mL超純水溶解20 min。磁力攪拌1 h后,收集上清液2 mL與1 mL的超純水(pH 3.00)混合。最后進行高效液相色譜分析,游離OS的質量(mfree,g)由峰面積和標準曲線(Y=19.369X-0.066,R2=0.999)決定。
精確稱取OS-GA(m2,0.500 0 g),置于50 mL離心管中,向其中加入10 mL 4 mol/L的氫氧化鈉溶液,在磁力攪拌下水解24 h。將水解后的2 mL OS-GA溶液轉移至25 mL容量瓶中,向其中加入18 mL 1 mol/L鹽酸溶液,用乙腈定容。最后進行高效液相色譜分析,總OS的質量(mtotal,g)由峰面積和標準曲線決定。OS接入量計算公式如式(1)~(3):

1.3.5 紅外光譜測定
將OS-GA用無水乙醇重復洗滌5 次,除去未參加反應的OSA,放置在40 ℃的干燥箱,干燥6 h后,采用傅里葉變換紅外光譜,以KBr壓片法,分析OS-GA產品的光譜學特性。紅外光譜儀的波長寬度設定為400~4 000 cm-1。
1.3.6 樣品乳化性能的測定[18-19]
將0.60 g GA和洗滌后的OS-GA(同1.3.5節)分別溶于60 ℃蒸餾水中,配制成質量分數為7.5%的樣品溶液,分別向其中加入2.00 g的月見草油,5檔,剪切分散2 min后,立即從乳液底部取30 μL,稀釋于25 mL 0.1%十二烷基磺酸鈉(sodium dodecyl sulfate,SDS)溶液中,以0.1% SDS溶液為空白對照,利用分光光度計在500 nm波長處測定其吸光度即乳化能力。
分別用蒸餾水將少量剛制備的乳狀液和在室溫條件下貯藏48 h后的乳狀液稀釋1 000 倍,采用激光粒度儀對其粒徑進行測定[20]。
2 結果與分析
2.1 單因素試驗結果
2.1.1 OSA添加量對酯化反應的影響
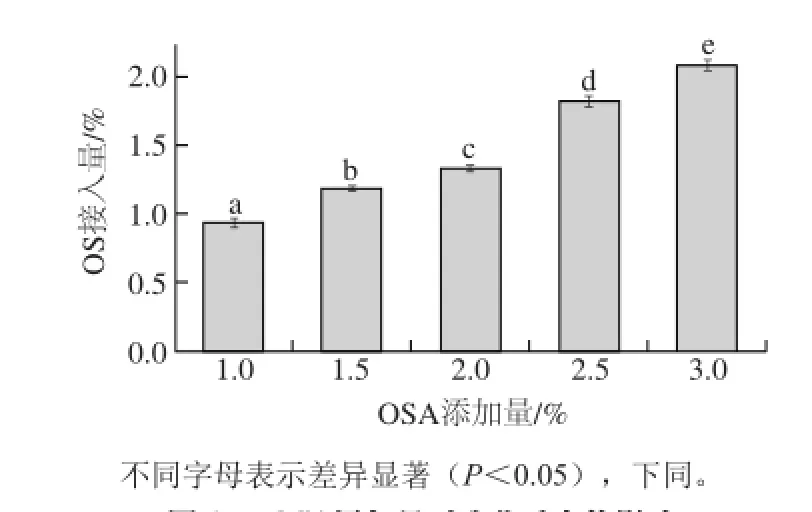
圖1 OSA添加量對酯化反應的影響Fig.1 Effect of OSA concentration on OS grafting rate
OSA作為反應試劑,其添加量直接影響到最終產品的OS接入量。聯合國糧食及農業組織規定合成OS-GA的OSA添加量不能超過3.0%。在保持GA溶液初始質量濃度30 g/100 mL、反應體系pH 8.00、反應溫度40 ℃、反應時間1.5 h的條件下,考察OSA添加量對酯化反應的影響(圖1),隨OSA添加量的增加,OS-GA的OS接入量顯著增大,這是由于增加反應物的量可使反應物分子之間的接觸機會增大,反應更易向產物方向進行[21],OSA添加量選用3.0%。
2.1.2 GA溶液初始質量濃度對酯化反應的影響
在OSA添加量3.0%、反應體系pH 8.00、反應溫度40 ℃、反應時間1.5 h的條件下,改變GA溶液初始質量濃度,見圖2。當GA溶液初始質量濃度從25%升高到40%時,OS接入量從1.57增大到1.79,質量濃度在40 g/100 mL時,OS接入量最大。當質量濃度升高到45 g/100 mL時,OS接入量有下降趨勢。這是因為酯化反應是可逆的競爭性反應,在低質量濃度時提高GA的質量濃度,增加了GA上離子化的羥基基團和疏水性酸酐的接觸機會,同時由于反應體系中水含量的減少也可促進酯化反應向產物進行,表現為OS接入量增加。當質量濃度超過一定數值后,反應液黏度增大,攪拌困難,OSA在反應體系中擴散不充分,從而影響OSA與GA中羥基接觸的機會,導致OS-GA的OS接入量下降。因此,初始質量濃度選用40 g/100 mL。
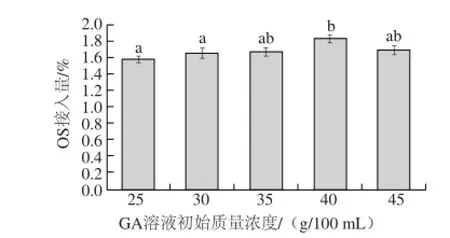
圖2 GA溶液初始質量濃度對酯化反應的影響Fig.2 Effect of initial concentration of GA on OS grafting rate
2.1.3 反應體系pH值對酯化反應的影響

圖3 反應體系pH值對酯化反應的影響Fig.3 Effect of reaction pH on OS grafting rate
在O S A添加量3.0%、G A溶液初始質量濃度40 g/100 mL、反應溫度40 ℃、反應時間1.5 h的條件下,改變溶液的pH值(圖3)。當pH值不大于9.00時,OS-GA的OS接入量隨pH值的增加而增大,而當pH 9.50時,OS-GA的OS接入量減小。這可能是由于反應體系pH值較低時,GA分子上的羥基難形成有效的親核基團,從而影響GA羥基和疏水酸酐的順利反應;而pH值過高時,易發生和酯化反應競爭的產物水解、OSA與堿反應及OSA自身水解等副反應。因此,GA與OSA酯化反應的pH值選9.00最為合適。
2.1.4 反應溫度對酯化反應的影響
適當的反應溫度,不僅能提高OS-GA的OS接入量,還能降低體系能量的消耗和制備的成本。在OSA添加量3.0%、GA溶液初始質量濃度40 g/100 mL、反應體系pH 9.00、反應時間1.5 h不變的情況下,考察反應溫度對產品OS接入量的影響,如圖4所示。反應初期,隨著溫度的升高產物的OS接入量增大;溫度超過30 ℃后,OS接入量開始下降。這是由于溫度升高有利于OSA在反應溶液中擴散,從而使反應速率增加,OS接入量增大,但溫度偏高,易造成酯化產物、OSA等發生水解副反應,致使產物的OS接入量減小[16]。GA與OSA酯化反應溫度控制在30 ℃最為合適。

圖4 反應溫度對酯化反應的影響Fig.4 Effect of reaction temperature on OS grafting rate
2.1.5 反應時間對酯化反應的影響

圖5 反應時間對酯化反應的影響Fig.5 Effect of reaction time on OS grafting rate
在O S A添加量3.0%、G A溶液初始質量濃度40 g/100 mL、反應體系pH 9.00、反應溫度30 ℃的條件下,考察反應時間對OS接入量的影響。如圖5所示,0.5~2.0 h內,OS接入量隨著反應時間的延長而增大,在2.5 h時,反而減小。這可能是由于酯化反應過程中存在著酯化與水解的可逆反應,在反應的初始階段正反應處于主導地位,故產品的OS接入量呈上升趨勢。當反應到一定的時間,隨著產物的濃度增大,逆反應逐漸處于主導地位,使得產品的OS接入量緩慢下降。GA與OSA酯化反應時間控制在2.0 h最為合適。
2.2 響應面試驗結果
根據三因素三水平的響應面試驗設計,共建立15 個試驗點,試驗結果見表2,方差分析見表3,各因素交互作用對響應值的影響見圖6。采用統計軟件Design-Expert進行數據處理。

表2 GA酯化反應響應面試驗設計及結果Table2 Response surface design with experimental results for GA esterif i cation
對表2數據進行分析,各個因素與OS接入量之間的多元二次回歸方程如下:
Y=2.00-0.044A+0.069B+0.072C+0.0025AB+ 0.015AC-0.035BC-0.064A2-0.11B2-0.091C2

表3 GA酯化反應響應面試驗方差分析結果Table3 Analysis of variance of the developed regression model
如表3所示,模型的回歸項顯著(P=0.019 2<0.05),而失擬項不顯著(P=0.511 2>0.05),說明此方程具有較高的可信性。此外,響應面模型對應的回歸方程,其一次項B(反應溫度)和C(反應時間)和二次項B2和C2的影響都是顯著的,在選取的因素水平范圍內,對酯化反應的OS接入量的影響大小依次為:反應時間>反應溫度>反應體系pH值。


圖6 各因素交互作用對酯化反應的影響Fig.6 Response surface plots showing the effects of reaction conditions on OS grafting rate
如圖6所示,AB、AC、BC的等高線接近于圓形,由于等高線的形狀可反映出交互效應的強弱,橢圓形表示兩因素交互作用顯著,越接近圓形,交互作用越弱[22],故交互作用不顯著。
2.3 OS-GA合成最優工藝條件確定
應用響應面法對回歸模型進行分析得到最優結果為反應體系pH 8.85、反應溫度32.6 ℃、反應時間129.6 min。最大OS-GA的OS接入量的預測值為2.03%。考慮到實際操作條件的限制,確定最優工藝參數為反應體系pH 8.85、反應溫度33 ℃、反應時間130 min。根據選取的工藝條件進行3 次重復驗證實驗,測定結果取平均值,得到產物OS接入量為1.99%,相對標準偏差為1.34%。相對標準偏差較小,說明模型可信度較高。
2.4 紅外光譜分析

圖7 GA與OS-GA的紅外光譜圖Fig.7 FTIR spectra of GA and OS-GA
GA和OS-GA(OS接入量為1.80)的OS-GA的紅外光譜圖如圖7所示。經OSA酯化后的樣品的紅外光譜圖在波數為1 724 cm-1左右處出現了新的羰基(C=O)伸縮振動吸收峰[23],說明OSA與GA發生了酯化反應[14],并以酯鍵的形式與GA上羥基相連。除波數1 724 cm-1外,GA與OS-GA的紅外吸收光譜圖基本相同,說明改性除了引入OS基團外,未引入其他物質,一方面保持了原GA的基本結構和性質,保障其食用安全;另一方面引入了新的疏水性基團,提高其乳化性能,使其應用領域更加廣泛。
2.5 樣品的乳化性能
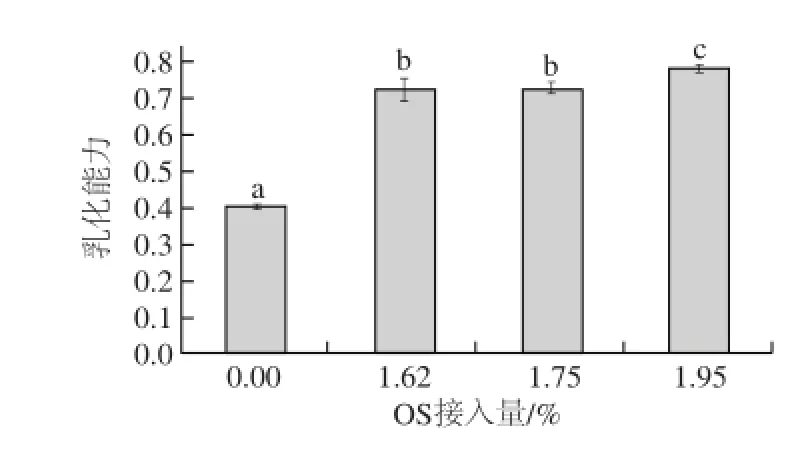
圖8 GA與不同OS接入量的OS-GA的乳化能力Fig.8 Emulsifying capacity of GA and OS-GA with different OS grafting rate
GA與不同OS接入量的OS-GA的乳化能力如圖8所示,GA經OSA酯化后乳化能力顯著增強,并隨OSA接入量的增加而增強,OS接入量為1.95%的OS-GA的乳化能力比GA增大近1 倍。這是由于OS-GA引入了親水的羧酸基團和疏水的烯基長鏈,對水、油的親和能力提高,在一定范圍內,OS接入量值越大,羧酸和烯基長鏈的含量就越高,乳化能力越強[24]。

表4 GA與OS-GA的乳狀液平均粒徑Table4 Average particle sizes of emulsions stabilized by GA and OS-GA
GA與不同OS接入量的OS-GA乳狀液平均粒徑見表4。酯化改性后的GA的平均粒徑均顯著低于GA,但3 種改性GA的平均粒徑無顯著性差異。這可能是由于在制備乳狀液剪切過程中,在一定范圍內,乳化能力越強,吸附在油滴上的速度越快,乳液粒徑就越小。貯藏48 h后的乳狀液,GA明顯分層,而酯化改性后的GA無分層現象,這可能是由于GA經過OSA酯化改性后,形成的油水界面壓力降低,油水界面膜更穩定,從而使乳狀液更穩定[25]。OS-GA3的平均粒徑小于OS-GA1、OS-GA2,且貯藏前后幾乎無變化,表明乳狀液的穩定性與OS接入量密切相關。
3 結 論
在單因素試驗的基礎上利用響應面軟件優化制備OS-GA的最佳條件,得出對酯化反應影響的3 個因素顯著性順序為:反應時間>反應溫度>反應體系pH值。在分析上述3 個因素對整個反應的交互作用的基礎上獲得制備產品的最佳條件為在OSA添加量3.0%(以干基GA計)、GA溶液初始質量濃度40 g/100 mL的反應體系中,控制pH值為8.85、反應溫度33 ℃、反應時間130 min,所得OS-GA的OS接入量為1.99%。改性后的GA的乳化性能得到顯著提高。
[1] 胡國華. 阿拉伯膠在食品工業中的應用[J]. 糧油食品科技, 2003, 11(2): 7-8. DOI:10.16210/j.cnki.1007-7561.2003.02.004.
[2] BUFFO R A, REINECCIUS G A, OEHLERT G W. Inf l uence of timetemperature treatments on the emulsifying properties of gum acacia in beverage emulsions[J]. Journal of Food Engineering, 2002, 51(4): 341-345. DOI:10.1016/S0260-8774(01)00076-0.
[3] HERMANTO R F, KHASANAH L U, ATMAKA W, et al. Physical characteristics of cinnamon oil microcapsule[C]//IOP Conference Series: Materials Science and Engineering, 2016, 107(1): 012064.
[4] SHI Yan, WANG Shujie, TU Zongcai, et al. Quality evaluation of peony seed oil spray-dried in different combinations of wall materials during encapsulation and storage[J]. Journal of Food Science and Technology, 2016, 53(6): 1-9. DOI:10.1007/s13197-016-2225-9.
[5] PATEL S, GOYAL A. Applications of natural polymer gum arabic: a review[J]. International Journal of Food Properties, 2015, 18(5): 986-998. DOI:10.1080/10942912.2013.809541.
[6] IDRIS O H M, WILLIAMS P A, PHILLIPS G O. Characterisation of gum from Acacia senegal trees of different age and location using multidetection gel permeation chromatography[J]. Food Hydrocolloids, 1998, 12(4): 379-388. DOI:10.1016/S0268-005X(98)00058-7.
[7] Al-ASSAF S, PHILLIPS G O, WILLIAMS P A. Studies on Acacia exudate gums: part Ⅱ. molecular weight comparison of the Vulgares and Gummiferae series of Acacia gums[J]. Food Hydrocolloids, 2005, 19(4): 661-667. DOI:10.1016/j.foodhyd.2004.09.003.
[8] 王衛平. 阿拉伯膠的種類及性質與功能的研究[J]. 中國食品添加劑, 2002(2): 22-28.
[9] 呂怡, 張曉鳴. 阿拉伯膠種類對復合凝聚微膠囊成囊性質研究[J]. 食品工業科技, 2012, 33(10): 124-127. DOI:10.13386/ j.issn1002-0306.2012.10.053.
[10] 李景恩. 江香薷多糖和兩種阿拉伯膠的結構解析及功能特性[D]. 南昌: 南昌大學, 2014: 94-95.
[11] 楊雷, 仇丹, 周逸奎, 等. 阿拉伯膠的結構特征和乳化性能研究進展[J]. 食品工業科技, 2013, 34(12): 353-356. DOI:10.13386/ j.issn1002-0306.2013.12.049.
[12] Al-ASSAF S, PHILLIPS G O, AOKI H, et al. Characterization and properties of Acacia senegal (L.) Willd. var. senegal with enhanced properties (Acacia (sen) SUPER GUM?): Part 1: controlled maturation of Acacia senegal var. senegal to increase viscoelasticity, produce a hydrogel form and convert a poor into a good emulsif i er[J]. Food Hydrocolloids, 2007, 21(3): 319-328. DOI:10.1016/ j.foodhyd.2006.04.011.
[13] AOKI H, Al-ASSAF S, KATAYAMA T, et al. Characterization and properties of Acacia senegal (L.) Willd. var. senegal with enhanced properties (Acacia (sen) SUPER GUM?): Part 2: mechanism of the maturation process[J]. Food Hydrocolloids, 2007, 21(3): 329-337. DOI:10.1016/j.foodhyd.2006.04.002.
[14] WANG H, WILLIAMS P A, SENAN C. Synthesis, characterization and emulsification properties of dodecenyl succinic anhydride derivatives of gum Arabic[J]. Food Hydrocolloids, 2014, 37: 143-148. DOI:10.1016/j.foodhyd.2013.10.033.
[15] SARKAR S, SINGHAL R S. Esterif i cation of guar gum hydrolysate and gum arabic with n-octenyl succinic anhydride and oleic acid and its evaluation as wall material in microencapsulation[J]. Carbohydrate Polymers, 2011, 86(4): 1723-1731. DOI:10.1016/ j.carbpol.2011.07.003.
[16] RUAN Hui, CHEN Qihe, FU Mingliang, et al. Preparation and properties of octenyl succinic anhydride modified potato starch[J]. Food Chemistry, 2009, 114(1): 81-86. DOI:10.1016/ j.foodchem.2008.09.019.
[17] DAN Qiu, BAI Yanjie, SHI Yongchen. Identification of isomers and determination of octenylsuccinate in modified starch by HPLC and mass spectrometry[J]. Food Chemistry, 2012, 135(2): 665-671. DOI:10.1016/j.foodchem.2012.04.117.
[18] CHIKAMAI B N, BANKS W B, ANDERSON D M W, et al. Processing of gum arabic and some new opportunities[J]. Food Hydrocolloids, 1996, 10(3): 309-316. DOI:10.1016/S0268-005X(96)80006-3.
[19] PEARCE K N, KINSELLA J E. Emulsifying properties of proteins: evaluation of a turbidimetric technique[J]. Journal of Agricultural and Food Chemistry, 1978, 26(3): 716-723. DOI:10.1021/jf60217a041.
[20] LIU Chengmei, ZHONG Junzhen, LIU Wei, et al. Relationship between functional properties and aggregation changes of whey protein induced by high pressure microfluidization[J]. Journal of Food Science, 2011, 76(4): E341-E347. DOI:10.1111/j.1750-3841.2011.02134.x.
[21] 劉強, 鄔應龍, 何靖柳. 響應面法優化氧化辛烯基琥珀酸甘薯淀粉酯的制備工藝[J]. 食品科學, 2011, 32(20): 13-16.
[22] 黃群, 麻成金, 余佶, 等. 產Monacolin K紅曲霉篩選及響應面法優化發酵條件[J]. 食品科學, 2011, 32(21): 177-182.
[23] ZHANG Bin, HUANG Qiang, LUO Faxing, et al. Effects of octenylsuccinylation on the structure and properties of high-amylose maize starch[J]. Carbohydrate Polymers, 2011, 84(4): 1276-1281. DOI:10.1016/j.carbpol.2011.01.020.
[24] 梁葉星, 熊家艷, 王永紅, 等. 辛烯基琥珀酸魔芋葡甘聚糖酯的微波半干法制備工藝及性能[J]. 食品科學, 2013, 34(14): 163-168. DOI:10.7506/spkx1002-6630-201314033.
[25] 魏本喜, 張曉紅, 管小宇, 等. 辛烯基琥珀酸白糊精酯的制備與乳化性質[J]. 食品與發酵工業, 2013, 39(11): 58-61. DOI:10.13995/ j.cnki.11-1802/ts.2013.11.026.
Synthesis and Emulsif i cation Properties of Octenyl Succinic Anhydride-Modif i ed Gum Arabic
SHI Yan1, LI Cui1, LUO Qi1, OUYANG Bailing1, TU Zongcai1,2, WANG Hui1, HUANG Tao1, ZHANG Xiaorong1
(1. State Key Laboratory of Food Science and Technology, School of Food Science and Technology, Nanchang University, Nanchang 330047, China; 2. Key Laboratory of Functional Small Organic Molecule, Ministry of Education, Jiangxi Normal University, Nanchang 330022, China)
Octenyl succinic anhydride modified-gum arabic (OS-GA) was prepared from gum arabic (GA) and octenyl succinic anhydride (OSA) by a wet method. The synthesis process was optimized by the combined use of one-factor-at-atime method and response surface methodology, and emulsif i cation properties of the synthesized product were determined. The optimal synthesis conditions for OS-GA were determined as follows: OSA, 3.0% (based on the dry weight of GA); initial mass concentration of GA, 40 g/100 mL; pH, 8.85; reaction temperature, 33 ℃; and reaction time, 130 min. Under these conditions, the grafting rate of OS in OS-GA was 1.99%, and its emulsion capacity and emulsion stability were enhanced signif i cantly compared with those of GA.
gum arabic; octenyl succinic anhydride; octenyl succinic acid-GA ester; response surface analysis; emulsif i cation properties
10.7506/spkx1002-6630-201704034
TS202.3
A
1002-6630(2017)04-0211-06
石燕, 李翠, 羅琦, 等. 辛烯基琥珀酸-阿拉伯膠酯的合成工藝及乳化性能[J]. 食品科學, 2017, 38(4): 211-216.
DOI:10.7506/spkx1002-6630-201704034. http://www.spkx.net.cn
SHI Yan, LI Cui, LUO Qi, et al. Synthesis and emulsification properties of octenyl succinic anhydride-modified gum arabic[J]. Food Science, 2017, 38(4): 211-216. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201704034. http://www.spkx.net.cn
2016-05-29
國家自然科學基金地區科學基金項目(31360390);江西省重點研發計劃農業領域項目(20161BBF60097)
石燕(1964—),女,教授,博士,研究方向為微膠囊技術在食品中的應用。E-mail:shiyan@ncu.edu.cn

