黃酒中總糖與還原糖含量測定方法比較
魏茹霞


摘 要:新環境之下,消費者對酒類的消費觀念得到了提升,黃酒的總糖含量是區別不同類型黃酒的主要指標。分別通過廉愛農法和亞鐵氰化鉀滴定法測定黃酒中總糖與還原糖的含量,基于實驗測定和參與能力,對式樣樣品處理效果作了簡要的分析、探討,結果分析得出黃酒中的總糖比還原糖的糖含量高。
關鍵詞:黃酒;總糖;還原糖;含量測定
中圖分類號:TS262.4 文獻標識碼:A DOI:10.15913/j.cnki.kjycx.2016.22.118
黃酒(Chineserice wine)是以稻米、黍米、玉米、小米或小麥等為主要原料,經蒸煮、加曲、糖化、發酵、壓榨、澄清、過濾、煎酒、貯存和勾兌而成的釀造酒,是中華民族的傳統酒,也是華夏瑰寶和酒中奇葩。當前,隨著我國經濟的快速發展、人民生活質量的提高和健康意識的增強,廣大消費者對酒類消費已從嗜好性向娛樂和鑒賞的方式過渡。愛高度、嗜烈性和求刺激的不良飲酒習俗日益為人們所摒棄,而健康、營養、安全和保健的新的飲酒觀念開始盛行,對黃酒的類型、品質也就有了更高的要求與追求。其中,黃酒的總糖含量是區別不同類型黃酒的主要指標,根據其中的總糖含量,可將黃酒分為干黃酒、半干黃酒、半甜黃酒、甜黃酒。總糖的測定方法較多,有廉愛農法、亞鐵氰化鉀滴定法、硫酸一苯酚法、蒽酮比色法和3,5一二硝基水楊酸比色法等。還原糖的操作方法與測定總糖的方法一樣,但其操作中樣品不需要經過水解處理。目前,用廉愛農法、亞鐵氰化鉀法測定黃酒中總糖、還原糖是工業化生產判斷黃酒類型的一種快速、精密度良好、成本低的測定方法。
1 材料
1.1 材料與試劑
黃酒酒樣:取自超市和農貿市場。
斐林甲、乙液;質量濃度為2.5 g/L的葡萄糖標準溶液;質量濃度為10 g/L的次甲基藍指示劑;物質的量濃度為6 mol/L的鹽酸溶液;質量濃度為1 g/L的甲基紅指示液;質量濃度為200 g/L的氫氧化鈉溶液(按GB/T 13662—20086.2.1.2試劑配制);微量甲、乙液;質量濃度為1 g/L的葡萄糖標準溶液(按GB/T 13662—2008中6.2.2.2規定配制)。
1.2 儀器
分析天平:感量為0.1 mg;分析天平:感量為0.01 g;電爐:300~500 W;電熱干燥箱;電熱恒溫水浴鍋;250 mL錐形瓶;滴定管。
2 方法
2.1 測定原理
廉愛農法的原理是:斐林溶液與還原糖共沸生成氧化亞銅沉淀,以次甲基藍為指示液,用試樣水解液滴定沸騰狀態的斐林溶液,達到終點時,稍微過量的還原糖將次甲基藍還原成無色為終點,依據試樣水解液的消耗體積,計算總糖含量。
亞鐵氰化鉀法的原理是:斐林溶液與還原糖共沸,在堿性
溶液中將銅離子還原成亞銅離子,并與溶液中的亞鐵氰化
鉀結合而呈黃色,以次甲基藍為指示劑,達到終點時,稍微過量的還原糖將次甲基藍還原成無色為終點,依據試樣水解液的消耗體積,計算總糖含量。
2.2 測定步驟
2.2.1 廉愛農法
2.2.1.1 標定斐林溶液預滴定
準確吸取斐林甲、乙液各5 mL于250 mL錐形瓶中,加水30 mL,混合后置于電爐上加熱至沸騰。滴入葡萄糖標準溶液,保持沸騰,待試液藍色即將消失時,加入次甲基藍指示液2滴,繼續用葡萄糖標準溶液滴定至藍色剛好消失為終點。記錄消耗葡萄糖標準溶液的體積(V)。
2.2.1.2 斐林溶液的標定
準確吸取斐林甲、乙液各5 mL于250 mL錐形瓶中,加水30 mL。混勻后加入比預滴定體積(V)少1 mL的葡萄糖標準溶液,置于電爐上加熱至沸騰,加入次甲基藍指示液2滴,保持沸騰2 min,繼續用葡萄糖標準溶液滴定至藍色剛好消失為終點,記錄消耗葡萄糖標準溶液的體積(V1)。全部滴定操作需在3 min內完成。
2.2.1.5 精密度
在重復性條件下獲得的兩次獨立測定結果的絕對差值不得超過算術平均值的5%.
2.2.2 亞鐵氰化鉀法
2.2.2.1 試樣處理
經品嘗預計含糖量高低吸取試樣2~10 mL(將水解液含糖量控制在1~2 g/L)于100 mL容量瓶中,加水30 mL和鹽酸溶液(物質的量濃度為6 mol/L)5 mL,在68~70 ℃水浴中加熱水解15 min冷卻后,加入甲基紅指示液2滴,再用氫氧化鈉溶液(質量濃度為200 g/L)中和至紅色消失(近似中性),加水定容至100 mL搖勻,用濾紙過濾后,作為試樣水解液備用。
2.2.2.2 空白試驗
準確吸取甲、乙液各5 mL于100 mL錐形瓶中,并加玻璃珠兩三粒,加入葡萄糖標準溶液9 mL,混勻后置于電爐上加熱,在2 min內沸騰,然后以4~5 s一滴的速度繼續滴入葡萄糖標準溶液,直至藍色消失立即呈現黃色為終點,記錄消耗葡萄糖標準溶液的總量(V0)。
2.2.2.3 預滴定
準確吸取甲、乙溶液各5 mL和試樣水解液5 mL于100 mL錐形瓶中,并加玻璃珠兩三粒,混勻后置于電爐上加熱至沸騰后,用葡萄糖標準溶液滴定至終點,記錄消耗葡萄糖標準溶液的體積。
2.2.2.4 正式滴定
準確吸取甲、乙液各5 mL和試樣水解液5 mL于100 mL錐形瓶中,并加玻璃珠兩三粒,加入比預滴定少1.00 mL葡萄糖標準溶液,搖勻后置于電爐上加熱至沸騰,繼續滴入葡萄糖標準溶液滴定至終點。記錄消耗葡萄糖標準溶液的總體積(V)。接近終點時,滴入的葡萄糖標準溶液的用量應控制在0.5~1.0 mL。
2.2.2.5 計算結果
2.2.2.6 精密度
在重復性條件下獲得的兩次獨立測定結果的絕對差值不得超過算術平均值的5%.
3 結果與分析
廉愛農法測定黃酒樣品中總糖與還原糖的數據結果如表1所示。由表1可知,利用廉愛農法測定黃酒樣品中的總糖與還原糖時,總糖比還原糖的糖含量高,兩者之間存在一定差距,但差距不大。
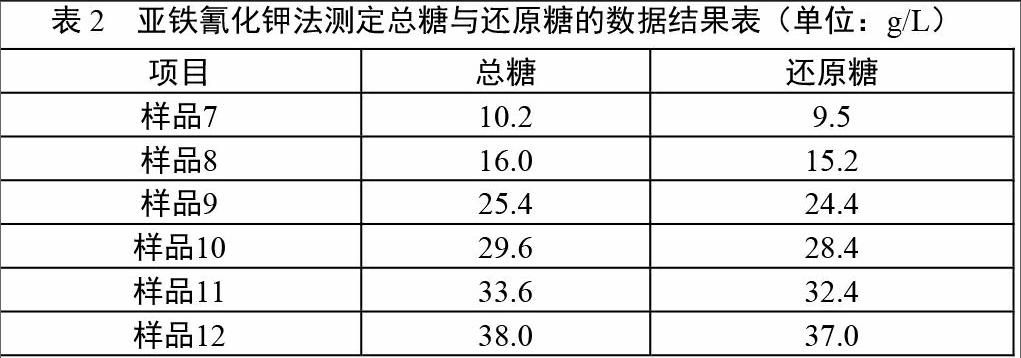
利用亞鐵氰化鉀法測定黃酒樣品中總糖與還原糖的數據結果如表2所示。由表2可知,利用亞鐵氰化鉀法測定黃酒樣品中的總糖與還原糖時,總糖比還原糖的糖含量相對要高,兩者之間存在一定差距,但差距不大。
4 結論
總之,糖是食品的重要成分之一。由于各種糖測定比較困難,目前食品中涉及糖的項目多以還原糖或總糖來表示,結果只能籠統地以還原糖或總糖表示,并不能給出各種糖的具體含量。本文就是結合實驗研究,總結分析了利用廉愛農法、亞鐵氰化鉀法測定黃酒中總糖、還原糖的情況,并得出初步的結論,可為黃酒總糖和還原糖的含量測定提供一定的理論依據。就目前而言,測定黃酒中的糖類的研究還是比較少,因此加強對黃酒中糖類測定的研究很有必要。
參考文獻
[1]李軍鵬,蘇其美,馮舉耀,等.清爽型黃酒中總糖測定方法比較[J].釀酒科技,2010(5):102-103.
[2]馬駿.黃酒總糖的測定[J].時代報告:學術版,2012(8):51.
[3]姚正堂,蔣巳峰,郝宇紅.黃酒中總糖的鐵氰化鉀滴定測定法[J].職業與健康,2007,23(6):422-423.
〔編輯:王霞〕

