淺析原子堆積中的空隙問題
衛(wèi)卓凡
高中化學(xué)選修三物質(zhì)結(jié)構(gòu)與性質(zhì)中有一類關(guān)于原子的最密堆積試題中經(jīng)常會考查微粒之間的距離以及微粒之間的空隙大小等問題,這是在晶體結(jié)構(gòu)中相對比較復(fù)雜的一類計(jì)算,因?yàn)樯婕暗娇臻g想象能力和數(shù)學(xué)運(yùn)算能力的考查,有些同學(xué)遇到此類問題往往無從下手。有的同學(xué)雖然也能解出結(jié)果,但并不是很清楚這晶體中的微粒之間的分布規(guī)律和對應(yīng)的位置關(guān)系,因此不能做到舉一反三。
原子堆積空隙等徑球最密堆積中的空隙分兩種:
(1)四面體空隙:由四個(gè)球體圍成的空隙,球體中心線圍成四面體;
(2)八面體空隙:由六個(gè)球圍成的空隙,球體中心線圍成八面體形。
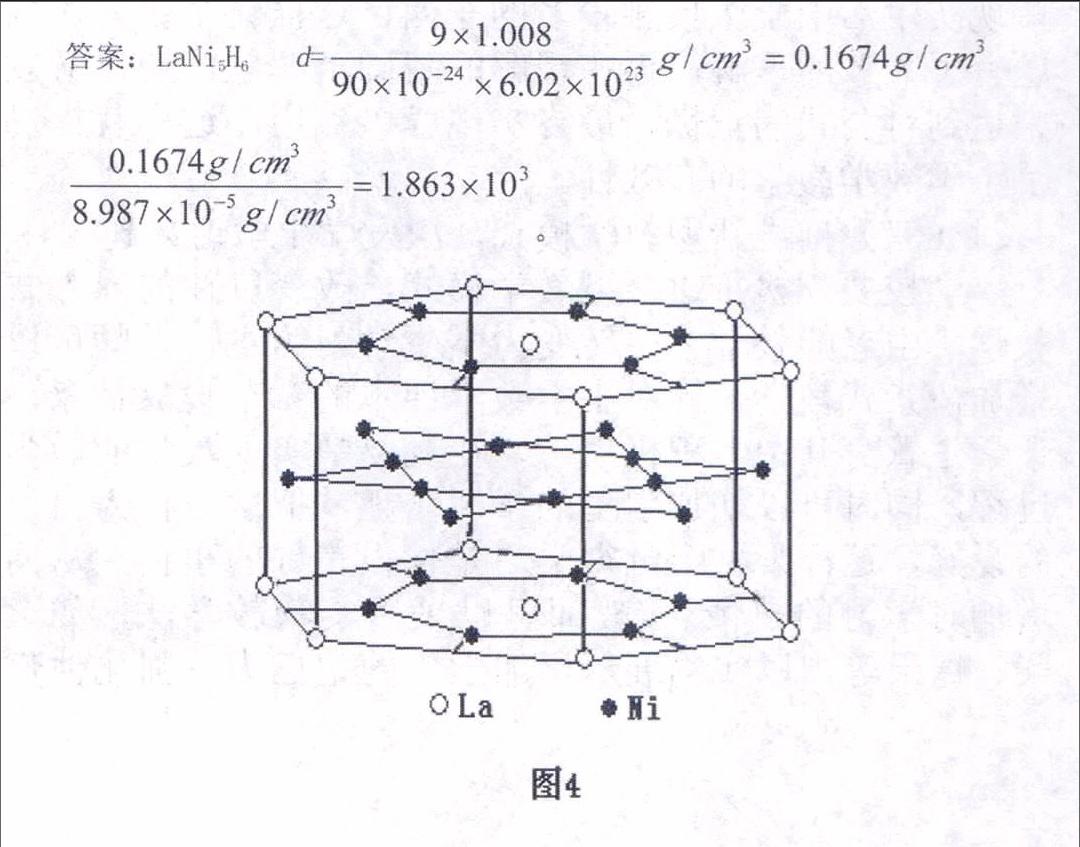
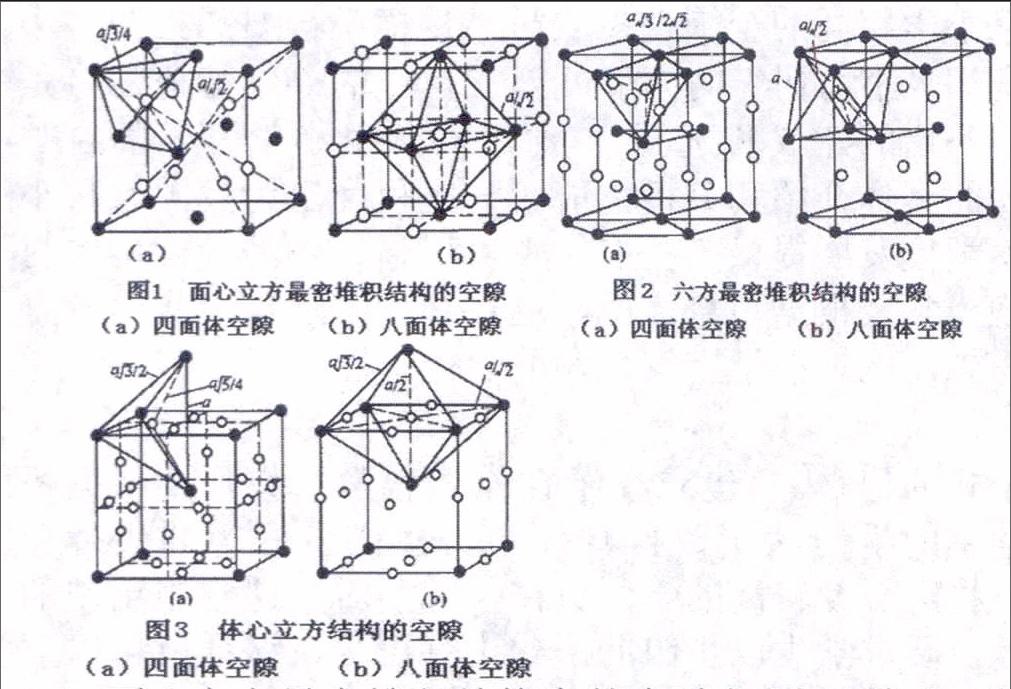
面心立方最密堆積結(jié)構(gòu)中的空隙如圖1所示,六方最密堆積結(jié)構(gòu)的空隙如圖2所示,體心立方堆積結(jié)構(gòu)的空隙如圖3所示。
以金屬Cu晶胞為例,來說明面心立方緊密堆積中的八面體和四面體空隙的位置和數(shù)量:
以Cu晶胞中上面心的一個(gè)球?yàn)檠芯繉ο螅恼路接?個(gè)八面體空隙(體心位置)。與其對稱,正上方也有1個(gè)八面體空隙;前后左右各有1個(gè)八面體空隙(棱心位置)。所以一個(gè)球共參與形成了6個(gè)八面體空隙,由于每個(gè)八面體空隙由6個(gè)球構(gòu)成,所以屬于這個(gè)球的八面體空隙數(shù)為6×1/6=1。
在這個(gè)晶胞中,上面心這個(gè)球還與另外兩個(gè)相鄰面面心處的2個(gè)球及頂角上的1個(gè)球,共能構(gòu)成4個(gè)四面體空隙(即1/8小立方體的體心位置);由于對稱性,在上面的晶胞中,也有4個(gè)四面體空隙由這個(gè)球參與構(gòu)成。……

