應用生物膜干涉技術檢測魚腥藻HetR結合靶DNA的親和力
張良林王 帥高 宏
(1. 中國科學院水生生物研究所, 中國科學院藻類生物學重點實驗室, 武漢 430072; 2. 中國科學院大學, 北京 100049)
應用生物膜干涉技術檢測魚腥藻HetR結合靶DNA的親和力
張良林1,2王 帥1,2高 宏1
(1. 中國科學院水生生物研究所, 中國科學院藻類生物學重點實驗室, 武漢 430072; 2. 中國科學院大學, 北京 100049)
魚腥藻PCC7120是一種固氮絲狀藍藻, 當環境中化合態氮源充足時, 其藻絲只有進行光合作用的營養細胞;在環境中缺乏可利用的氮源時, 部分營養細胞會在藻絲上以一種半規律的格式分化成異形胞(異形胞間隔約10個營養細胞), 從而進行固氮作用。早在1984年, Wolk實驗室通過與大腸桿菌接合轉移的方式, 成功地將穿梭質粒轉入魚腥藻PCC7120, 建立了遺傳轉移系統[1]。在2001年, 日本Kazusa研究中心完成了對魚腥藻PCC7120全基因組測序[2]。有規律的細胞分化格式, 成熟的遺傳轉移系統以及完整可用的基因組序列使得魚腥藻PCC7120成為了研究原核細胞分化的模式生物。
魚腥藻PCC7120異形胞的分化是一個復雜的過程,涉及多個基因的協調參與。根據目前的研究, HetR被公認為是異形胞分化的主調控因子。文獻報道, HetR是一個具有雙鏈DNA結合活性的同源二聚體[3], 通過結合基因啟動子區域(包括其自身啟動子)從而調控基因的轉錄表達[4,5]。對于HetR蛋白和靶DNA的結合力的研究, 研究者主要采用的經典的EMSA方法[4—6], 該方法通過觀察DNA條帶的遷移能直觀的反應蛋白與DNA的結合情況。然而, 該方法局限性是不能對蛋白結合靶DNA親和力進行準確地定量。因而研究者們正試圖嘗試一些新的方法, 探究HetR結合靶DNA的奧秘。
生物膜干涉技術(Bio-Layer Interferometry, BLI))是一種快速檢測分子間相互作用的方法, 該方法由ForteBio公司開發設計, 在Octet系統中可完成實驗操作。其基本原理是, 在光纖制成的生物傳感器底端覆蓋生物分子相容層, 偶聯配體后形成生物膜層, 進而用配體與靶分子反應。大分子結合傳感器底端偶聯的配體時會導致生物膜層厚度增加, 反射光干涉光譜曲線將產生遷移, 儀器可以實時監測相位移的變化, 并將其轉化為可衡量分子間相互作用大小的參數。BLI技術對于研究蛋白與DNA結合有著廣泛的應用前景[7,8]。
本研究利用BLI技術, 研究了魚腥藻PCC7120異形胞分化主調控因子HetR與其靶DNA(PhetP與PhetZ)的結合情況, 并對其親和力進行了定量分析。本文也是BLI技術在魚腥藻異形胞發育研究領域應用的首次報道, 為該領域的研究提供了新的研究方法。
1 材料與方法
1.1 EF-Ts-HetR蛋白的表達純化及定量
本研究使用的蛋白是EF-Ts-HetR, 在HetR的N-端融合了一個EF-Ts標簽。表達菌株由本實驗室杜野博士構建[5]。蛋白C-端含有6His標簽, 因而利用Ni2+柱親和層析的方法, 具體方法按照His·Bind Purification Kit (Novagen)進行。純化后的蛋白用20 mmol/L Tris-HCl pH 8.0緩沖液在超濾管(Millipore, 截留分子量3 K)中脫鹽純化。蛋白定量采用康維世紀的Super-Bradford Protein Assay Kit試劑盒。
1.2 Biotin-DNA的制備
本研究中使用DNA片段為魚腥藻PCC7120中hetP和hetZ基因的啟動子區域50/40 bp片段, 均采用5′-biotin標記的方法。其中, biotin-ssDNA直接由公司合成標記; biotin-dsDNA需要將其中的一條biotin-ssDNA與另一條非標記的ssDNA退火形成, 退火緩沖液采用碧云天公司的Annealing Buffer for DNA Oligos (5X)。退火體系總體積100 μL, 各組分及用量如下: Annealing Buffer for DNA Oligos (5×), 20 μL; DNA oligo A (50 μmol/L), 20 μL; DNA oligo B (50 μmol/L) 20 μL; Nuclease-free water, 40 μL。反應程序如下: step1 95℃, 2min, 1 cycle; step2 -0.1 ℃/ cycle, 8s, 700 cycles; Step3 4℃ forever。
1.3 BLI實驗
生物膜干涉實驗(Bio-Layer Interferometry, BLI)在Octet RED96系統中完成。實驗采用與儀器匹配的96孔板(Fluotrace 600, LOT E110103S), 反應體積為200 μL, 反應溫度為28℃。實驗具體方法參考相關文獻[7,8]并有相應改進。方法如下: 將Streptavidin (SA)標記的探針于超純水中浸濕5min, 進而轉移入A Buffer (20 mmol/L Tris-HCl pH 8.0, 200 mmol/L NaCl, 1 mmol/L MgCl2, 1 mmol/ L DTT, 0.5 mmol/L EDTA)中進行第一次基線(Baseline)步驟, 時間100s; 探針轉移入含有500 nmol/L biotin標記的DNA的A Buffer中進行DNA固定, 時間200s; 將固定有DNA的探針重新轉移到B Buffer中進行第二次基線(Baseline)步驟(B Buffer為含有 6 mg/ mL BSA、1.2% Tween20、10 μg/mL超聲后鮭魚精DNA的A Buffer),時間200s; 將探針轉移至含有終濃度為C buffer中進行蛋白和DNA的結合步驟(C buffer為含有10 μmol/L EF-TSHetR的B Buffer), 時間300s; 最后將探針轉移至B Buffer中進行解離步驟, 時間300s。
結合動力學參數利用Data analysis (ForteBio, version 7.1)進行數據分析。KD值根據結合和解離曲線, 利用nonlinear global fitting model模擬計算。計算KD值的實驗設置蛋白濃度梯度為10、5、2.5和1.25 μmol/L。最終KD值計算取3次獨立實驗的平均值。
2 結果
2.1 BLI對HetR結合PhetP50與PhetZ50的差異比較
文獻已報道HetR可以結合hetP和hetZ啟動子的識別位點, 從而可以調控hetP與hetZ的表達[4,5]。我們利用BLI技術對EF-Ts-HetR與包含識別位點的雙鏈DNA片段PhetP50 (5′-AAATGCACAGTAGGCGGGGGTCTAA CCCCTCATTACCTAGTAGAAAATG-3′)和PhetZ50 (5′-TCTGCCCACTAATGTGAGGGTCTAGCCCAGCAGGT GGGATTAGAGAAACA-3′)的結合進行了檢測。結果顯示, HetR與靶DNA結合在Octet系統中有明顯的信號(圖1)。HetR與不同靶DNA的結合解離曲線已在圖中標出(PhetP和PhetZ), control代表不固定DNA的探針與HetR反應的陰性對照。曲線縱坐標為相位移變化, 反映了結合信號強弱; 橫坐標為結合解離持續時間。

圖 1 HetR與PhetP50和PhetZ50的結合Fig. 1 Binding of HetR with PhetP50 and PhetZ50
2.2 HetR結合PhetP50與PhetZ50親和力(KD)計算
圖 1顯示EF-Ts-HetR與PhetP50和PhetZ50有著不同的結合解離曲線, 進而我們同樣利用BLI技術對HetR與PhetP50和PhetZ50的結合進行了定量。Octet系統中給出的KD值反映了分子相互作用力的大小。KD值是根據結合解離曲線算出的解離常數(Kd)與結合常數(Ka)的比值, 反映了分子間親和力的大小。
為準確計算KD值, 我們設置了EF-Ts-HetR濃度梯度,如圖 2、圖 3中標注所示, 曲線分別代表10、5、2.5和1.25 μmol/L的EF-Ts-HetR結合靶DNA。根據曲線計算出, HetR與PhetP50和PhetZ50結合的KD值分別為0.29±0.07和1.48±0.29。
3 討論
HetR作為有特異位點的DNA結合蛋白, 在魚腥藻PCC7120基因組中有著多個靶標位點。文獻報道HetR可以結合hetP、hetZ、patA、hetR、hepA、alr0202和alr3234的啟動子序列, 并且由于這些基因啟動子包含的HetR結合位點完整性的差異, HetR對于不同片段有著不同的親和力[9]; 經典的EMSA實驗多次證明HetR對hetP和hetZ啟動子片段有著相對較強的結合力。因而在本研究中, 我們選取了PhetP和PhetZ50 bp片段, 利用BLI技術對HetR結合靶DNA進行了定量和定性的分析。
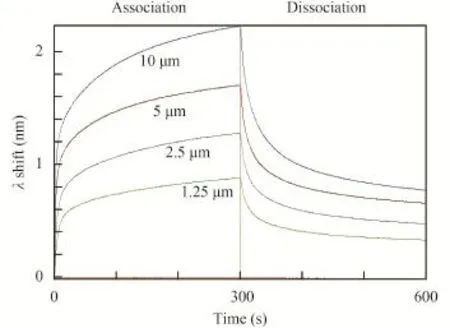
圖 2 不同濃度的EF-Ts-HetR與PhetP50的結合Fig. 2 Binding of HetR at different concentration with PhetP50
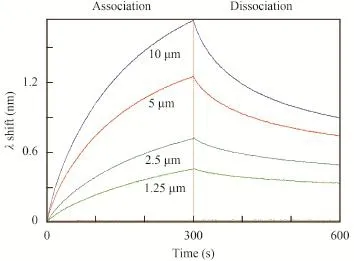
圖 3 不同濃度的EF-Ts-HetR與PhetZ50的結合Fig. 3 Binding of HetR at different concentration with PhetZ50
通過對HetR與PhetP50和PhetZ50片段結合解離曲線(圖 1)的比較我們可以看出, HetR與PhetP50的結合和解離速率都明顯快于PhetZ50; 在300s內, HetR與PhetP50的結合信號(λ shift)要強于HetR與PhetZ50的結合信號。但BLI的原理, 結合信號的大小并不能直接反應親和力的強弱, 為了對HetR與PhetP50和PhetZ50片段的親和力進行定量, 我們利用HetR濃度梯度進行了KD值精確計算; KD值即為親和力常數, 它只與分子間相互作用大小有關, 與分子濃度無關, 其數值越小代表的分子間親和力越強。通過KD值的比較我們看出, HetR與PhetP50片段的親和力要明顯強于HetR與PhetZ50片段的親和力, 在數值上前者約是后者的1/5, 因而我們可以判斷HetR與hetP啟動子片段的親和力約是與hetZ片段親和力的5倍。
研究者曾利用EMSA手段, 定性分析了HetR對不同片段的結合[9], 發現HetR在0.125 μmol的時候即可與hetP啟動子片段結合, 而當HetR濃度提高到0.5 μmol/L的時候才可以和hetZ啟動子片段結合。通過EMSA簡單的定量分析, 我們可以看出HetR與hetP啟動子片段的親和力約是hetZ啟動子片段親和力的4倍左右, 與本研究報道的5倍十分接近。BLI技術在蛋白-DNA相互作用研究中將會發揮越來越大的作用。
[1]Wolk C P, Vonshak A, Kehoe P, et al. Construction of shuttle vectors capable of conjugative transfer from Escherichia coli to nitrogen-fixing filamentous cyanobacteria [J]. Proceedings of the National Academy of Sciences of the USA, 1984, 81(5): 1561—1565
[2]Kaneko T, Nakamura Y, Wolk C P, et al. Complete genomic sequence of the filamentous nitrogen-fixing cyanobacterium Anabaena sp. Strain PCC 7120 [J]. DNA Research, 2001, 8(5): 205—213
[3]Kim Y C, Ye Z, Joachimiak G, et al. Structures of complexes comprised of Fischerella transcription factor HetR with Anabaena DNA targets [J]. Proceedings of the National Academy of Sciences of the USA, 2013, 110(19): 1716—1723
[4]Higa K C, Callahan S M. Ectopic expression of hetP can partially bypass the need for hetR in heterocyst differentiation by Anabaena sp. Strain PCC 7120 [J]. Molecular Microbiology, 2010, 77(3): 562—574
[5]Du Y, Cai Y, Hou S, et al. Identification of the HetR recognition sequence upstream of hetZ in Anabaena sp. strain PCC 7120 [J]. Journal of Bacteriology, 2012, 194(9): 2297—2306
[6]Hou S W, Zhou F, Peng S, et al. The HetR-binding site that activates expression of patA in vegetative cells is required for normal heterocyst patterning in Anabaena sp. PCC 7120 [J]. Science Bulletin, 2015, 60(2): 192—201
[7]Adams C J, Pike A C, Maniam S, et al. The p53 cofactor strap exhibits an unexpected TPR motif and oligonucleotide-binding (OB)-fold structure [J]. Proceedings of the National Academy of Sciences of the USA, 2012, 109(10): 3778—3783
[8]Cukier C D, Hollingworth D, Martin S R, et al. Molecular basis of FIR-mediated c-myc transcriptional control [J]. Nature Structural & Molecular Biology, 2010, 17(9): 1058—1064
[9]Hou S W. The recognition sequence of HetR, the master regulator of heterocyst differentiation, in Anabaena sp. PCC 7120 [D]. Thesis for Master of Science. Institute of Hydrobiology, Chinese Academy of Sciences, Wuhan. 2013 [侯圣偉. 魚腥藻PCC7120異形胞分化主調控因子HetR的識別序列. 碩士學位論文, 中國科學院水生生物研究所, 武漢. 2013]
DETECTION OF THE AFFINITY OF HETR, THE KEY REGULATOR OF HETEROCYST DIFFERENTIATION, WITH ITS TARGET DNA IN ANABAENA BY BIOLAYER INTERFEROMETRY
ZHANG Liang-Lin1,2, WANG Shuai1,2and GAO Hong1
(1. Key Laboratory of Algal Biology, Institute of Hydrobiology, Chinese Academy of Sciences, Wuhan 430072, China; 2. University of Chinese Academy of Sciences, Beijing 100049, China)
生物膜干涉技術; PCC7120; HetR; DNA結合能力
Biolayer interferometry; PCC7120; HetR; DNA binding ability
Q344+.1
A
1000-3207(2017)02-0483-03
10.7541/2017.61
2016-03-21;
2016-06-12
國家自然科學基金(31270132)資助 [Supported by the National Natural Science Foundation of China (31270132)]
張良林(1986—), 男, 安徽亳州人; 碩士研究生; 研究方向為藻類遺傳學。E-mail: 409663786@qq.com
高宏, E-mail: gaoh@ihb.ac.cn

