銅綠假單胞菌臨床感染分布及耐藥性分析
李江萍 廖國林
·藥物研究·
銅綠假單胞菌臨床感染分布及耐藥性分析
李江萍 廖國林
目的 研究銅綠假單胞菌的臨床分布特點及其對各種抗菌藥物的耐藥性,為臨床合理使用抗菌藥物提供經驗依據。方法 用WHONET5.6軟件統計分析2013年1月至2015年12月分離的銅綠假單胞菌占同期分離細菌的百分比,以及其在各類標本、病區中的分布及耐藥情況。結果 3年共分離銅綠假單胞菌1 261株,占所有分離菌株的14.9%;痰標本中分離的銅綠假單胞菌最多,共 944 株占74.9%;綜合ICU分離的銅綠假單胞菌居各病區首位,共432株占34.3%;銅綠假單胞菌對左氧氟沙星、環丙沙星、慶大霉素、妥布霉素、亞胺培南、美洛培南耐藥率較高(>20%);對阿米卡星、哌拉西林/他唑巴坦耐藥率較低(<10%)。結論 銅綠假單胞菌主要分布在痰標本和綜合ICU病區,是醫院感染最常見病原菌之一,且易產生多重耐藥性,了解其臨床分布及耐藥性變化,可為臨床治療提供資料,更好的控制銅綠假單胞菌的感染。
銅綠假單胞菌;分布;抗菌藥; 耐藥性
銅綠假單胞菌是一種常見的院內獲得性感染的條件致病菌[1,2],因其具有天然的耐藥性且耐藥機制復雜,給臨床治療帶來極大困難,故加強對其耐藥性監測十分重要。本文通過回顧分析我院1 261株銅綠假單胞菌的臨床分布及藥敏結果,為臨床抗感染治療合理使用抗菌藥提供經驗依據。
1 材料與方法
1.1 菌株來源 2013年1月至2015年12月我院送檢的各種住院患者標本,按常規方法進行培養與分離,共分離到銅綠假單胞菌1 261株(刪除重復分離菌株)。
1.2 細菌鑒定 所有菌株均采用MicroScan WalkAway 40全自動細菌鑒定儀進行鑒定。
1.3 藥敏試驗 藥敏試驗采用美國臨床實驗室標準化協會(CLSI)推薦的K-B藥敏紙片法進行測定,藥敏結果按CLSI 2016 版的標準進行判定[3]。抗菌藥物紙片均購自英國Oxoid公司,M-H瓊脂平皿購自法國梅里埃(上海)生物制品有限公司。
1.4 質控菌株 銅綠假單胞菌ATCC 27853、金黃色葡萄球菌ATCC25923和大腸埃希菌ATCC25922,由國家衛計委臨床檢驗中心提供。
2 結果
2.1 銅綠假單胞菌的分布率 2013至2015年我院共分離銅綠假單胞菌1 261株,僅次于大腸埃希菌(2 298株)和肺炎克雷伯菌(1 539株),居臨床分離菌第三位。其中黏液型銅綠假單胞菌107株,占分離銅綠假單胞菌的8.5%,3年分離的銅綠假單胞菌依次為470、431、360株,銅綠假單胞菌在臨床分離的細菌中的分布率在11.0%~15.0%,呈較穩定態勢。見表1。
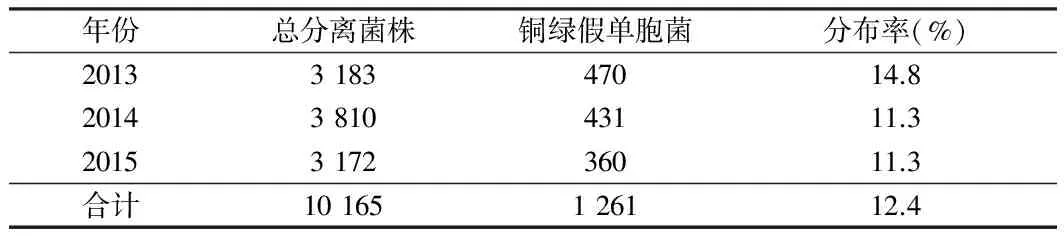
表1 2013至2015年銅綠假單胞菌在臨床分離菌中的分布 %
2.2 標本來源分布構成 2013至2015年分離的銅綠假單胞菌在臨床各種標本中的分布:銅綠假單胞菌主要分離自痰液(74.9%)、尿液(10.3%)、分泌物(8.5%)等標本中。見表2。
2.3 科室分布 銅綠假單胞菌在各科室均有不同程度的分布,但主要分離自綜合ICU(34.3%)、神經外科(17.9%)和呼吸內科(11.7%)。見表3。
2.4 耐藥性分析 銅綠假單胞菌對左氧氟沙星、環丙沙星、慶大霉素、妥布霉素、亞胺培南、美洛培南耐藥率較高,均超過20%;對阿米卡星、哌拉西林/他唑巴坦耐藥率較低,均低于10%。耐碳青霉烯酶銅綠假單胞菌(CRPA)分離率達20%以上。見表4。
3 討論
3.1 銅綠假單胞菌的分布 銅綠假單胞菌是臨床重要的條件致病菌,可引起人體各個部位的感染。在我院臨床常見病原菌中,銅綠假單胞菌分離率僅次于大腸埃希菌和肺炎克雷伯菌,居臨床分離菌第三位。本研究顯示,臨床各類標本均可分離到銅綠假單胞菌,送檢標本中銅綠假單胞菌以呼吸道標本為主(74.9%),其次是尿液(10.3%)和分泌物(8.5%),提示銅綠假單胞菌所致疾病在我院以呼吸道感染為主。本研究顯示,臨床各科室均可分離到銅綠假單胞菌,銅綠假單胞菌的病區分布排在前3位的是綜合ICU(34.3%)、神經外科(17.9%)和呼吸內科(11.7%),其中綜合ICU所占比例最大;究其原因,綜合ICU、神經外科和呼吸內科患者由于存在嚴重的基礎疾病,長期使用呼吸機及各種侵入性操作,大劑量應用廣譜抗菌藥,以及機體免疫功能下降,致銅綠假單胞菌的感染機會增加[1,4,5]。另外銅綠假單胞菌易黏附于各種腔道表面,分泌黏附因子及多糖蛋白生物被膜[6,7],致使各種侵入性儀器消毒困難而引發交叉感染,尤其是在綜合ICU特別嚴重,極易引起院感爆發。
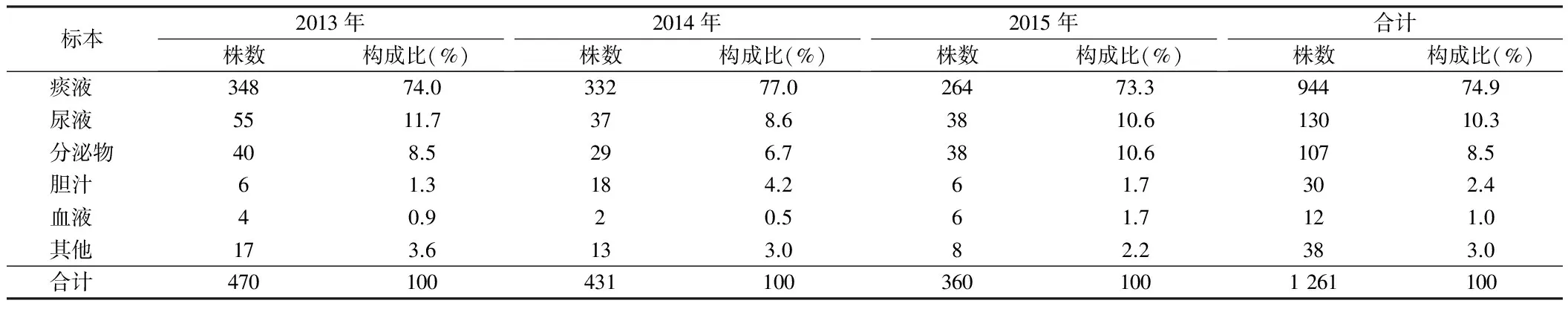
表2 2013至2015年分離的銅綠假單胞菌在臨床各種標本中的分布
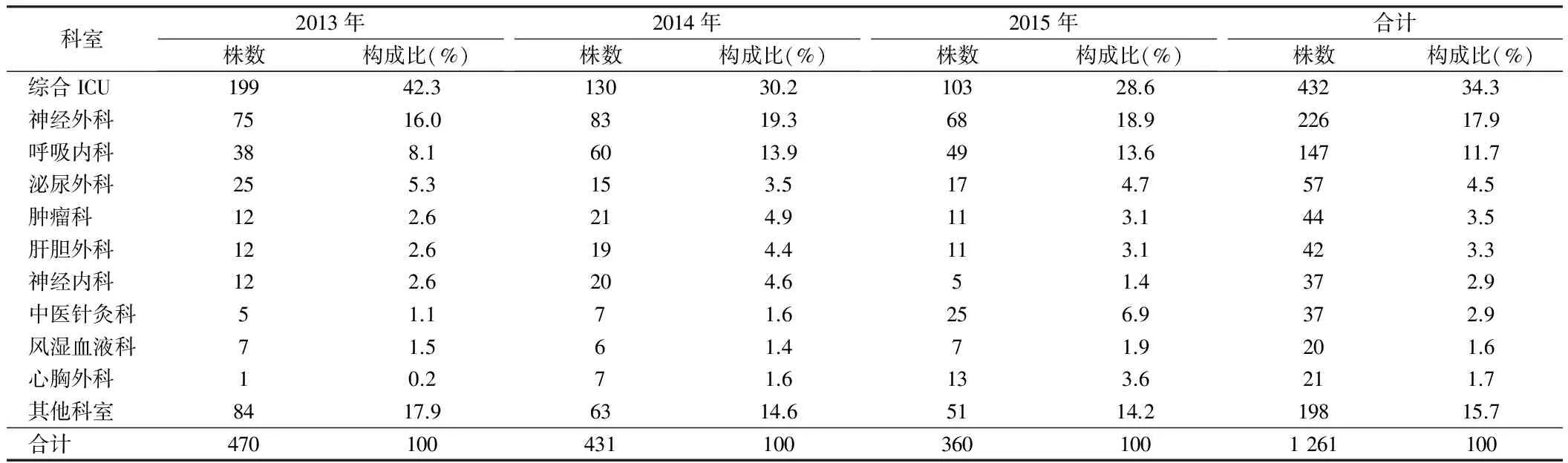
表3 2013至2015年銅綠假單胞菌在臨床科室中的分布
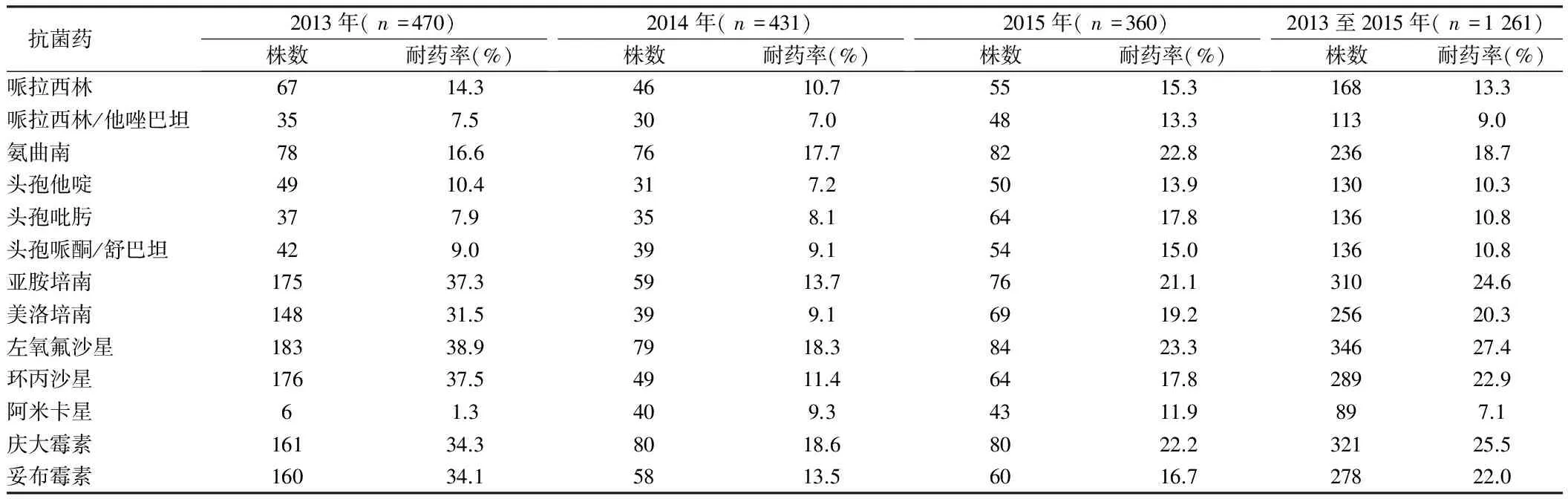
表4 2013至2015年銅綠假單胞菌對抗菌藥的耐藥率 %
3.2 銅綠假單胞菌的耐藥機制 由于廣譜抗菌藥、免疫抑制劑以及激素的大量使用,導致銅綠假單胞菌可快速對多種抗菌藥產生耐藥性,細菌產生這種耐藥性往往是多種耐藥機制的聯合作用結果。銅綠假單胞菌耐藥機制主要體現在以下幾個方面:(1)產生多種滅菌酶,如AmpC酶、β-內酰胺酶、氨基糖苷類鈍化酶和修飾酶等;(2)外膜通透性降低,如OprD2 通道蛋白的丟失或減少,就會造成銅綠假單胞菌對碳青霉烯類抗菌藥的耐藥;(3)銅綠假單胞菌表達出以藻酸鹽為主要成分的黏液性脂多糖基質有很強的黏附作用;(4)細菌的主動外排泵,導致其對許多抗菌藥固有耐藥;(5)藥物作用靶位的改變;(6)生物膜障礙與主動轉動系統阻止藥物到達其靶位點[8],這些耐藥機制造成了抗菌藥物在菌體內沒有達到有效濃度,從而導致其未完全發揮抗菌作用而產生耐藥[9]。本研究顯示,黏液型銅綠假單胞菌占分離銅綠假單胞菌的8.5%,雖然黏液型銅綠假單胞菌體外對常用抗菌藥比較敏感[4],但由于其在體內生物膜的形成及黏附因子的作用,往往產生較高的耐藥性,從而導致抗菌治療失敗。
3.3 銅綠假單胞菌的耐藥性 本研究顯示,2013至2015年,銅綠假單胞菌對阿米卡星、氨曲南、頭孢哌酮/舒巴坦耐藥率呈持續上升趨勢,而對其余10種抗菌藥耐藥率呈先下降而后又上升的趨勢,提示銅綠假單胞菌耐藥性易出現反復,因此臨床科室應積極采取應對措施,在細菌培養結果尚未出來之前,應根據我院細菌耐藥監測信息經驗用藥,當培養結果出來后應根據藥敏結果及時調整抗菌藥物。我院分離的銅綠假單胞菌對13種抗菌藥物敏感性與中國細菌耐藥性監測網報道[10]的基本一致。銅綠假單胞菌對阿米卡星、哌拉西林/他唑巴坦耐藥率較低,均低于10%;但對左氧氟沙星、環丙沙星、慶大霉素、妥布霉素、亞胺培南、美洛培南耐藥率均超過20%,耐碳青霉烯銅綠假單胞菌(CRPA)分離率超過20%,使臨床醫師抗感染治療非常棘手。CRPA一旦在病區出現,將很難徹底清除,極有可能引起院感爆發,因此應重點加強對耐碳青霉烯銅綠假單胞菌的控制與隔離。
3.4 預防和控制措施 銅綠假單胞菌耐藥率有不斷上升的趨勢,給臨床抗感染治療帶來極大挑戰,尤其是在多重耐藥和泛耐藥銅綠假單胞菌感染治療未取得明顯進展之前,預防與控制仍將是醫院的重點工作,各臨床科室特別是綜合ICU、神經外科和呼吸內科等感染高危科室醫師,更應重視感染性疾病的病原學檢測,力爭做到早送檢、早確診、早治療,根據細菌藥敏試驗結果合理用藥,采取聯合用藥、交叉用藥等方式,盡可能把耐藥菌株的控制在最低水平;同時應做到嚴格無菌操作,盡可能減少侵入性操作的頻率,從而降低醫院感染的發生。加強對銅綠假單胞菌污染物的滅菌、消毒處理,改進醫院衛生環境,有效的控制院內感染,可以明顯減緩耐藥菌的擴散與流行。
1 廖國林,李江萍,吳真,等.老年住院患者痰培養臨床分離菌的分布及耐藥性分析.中國感染與化療雜志,2015,15:349-353.
2 丁軍穎,桂紅,洪燕英,等.基于耐藥基因OPRD2探討銅綠假單胞茵的臨床感染特性.解放軍醫藥,2015,37:69-71.
3ClinicalandLaboratoryStandardsInstitute(CLSI).PerformanceStandardsforAntimicrobialSusceptibilityTesting;Twenty-SixthInformationalSupplement.2016.M100-S26.
4 廖國林,李江萍,孫沛,等.重癥監護病房患者痰培養臨床分離菌分布及耐藥性分析.中國微生態學雜志,2015,27:844-847.
5 張曉山,崔迎春,張業婉.銅綠假單胞菌引發視網膜下膿腫部析.臨床誤診誤治,2016,29:57-58.
6PiresdosSantosR,JacobyT,PiresMachadoD,etal.Handhygiene,andnotertapenemuse,contributedtoreductionofcarbapenem-resistantPseudomonasaeruginosarates.InfectControlHospEpidemiol,2011,32:584- 590.
7 李曉燕,趙杰,趙麗雅,等.黏液性銅綠假單胞菌的耐藥性分析.河北醫藥,2015,37:1247-1249.
8 張家云.銅綠假單胞菌醫院感染現狀及耐藥性探討.中華醫院感染學雜志,2011,21:1232-1233.
9 袁晨燕,韓勍,陳建明,等.銅綠假單胞菌細菌生物膜形成及耐藥性分析.中華醫院感染學雜志,2011,21:2161-2163.
10 胡付品,朱德妹,汪復,等.2014年CHINET中國細菌耐藥性監測.中國感染與化療雜志,2015,15:401-410.
10.3969/j.issn.1002-7386.2017.09.042
430081 湖北省武漢市普仁醫院輸血科(李江萍),檢驗科(廖國林)
廖國林,430081 湖北省武漢市普仁醫院檢驗科;
E-mail:shuqiaonet@126.com
R 195
A
1002-7386(2017)09-1418-03
2016-10-20)

