火焰原子吸收光譜法測定黃山獼猴桃中金屬元素的含量
蘭艷素,張文峰,張猛,黃波 (黃山學院化學化工學院,安徽 黃山 245041)
火焰原子吸收光譜法測定黃山獼猴桃中金屬元素的含量
蘭艷素,張文峰,張猛,黃波
(黃山學院化學化工學院,安徽 黃山 245041)
采用火焰原子吸收光譜法對黃山獼猴桃(ActinidiachinensisPlanch)中Na、K、Cd、Ca、Cu、Fe、Mg、Mn、Pb、Zn的含量進行了測定。結果顯示,含量較高的有K、Mg,其次是Na、Ca、Fe,含量較低的是重金屬Cd、Pb,各元素回收率均介于97.50%~103.18%之間。該法高效、簡單、準確。
火焰原子吸收光譜法;獼猴桃(ActinidiachinensisPlanch);金屬元素;含量
獼猴桃(ActinidiachinensisPlanch)又叫獼猴梨,黃山地區又稱之為楊桃,是獼猴桃屬(Actinidia)植物的果實[1]。獼猴桃不僅營養價值較高,而且酸甜可口,被譽為“水果之王”[2]。研究發現,獼猴桃的化學成分中多糖[3]、維生素C的含量較高,還含有生物堿、黃酮類、三萜類、揮發油、氨基酸等成分[4~6]。獼猴桃不僅具有一定的降血脂、抗腫瘤、抗畸形、抗氧化等功效,而且能清熱解毒、調節機體免疫力[7,8],若經常食用,可以有效治療食欲不振、便秘、消化不良等癥。
檢測微量元素的方法較多,現階段常用的有原子發射光譜法、原子吸收光譜法、X射線熒光光譜分析法等[9]。其中火焰原子吸收光譜法的檢出極限非常低,而且方法成熟,儀器操作比較簡單,準確度高,成為廣泛應用于中草藥及食品中微量元素含量測定方法之一。
到目前為止,對獼猴桃中的有效成分以及藥理活性均已有研究,但對于黃山獼猴桃中微量元素的研究尚未見報道。本研究采用濕法消解-火焰原子吸收光譜法測定黃山獼猴桃中10種金屬元素的含量,以期為黃山地區野生獼猴桃資源的進一步開發提供參考依據。
1 材料與方法
1.1 材料
樣品:新鮮獼猴桃于2015年10月采自安徽省黃山風景區。
試劑:所用鈉、鉀、鎂、銅、鉛、錳、鎘、鋅、鈣、鐵標準溶液濃度均為1000μg/mL,HNO3、H2O2為優級純,其他試劑為國產分析純。
主要儀器:WFX-210型火焰原子吸收分光光度儀(北京瑞利分析儀器公司產品);空心陰極燈(北京有色金屬研究總院產品);FST-YZ-40超純水機(上海富詩特儀器設備有限公司產品);ECH-II微機控溫電熱板(上海新儀微波化學科技有限公司產品);電子分析天平(上海梅特勒-托利多儀器有限公司產品);GZX-9030MBE電熱鼓風干燥箱(上海博迅實業有限公司醫療設備廠產品);FW100型高速萬能粉碎機(天津市泰斯特儀器有限公司產品)。
1.2 方法1.2.1 火焰原子吸收光譜儀測定條件
實驗采用乙炔-空氣火焰原子吸收光譜法測定各種金屬元素的含量,通過預實驗,對電流、燃燒高度等參數進行優化,得到儀器工作的最佳參數,詳見表1。

表1 火焰原子吸收光譜儀工作參數
1.2.2 材料前處理
將新采摘的黃山獼猴桃用重蒸水清洗干凈,然后用小刀切成薄片,放到電熱鼓風干燥箱內,設置溫度為50℃,干燥24h至恒重,用粉碎機進行粉碎,過100目篩,陰涼處保存備用。所用玻璃儀器均采用6% HNO3浸泡24h,再用重蒸水沖洗2~3次,烘干后備用。
1.2.3 空白溶液、待測溶液的制備
取2個(編號為0號、1號)250mL三角瓶,精密稱取1份黃山獼猴桃粉末0.5000g,放入1號瓶中,在通風櫥中分別向2個三角瓶中加入 9mL濃硝酸,蓋上表面皿,室溫下浸泡24h后再往三角瓶中加入雙氧水3mL后,一起置于電熱板上進行加熱,加熱溫度先設置為60℃,保持5min,逐步升高至160℃,溶液慢慢沸騰,保持微微沸騰狀態10min,冒出棕色煙霧,繼續加熱,溶液不再冒白煙,約剩1mL無色透明溶液,小心取下三角燒瓶,在室溫條件下放置冷卻,最后將得到的樣液吸出,并用1% HNO3多次洗滌三角瓶和表面皿,與樣液合并后,定容于50mL容量瓶中,即得到空白溶液和樣品待測溶液。
1.2.4 標準曲線的制作
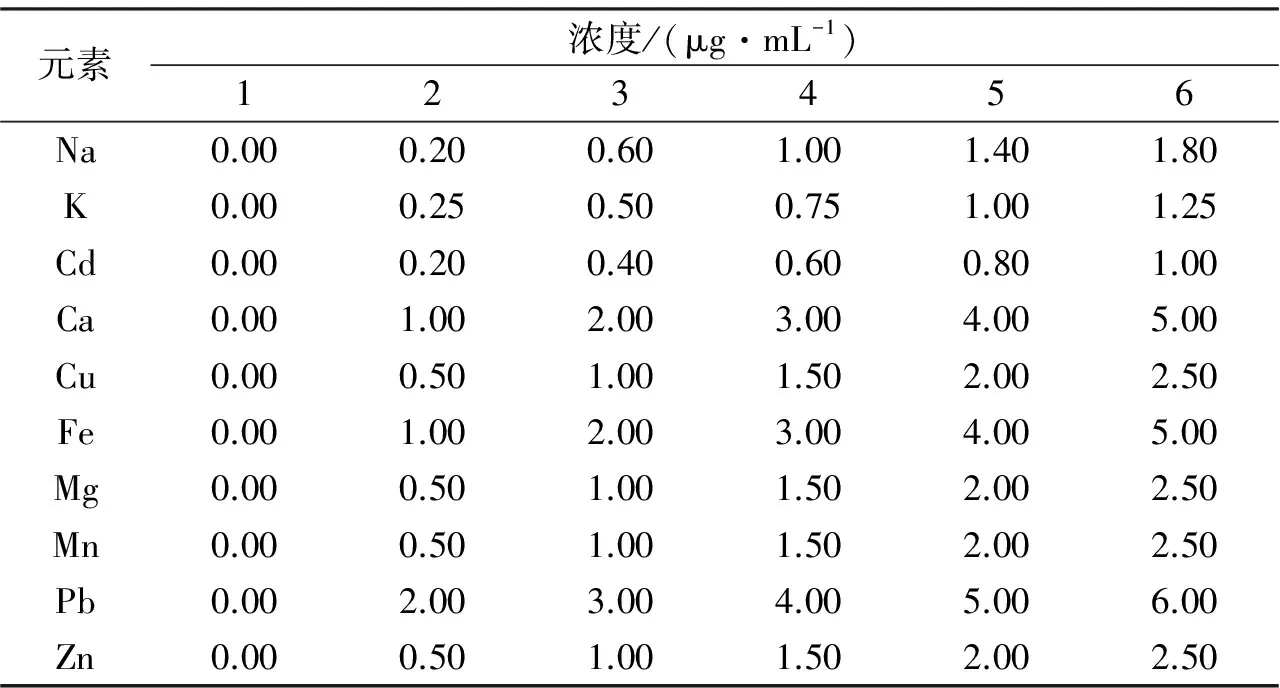
表2 各金屬元素標準溶液質量濃度
從冰箱中取出10種元素的標準溶液(濃度1000μg/mL),先將各溶液稀釋10倍,再移取一系列不同體積稀釋后的標準溶液,用1% HNO3定容于50mL容量瓶中,得到用于制作標準曲線的溶液,各元素質量濃度系列見表2。開機預熱,在已確定的儀器工作條件下,先用空白溶液調零,并從低到高質量濃度依次進樣,測定各標準溶液的光密度,分別以金屬元素的質量濃度為橫坐標、光密度為縱坐標繪制10種金屬元素的標準曲線。
1.2.5 樣品測定
打開儀器,預熱0.5h后,移取適量空白溶液、待測樣品溶液,用1%硝酸將溶液進行稀釋,再用稀釋后的空白溶液進行調零,測定樣品溶液的光密度。依次調換陰極燈,待光源穩定后,依次測定不同金屬元素的含量。
1.2.6 精密度試驗
移取2mL消解處理好的樣品、空白溶液,用1%HNO3稀釋,用空白溶液調零,光源穩定5min后,連續5次進樣,計算RSD值。
1.2.7 重復性試驗
稱取5份等質量的黃山獼猴桃粗粉,以HNO3和H2O2作為消解液,經浸泡、消解制備待測、空白溶液,依次測定5份溶液中10種金屬元素的含量。
1.2.8 加標回收率試驗
稱取31份獼猴桃粗粉,每份0.5000g,每種金屬元素的加標樣量約等于樣品中含有的量,然后加入等體積消解液,放在電熱板上加熱,消解至無白煙冒出,樣品溶液轉移、定容到容量瓶中,每種金屬元素做3個平行試驗,剩余的一份樣品不加標準溶液,浸泡后同法消解,得到待測液以及10種元素的加標消解樣液,稀釋不同倍數,依次進樣測定各溶液的光密度值。
2 結果與分析
2.1 消解試劑的確定
濕法消解常采用的消解液體系有濃HNO3、HNO3-HClO4、HNO3-H2O2、HF等,強酸性條件下,樣品能被完全消解,但在強酸性條件下進行測定,會對原子吸收光譜儀有較大損傷,而且實驗操作過程中存在不安全因素,因而選取HNO3-H2O2進行預實驗。結果發現:HNO3-H2O2(3︰1)體系對黃山獼猴桃樣品的消解效果最好,硝化后所得溶液澄清,消解比較徹底,并具有省時、安全、操作簡單、損失少、污染小等優點。所以,選用體積比為3︰1的HNO3-H2O2溶液作為消解液進行后續實驗。
2.2 各金屬元素的標準曲線

表3 各元素回歸方程及相關系數
測定所得數據采用origin軟件分別作圖,得到各元素標準曲線的線性回歸方程以及相關系數見表3。由表3可知,在設定的濃度范圍內,各元素曲線的線性關系良好(0.9988~0.9999),滿足實驗需要。
2.3 樣品含量測定結果
為了使測定的樣品溶液中所含金屬元素的質量濃度均位于標準曲線的線性范圍之內,在對含量較高K、Mg、Na元素的光密度進行測定時,先將原待測液分別稀釋20、10、10倍后,再進樣,將所得數據代入標準曲線方程,計算得到樣液中各金屬元素的含量,重復操作3次,結果見表4。
由表4可見,黃山獼猴桃中均含有Na、K、Cd、Ca、Cu、Fe、Mg、Mn、Pb、Zn等金屬元素,其中K的含量最高,大于1000μg/g,其次為Mg,含量相對較高的還有Na、Ca,重金屬Cd、Pb的含量很少。各金屬含量由低到高的順序為:Pb 表4 黃山獼猴桃中各元素含量(n=3) 表5 回收率試驗結果 2.4 方法學考察 按照1.2.6的方法進行精密度試驗,每種金屬元素均得到5個光密度值,結果表明10種元素的RSD較小(0.91%~1.76%),說明儀器的精密度較好,實驗數據可靠。 按1.2.7的方法進行重復性試驗,待光源穩定5min后,依次測定樣品溶液中各金屬元素的光密度值,結果RSD均小于2.36%(n=5),可見試驗的重現性較好。 按照1.2.8的方法進行加標回收試驗,得到10種元素的回收率結果見表5。 由試驗數據可知,所測10種元素的回收率均介于97.50%~103.18%之間,加標回收率良好,說明試驗所采用的方法具有較高的準確度,滿足試驗要求。 本研究采用火焰原子吸收光譜法對黃山獼猴桃中的 Na、K、Cd、Ca、Cu、Fe、Mg、Mn、Pb、Zn元素含量進行測定。結果表明,黃山獼猴桃中含有豐富的對人體有益的微量元素,其中K的含量最為豐富,其次是Mg、Na、Ca,含量均≥350μg/g,其中Ca、Mg元素具有很好的解毒效果[10],這與獼猴桃具有的清熱解毒功效相呼應。Fe、Zn的含量也不低,可以不同程度增強人體的免疫力[11]。重金屬Pb、Cd的含量遠遠低于國家食品安全標準,Cu的含量稍高,但也沒有超出國家標準(小于20μg/g),可以放心食用。與黔東南州[12]、江西宜春[13]、浙江產獼猴桃[14]相比較,黃山獼猴桃中所含的金屬元素含量偏高,可能是黃山特有氣候以及植物所生長的土壤成分不同引起。可見,黃山獼猴桃不僅含有補充人體所需的各種微量元素,還具有一定的藥用價值,值得進一步開發與利用。 [1]中國科學院中國植物志編輯委員會.中國植物志[M].北京:科學出版社,1984:261~263. [2]陳海峰,劉 晴,曾書琴.獼猴桃蒸汽熱燙去皮工藝研究[J].食品科技,2016,41(6):117~120. [3]單云崗,陳錫林,傅躍青.野生獼猴桃多糖提取工藝研究[J].浙江中醫雜志,2015,50(2):146~147. [4]杜彥影,劉長江,劉旸旸.響應面設計法優化軟棗獼猴桃莖中總生物堿的提取工藝[J].食品工業科技,2015,36(13):220~224. [5]李然紅,金志民,陳鑫,等.狗棗獼猴桃研究進展[J].中國林副特產,2015,135(2):84~85. [6]Takano F,Tanaka T,Tsukamoto W,etal.Isolation of (+)-catenin and (-)-epicatenin fromActinidiaargutaas bone marrow cell proliferation promoting compounds [J].Planta Med,2003,69:321~326. [7]Guan D,Zhang Z,Yang Y,etal.Antioxidant and antitumor activities of water extracts from the root ofActinidiakolomikta[J].Exp Ther Med,2011,2:33~39. [8]馬鳳愛.中華獼猴桃果實化學成分及生物活性研究[D].合肥:安徽中醫藥大學,2015. [9]楊柳,曹雪瑩,孟東陽.煤中微量元素含量常用測定方法[J].中國礦業,2014,23(2):293~300. [10]烏蘭其其格,寶力道,路洪波,等.蒙藥阿嘎日中鐵等10種微量元素初級形態研究[J].遼寧中醫雜志,2016,43(7):1447~1449. [11]付金娥,滕紅麗,郭力城.微波消解-ICP-OES分析白骨壤果實中微量元素[J].藥物分析雜志,2015,35(1):41~45. [12]蔣天智,柴東方.野生獼猴桃的微量元素研究[J].凱里學院學報,2014,32(6):53~55. [13]王艷燕,劉 臨.原子吸收分光光度法測定獼猴桃中微量元素[J].微量元素與健康研究,2008,25(6):42~43. [14]劉建軍,陳衛紅.中華獼猴桃微量元素測定分析[J].廣東微量元素科學,2001,8(4):63~65. [編輯] 余文斌 2016-10-28 安徽省高校省級優秀青年人才基金重點項目(2013SQRL088ZD);安徽省黃山市科技計劃項目(2015Z-02); 安徽省自然科學研究項目(KJ2015A259)。 蘭艷素(1985-),女,碩士,助教,主要從事天然產物提取分離與活性研究,ls7536858@163.com。 O657.31;TS201.2 A 1673-1409(2017)06-0063-04 [引著格式]蘭艷素,張文峰,張猛,等.火焰原子吸收光譜法測定黃山獼猴桃中金屬元素的含量[J].長江大學學報(自科版),2017,14(6):63~66,84.

3 結論

