蒼耳化學成分及生物活性研究
張文治 栗娜 白麗明 高鴻悅 張樹軍
摘要: 采用硅膠柱色譜、制備薄層色譜、正反高效液相色譜和重結晶等方法,對蒼耳石油醚、乙酸乙酯萃取物進行分離,研究了中藥蒼耳(Xanthium sibiricum)全草的化學成分和抗菌活性。 結果表明:共得到14個化合物。根據理化性質和波譜數據分析,鑒定化合物結構分別為對甲氧基苯甲酸(1)、蒲公英賽醇(2)、羽扇豆醇(3)、熊果酸(4)、豆甾醇(5)、齊墩果酸(6)、lasidiol pmethoxybenzoate(7)、羽扇豆酮(8)、蒼耳亭(9)、α菠甾醇(10)、槲皮素(11)、蒼耳皂素(12)、芹菜素(13)、羽扇豆醇乙酸酯(14)。化合物2、7、8為首次從該植物中分離得到。以平板打孔法測試提取化合物對不同菌種的抑制作用,結果表明化合物2、8、9、12對蕃茄早疫、黃瓜枯萎、蕃茄灰霉和蘋果腐爛病菌有較好的抑菌活性。
關鍵詞: 蒼耳, 化學成分, 分離, 抑菌活性
中圖分類號: Q946.91, R284.1
文獻標識碼: A
文章編號: 10003142(2017)05062106
Abstract:
We studied the chemical constituents and bioactivity of Xanthium sibiricum, and fourteen compounds were isolated from the PE and EtOAc extract by the methods of column chromatography, thin layer chromatography, semiprepared HPLC, and recrystallization. The structures were elucidated by the analysis of spectral data and physicalchemical properties and identified as anisic acid(1), taraxerol(2), lupeol(3), ursolic acid(4), stimastero(5), oleanolic acid(6), lasidiol pmethoxybenzoate (7), lupenone(8), xanthatin(9), αspinasterol(10), quercetin (11), xanthinosin(12), apigenin(13) and oleanic acid(14); Compounds 2,7,8 were isolated from Xanthium sibiricum for the first time. The compounds were tested by plate diffusion method for the inhibitory effect of different strains. The results showed that the compounds taraxerol(2), lupenone(8), xanthatin(9) and xanthinosin(12) displayed antibacterial activity to Alternaria solani, Fusarium oxysporum. sp. susumebrium, Botrytis cinerea and Cytospora sp.
Key words: Xanthium sibiricum, chemical constituent, separation, antibacterial activity
蒼耳(Xanthium sibiricum)為菊科蒼耳屬植物,廣布我國各省區。其味辛苦,性溫,在臨床上被用來治療風寒頭痛、皮膚濕疹、鼻塞流涕等癥狀,具有抗炎、抗過敏、抗氧化、抗菌、抗腫瘤等藥理作用(王蓓和趙衛星,2011)。本課題組前期對蒙古蒼耳的莖葉及甲醇提取物進行了化學成分研究,分離得到25個化合物(張文治等,2009;張樹軍等,2015)。本文報道其全草95%乙醇提取物的化學成分,從中分離得到14個化合物,分別鑒定為對甲氧基苯甲酸(Anisic acid,1)、蒲公英賽醇(taraxerol,2)、羽扇豆醇(lupeol,3)、熊果酸(ursolic acid,4)、豆甾醇(stimastero,5)、齊墩果酸(oleanolic acid,6)、lasidiol pmethoxybenzoate(7)、羽扇豆酮(lupenone,8)、蒼耳亭(xanthatin,9)、α菠甾醇(αspinasterol,10)、槲皮素(quercetin,11)、蒼耳皂素(xanthinosin,12)、芹菜素(apigenin,13)、羽扇豆醇乙酸酯(oleanic acid,14)。化合物2、7、8為首次從該植物中分離得到。
為了進一步研究其藥理活性,開發利用植物資源,本研究對化合物2、8、9、12分別進行6種植物致病菌的抑菌活性篩選,其中4種化合物對蕃茄早疫、黃瓜枯萎、蕃茄灰霉和蘋果腐爛病菌有較好的抑制作用。
1儀器與材料
瑞士BRUKER公司 AM600 型核磁共振儀,高效液相色譜儀 (Waters 2489),RE5200 旋轉蒸發儀,Yanako熔點儀,硅膠(200 ~ 300目)為青島海洋化工廠產品。實驗用試劑如石油醚、乙酸乙酯、正丁醇、甲醇為天津凱通化學試劑公司所生產,HPLC使用色譜純度的試劑。蘋果腐爛病菌(Cytospora sp.)、蕃茄早疫病菌(Alternaria solani)、蕃茄灰霉病菌(Botrytis cinerea)、草莓灰霉病菌(Bofrytis cinerea)、黃瓜枯萎病菌(Fusarium oxysporum sp. susumebrium)、小麥赤霉病菌(Fusarium graminearum)6種菌種均從中國農業大學購買所得,葡萄糖為凱通化學試劑公司生產,瓊脂為博興生物技術公司生產。
所用材料于2013年8月采自黑龍江省蘭西縣。經齊齊哈爾大學生命學院楊曉杰教授鑒定為菊科植物蒼耳(Xanthium sibiricum)。
2提取與分離
干燥蒼耳全草 (30.0 kg) 粉碎,用90 L乙醇分四次浸泡7 d,濃縮至1 200 mL浸膏,加適量蒸餾水后,依次用三種不同極性的溶劑進行萃取,得到石油醚、乙酸乙酯和正丁醇萃取物,分別為198.8、160.2和55.5 g。
取石油醚萃取物 (198.8 g) 用石油醚和乙酸乙酯的混合溶劑進行硅膠柱色譜反復洗脫后,利用HPLC純化得到化合物 1(20.9 mg)、化合物 2(14.6 mg)、 3(19.2 mg)和化合物 4(18.7 mg)。
取乙酸乙酯萃取物 (160.2 g) 用硅膠柱色譜進行反復多次洗脫后,利用HPLC純化,得到化合物 5(187.2 mg)、6(30.2 mg)、7(11.2 mg)、8(53.7 mg)、9(84.3 mg)、10(22.9 mg)、11(12.7 mg)、12(15.5 mg)、13(17.6 mg)和 14(18.2 mg)。
3結構鑒定
化合物 1白色粉末(石油醚-乙酸乙酯),mp 181~186 ℃。易溶于甲醇。1HNMR(600 MHz,MeOD) δ: 7.98 (2H,dd,J=8.5,2.0 Hz,H2,6),6.99 (2H,d,J=8.5,2.0 Hz,H3,5),3.87 (3H,s,HOCH3);13CNMR(150MHz,MeOD) δ: 122.6 (C1),131.4 (C2),113.3 (C3),163.7 (C4),113.3 (C5),131.4 (C6),54.6 (C OCH3)。以上數據與華會明等(2005)對照,可鑒定化合物 1為對甲氧基苯甲酸。
化合物 2白色粉末(EtOAc),mp 271~272 ℃,易溶于氯仿。1HNMR (600 MHz,CDCl3) δ: 5.53 (1H,dd,J=10.5,4.0 Hz,H21),3.20 (1H,t,J=5.2,11.2 Hz,H3);1.63,2.05(6H,s),0.82,0.85,0.87,0.95,0.99,1.05(each 3H,s);13CNMR (150 MHz,CDCl3) δ:38.0 (C1),26.1 (C2),76.2 (C3),39.2 (C4),55.9 (C5),18.8 (C6),35.1 (C7),38.8 (C8),48.9 (C9),37.5 (C10),17.4 (C11),35.8 (C12),37.7 (C13),158.1 (C14),116.9 (C15),36.7 (C16),37.4 (C17),49.3 (C18),41.3 (C19),28.9 (C20),33.8 (C21),33.1 (C22),28.2 (C23),15.2 (C24),15.4 (C25),29.8 (C26),25.1 (C27),29.7 (C28),33.5 (C29),21.6 (C30)。以上結果與吳雙慶等(2012)基本一致,可判斷化合物 2 為蒲公英賽醇。
化合物 3白色無定形粉末(石油醚乙酸乙酯),易溶于氯仿,石油醚,乙酸乙酯,mp 216~218 ℃。1HNMR(600MHz,CDCl3) δ: 4.69(1H,d,J=2.5 Hz,H29b),4.57 (1H,d,J=2.5 Hz,H29a),3.18 (1H,dd,J=5.1,11.2 Hz,H3),1.69 (3H,s,H30),1.04 (3H,s,H26),0.97 (3H,s,H25),0.91 (3H,s,H23),0.83 (3H,s,H27),0.79 (3H,s,H28),0.76 (3H,s,H24);13CNMR (150MHz,CDCl3) δ: 38.7 (C1),27.5 (C2),78.8 (C3),38.9 (C4),55.3 (C5), 18.3 (C6), 34.2 (C7),40.8 (C8),
50.5 (C9),37.2 (C10),21.1 (C11),25.2 (C12),38.1 (C13),42.7 (C14),27.4 (C15),25.5 (C16),42.6 (C17),48.3 (C18),47.9 (C19),150.9 (C20),29.7 (C21),40.0 (C22),27.9 (C23),15.4 (C24),16.1 (C25),16.0 (C26),14.6(C27),18.1 (C28),109.3 (C29),19.4 (C30)。以上數據與張樹軍等(2015)對照基本一致,鑒定化合物 3 為羽扇豆醇。
化合物 4白色粉末(MeOH),mp 278~280 ℃,易溶于甲醇。1HNMR (600 MHz,DMSOd6) δ: 12.75 (1H,s,HOH),5.22 (1H,d,J=4.6 Hz,H12),3.81 (1H,m,H3),1.62 (3H,d,J=6.8 Hz,H29),1.71(3H,d,J=7.4 Hz,H30),1.48,1.52,1.56,1.68,1.70,1.72,1.85 (each 3H,s,H23~27); 13CNMR (150MHz,DMSOd6) δ: 38.6 (C1),24.1(C2),79.3 (C3),37.1 (C4),55.5 (C5),18.3(C6),32.6(C7),39.8(C8),47.7(C9),37.2 (C10),23.2(C11),125.9(C12),138.2(C13),41.3 (C14),27.7 (C15),23.4 (C16),47.6 (C17),53.3 (C18),39.8 (C19),38.6 (C20),30.8 (C21),34.4 (C22),28.2 (C23),16.6 (C24),15.4(C25),17.6 (C26),23.7(C27),182.2 (C28),17.1 (C29),19.6 (C30)。以上數據與張俊燕等(2014)比較分析,推斷化合物 4為熊果酸。
化合物 5無色針晶(石油醚醋酸乙酯),mp 167~168 ℃,易溶于氯仿、丙酮。1HNMR (600 MHz,CDCl3) δ: 5.14 (1H,m,H6),5.02 (1H,dd,J=8.4,15.0 Hz,H22),5.01 (1H,dd,J=15.0,8.4 Hz,H23),3.57 (1H,m,H3),1.03 (3H,d,H21),1.01 (3H,s,H19),0.81 (3H,t,J=2.8 Hz,H29),0.79 (3H,s,H27),0.54 (3H,s,H18); 13CNMR (150MHz,CDCl3) δ: 37.1 (C1),31.8 (C2),71.8 (C3),43.2 (C4),121.7 (C5) 140.1 (C6),40.3 (C7),31.8 (C8), 50.2 (C9),36.5 (C10),21.2 (C11),39.8 (C12), 42.2 (C13),32.0(C14),25.4(C15),28.6(C16), 56.0(C17),12.2 (C18),19.2 (C19),40.1(C20),21.5(C21),138.2(C22),129.3(C23),51.3 (C24),31.8 (C25),21.7 (C26),19.1 (C27),25.3 (C28),12.3 (C29)。與吳希等(2008)的研究結果一致,可鑒定化合物 5 為豆甾醇。
化合物 6白色粉末(EtOAc),mp 278~280 ℃,易溶于氯仿,丙酮。1HNMR (600 MHz,CDCl3) δ: 5.25(1H,s,H12),3.22 (1H,dd,J=4.9,5.4 Hz,H3),2.82 (1H,dd,J=13.7,4.3 Hz,H18),1.13 (3H,s,H27),0.99 (3H,s,H25),0.93 (3H,s,H30),0.91 (3H,s,H29),0.90 (3H,s,H24),0.77 (3H,s,H23),0.75 (3H,s,H26); 13CNMR (150 MHz,CDCl3) δ: 38.5 (C1),27.2 (C2),78.7 (C3),38.7 (C4),55.2 (C5),18.3 (C6),32.6 (C7),39.4 (C8),47.6 (C9),37.1 (C10),22.9 (C11),122.2 (C12),143.5 (C13),41.6(C14),27.7 (C15),23.4 (C16),46.6 (C17),41.3(C18),45.8 (C19),30.6 (C20),33.8 (C21),32.4 (C22),28.1 (C23),15.6 (C24),15.3(C25),16.8 (C26),25.9(C27),183.3(C28),33.1(C29),23.6(C30)。以上數據與陳勇等(2015)的報道一致,故確定化合物 6 為齊墩果酸。
化合物 7淡黃色蠟狀物(EtOAc), mp 42.9~48.8 ℃。1HNMR (600 MHz,CDCl3) δ:8.01 (2H,d,J=9.0 Hz,H2′,6′),6.89 (2H,d,J=9.0 Hz,H3′,5′),5.49 (1H,br d,J=4.3 Hz,H2),5.32 (1H,d,J=4.3 Hz,Hl),3.86 (3H,s,OCH3),2.42 (1H,m,H4),2.32 (1H,m,H5),2.08 (1H,m,H10),2.07 (1H,d,H11),1.70 (3H,br s,H15),1.08 (3H,s,H14);13CNMR (150MHz,CDCl3) δ: 77.9 (C1),121.4 (C2),143.1 (C3),30.3 (C4),35.9 (C5),24.7 (C6),36.1 (C7),56.8 (C8),26.6 (C9),24.6(C10),21.5 (C11),25.2 (C12),24.6(C13),22.9 (C14), 25.8 (C15),165.5 (C1′),123.0(C2′),131.5(C3′),113.6 (C4′),163.3 (C5′),113.6 (C6′),131.5 (C7′),55.5 (C8′)。以上數據與劉旭剛等(2014)的報道一致,判定化合物 7 為 lasidiol pmethoxybenzoate。
化合物 8白色針晶(石油醚醋酸乙酯),mp 165~167 ℃。1HNMR(600MHz,CDCl3) δ: 4.57(1H, br s, J=2.4 Hz, H29b), 4.69 (1H, br s, J=2.4 Hz, H29a), 1.69 (3H, br s, H30), 1.07 (3H, s, H26), 1.05 (3H, s, H23), 1.03 (3H, s, H24), 0.96 (3H, s, H27), 0.93 (3H, s, H25), 0.80 (3H, s, H28); 13CNMR (150MHz, CDCl3) δ: 39.8 (C1), 34.2 (C2), 218.1 (C3), 47.5 (C4), 54.9 (C5), 19.6 (C6), 33.6 (C7), 40.7 (C8), 50.0 (C9), 36.9 (C10), 21.6 (C11), 25.2 (C12), 38.1 (C13), 42.9 (C14), 27.3 (C15), 35.5 (C16), 42.9 (C17), 48.3 (C18), 47.8 (C19), 150.9 (C20), 29.8 (C21), 39.9 (C22), 26.7 (C23), 21.0 (C24), 15.8 (C25), 15.9 (C26), 14.6(C27), 18.0 (C28), 109.3 (C29), 19.2 (C30)。以上數據與彭小冰等(2012)的結果對照,可確定化合物 8 為羽扇豆酮。
化合物 9塊狀透明晶體(EtOAc),mp 114.5~115 ℃。1HNMR (600 MHz, CDCl3) δ: 7.07 (1H, d, J=16.0 Hz, H2), 6.28 (1H, dd, J=9.1, 3.4 Hz, H5), 6.20 (1H, d, J=16.0 Hz, H3), 6.18 (1H, d, J=3.3 Hz, H13a), 5.48 (1H, d, J=3.3 Hz, H13b), 4.29 (1H, dt, J=12.2, 2.6 Hz, H8), 2.80 (1H, ddd, J=16.7, 9.1, 2.5 Hz, H6a), 2.56 (1H, dt, J=12.2, 2.6 Hz, H7), 2.38 (1H, ddd, J=12.8, 3.9, 2.6 Hz, H9b), 2.30 (3H, s, H15), 2.20 (1H, ddd, J=16.7, 12.2, 3.3 Hz, H6b), 1.83 (1H, dt, J=12.8, 3.9 Hz, H9a), 1.16 (3H, d, J=7.4 Hz, H14); 13CNMR (150 MHz, CDCl3) δ: 144.8 (C1), 148.5 (C2), 124.7 (C3), 198.5 (C4), 138.1 (C5), 27.2 (C6), 47.4 (C7), 81.5 (C8), 36.6 (C9), 29.1 (C10), 139.2 (C11), 169.7 (C12), 118.9 (C13), 18.8 (C14), 27.9 (C15)。結合張文治等(2009),可鑒定出化合物 9 為蒼耳亭。
化合物 10無色針狀結晶(石油醚乙酸乙酯), mp 169~171 ℃。1HNMR (600 MHz, CDCl3) δ: 5.36 (1H, dd, J=15.0, 8.5 Hz, H23), 5.18 (1H, dd, J=15.0, 8.5 Hz, H23), 4.97 (1H, m, H7), 3.53 (1H, m, H3); 13CNMR (150 MHz, CDCl3) δ: 37.4 (C1), 31.6 (C2), 71.2 (C3), 38.2 (C4), 40.4 (C5), 29.9 (C6), 177.3 (C7), 139.6 (C8), 49.7 (C9), 34.5 (C10), 21.7 (C11), 39.6 (C12), 43.4 (C13), 55.2 (C14), 23.3 (C15), 28.3 (C16), 56.2 (C17), 12.6 (C18), 13.3 (C19), 40.7 (C20), 21.1 (C21), 138.1 (C22), 129.7 (C23), 51.4 (C24), 31.8 (C25), 19.2 (C26), 21.6 (C27), 25.3 (C28), 12.1 (C29)。根據文獻數據(趙曉亞等,2005),鑒定化合物 10 為α菠甾醇。
化合物 11黃色無定形粉末(甲醇), mp 311.9~314.9 ℃。1HNMR (600 MHz, DMSOd6) δ: 12.50 (1H, br s, 5OH), 10.80 (1H, br s, 7OH), 9.61 (1H, br s, 3′OH), 9.37 (1H, br s, 3OH), 9.32 (1H, s, 4′OH), 7.66 (1H, d, J=2.2 Hz, H2′), 7.54 (1H, dd, J=8.5, 2.2 Hz, H6′), 6.89 (1H, d, J=8.5Hz, H5′), 6.41 (1H, d, J=2.0 Hz, H8), 6.20 (1H, d, J=2.0 Hz, H6); 13CNMR (150 MHz, DMSOd6) δ: 156.1 (C2), 135.7 (C3), 176.1 (C4), 147.6 (C5), 98.1 (C6), 163.2 (C7), 93.3 (C8), 160.8 (C9), 102.9 (C10), 121.9 (C1′), 115.0 (C2′), 146.1 (C3′), 115.4 (C5′), 119.9 (C6′)。以上數據與楊寶等(2014)的研究結果一致,可確定化合物 11 為槲皮素。
化合物 12無色脂狀物。1HNMR (600 MHz, CDCl3) δ: 6.16 (1H, d, J=3.4 Hz, H13b), 5.53 (1H, dd, J=8.9, 2.9 Hz, H5), 5.44 (1H, d, J=3.4 Hz, H13a), 4.24 (1H, dt, J=12.6, 2.9 Hz, H8), 2.52 (1H, m, H6a), 2.19 (1H, m, H9b), 2.12 (3H, s, H15), 2.04 (1H, m, H6b), 1.77 (1H, m, H9a), 1.15 (3H, d, J=7.3 Hz, H14); 13CNMR (150 MHz, CDCl3) δ: 147.1 (C1), 34.5 (C2), 42.8 (C3), 208.4 (C4), 122.1 (C5), 25.8 (C6), 48.1 (C7), 82.0 (C8), 37.0 (C9), 33.7 (C10), 138.9 (C11), 170.2 (C12), 118.5 (C13), 18.6 (C14), 30.2 (C15)。以上數據與張樹軍等(2015)的結果一致,因此推斷化合物 12 為蒼耳皂素。
化合物 13黃色結晶 (甲醇), mp 348~350 ℃。1HNMR (600 MHz, DMSOd6) δ: 12.92 (1H, s, 5OH), 10.81 (1H, s, 7OH), 10.37(1H, s, 4′OH), 7.92 (2H, d, J=8.6 Hz, H2′6′), 6.92 (2H, d, J=8.8 Hz, H3′, 5′),6.77 (1H, s, H3), 6.48 (1H, d, J=1.9 Hz, H8), 6.19 (1H, d, J=1.9 Hz, H6); 13CNMR (150 MHz, DMSOd6) δ: 164.1 (C2), 103.2 (C3), 182.3 (C4), 160.6 (C5), 99.1 (C6), 163.4 (C7), 94.5 (C8), 158.2 (C9), 104.9 (C10), 121.8 (C1′), 129.0 (C2′), 116.4 (C3′), 129.0 (C6′), 116.4 (C5′), 160.1 (C4′)。以上數據與衛強等(2015)對照, 可鑒定化合物 13 為芹菜素。
化合物 14無色針狀結晶(石油醚乙酸乙酯), mp 213~215 ℃。1HNMR (600 MHz, CDCl3) δ: 4.67 (1H, s, H29), 4.62 (1H, s, H29), 4.51 (1H, dd, J=12.9, 6.4 Hz, H3), 2.18 (3H, s, COCH3), 1.67 (3H, s, H26), 1.05 (3H, s, H30), 0.99 (3H, s, H27), 0.96 (3H, s, H22), 0.88 (3H, s,H23), 0.87 (3H, s, H25), 0.86 (3H, s, H24), 0.83 (3H, s, H28);13CNMR (150 MHz, CDCl3) δ: 38.3 (C1), 23.3 (C2), 80.7 (C3), 37.7 (C4), 55.3 (C5), 18.2 (C6), 34.6 (C7), 39.3 (C8), 50.3 (C9), 36.9 (C10), 21.5 (C11), 25.4 (C12), 38.2 (C13), 42.9 (C14), 27.6 (C15), 36.5 (C16), 42.7 (C17), 48.7 (C18), 48.5 (C19), 150.6 (C20), 29.5 (C21), 40.7 (C22), 28.0 (C23), 16.2 (C24), 16.9 (C25), 16.4 (C26), 14.6 (C27), 18.0 (C28), 109.4 (C29), 19.1 (C30), 170.8 (CO), 21.3 (CH3COO)。以上結果與王延亮等(2014),徐菁等(2014)對照,鑒定化合物14為羽扇豆醇乙酸酯。
4生物活性
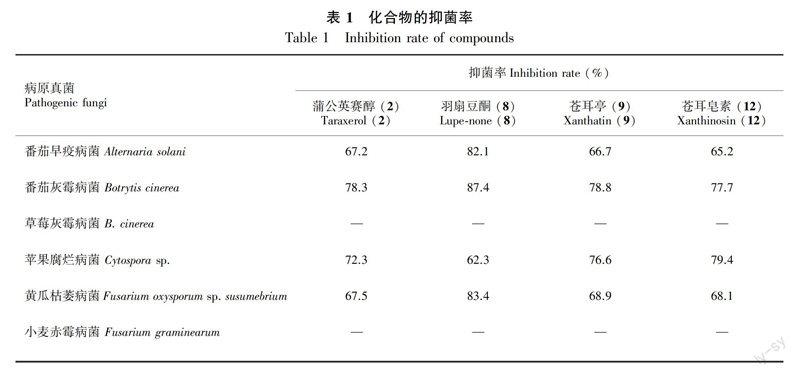
采用平板打孔法,測定化合物2、8、9、12對蕃茄早疫病菌、蕃茄灰霉病菌、草莓灰霉病菌、蘋果腐爛病菌、黃瓜枯萎病菌、小麥赤霉病菌的抑菌作用。將實驗所用菌種進行活化,并選用Φ = 9 cm的培養皿進行培養,實驗樣品用丙酮試劑溶解,對照樣品為丙酮溶劑(馬淑麗等,2015)。測量、計算、對比各菌落的半徑大小可以體現出各單體化合物抑菌活性的強弱。
由表1可知,化合物2、8、9、12除對草莓灰霉病菌和小麥赤霉病菌外,對其它四種病原真菌體現出良好的的抑制作用。其中,化合物2、9、12對蕃茄早疫和黃瓜枯萎病菌的抑菌率在65%以上,對蕃茄灰霉病菌和蘋果腐爛致病菌的抑菌率在75%以上;化合物8對蕃茄早疫和黃瓜枯萎病菌的抑制率均在80%以上,對蕃茄灰霉病菌的抑菌率為87.4%,且抑菌作用隨著濃度的增加而增強。
參考文獻:
CHEN Y, ZUO J, CHEN JW,et al, 2015. Chemical constituents from Claoxylon indicum stems [J]. J Chin Med Mat,38(4): 761-763. [陳勇,左堅,陳建偉,等,2015. 白桐樹枝干化學成分研究 [J]. 中藥材,38(4): 761-763.]
HUA HM,LI X,XING SE,et al,2005. Study on the chemical constituents of Linaria vulgaris [J]. Chin Pharm J,40(9): 653-656. [華會明,李銑,邢素娥,等,2005. 柳穿魚化學成分的研究 [J]. 中國藥學雜志,40(9): 653-656.]
ISAEV IM, MAMEDOVA RP, AGZAMOVA MA, et al,2007. Triterpene glycosides from Astragalus and their genins. L X X V. Sterols and triterpenoids from Astragalus orbiculatus [J]. Chem Nat Comp,43(3): 358-359.
LIU XY,XIE YF,ZHANG H,et al,2014. Chemical constituents from Pouzolzia zeylanica (L.) Benn. var. microphylla (Wedd.) W. T. Wang. [J]. Chin J Exp Trad Med Form,20(6): 43-47. [劉旭陽,謝郁峰,張慧,等,2014. 多枝霧水葛化學成分(I) [J]. 中國實驗方劑學雜志,20(6): 43-47. ]
MA SL, LI HH, LI N, et al, 2015. Chemical constituents and bioactivity of Crepis tectrum linn. [J]. J Qiqihar Univ, 31(2): 45-47. [馬淑麗, 李慧慧, 栗娜, 等, 2015. 還陽參化學成分及生物活性研究[J]. 齊齊哈爾大學學報, 31(2): 45-47. ]
PENG XB, GAO WL, HU DQ, et al, 2012. Chemical constituents from the aerial part of Stauntonia obovatifoliola Hayata subso. urophylla [J]. J Chin Med Mat, 36(11): 1795-1798. [彭小冰, 高偉略, 胡冬群, 等, 2012. 尾葉那藤地上部分化學成分研究 [J]. 中藥材, 36(11): 1795-1798.]
WANG B, ZHAO WX, 2011. The application and chemical constituents of Cocklebur [J]. Chem Ind Times, 25(7): 47-49. [王蓓, 趙衛星, 2011. 蒼耳化學成分研究及應用 [J]. 化工時刊, 25(7): 47-49.]
WANG YL, DUAN SL, ZHANG QY, et al, 2014. Chemical constituents from stems of Ficus tsiangii [J]. Chin Trad Herb Drugs, 45(3): 333-336. [王延亮, 段松冷, 張慶英, 等, 2014. 巖木瓜莖干的化學成分研究 [J]. 中草藥, 45(3): 333-336.]
WEI Q, JI XY, LONG XS, et al, 2015. Chemical constituents from leavea of “Chuju” Chrysanthemum morifolium and their antioxidant activities in vitro [J]. J Chin Med Mat, 38(2): 305-310. [衛強, 紀小影, 龍先順, 等, 2015. 滁菊葉化學成分及其體外抗氧化活性研究 [J]. 中藥材, 38(2): 305-310.]
WU SQ, SUN Q, CHU CJ, et al, 2012. Chemical constituents of Eupatorium lindleyanum [J]. Chin J Chin Mat Med, 37(7): 937-940. [吳雙慶, 孫群, 褚純雋, 等, 2012. 野馬追化學成分的研究 [J]. 中國中藥雜志, 37(7): 937-940.]
WU X, XIA HL, HUANG LH, et al, 2008. Chemical constituents from rhizomes of Cyperus rotundus [J]. J Chin Med Mat, 31 (7): 990-992. [吳希, 夏厚林, 黃立華, 等, 2008. 香附化學成分的研究 [J]. 中藥材, 31 (7): 990-992.]
XU J, GAO HY, MA SL, et al, 2014. Chemical constituents and bioactivity of Kalimeris indica [J]. Chin Trad Herb Drugs, 45(22): 3246-3250. [徐菁, 高鴻悅, 馬淑麗, 等, 2014.馬蘭化學成分及生物活性研究 [J]. 中草藥, 45(22): 3246-3250.]
YANG B, FAN Z, ZHU JP, et al, 2014. Chemical constituents from Phymatopteris hastate [J]. Chin Trad Herb Drugs, 45(21): 3053-3056. [楊寶, 范真, 朱錦萍, 等, 2014. 金雞腳化學成分研究 [J]. 中草藥, 45(21): 3053-3056.]
ZHANG JY, WANG Y, CHEN WH, et al, 2014. Chemical constituents from the stem of Saprosma hainanense [J]. Nat Prod Res Dev, 26(4): 1944-1947. [張俊燕, 王燕, 陳文豪, 等, 2014. 海南染木樹莖的化學成分研究(I) [J]. 天然產物研究與開發, 26(4): 1944-1947.]
ZHANG SJ, LIU H, LI J, et al, 2015. Study on the chemical constituents from whole herbs of Xanthium mongolicum [J]. Chin Trad Herb Drugs, 46(3): 329-333. [張樹軍, 劉煥, 李軍, 等, 2015. 蒙古蒼耳全草化學成分研究 [J]. 中草藥, 46(3): 329-333.]
ZHANG WZ, HAN W, LI Y, et al, 2009. Chemical constituents from Xanthium mongolicum [J]. Chin J Chin Mat Med, 34(13): 1687-1689. [張文治, 韓巍, 李盈, 等, 2009. 蒙古蒼耳化學成分研究 [J]. 中國中藥雜志, 34(13): 1687-1689.]
ZHAO XY, SUN HD, WU JZ, et al, 2005. Studies on chemical constituents from rhizome of Impatiens pritzellii var. hupehensis [J]. Chin J Chin Mat Med, 30(8): 584-586. [趙曉亞, 孫漢董, 吳繼洲, 等, 2005. 冷水七根莖的化學成分研究 [J]. 中國中藥雜志, 30(8): 584-586.]
XU M, WANG D, ZHANG YJ, et al, 2007. Dammarane triterpenoids from the roots of Gentiana rigescens [J]. J Nat Prod, 70(5): 880-883.
XU M, YANG CR, ZHANG YJ, 2009. Minor antifungal aromatic glycosides from the roots of Gentiana rigescens (Gentianaceae) [J]. Chin Chem Lett, 20(10): 1215-1217.
YANG HX, MA F, DU YZ, et al, 2014. Study on the Tibetan medicine Swertia mussotii Franch and its extracts by Fourier transform infrared spectroscopy [J]. Spectrosc Spectr Anal, 34(11): 2973-2977. [楊紅霞, 馬芳, 杜玉枝, 等, 2014. 藏藥川西獐牙菜及其不同提取物的紅外光譜分析 [J]. 光譜學與光譜分析, 34(11): 2973-2977.]
YU H, MACGREGOR JF, 2004. Post processing methods (PLSCCA): simple alternatives to preprocessing methods (OSCPLS) [J]. Chemometr Intell Lab Syst, 73(2): 199-205.
YU XZ, LI QH, SUN DJ, et al, 2015. Determination of the peroxide value of edible oils by FTIR spectroscopy using polyethylene films [J]. Anal Method, 7(5): 1727-1731.
ZHANG J, WIDER B, SHANG H, et al, 2012. Quality of herbal medicines: challenges and solutions [J]. Compl Ther Med, 20(1): 100-106.
ZHAO YL, ZHANG J, JIN H, et al, 2015. Discrimination of Gentiana rigescens from different origins by Fourier transform infrared spectroscopy combined with chemometric methods [J]. J AOAC Int, 98(1): 22-26.
ZHAO YL, ZHANG J, YUAN TJ, et al, 2014. Discrimination of wild Paris based on near infrared spectroscopy and high performance liquid chromatography combined with multivariate analysis [J]. PLoS ONE, 9(2): e89100.

