竹炭碳磺酸的制備及其催化性能
馬兵兵,劉細本,李傳亮,韋一,計偉榮
?
竹炭碳磺酸的制備及其催化性能
馬兵兵,劉細本,李傳亮,韋一,計偉榮
(浙江工業大學化工學院,浙江杭州 310014)
以富含纖維素的天然竹粉為原料,通過硫酸浸漬,炭化和磺化的過程,制備竹炭碳磺酸并將其應用于纖維素水解反應。首先對改性前后的竹粉及其主要成分進行熱重分析,發現硫酸能打破竹粉組分之間部分原有的化學鍵,促進竹粉的熱解過程,使竹粉在低溫下進行熱解與炭化。然后系統地研究浸漬比例、浸漬液濃度、炭化溫度和磺化溫度等因素對催化劑活性的影響,得到催化劑最優制備條件。最后采用XRD、BET、FT-IR和SEM等方法對竹炭碳磺酸進行表征,結果表明通過合理調控溫度能使竹炭磺酸具有良好的孔結構和較高的磺酸量,且磺酸量可能和芳香碳環上的活潑氫數目有關。
纖維素;竹炭碳磺酸;制備;水解;催化劑
引 言
經濟社會的發展離不開能源,隨著石油資源的快速消耗,能源危機問題已經引起人們的高度重視。纖維素作為主要的可再生能源,具有種類多、來源廣、可再生等優勢[1],它可以通過水解生成包括葡萄糖等在內的還原糖,再由這些還原糖轉化為乙醇、5-HMF、山梨醇等重要物質[2]。然而,纖維素的天然結構牢固,轉化較為困難,因而綠色高效地開發利用纖維素對當今社會的可持續發展具有重要意義。目前,纖維素水解主要采用的方式有酸催化[3]和酶催化[4],其中,液相酸催化和酶催化面臨的難題是催化劑和產品分離困難、催化劑回收利用過程復雜等問題。因此,近年來開發非均相固體酸催化劑成為研究熱點。碳基固體酸因制備簡單、成本低、環境污染少、可回收利用等優點而受到研究者的廣泛關注。Hara等[5]首次報道了將廉價碳水化合物進行不完全炭化,后經磺化得到層狀結構的芳香碳環,其表面帶有-SO3H、-OH、-COOH,然后將其用于纖維素水解,得到了較高的還原糖收率。隨后更多的學者分別以不同生物質碳源如葡萄糖[6]、竹屑[7]、纖維素[8]、酚渣[9]、柳木粉[10]等制備了碳基固體酸,用于纖維素水解反應并取得了一定的催化效果。這些碳基固體酸具有相似結構,縮合芳香環組成的無定形芳香碳層片,在其邊緣負載著具有催化活性的磺酸基。其中以纖維素為碳源制備碳磺酸的磺酸基密度最高。但大多數生物質碳磺酸在水解反應中都存在傳質效果差、催化效率不夠高的問題。這可能是由于纖維素分子的尺寸一般比較大,催化劑的孔道結構會影響大分子物質在催化劑中的擴散效果[11]。本實驗室曾對蜂窩狀大孔結構的竹炭碳磺酸[12]進行了初步探究,該催化劑對微晶纖維素水解有較好的催化效果。本文將對竹粉制備碳磺酸進行深入研究,重點研究竹粉的硫酸處理、炭化和磺化條件對竹炭碳磺酸的微觀結構和性能的調變,旨在開發表面結構和化學性質有利于纖維素水解的碳磺酸催化劑。
1 實驗部分
1.1 原料與設備
竹粉(纖維素:49.16%,半纖維素:16.25%,木質素:23.86%),購買自浙江麗水,烘干后過250mm篩備用。微晶纖維素(-cellulose,平均粒徑50 μm),葡萄糖(分析純),濃硫酸(分析純),均購買自阿拉丁。木質素購買自上海騰準生物科技。
實驗裝置:DF101S集熱式恒溫加熱磁力攪拌器,水熱合成反應釜(15 ml)。
1.2 催化劑表征
(1)磺酸量測定 根據文獻[13]的方法,取定量的催化劑與NaCl溶液通過超聲波進行離子交換,然后滴定濾液可以得出碳基固體酸催化劑中所含的磺酸量。
(2)熱重分析(TG/DTG)樣品在熱重分析儀(TG209F3,Netzsch,Germany)上測定。載氣是99.99%的高純氮,流量為40 ml·min?1,速率10℃·min?1。
(3)N2-物理吸附分析(BET)比表面積和孔結構通過N2-物理吸附,在貝士德儀器科技(北京)有限公司生產的3H-2000PS1型吸附儀上進行測定。
(4)掃描電子顯微鏡(SEM)催化劑的表面形貌在日本日立集團生產的Hitachi S-4700(Ⅱ)型掃描電子顯微鏡上觀察得到。
(5)X射線衍射分析(XRD)采用荷蘭PNAlytical公司生產的X'Pert Pro X射線衍射儀,掃描范圍2=20°~80°。
(6)紅外光譜分析(FT-IR)紅外實驗在美國Nicolet公司生產的IS50型傅里葉變換紅外光譜儀上進行,KBr壓片制樣。分辨率,4 cm?1;掃描次數,64次;測試范圍,650~4000 cm?1。
1.3 催化劑的制備
采用3個步驟制備竹炭碳磺酸,具體過程如下。
(1)浸漬 按一定浸漬比,將竹粉在一定濃度的硫酸溶液中浸漬6 h,過濾后在110℃下烘干備用。
(2)炭化 取5 g上述烘干的竹粉在20 ml·min?1N2保護下,在200℃下預碳化1 h,再以10℃·min?1升溫至一定溫度,炭化1 h后得到竹炭。將竹炭研磨成粉末過150mm篩網后備用。
(3)磺化 取1.0 g上述碳粉末加15 ml質量分數98%的濃硫酸置于水熱反應釜中,150℃下磺化6 h。冷卻后稀釋過濾,90℃以上去離子水洗滌黑色固體至濾液檢測不到硫酸根離子為止。最后將洗滌后的黑色固體在110℃下干燥12 h得到竹炭碳磺酸。
1.4 水解反應
將0.05 g微晶纖維素、0.05 g碳磺酸催化劑和3 ml去離子水投入反應釜中,升溫到160℃,攪拌反應6 h,經冷卻水冷卻到室溫,離心分離并取上層清液用DNS法測還原糖量[14]。同時使用島津HPLC分析產物葡萄糖,條件:伯樂糖分析柱Aminex HPX-87C (300 ×4.6 mm),RID檢測器(島津RI-10A),流動相是體積比為7:3的乙腈/水溶液。
產物計算方法
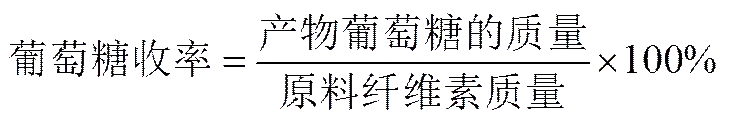
2 結果與討論
2.1 硫酸改性對竹粉炭化的影響
對硫酸浸漬改性前后的竹粉、纖維素、木質素進行了熱重分析并對結果進行了比較。
2.1.1 竹粉在改性前后TG/DTG的變化 圖1(a)、(b)分別呈現了改性前后竹粉的TG/DTG曲線。圖1(a)所示,在150℃之前,由于竹粉中自由水的揮發,竹粉發生緩慢失重。在220~460℃區間,發生半纖維素和纖維素的氫鍵斷裂和羥基脫水,生成大量的羰基、烯烴雙鍵和環醚結構,緊接著進行脫氧,重排、脫氫、縮合等反應[15],竹粉失重加快。在460℃以后,竹粉中的木質素發生分解,在720~785℃出現了一個小的失重峰后不再變化,說明竹粉炭化結束。在圖1(b)中可以看到,DTG曲線上水分揮發后出現了兩個失重峰。這是由于稀硫酸浸漬破壞了竹粉的細胞壁結構,溶解了部分果膠和半纖維素,打斷了纖維素、半纖維素和木質素部分原有分子間的結合鍵[16],促進竹粉的熱解。在150~315℃區間,纖維素和半纖維素發生分子內脫水和脫氧反應,木質素可能發生連接苯環的一些碳鏈斷裂,形成較小的木質素分子[17]。在315~585℃區間,纖維素發生脫氫反應,木質素大分子繼續分解,生成自由基,并發生重排或碳環縮合。585℃以后,竹粉的TG曲線逐漸平緩,炭化結束。
2.1.2 纖維素和木質素在改性前后TG/DTG的變化 圖2是改性前后纖維素的TG/DTG曲線。從圖2(a)可知,改性前纖維素在水分揮發后,出現一個失重峰,發生脫水、脫氧和脫氫等反應。從圖2(b)可知,纖維素改性后出現了兩個失重峰,可能因為酸破壞了糖苷鍵結構,使脫氧的反應溫度降低,而后發生脫氫反應,550℃左右炭化結束。比較改性前后纖維素的TG曲線,發現改性后纖維素的得碳率較改性前顯著提高。圖3是改性前后木質素的TG/DTG曲線。從圖3(a)可知,木質素在改性前發生緩慢失重,在150~720℃區間發生舊官能團斷裂和新官能團的生成與重組。從圖3(b)可知,改性后的木質素在120~280℃區間,發生苯環間連接的化學鍵斷裂。280~585℃區間是主要的失重區間,發生木質素熱解后的自由基重排和碳環縮合。改性木質素在600℃基本炭化結束,而未改性木質素在785℃結束炭化。由此得出:硫酸改性顯著促進了竹粉中木質素和纖維素在低溫下的熱解與炭化。
2.2 主要制備條件對竹炭碳磺酸催化活性的影響
2.2.1 浸漬比例對竹炭碳磺酸催化活性的影響 圖4是浸漬比例對竹炭碳磺酸催化活性的影響。將竹粉和硫酸按不同浸漬比例(1:2~5,質量比)浸漬6 h,在600℃下,當浸漬液濃度為1 mol·L?1、炭化時間為1 h時,隨著浸漬比的提高,還原糖和葡萄糖收率逐漸增加,當浸漬比為1:4時,二者收率達到最大值。由于浸漬比例的不同,相同時間內浸漬液對竹粉成分間化學鍵的破壞程度不同,竹粉的熱解速度不同,生成性質不同的竹炭,因此,在不同浸漬比例下的竹炭碳磺酸表現出不同的催化性能。
2.2.2 浸漬液濃度對竹炭碳磺酸催化活性的影響 圖5是浸漬液濃度對竹炭碳磺酸催化活性的影響。600℃下,按照1:4浸漬比,炭化1 h時,還原糖和葡萄糖收率隨著浸漬液濃度的升高出現先增大后減少的趨勢,當浸漬液濃度為1 mol·L?1時,二者的收率達到最大。因為浸漬液濃度不同,相同時間內浸漬液對竹粉組分間化學鍵的作用效果不一樣,竹粉的熱解速度不同,造成竹炭的表面化學性質有所差異,所以在不同浸漬液濃度下的竹炭碳磺酸表現出不同的催化效果。
(reaction condition: 0.05 g-cellulose, 0.05 g catalyst, 3 ml H2O, 160℃, 6 h)
(reaction condition: 0.05 g-cellulose, 0.05 g catalyst, 3 ml H2O, 160℃, 6 h)
2.2.3 炭化溫度對竹炭碳磺酸催化活性的影響 圖6是炭化溫度對竹炭碳磺酸催化活性的影響。竹炭碳磺酸在溫度區間400~700℃內,隨著炭化溫度的升高,還原糖和葡萄糖的收率先增加后減少,在600℃二者收率都達到最大,隨后則隨著溫度的升高而逐漸降低。結合表1可以看出,炭化溫度能顯著影響竹炭碳磺酸的性質和催化活性。隨著炭化溫度的升高,竹炭碳磺酸的孔徑變大,磺酸量增多,纖維素分子很容易進入化劑內部,接觸到孔道內部的活性中心,從而實現纖維素分子的高效轉化。綜合以上得到:600℃是比較合適的炭化溫度,在此炭化溫度下制備的竹炭碳磺酸的磺酸量高,表現出較強的催化活性。
(reaction condition: 0.05 g-cellulose, 0.05 g catalyst, 3 ml H2O, 160℃, 6 h)

表1 炭化溫度對竹炭磺酸孔結構和磺酸量的影響
① 2 BJH method. ② Acid-base back titration. ③ Turnover freqnency.
2.2.4 磺化溫度對竹炭碳磺酸催化活性的影響 圖7是磺化溫度對竹炭碳磺酸催化活性的影響。竹炭在不同溫度下磺化6 h后得到不同性質的竹炭碳磺酸。從圖7中看出,還原糖和葡萄糖收率隨著磺化溫度的升高,也出現一個先增大后減少的趨勢,在磺化溫度為150℃時還原糖和葡萄糖的收率達到最大。當磺化溫度過高時,碳材料會發生嚴重氧化,造成催化劑活性下降。因此選擇150℃為最適磺化溫度。
(reaction condition: 0.05 g-cellulose, 0.05 g catalyst, 3 ml H2O, 160℃, 6 h)
從以上討論可以得到:浸漬比例、浸漬液濃度、炭化溫度和磺化溫度等主要制備條件都會影響竹炭碳磺酸的催化性能。在1 mol·L?1硫酸溶液中按1:4質量比浸漬6 h的竹粉,經600℃炭化1 h,然后在150℃磺化6 h。得到的竹炭碳磺酸磺酸量高,反應活性強。通過該方法制備的竹炭碳磺酸的催化性能與文獻中的其他固體酸催化劑作比較,結果如表2所示。從TOF比較中可看出該竹炭碳磺酸催化效果較為突出。下文將研究該竹炭碳磺酸的微觀特性來分析原因。
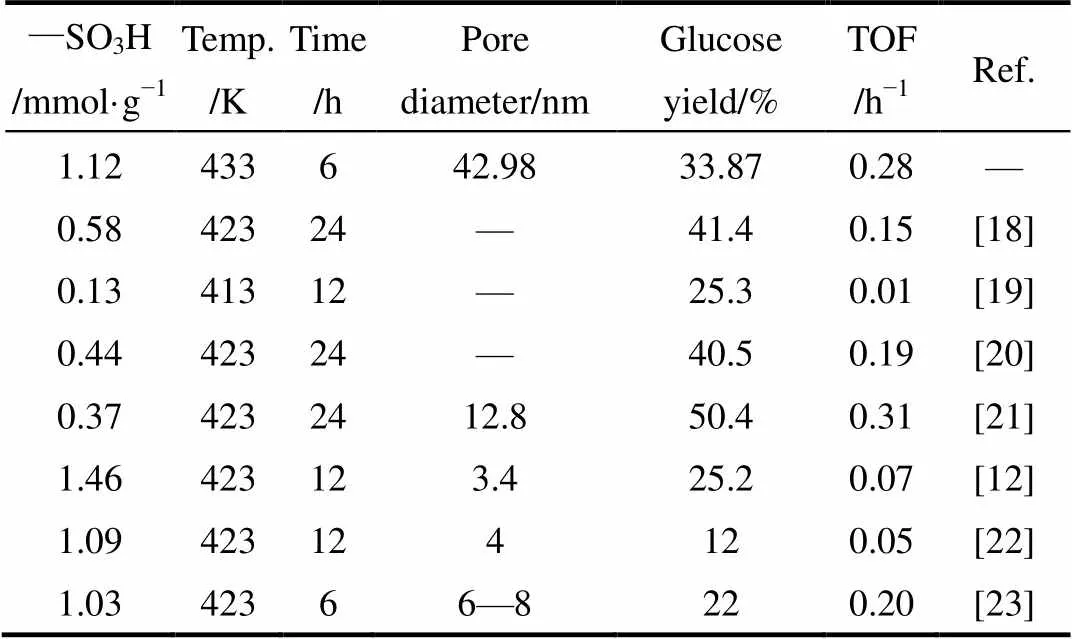
表2 竹炭碳磺酸與其他催化劑的催化性能比較
Note: TOF was estimated on basis of formation rate of glucose calculated by glucose yield.
2.3 竹炭碳磺酸催化劑性能影響的微觀分析
采用不同催化劑表征手段,重點對炭化溫度對竹碳磺酸催化劑性能的影響進行微觀分析。
2.3.1 BET 表1是不同炭化溫度下測定的竹炭碳磺酸的比表面、孔徑以及表面磺酸量。從表1中得知炭化溫度對竹炭碳磺酸的結構和磺酸量具有很大影響。隨著炭化溫度升高,竹炭碳磺酸的比表面積和平均孔徑呈現的是先增大后減小的趨勢。但400℃下可能由于活化劑沒有對竹炭本身中空結構造成過多的破壞,因此該溫度下竹炭碳磺酸的比表面積比其他溫度下的比表面積略高一點。隨著炭化溫度升高,活化劑造孔明顯,比表面積增加,孔徑變大。但過高的炭化溫度使活化劑對竹炭的剝蝕程度加深,孔道結構遭到破壞,比表面積下降,孔徑變小。磺酸量隨著炭化溫度的不同也出現先增大后減小的趨勢,這是由于隨著炭化溫度升高,孔結構充分發育,活性位點增多,磺酸量上升;但過高的炭化溫度造成竹炭石墨化加深,活性位點減少,磺酸量下降。因此,選擇合適的炭化溫度能使竹炭磺酸的微觀結構和磺酸量達到一個良好的平衡。
2.3.2 FT-IR 圖8(a)、(b)分別是竹炭在磺化前后的FT-IR圖。由圖8(a)可以看出,從400℃開始,碳環中的C-H鍵在875、815、758 cm?1處出現了3個非平面搖擺振動峰[24],表示竹炭中開始出現芳香碳環不同程度的縮合,在升溫至700℃過程中,分別在1580、1700 cm?1處的C=C[25]、C=O[26]鍵的振動峰強度逐漸減弱,而在875 cm?1處C-H鍵的振動峰強度不斷增強,說明隨著炭化溫度的升高,芳香碳環的縮合程度升高,碳環中的取代位置增多。但過高的炭化溫度使竹炭石墨化程度加深,碳環上被取代位置減少。磺化后如圖8(b)所示,在1042和1167 cm?1處出現-SO3H[27]的伸縮振動峰,表明磺酸基已成功負載在碳材料上。從圖8(b)還可以看出,磺化后在875 cm?1處C-H振動峰強度立即減弱,這種減弱程度越明顯,說明碳材料上的磺酸基負載量越多。文中采用峰面積比(:875 cm?1處振動峰面積占875、815、758 cm?1三者振動峰總面積的比值)來比較磺化前后在875 cm?1處C-H振動峰強度變化,結果見表3。其中3隨炭化溫度變化趨勢和表1中磺酸量隨炭化溫度變化的趨勢相符合。紅外表明:竹炭碳磺酸的磺酸量可能和芳香碳環上產生的活潑氫數目有關。

表3 磺化前后峰面積比的變化
Note:1is peak area ratio before sulfonation,2is peak area ratio after sulfonation,3=1?2.
2.3.3 XRD 圖9是不同炭化溫度下的竹炭的XRD圖,在溫度區間400~700℃,4個樣品在衍射角2=15°~35°范圍內都出現屬于002晶面衍射峰,說明它們都屬于無定形碳,由大量不均勻的芳香片層以隨機的方式排列而成[28]。隨著炭化溫度升高,002面衍射峰寬度變窄,強度值增大,600℃時在2=40°~50°處出現了強度較弱的101面晶體衍射峰。說明石墨化的晶體結構出現,芳香碳環片層增大[29]。由于炭化溫度不同,碳載體骨架結構會發生改變,活性組分與碳載體之間的相互作用也存在差距,所以不同炭化溫度下制備的竹炭磺酸在纖維素水解中表現出不同的催化活性。
2.3.4 SEM 通過SEM來觀察該竹炭碳磺酸的形貌,發現竹炭碳磺酸表面局部存在許多不規整的大孔結構,如圖10(a),竹孔內壁比較光滑,給纖維素大分子提供了良好的反應場所。從圖10(b)還可以看到磺化后的竹炭內部存在部分圓柱形“大通道”,外部邊緣還有許多規整孔道。竹炭表面這些結構的存在是有利于反應物或產物傳質的。
綜合分析表征結果:經硫酸浸漬的竹粉,通過控制炭化溫度來調變竹炭結構和碳載體上活性位點數目,能得到適合纖維素分子傳質的孔結構和負載大量磺酸基團的竹炭碳磺酸催化劑,該催化劑可實現對纖維素的高效催化。
3 結 論
(1)硫酸浸漬能有效破壞竹粉中部分纖維素和木質素分子內和分子間的結合鍵,促進竹粉從外到內的熱解,使竹粉在低溫下進行熱解與炭化,影響竹炭結構的形成。
(2)炭化溫度的高低不僅影響竹碳磺酸的微觀結構,而且影響芳香碳及其活潑氫的數量,進而可能影響磺酸量的大小。通過合理調控炭化溫度能使竹炭磺酸具有良好的孔結構和較高的磺酸量。
(3)竹炭碳磺酸表面具有一定數量的大孔,孔道結構有利于纖維素分子的傳質遷移,碳載體上負載有大量磺酸基團,這可能是其在纖維素水解反應中具有較好催化效果的重要原因。
References
[1] WANGY, SONG H, PENG L,Recent developments in the catalytic conversion of cellulose[J]. Biotechnology & Biotechnological Equipment, 2014, 28(6): 981-988.
[2] HUANG Y B, FU Y. Hydrolysis of cellulose to glucose by solid acid catalysts[J]. Green Chem., 2013, 44(31): 1095-1111.
[3] TORGET R W, KIM J S, LEE Y Y. Fundamental aspects of diluteacid hydrolysis/fractionation kinetics of hardwood carbohydrates[J]. Industrial & Engineering Chemistry Research, 2000, 39(8): 2817-2825.
[4] ZHANG Y-H P, LYND L R. Toward an aggregated understanding of enzymatic hydrolysis of cellulose: noncomplexed cellulase systems[J]. Biotechnology and Bioengineering, 2004, 88(7): 797-824.
[5] SUGANUMA S, NAKAJIMA K, KITANO M,. Hydrolysis of cellulose by amorphous carbon bearing SO3H, COOH, and OH groups[J]. Journal of the American Chemical Society, 2008, 130(38): 12787-12793.
[6] JIANG Y J, LI X T, CAO Q,. Acid functionalized, highly dispersed carbonaceous spheres: an effective solid acid for hydrolysis of polysaccharides[J]. J. Nanopart. Res., 2011, 13(13): 463-469.
[7] WU Y Y, FU Z H, YIN D L,. Microwave-assisted hydrolysis of crystalline cellulose catalyzed by biomass char sulfonic acids[J]. Green Chem., 2010, 12(4): 696-700.
[8] SATOSHI S, KIYOTAKA N, MASAAKI K,. Synthesis and acid catalysis of cellulose-derived carbon-based solid acid[J]. Solid State Sciences, 2010, 12(6): 1029-1034.
[9] SHEN S G, WANG C Y, CAI B,. Heterogeneous hydrolysis of cellulose into glucose over phenolic residue-derived solid acid[J]. Fuel, 2013, 113(6): 644-649.
[10] SUN Z, TAO M L, ZHAO Q,. A highly active willow-derived sulfonated carbon material with macroporous structure for production of glucose[J]. Cellulose, 2015, 22(1): 675-682.
[11] DOUGLAS M R. Diffusion in Zeolites and Other Microporous Solids[M]. New York: John Wiley & Sons Inc., 1992: 605
[12] 蔡新興, 汪祝勝, 李瑛, 等. 生物質碳磺酸的制備以及其催化水解纖維素性能[J]. 化工學報, 2015, 66(8): 3106-3112.CAI X X, WANG Z S, LI Y,. Preparation of biomass carbon-based solid acid and its catalytic characteristics in hydrolysis of cellulose[J]. CIESC Journal, 2015, 66(8): 3106-3112.
[13] ISA K M, DANIELA R R, VICTOR S Y L,. Organosulfonic acid-functionalized mesoporous silicas for the esterification of fatty acid[J]. Journal of Catalysis, 2003, 219(2): 329-336.
[14] LI C Z, ZHAO Z B K. Efficient acid-catalyzed hydrolysis of cellulose in ionic liquid[J]. Advanced Synthesis &Catalysis, 2007, 349(11/12): 1847-1850.
[15] 辛善志, 米鐵, 楊海平, 等. 纖維素低溫炭化特性[J].化工學報, 2015, 66(11): 4603-4610. XIN S Z, MI T, YANG H P,. Features of low temperature carbonization of cellulose[J]. CIESC Journal, 2015, 66(11): 4603-4610.
[16] KARIN O, RENATA B, JACK S G. Effect of hemicellulose and lignin removal on enzymatic hydrolysis of steam pretreated corn stover[J]. Bioresource Technology, 2007, 98(13): 2503-2510.
[17] 程輝, 余劍, 姚梅琴, 等. 木質素慢速熱解機理[J]. 化工學報, 2013, 64(5): 1757-1765. CHENG H, YU J, YAO M Q,. Mechanism analysis of lignin slow pyrolysis[J]. CIESC Journal, 2013, 64(5): 1757-1765.
[18] AYUMU O, TAKAFUMI O, KAZUMICHI Y. Hydrolysis of cellulose selectively into glucose over sulfonated activated-carbon catalyst under hydrothermal conditions[J]. Topics in Catalysis, 2009, 52(6): 801-807.
[19] ZHANG C B, WANG H Y, LIU F D,. Magnetic core-shell Fe3O4@C-SO3H nanoparticle catalyst for hydrolysis of cellulose[J]. Cellulose, 2013, 20(1): 127-134.
[20] AYUMU O. Selective hydrolysis of cellulose and polysaccharides into sugars by catalytic hydrothermal method using sulfonated activated-carbon[J]. Journal of the Japan Petroleum Institute, 2012, 55(2): 73-86.
[21] VAN DE VYVER S, PENG L, GEBOERS J,. Sulfonated silica/carbon nanocomposites as novel catalysts for hydrolysis of cellulose to glucose[J]. Green Chem., 2010, 12(9): 1560-1563.
[22] LAI D M, DENG L, LI J,. Hydrolysis of cellulose into glucose by magnetic solid acid[J]. ChemSusChem, 2011, 4(1): 55-58.
[23] ZHANG X C, ZHANG Z, WANG F,. Lignosulfonate-based heterogeneous sulfonic acid catalyst for hydrolyzing glycosidic bonds of polysaccharides[J]. Journal of Molecular Catalysis A: Chemical, 2013, 377(377): 102-107.
[24] YANG H P, YAN R, CHEN H P,. Characteristics of hemicellulose, cellulose and lignin pyrolysis[J]. Fuel, 2007, 86(12/13): 1781-1788.
[25] LOU W Y, GUO Q, CHEN W J,. A highly active bagasse-derived solid acid catalyst with properties suitable for production of biodiesel[J]. ChemSusChem, 2012, 5(8): 1533-1541.
[26] TORREN R C, JUNGHO J, LIN Y C,. Catalytic fast pyrolysis of glucose with HZSM-5: the combined homogeneous and heterogeneous reactions[J]. Journal of Catalysis, 2010, 270(1): 110-124.
[27] KIYOTAKA N, MICHIKAZU H. Amorphous carbon with SO3H groups as a solid Br?nsted acid catalyst[J]. ACS Catal., 2012, 2(7): 1296-1304.
[28] SATOSHI S, KIYOTAKA N, MASAAKI K,. Synthesis and acid catalysis of cellulose-derived carbon-based solid acid[J]. Solid State Sciences, 2010, 12(6): 1029-1034.
[29] MAI O, ATSUSHI T, MASAKAZU T,. Acid-catalyzed reactions on flexible polycyclic aromatic carbon in amorphous carbon[J]. Chem. Mater., 2006, 18(13): 3039-3045.
Preparation of bamboo carbon-based solid acid and its catalytic properties
MA Bingbing, LIU Xiben, LI Chuanliang, WEI Yi, JI Weirong
(College of Chemical Engineering, Zhejiang University of Technology, Hangzhou 310014, Zhejiang, China)
Bamboo carbon-based solid acid was preparedsulfuric acid impregnation, carbonization and sulfonation with cellulose-rich bamboo powder as feedstock, and its application in cellulose hydrolysis was studied. Firstly, the results obtained by TG of raw and modified bamboo powders and their main components showed that sulfuric acid had significant effects on breaking the chemical bonds in bamboo power to promote the pyrolysis and carbonization processes at lower temperature. The systematically research was conducted on the impregnation ratio, impregnation concentration, carbonization temperature and sulfonation temperature, which strongly affected the catalytic properties of bamboo carbon-based solid acid. Then, the optimal preparation conditions were obtained. Finally, the bamboo carbon-based solid acid was characterized by XRD, BET, FT-IR and SEM. These results indicated that the bamboo carbon-based solid catalyst had a favourable textile structure and considerable sulfonic acid content, showing that the sulfonic acid content was related to the number of active hydrogen on the aromatic carbon.
cellulose; bamboo carbon-based solid acid; preparation; hydrolysis; catalyst
10.11949/j.issn.0438-1157.20161850
TQ 127.1; TQ 353.6; TK 6
A
0438—1157(2017)06—2386—08
計偉榮。
馬兵兵(1991—),男,碩士研究生。
浙江省錢江人才計劃項目(2006R10017)。
2017-01-02收到初稿,2017-02-26收到修改稿。
2017-01-02.
Prof. Ji Weirong, weirong.ji@zjut.edu.cn
supported by the Qianjiang Talent of Zhejiang Province (2006R10017).

