殺菌劑氟嘧菌酯的合成
婁萬喬,張大永
(中國藥科大學 藥物科學研究院,南京 210009)
◆研究與開發◆
殺菌劑氟嘧菌酯的合成
婁萬喬,張大永
(中國藥科大學 藥物科學研究院,南京 210009)
報道了殺菌劑氟嘧菌酯的合成工藝研究。以4-羥基香豆素為原料,依次經過硝化、堿水解、甲胺化、環合、醚化和堿重排環合反應得到(E)-(5,6-二氫-[1,4,2]-二嗪-3-基)-(2-羥基苯基)-甲酮-O-甲基肟(中間體F);以2-氟丙二酸二乙酯為原料,經與醋酸甲脒成環后進行氯化反應合成中間體4,6-二氯-5-氟嘧啶;中間體F先后與4,6-二氯-5-氟嘧啶和2-氯苯酚進行醚化反應得到目標產物氟嘧菌酯。以4-羥基香豆素計,合成總收率達17%,產品質量分數為96%(HPLC)。
氟嘧菌酯;合成;4-羥基香豆素;4,6-二氯-5-氟嘧啶
氟嘧菌酯(fluoxastrobin)化學名稱為(E)-{2-[6-(2-氯苯氧基)-5-氟嘧啶-4-基氧]苯基}(5,6-二氫-1, 4,2-二嗪-3-基)甲酮-O-甲基肟。其是由拜耳公司開發的甲氧基丙烯酸酯類殺菌劑,為線粒體呼吸作用抑制劑,通過抑制細胞色素b和c1間的電子傳遞,進而阻止能量(ATP)產生,最終導致細胞死亡[1]。氟嘧菌酯1994年由拜耳發現,2004年進入歐洲主要市場,2005年在德國、法國、美國等相繼上市。其2009年全球銷售額在1.5億美元,2011年為1.75億美元,2014年升至2.20億美元,2015年回落至2.00億美元,該產品具有良好的銷售前景[2]。氟嘧菌酯在中國的化合物專利于2017年到期,因此對氟嘧菌酯的合成進行研究具有重要意義。
文獻報道合成氟嘧菌酯的主要中間體有(E)-(5,6-二氫-[1,4,2]-二嗪-3-基)-(2-羥基苯基)-甲酮-O-甲基肟、4,6-二氯-5-氟嘧啶以及2-氯苯酚[3-4]。其合成路線如下:

參考關于中間體(E)-(5,6-二氫-[1,4,2]-二嗪-3-基)-(2-羥基苯基)-甲酮-O-甲基肟的合成綜述[5-6],選定下述合成路線。
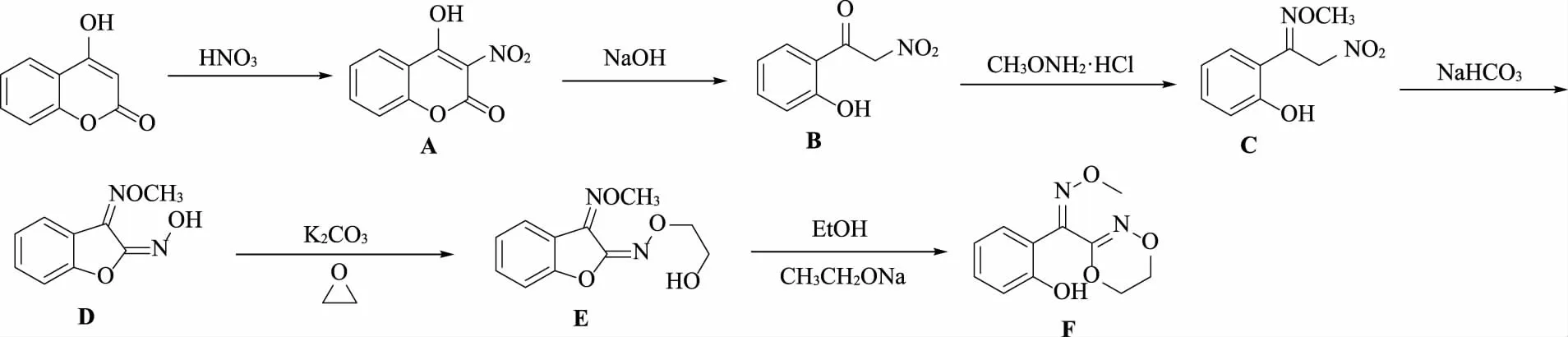
為避開條件苛刻的氟代反應,本文參考文獻[7],以2-氟丙二酸二乙酯為原料合成中間體4,6-二氯-5-氟嘧啶,具體反應路線如下。
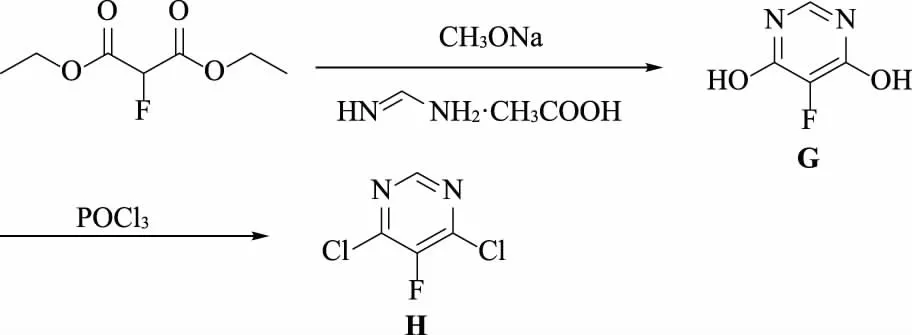
1 實驗部分
1.1 試劑與儀器
試劑:4-羥基香豆素、甲氧基胺鹽酸鹽、環氧乙烷、2-氟丙二酸二乙酯、醋酸甲脒。
儀器:Burker Avance 300型核磁共振儀(以TMS為內標)、Shimadzu LC-20AT高效液相色譜儀、Bruker Esruire 3000 Plus ESI/MS型質譜儀、JH30全自動熔點儀、ZF-I型三用紫外分析儀。
1.2 合成
1.2.1 3-硝基-4-羥基香豆素(中間體A)的合成
在500m L三頸瓶中加入50 g(0.31mol)4-羥基香豆素,使其溶于200m L氯仿,冰浴下緩慢滴加65%濃硝酸0.62mol,控制溫度在10℃左右,反應3 h。反應完全后,抽濾,少量水洗,真空干燥,得到橙黃色片狀固體中間體A,收率為89%。熔點174~176℃(文獻值174~175℃[8])。
1H NMR(300 MHz,CDCl3)δ:8.175(d,1H,aromatic), 7.854(t,1H,aromatic),7.488(t,1H,aromatic),7.402(d,1H, aromatic)。ESI-MS(m/z):206.0[M-H]-。
1.2.2 2-羥基-2'-硝基苯乙酮(中間體B)的合成
在1 L三頸瓶中投入45 g(0.22mol)3-硝基-4-羥基香豆素,使其溶于500m L 5%NaOH水溶液,加熱至70℃,反應4 h后冷卻至室溫,加10%稀鹽酸調pH值至固體不再析出。當pH值約為2時,濾液較稀,便于抽濾,抽濾得固體產物中間體B,收率為94%。熔點107~108℃(文獻值106℃[9])。
1H NM R(300 MHz,CDCl3)δ:7.621(t,1H,aromatic), 7.457(d,1H,aromatic),7.103(d,1H,aromatic),7.005(t,1H, aromatic),5.933(s,2H,CH2)。ESI-MS(m/z):180.0[M-H]-。
1.2.3 1-(2-羥基苯基)-2-硝基-乙酮-O-甲基肟(中間體C)的合成
在500m L三頸瓶中,將32.2 g(0.38mol)甲氧基胺鹽酸鹽在冰浴條件下溶解于210m L甲醇中,15 m in后加入35 g(0.19mol)2-羥基-2'-硝基苯乙酮,升溫至60℃,攪拌6 h,反應完全后冷卻至室溫。冷卻后將反應液傾入300m L冰水中,不斷攪拌,抽濾得中間體C。純品為白色晶狀固體,收率為82%。
1H NMR(300MHz,CDCl3)δ:10.355(s,1H,OH),7.332 (m,2H,aromatic),7.063 (d,1H,aromatic),6.968 (t,1H,aromatic),5.722(s,2H,CH2),4.138(s,3H,CH3)。ESI-MS(m/z): 211.0[M+H]+。
1.2.4 苯并呋喃-2,3-二酮-3-(O-甲基肟)-2-肟(中間體D)的合成
在500m L三頸瓶中加入48 g(0.56mol)碳酸氫鈉,使其溶解于300m L水中,加入30 g(0.14mol)1-(2-羥基苯基)-2-硝基-乙酮-O-甲基肟,升溫至65℃反應,反應5 h后直接冷卻至室溫,抽濾,得米黃色粒狀固體,其為中間體D的2種立體異構體混合物,收率為94%。
1H NMR(300 MHz,CDCl3)δ:8.040(m,1H,aromatic), 7.463(m,1H,aromatic),7.194(m,2H,aromatic),4.225(s,3H, CH3)。ESI-MS(m/z):193.0[M+H]+,215.0[M+Na]+。
1.2.5 苯并呋喃-2,3-二酮-2-[O-(2-羥乙基)肟]-3-O-甲基肟(中間體E)的合成
在2 L三頸瓶中加入70.5 g(0.51mol)碳酸鉀,溶于1 000m L水中,投入97.6 g(0.51mol)苯并呋喃-2, 3-二酮-3-(O-甲基肟)-2-肟,室溫攪拌2 h,加入50m L環氧乙烷,反應12 h后處理。抽濾,將濾餅用乙酸乙酯溶解,母液繼續用乙酸乙酯萃取3次,每次200 m L,合并有機相。有機相先用10%稀鹽酸洗滌2次,再用飽和氯化鈉溶液洗滌2次,無水硫酸鈉干燥。有機相旋干后得到含有2種立體異構體的中間體E,紅棕色黏稠液,反應收率為78%。1H NMR(300 MHz,CDCl3)δ:7.326 (t,1H,aromatic), 7.213(d,1H,aromatic),6.957(m,2H,aromatic),4.483(t,2H, CH2),4.198(t,2H,CH2),4.089(s,3H,CH3)。ESI-MS(m/z): 259.1[M+Na]+。
500m L四口瓶中加入14.2 g(0.21mol)乙醇鈉,將其溶于240m L乙醇,將49.3 g(0.21mol)苯并呋喃-2,3-二酮-2-[O-(2-羥乙基)肟]-3-O-甲基肟加入上述溶液中,并加熱至60℃左右,TLC點板跟蹤,反應8~9 h。反應完全后冷卻,用冰醋酸調節pH值為5~6,過濾,得到固體產物中間體F,收率為50%。
1H NMR(300MHz,CDCl3)δ:10.102(s,1H,OH),7.354 (d,1H,aromatic),7.286(t,1H,aromatic),6.986(d,1H,aromatic),6.904 (t,1H,aromatic),4.476 (t,2H,CH2),4.261 (t,2H, CH2),4.047(s,3H,CH3)。ESI-MS(m/z):259.1[M+Na]+。
1.2.7 4,6-二氯-5-氟嘧啶(中間體H)的合成
在250m L三頸瓶中,加入50.4 g(0.28mol)30%甲醇鈉甲醇溶液,冰浴下加入32.1 g(0.28mol)醋酸甲脒,攪拌1 h后再在冰浴下滴加50 g(0.28 mol)2-氟丙二酸二乙酯,后撤去冰浴室溫攪拌過夜。反應液用稀鹽酸調pH值為4,抽濾得到中間體G白色固體,為粗品,真空干燥,直接作為下一步反應的原料。收率為85%。
向250m L三頸瓶中加入36 g(0.28mol)上步所得粗品4,6-二羥基-5-氟嘧啶、42.9 g(0.28mol)三氯氧磷,攪拌混合,升溫至95℃回流反應,TLC點板跟蹤,約2.5 h反應完全,將反應液緩慢加入冰水中,有固體析出,加入200m L乙酸乙酯繼續攪拌,分液,水層用乙酸乙酯萃取2次,每次100m L。合并有機相,用飽和碳酸氫鈉溶液和飽和氯化鈉溶液各洗滌有機相1次,無水硫酸鈉干燥,活性炭干燥,旋干后得到淺黃綠色液體,冷凍后析出白色結晶中間體H,收率為78%。
1H NMR(300MHz,CDCl3)δ:8.684(s,1H,H-2)。ESI-MS (m/z):147.0[M-F]-。
1.2.8 氟嘧菌酯的合成
在250m L三頸瓶中投入10.5 g(0.08mol)碳酸鉀,使其溶于30m L乙腈中,加入5.2 g(0.04mol)4,6-二氯-5-氟嘧啶,攪拌并升溫至50℃,維持溫度滴加溶有9 g(0.04mol)(E)-(5,6-二氫-[1,4,2]-二嗪-3-基)-(2-羥基苯基)-甲酮-O-甲基肟的乙腈溶液(20 m L),50℃反應并TLC跟蹤,反應后加入5.39 g(0.04 mol)2-氯苯酚,加熱至60℃攪拌反應,反應10 h后處理。旋干乙腈,加水溶解,乙酸乙酯萃取,合并有機相,無水硫酸鈉干燥,旋干溶劑得淡黃色油狀粗品,用甲醇重結晶得白色固體產物氟嘧菌酯。收率為70%,質量分數為96%。
1H NMR(300 MHz,CDCl3)δ:8.069(s,1H,H-2),7.247-7.515(m,8H,aromatic),4.460(t,2H,CH2),4.145(t,2H,CH2), 3.845(s,3H,CH3)。ESI-MS(m/z):481.1[M+Na]+。
2 結果與討論
2.1 關鍵中間體(E)-(5,6-二氫-[1,4,2]-二嗪-3-基)-(2-羥基苯基)-甲酮-O-甲基肟合成討論
此路線反應條件溫和,后處理簡單,以4-羥基香豆素合成苯并呋喃-2,3-二酮-3-(O-甲基肟)-2-肟(中間體D)的收率高達64%。中間體E采用環氧乙烷進行羥乙基化,不同于報道的2-氯乙醇羥乙基化。2-氯乙醇是劇毒品,購買受到限制,采用環氧乙烷代替,不僅價格更加便宜,而且有利于工業化生產。采用乙醇鈉代替文獻[10]報道的氫氧化鈉合成關鍵中間體F,堿性條件下進行重排,釋放H質子,用堿性更強的乙醇鈉加速了反應進程。
2.2 關鍵中間體4,6-二氯-5-氟嘧啶合成討論
以2-氟丙二酸二乙酯為原料,避免采用KF進行氟代反應。據文獻[11]報道,氟代反應條件苛刻,工業生產存在極大的困難。直接以2-氟丙二酸二乙酯為原料,縮短了工藝路線,提高了收率。2-氟丙二酸二乙酯經由與醋酸甲脒環合、氯代,反應總收率有66%。4,6-二氯-5-氟嘧啶(中間體G)對皮膚有刺激性,在處理時應注意做好防護措施。
3 結論
以4-羥基香豆素為原料經過硝化、堿水解得到中間體2-羥基-2'-硝基苯乙酮;而后與甲氧基胺鹽酸鹽甲胺化,再在堿性條件下成環得到苯并呋喃-2,3-二酮-3-(O-甲基肟)-2-肟;與環氧乙烷發生羥乙基化反應,最后在堿性條件下重排得到關鍵中間體(E)-(5,6-二氫-[1,4,2]-二嗪-3-基)-(2-羥基苯基)-甲酮-O-甲基肟。
另一關鍵中間體以2-氟丙二酸二乙酯為原料,與醋酸甲脒環合,得到4,6-二羥基-5-氟嘧啶,再用三氯氧磷進行氯化反應得到關鍵中間體4,6-二氯-5-氟嘧啶。最后中間體(E)-(5,6-二氫-[1,4,2]-二fffff4嗪-3-基)-(2-羥基苯基)-甲酮-O-甲基肟先與4,6-二氯-5-氟嘧啶醚化,再與2-氯苯酚反應得到目標產物氟嘧菌酯。本合成工藝操作簡便,反應條件溫和,收率較高。
[1]關愛瑩,劉長令.高效殺菌劑氟嘧菌酯 [J].農藥,2003,41(3): 40-42.
[2]柏亞羅.氟嘧菌酯2017年1月專利到期,其市場競爭將更加激烈[DB/OL].(2017-03-21)[2017-04-01].http://www.agroinfo.com. cn/other_detail_3870.htm l.
[3]Heinemann U,Gayer H,Gerdes P,et al.Halogen Pyrim idines and Its Use Thereof as Parasite Abatement Means:US,6103717[P]. 2000-08-15.
[4]Vic P,Rama M H,Avinash SM,etal.Process for Preparing Fluoxastrobin:US,2015011753[P].2016-11-14.
[5]武恩明,孫克,張敏恒.氟嘧菌酯合成方法述評[J].農藥,2014,53 (7):537-541.
[6]郭棟,廖道華,高倩,等.氟嘧菌酯中間體(E)-(5,6-二氫-[1,4,2]-二嗪-3-基)-(2-羥基苯基)-甲酮-O-甲基肟的合成[J].農藥,2014, 53(5):322-324.
[7]Stanislaw O,Jadwiga S,M ieczyslaw M.A Preparative Method for Synthesis of 4,5,6-Trichloropyrim idine [J].Arkivoc,2000(vi): 905-908.
[8]Buckle D R,Cantello B C,Sm ith H.Antiallergic Activity of 4-Hydroxy-3-nitrocoumarins[J].JournalofMedicinalChemistry,1975, 18(4):391-394.
[9]Cushman M,Mathew J.Nitration of the Lithium Potassium Dianionsof Phenolic Alkyl Aryl Ketonesw ith Propyl Nitrate:Synthesis of 1-Nitroalkyl Hydroxyphenyl Ketones[J].Synthetic Communications,1982,5:397-399.
[10]Gayer H,Gallenkamp B,Gerdes P,et al.Process for Preparing 3-(1-Hydroxyphenyl-1-alkoxim inomethyl)Dioxazines:US,6150521 [P].2000-11-21.
[11]Pleschke A,Marhold A.Process for Preparing Ring-fluorinated Aromatics:US,2008182986[P].2008-07-31.
(責任編輯:顧林玲)
Synthesis of Novel Fungicide Fluoxastrobin
LOUWan-qiao,ZHANGDa-yong
(Institute of PharmaceuticalSciences,China PharmaceuticalUniversity,Nanjing 210009,China)
The synthesis of fluoxastrobin was reported.(E)-(5,6-Dihydro-[1,4,2]-dioxazin-3-yl)-(2-hydroxyphenyl)-methanone-O-methyloxime(the intermediate F)was synthesized from 4-hydroxycoumarin via nitration,hydrolysis,cyclization,methylam ination,cyclization,etherification and alkaline rearrangement.4,6-Dichloro-5-fluoropyrimidinewas synthesized from diethyl fluoromalonate via the reactions of cyclization and chlorination.The target product fluoxastrobin was synthesized from the intermediate F,4,6-dichloro-5-fluoropyrim idine and 2-chlorophenol.Based on 4-hydroxycoumarin, the totalyield of the reactionwas17%,the purity of the productwas96%(HPLC).
fluoxastrobin;synthesis;4-hydroxycoumarin;4,6-dichloro-5-fluoropyrim idine
TQ 455.4+7
A
10.3969/j.issn.1671-5284.2017.03.003
2017-02-24;
2017-03-28
婁萬喬(1992—),女,安徽省蕪湖市人,碩士研究生。研究方向:藥物化學。E-mail:2267096203@qq.com

