組織因子監測在預防癌癥病人PICC靜脈血栓中的應用觀察
梁 良,王梅林,王慶華,劉玉霞
?
·科研論著·
組織因子監測在預防癌癥病人PICC靜脈血栓中的應用觀察
梁 良,王梅林,王慶華,劉玉霞
[目的]通過檢測經外周靜脈置入中心靜脈導管(PICC)腫瘤病人血漿中的組織因子、C-反應蛋白(CRP)、白細胞介素-6(IL-6),了解組織因子、CRP,IL-6在PICC置管腫瘤病人血漿中的表達及臨床意義。[方法]收集50例首次置入PICC導管的腫瘤病人,在病人置管前、置管后48 h~72 h、化療后分別抽取清晨空腹血2 mL,用酶聯免疫吸附試驗(ELISA)檢測血清中的組織因子、CRP、IL-6的表達水平;另外收集50例健康人的血清作為對照組。[結果]各時間點組織因子濃度變化差異有統計學意義(P<0.001),且逐漸升高;CRP,IL-6各時間點的濃度變化差異均有統計學意義(P<0.05),且呈升高趨勢。[結論]血漿中組織因子的表達水平可作為PICC置管的腫瘤病人微血栓發生的預測指標,CRP、炎癥因子(IL-6)的表達水平可作為預防微血栓發生的輔助檢測指標。
PICC; 組織因子;CRP;IL-6;微血栓;腫瘤病人
經外周靜脈置入中心靜脈導管(PICC)是一種從外周靜脈導入且末端位于中心靜脈的深靜脈置管技術,現廣泛應用于臨床。但PICC相關的血栓發生率不容忽視,文獻報道PICC相關性血栓的發生率為2%~26%[1]。研究顯示無癥狀PICC相關血栓發生的概率為23%~39%[2-3],而有癥狀的需要拔管的PICC相關血栓發生概率為3.4%~3.9%[4-5]。目前臨床對出現明顯的血栓癥狀時才給予治療,缺乏對早期微血栓形成的診斷及預防。研究發現,組織因子(tissue factor,TF)在微血栓形成中起重要作用。Falati等[6]研究發現:組織因子不僅參與血栓形成的始動過程,而且還參與血栓的不斷增大以及血栓形成的整個過程,所以早期檢測血漿中的組織因子,對預防PICC導管相關性血栓的發生有重要意義。本研究旨在檢測組織因子在留置PICC導管的腫瘤病人血漿中的表達,探討組織因子與炎癥因子的相關性以及與血栓發生的關系,從而為臨床預防微血栓的發生提供依據。
1 資料與方法
1.1 一般資料 本研究通過醫院倫理委員會的同意,病人均簽署知情同意書。選擇2015年8月—2016年5月某三級甲等醫院腫瘤科行PICC置管的病人。入選標準:惡性腫瘤擬行周期性輸注化療藥物需置入PICC導管的病人;年齡18歲~60歲;近期無靜脈血栓發生的病人;來自同一種族;同意參與本研究,并簽署PICC置管和本研究知情同意書。排除標準:凝血功能異常的病人;應用抗凝藥物的病人;伴有各種嚴重性疾病的病人如糖尿病、腎功能不全的病人;置管后<6周拔管的病人。采用非概率便利抽樣法,在資料收集期間將符合入選標準的所有置入PICC導管的腫瘤病人納入研究作為試驗組。試驗組50例,男28例,女22例,年齡(48.90±1.99)歲,置入靜脈均為右側貴要靜脈。其中白血病20例,淋巴瘤10例,肺癌11例,結直腸癌9例。另外,收集50例健康人群為對照組,男26例,女24例,年齡(43.43±2.03)歲,無高血壓、高血脂、高血糖及血栓病史,半月內未使用任何影響血小板功能的藥物,排除可能存在的自身免疫性疾病。兩組年齡、性別差異均無統計學意義(P>0.05)。見表1。

表1 兩組一般資料比較 例(%)
1.2 方法
1.2.1 標本收集和處理 試驗組分別于置入PICC導管前、置管后48 h~72 h、第1次化療后、最后1次化療后抽取空腹靜脈血2 mL,置3.8%枸櫞酸鈉抗凝管中,室溫條件下,2 000 r/min離心15 min,離心2次,得到貧血小板血漿(platelet poor plasma,PPP),吸取上層血漿置于-80 ℃冰箱凍存,2 h內完成標本處理。對照組抽取空腹靜脈血,處理方法同試驗組。
1.2.2 指標檢測 采用酶聯免疫吸附試驗(ELISA)檢測病人血漿中組織因子、C反應蛋白(CRP)、白細胞介素-6(IL-6),所有操作均在標準實驗室條件下進行。購買的ELISA試劑盒為廈門慧嘉科技生物有限公司生產,試劑盒性能:樣品線性回歸與預期濃度相關系數(r)為0.95以上,批內與批間分別小于9%和11%。
2 結果
2.1 試驗組不同時間點組織因子、CRP、IL-6濃度比較 以標準物的濃度為縱坐標,吸光度(OD)值為橫坐標,建立組織因子、CRP、IL-6的標準曲線(見圖1~圖3),將各組樣品吸光度值代入標準曲線,計算組織因子、CRP、IL-6的濃度。組織因子、CRP各時間點的濃度值符合正態分布,采用重復測量方差分析,由于Mauchly球形假設均不成立(P<0.01),使用校正后的Greenhouse-Geisser結果:組織因子各時間點的濃度變化差異有統計學意義(P<0.001),且逐漸升高;CRP各時間點的濃度變化差異有統計學意義(P=0.017),且呈升高趨勢。由于IL-6各時間點的濃度值不符合正態分布,采用非參數檢驗,結果IL-6各時間點的濃度變化差異有統計學意義(P<0.001),且呈升高趨勢。見表2。
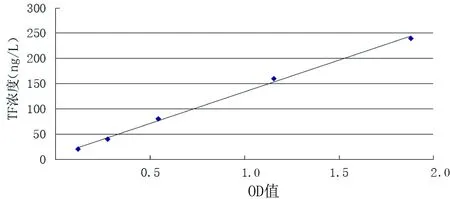
圖1 組織因子濃度標準曲線
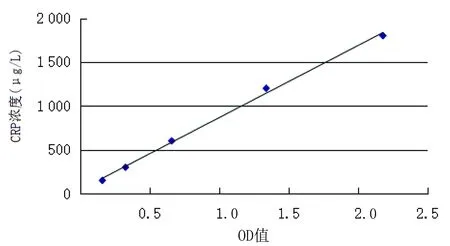
圖2 CRP濃度標準曲線
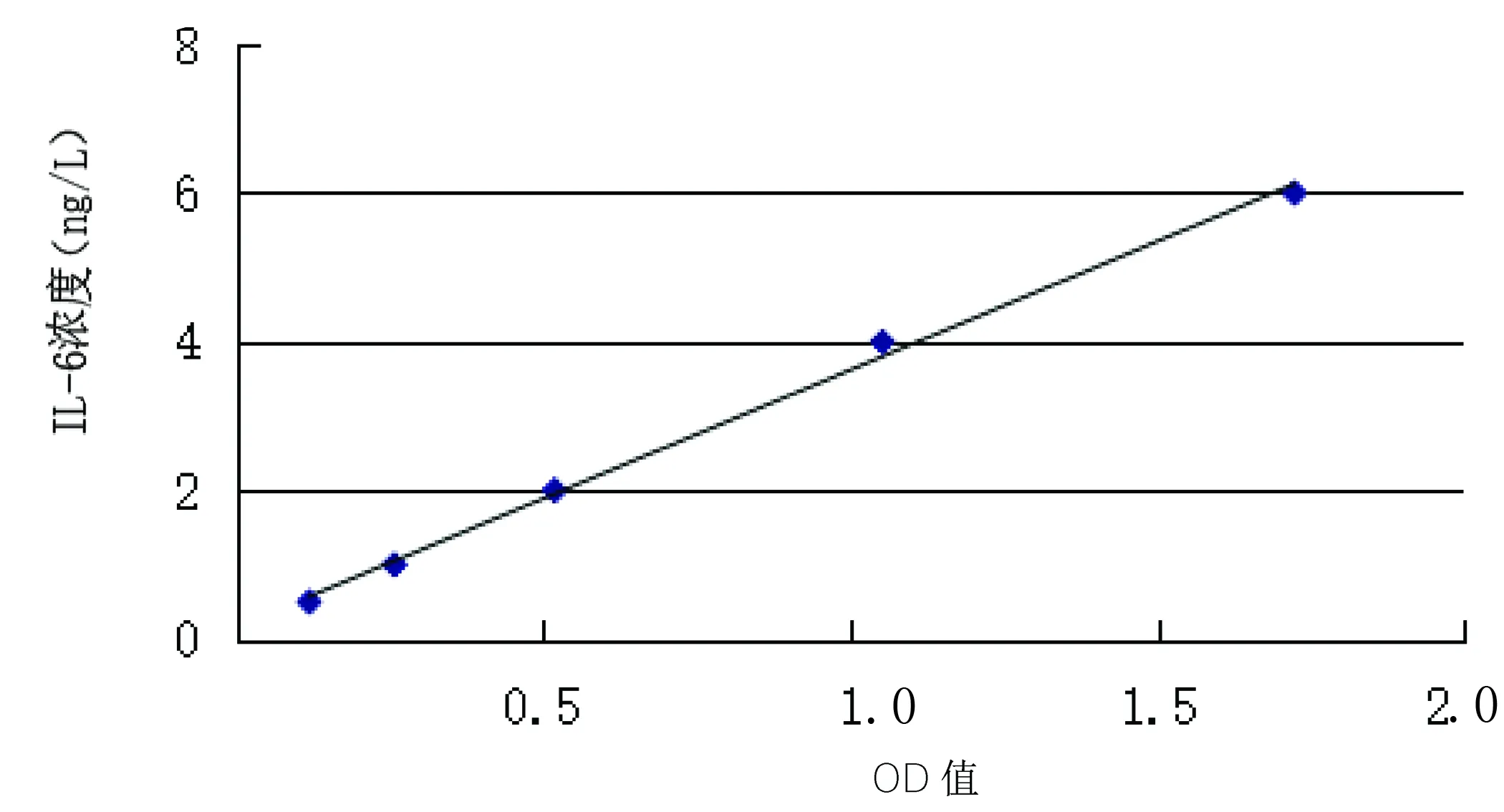
圖3 IL-6濃度標準曲線

表2 置管不同時間點組織因子、CRP、IL-6濃度比較(n=50)
2.2 兩組化療前組織因子、CRP,IL-6濃度比較(見表3)
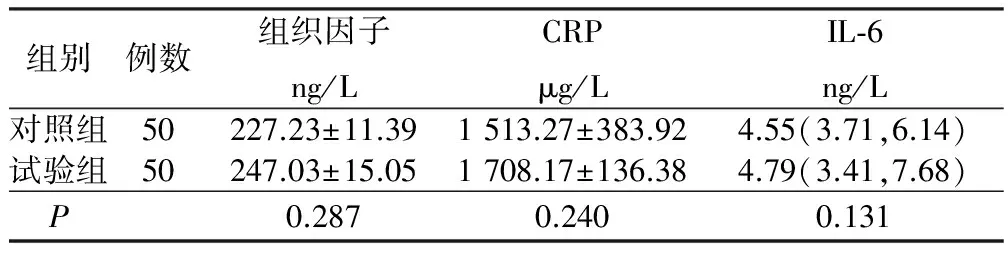
表3 兩組化療前組織因子、CRP,IL-6濃度比較
3 討論
3.1 PICC相關性血栓的檢測方法 PICC置管后形成靜脈血栓,可以發生于導管途徑的任何部位,包括潛靜脈和(或)深靜脈,越靠近心臟的深靜脈血流速度越快,栓子脫落后造成肺栓塞的風險性越大[7]。PICC相關性血栓的發生越來越受到醫護工作者的重視,目前臨床上檢測PICC置管的腫瘤病人微血栓的發生主要手段包括B超、凝血系列、深靜脈造影等。采用彩色多普勒超聲檢查主要發現晚期大范圍的血栓形成,甚至管腔完全栓塞的病例,多數已錯過有效治療時機[8]。深靜脈造影是一種侵入性操作,對技術要求比較高,并不作為PICC相關性靜脈血栓首選的診斷方法[9]。臨床上凝血系列檢查容易受藥物、腫瘤、感染等外在因素的影響,有時檢測結果的針對性差。這些檢測方法的共同特點是預防微血栓發生敏感性差,因此,需要一種在微血栓出現明顯臨床癥狀前的檢測方法。
3.2 組織因子檢測在預防PICC相關性血栓發生中的作用及臨床意義 組織因子在微血栓發生中的預警作用受到越來越多學者的關注。組織因子即凝血因子Ⅲ,是一個由263個氨基酸殘基組成的跨膜單鏈糖蛋白,分子量約為47 kDa,其通過胞外區與其他凝血因子相結合,是凝血級聯反應的啟動子,與血中絲氨酸蛋白酶因子Ⅶ/Ⅶa結合形成復合物,啟動外源性凝血途徑。在正常生理條件下,血管內皮細胞充當著組織因子表達細胞和血液之間的屏障,從而避免激活不必要的凝血因子,然而受到損壞的血管壁會觸發組織因子 介導的凝血功能來保護血管的完整性,防止失血。因此,組織因子是止血的核心和關鍵介質[10]。Uno等[11]的研究發現:在卵巢癌病人中,高表達的組織因子被認為是深靜脈血栓發生的獨立危險因素。Tesselaar等[12]還發現:在發生深靜脈血栓的癌癥病人中,血漿中組織因子微顆粒的水平高于沒有發生深靜脈血栓的癌癥病人。Tesselaar等[12]還發現:在發生轉移的胸腺癌及胰腺癌病人中,組織因子微顆粒水平顯著高于健康人及發生深靜脈血栓但沒有轉移的癌癥病人。癌癥病人發生深靜脈血栓的風險和一般人群相比,增加了4倍,化療將這種風險增加了6倍~7倍[13]。本研究化療后病人血漿中組織因子水平顯著升高,高于化療前,且以化療療程結束后第4次升高最為明顯,差異有統計學意義(P<0.05),化療結束后組織因子升高的數值近似健康人血漿中組織因子的2倍。化療藥物引起癌癥病人發生深靜脈血栓的可能機制為:化療直接破壞血管內皮細胞,或者通過減少內皮細胞產生抗凝蛋白如蛋白C、蛋白S,在化療藥物引起細胞破壞和腫瘤溶解的過程中也引起細胞因子及促凝分子的釋放,如組織因子[14-17]。因此,可以通過檢測血漿中組織因子的含量來判斷PICC置管的腫瘤病人微血栓發生的可能性。這與Data等[18]的研究推論一致,認為腫瘤細胞表達的組織因子水平或促凝顆粒的水平可能作為判斷發生深靜脈血栓的生物標志物。
3.3 組織因子與CRP、IL-6的相關性及在預防PICC相關性血栓中的作用 CRP是一種細胞膜糖蛋白,可通過刺激誘導機體單核細胞分泌組織因子啟動機體凝血瀑布反應產生血栓[19]。CRP還可介導補體活性,經由經典途徑激活補體系統,使血管內膜損傷,促進血栓形成[21]。 Roumen-Klappe等[21]發現急性下肢深靜脈血栓(deep vein thrombosis,DVT)病人血漿CRP等炎癥因子顯著提高;Fox 等[22]觀察到急性靜脈血栓病人血漿 CRP 水平升高 2倍~6 倍:均提示急性靜脈血栓形成過程中伴有機體炎癥反應機制的激活。本研究結果顯示化療后病人血漿中CRP水平顯著升高,高于化療前,且以化療結束后第4次升高最為明顯,差異有統計學意義(P<0.05)。癌癥病人化療前血漿CRP水平略微高于健康人,但二者差異不大(P>0.05),可能與CRP是一種急性期蛋白,在多種機體病理生理狀態下(如腫瘤、創傷和激素替代治療等)均可增高。本研究與楊林等[23]的研究結果一致,通過比較急性下肢深靜脈血栓病人(DVT組)與健康志愿者(對照組)的血漿CRP水平,發現DVT組血清CRP水平明顯高于對照組(n=30,P<0.001),下肢DVT與急性炎癥因子相互影響,CRP可能成為評價DVT預后的指標之一。
IL-6是細胞因子網絡中的一種重要促炎癥性細胞因子,由單核細胞、吞噬細胞、T細胞、B細胞、 血管內皮細胞、成纖維細胞和其他細胞對白細胞介素1 和少量腫瘤壞死因子α起反應時合成的多效應性細胞因子[24]。IL-6主要通過增加組織因子、纖維蛋白原、因子Ⅷ和血管性血友病因子(VwF),激活內皮細胞,增加血小板量和減少抗凝血酶和蛋白S等凝血抑制因子,誘導高凝狀態,增加血栓性疾病發生的機會。Maria等[25]的研究發現:發生DVT的癌癥病人與沒有發生DVT的癌癥病人相比,血漿中IL-6水平顯著升高。本研究結果也顯示:化療后血漿中IL-6水平顯著升高,高于化療前,差異有統計學意義(P<0.05),癌癥病人化療前血漿中的IL-6水平與健康人相比差異不大(P>0.05)。表明血漿中IL-6水平可作為檢測PICC相關性血栓形成的輔助指標之一。
4 小結
在PICC置管的腫瘤病人中,化療后血漿中組織因子的表達水平明顯升高,可作為預防微血栓發生的重要預測指標,化療后血漿中的CRP、IL-6的表達水平也有所升高,可作為檢測微血栓發生的輔助指標。然而,本研究中癌癥病人的化療方案不統一,不同的化療藥物對血漿中的組織因子、炎癥因子表達水平可能產生不同的影響。本研究樣本量小,仍需大量的擁有統一化療方案的大樣本試驗研究加以證實。
[1] 丁紅娟,姚凱.腫瘤病人深靜脈血栓護理研究進展[J].中華現代護理學雜志,2011,8(1):53.
[2] Allen AW,Megargell JL,Brown DB,etal.Venous thrombosis associated with the placement of peripherally inserted central catheters[J].J Vasc Interv Radiol,2000,11(10):1309-1314.
[3] Abdullah BJ,Mohammad N,Sangkar JV,etal.Incidence of upper limb venous thrombosis associated with peripherally inserted central catheters(PICC)[J].Br J Radiol,2005,78(931):596-600.
[4] Grove JR,Pevec WC.Venous thrombosis related to peripherally inserted central catheters[J].J Vasc Interv Radiol ,2000,11(7):837-840.
[5] Walshe LJ,Malak SF,Eagan J,etal.Complication rates among cancer patients with peripherally inserted central catheters[J].J Clin Oncol ,2002,20(15):3276-3281.
[6] Falati S,Gross P,Merrill SG,etal.Real time in CICO imaging of platelets,tissue factor and fibrin during arterial thrombus formation in the mouse[J].Nat Med,2002,8(10):1175-1181.
[7] 趙銳瑋,申屠英琴,陳春芳,等.PICC相關性血栓形成后保留導管患者的觀察與護理[J].中華護理雜志,2012,47(11):1014-1016.
[8] 趙華生,成濤,宋云霞,等.彩色多普勒超聲在深靜脈置管血栓形成定期隨訪中的意義[J].中華醫學超聲雜志,2007,12(6):348-350.
[9] Fallouh N,McGuirk HM,Flanders SA,etal.Peripherally inserted central catheter-associated deep vein thrombosis:a narrative review[J].Am J Med,2015,128(7):722-738.
[10] 盧彥霖,范理宏.組織因子在惡性腫瘤中的研究進展[J].現代腫瘤醫學,2015,23(5):709-712.
[11] Uno K,Homma S,Satoh T,etal.Tissue factor expression as a possible determinant of thromboembolism in ovarian cancer[J].Br J Cancer,2007,96:290-295.
[12] Tesselaar ME,Romijn FP,Van Der Linden IK,etal.Microparticle associated tissue factor activity:a link between cancer and thrombosis?[J].J Thromb Haemost,2007,5(3):520-527.
[13] Kasthuri RS,Taubman MB.Role of tissue factor in cancer[J].Journal of Clinical Oncology,2009,27(29):4834-4838.
[14] Falanga A,Russo L.Epidemiology,risk and outcomes of venous thromboembolism in cancer[J].Hamostaseologie,2012,32(2):115-125.
[15] Furie B,Furie BC.Cancer-associated thrombosis[J].Blood Cells Mol Dis,2006,36(2):177-181.
[16] Haddad TC,Greeno EW.Chemotherapy-induced thrombosis[J].Thromb Res,2006,118(5):555-568.
[17] Sousou T,Khorana AA.New insight into cancer-associated thrombosis[J].Arterioscler Thromb Vasc Biol,2009,29(3):316-320.
[18] Date K,Hall J,Greenman J,etal.Tumour and microparticle tissue factor expression and cancer thrombosis[J].Thromb Res,2013,131(2):109-115.
[19] Paffen E,Vos HL,Bertina RM.C-reactive protein does not directly induce tissue factor in human monocytes[J].Arterioscler Thromb Vasc Biol,2004,24(5):975-981.
[20] 余國膺.CRP不僅是個標志,它直接參與血栓形成[J].嶺南心血管病雜志,2003,9:456.
[21] Roumen-Klappe EM,den Heijer M,van Uum SH,etal.Inflammatory response in the acute phase of deep vein thrombosis[J].J Vasc Surg,2002,35(4):701-706.
[22] Fox EA,Kahn SR.The relationship between inflammation and venous thrombosis:a systematic review of clinical studies[J].Thromb Haemost,2005,94(2):362-365.
[23] 楊林,祁光裕,李艷姿,等.C-反應蛋白與急性下肢深靜脈血栓炎癥反應的研究[J].中國現代普通外科進展,2007,10(5):398-400.
[24] DeLong WG Jr,Born CT.Cytokines in patients with polytrauma[J].Clin Orthop Relat Res,2004,422:57-65.
[25] Maria Teresa Sartori,Alessandro Della Puppa,Andrea Ballin,etal.Circulating microparticles of glial origin and tissue factor bearing in high-grade glioma:a potential prothrombotic role[J].Thromb Haemost,2013,110(2):378-385.
(本文編輯李亞琴)
Application of tissue factor monitoring in prevention of PICC venous thrombosis in cancer patients
Liang Liang,Wang Meilin,Wang Qinghua,etal
(Binzhou Medical University,Shandong 256600 China)
Objective:To understand the expression and clinical significance of tissue factor(TF),C-reaction protein(CRP),and interleukin-6(IL-6) in plasma of cancer patients with peripherally inserted central catheter(PICC) by investigating TF,CRP,and IL-6.Methods:Fifty cancer patients with first PICC catheter were collected as subjects.2 mL morning fasting blood was collected before PICC and 48-72 h after catheter and after chemotherapy.The method of enzyme-linked immunosorbent assay(ELISA) was used to measure the level of TF,CRP,and IL-6.Serum of 50 healthy subjects was collected as the control group.Results:The changes of TF concentration at each time point were statistically significant (P<0.001),and gradually increased.The concentration changes of CRP and IL-6 at different time points were significantly different (P<0.05),and showed an increasing trend.Conclusions:The expression level of TF in plasma could be used as a predictor of microthrombus in cancer patients with PICC and the expression level of CRP and IL-6 could be used as the auxiliary indexes for the prevention of micro-thrombosis.
PICC;tissue factor;CRP;IL-6;microthrombus;cancer patient
2015年度山東省醫藥衛生科技發展計劃項目,編號:2015WS0489。
梁良,碩士研究生在讀,單位:256600,濱州醫學院;王梅林(通訊作者)、劉玉霞單位:256600,濱州醫學院附屬醫院;王慶華單位:256600,濱州醫學院。
信息 梁良,王梅林,王慶華,等.組織因子監測在預防癌癥病人PICC靜脈血栓中的應用觀察[J].護理研究,2017,31(19):2321-2324.
R472.9
A
10.3969/j.issn.1009-6493.2017.19.007
1009-6493(2017)19-2321-04
2016-11-24;
2017-06-15)

