聯合使用固力康和特立帕肽對去卵巢大鼠股骨干骺端骨量、骨強度的影響
謝輝
湖北省荊門市第一人民醫院創傷手足外科,湖北 荊門 448000
骨量嚴格受骨形成和骨吸收的平衡調控,當兩者之間的平衡被打破時就會出現一系列的疾病包括骨質疏松。骨質疏松表現為骨吸收相對增強,漸漸出現骨量減少、骨脆性增加,容易在低能量創傷下出現骨折,這也是這類疾病的主要危害[1]。目前抗骨質疏松藥物主要通過促進骨吸收和/或抑制骨吸收來防治骨質疏松,如甲狀旁腺激素(1-34,PTH),雙膦酸鹽類,然而對于嚴重的骨質疏松, PTH和雙膦酸鹽類聯合使用對患者的骨密度提高并沒有疊加作用,可能是雙膦酸鹽類降低骨轉換和限制了骨重建的進程[2]。組織蛋白酶K是在破骨細胞中高表達的半胱氨酸蛋白酶,對I型膠原的降解起著重要的作用[3]。早期的研究表明組織蛋白酶K抑制劑(KKI),它選擇性抑制骨吸收,對骨形成影響很小[4,5]。綜上所述,我們假設,組織蛋白酶K抑制劑和PTH聯合使用可能有助于增加骨量,骨強度。
本研究通過聯合使用KKI和PTH來治療去卵巢大鼠,觀察其對大鼠股骨干骺端的療效,為臨床上兩者藥物聯合的使用提供實驗基礎。
1 材料和方法
1.1 實驗動物
12 周齡SPF級SD 雌性大鼠50只,體重225~250 g,由上海斯萊克動物公司提供許可證號:(SCXK(滬)2007-0005,合格證號:2007- 000548429)。所有動物在溫度為(24.0±0.5) ℃,濕度為45%~50%, 通風良好的環境下飼養,每周稱體重 1 次。每次手術后前3天所以大鼠給予青霉素肌肉注射(2.5萬U/kg)預防感染。
1.2材料
固力康(日本衛材株式會社);PTH(GIBCO 公司);Micro-CT (SkyScan1176,荷蘭),顯微鏡(ZEISS Axio Imager M1,德國),Image-Pro Plus全自動圖像分析儀(Media Cybernetics,美國),生物力學實驗機(MTS-858,美國)。
1.3 骨質疏松動物模型的建立及治療
50只大鼠隨機分成2組即OVX組(n=45)切除雙側卵巢以建立骨質疏松動物模型和Sham組不切除雙側卵巢建立假手術模型。手術開始前,所有大鼠稱重,根據體重,適量腹腔注射10% 水合氯醛(3 mL/kg)進行麻醉,麻醉成功后,于大鼠背部正中線中下 1/3處作一長約 2 cm 縱行切口,向兩側鈍性分離皮下軟組織,于脊柱旁開0.5 cm處鈍性分開肌肉組織,顯露卵巢脂肪包被組織,輕輕提起卵巢,于輸卵管卵巢交界處絲線結扎,完整摘除雙側卵巢,逐層縫合,關閉創口。正常環境下飼養12 w后各組取5只大鼠處死股骨行骨密度測量儀檢測來檢驗骨質疏松建立模型建立情況。隨后所有的去卵巢(OVX)大鼠隨機的分成4組:OVX組、KKI組、PTH組、PTH+KKI組。KKI組、PTH組、PTH+KKI組大鼠術后給予固力康6 mg/(kg·d)灌胃,特立帕肽60 μg/kg皮下注射,每周3次、固力康6 mg/(kg·d)灌胃加特立帕肽60 μg/kg皮下注射,每周3次直至去卵巢術后12 w。隨后所有大鼠處死取股骨行Micro-CT、骨生物力學、HE組織切片檢測。
1.4 Micro-CT檢測
所有存活的大鼠在術后12 w時處死,完整取下大鼠雙側股骨,剔除周圍軟組織, 生理鹽水沖洗后,采用10%多聚甲醛固定用于Micro-CT 檢測。掃描條件為:圖像矩陣為2048 ×2048, 整合時間為 200 ms,能量/強度為70 kVp、 114 μA、 8 W。以 0°旋轉, 進行掃描。掃描完成后, 選取生長板遠端1.0 mm、 層厚2.0 mm的骨組織為松質骨感興趣區域(region of interest,ROI)進行三維重組, 最低閾值為 160 提取圖像信息。獲得大鼠股骨感興趣區域骨微結構參數骨體積分數 (bone volume/total volume,BV/TV)、骨小梁厚度(trabecular thickness,Tb.Th)、骨小梁數量(trabeculae number,Tb.N)、 骨小梁分離度(trabecular spacing,Tb.Sp)、連接密度(connective density,Conn.D.)及骨密度(BMD)。
1.5 HE組織切片
待所有股骨經過Micro-CT檢測后,所有標本用4%多聚甲醛固定,梯度酒精脫水,甲基丙烯酸甲酯包埋。包埋塊修整后置于硬組織切片機沿脛骨縱軸冠狀面切片,清洗打磨拋光,切片最終厚度約為30~40 μm,切片在熒光顯微鏡及光鏡下觀察。然后將標本放置在EDTA 脫鈣液中浸泡,每3~4 d換液1 次,連續脫鈣4 w,X 線檢測是否脫鈣完全,然后充分水洗,乙醇梯度脫水,二甲苯透明,石蠟包埋,切片,HE染色,Olympus BX5l多功能顯微鏡下觀察股骨干骺端骨生長情況,骨小梁的微觀結構及分布。
1.6 生物力學測定
取右側股骨,將其置于MTS-858型生物力學實驗機上,支點跨距17 mm,中點為加壓點,加載速度為 2 mm/min,計算機記錄載荷-位移曲線,根據曲線計算最大載荷和剛度。
1.7 統計學處理
2 結果
2.1 手術對大鼠的影響
至實驗截止時間,有2只大鼠由于手術不當、麻醉不當和傷口感染死亡,它們都屬于OVX組,最終共有38只大鼠進入最終試驗結果評估。術后12 w時兩組大鼠股骨的骨密度變化由骨密度測量儀檢測所得,Sham組大鼠的股骨骨密度為241.21±31.78 (mg/cm2),而OVX組大鼠股骨骨密度為171.24±28.31 (mg/cm2)。相對Sham組,OVX組大鼠的骨密度下降40.93%(P<0.05),結果表明骨質疏松模型建立是成功的。
2.2 股骨骨密度的改變
藥物治療12 w時,大鼠股骨干骺端通過Micro-CT掃描后通過內置軟件所得的各組股骨骨密度如表1所示;相對于OVX組,KKI、PTH、PTH+KKI各組股骨骨密度分別增加了19.09%、28.62%、39.26%,有明顯的統計學意義(P<0.05)。從結果可以發現相對于單獨使用PTH和KKI,聯合使用兩者對去卵巢大鼠股骨骨密度提高更明顯。
注:與OVX組比較,*P<0.05;與SIM組比較,#P<0.05;與PTH組比較,&P<0.05
2.3 Micro- CT 三維重建分析及骨微觀參數
通過Micro- CT對感興趣區域進行三維重建,重建的結果如圖1所示,通過內置軟件計算的骨微觀參數如表1所示。通過觀察圖1可以明顯發現:相對OVX組而言,KKI、PTH、PTH+KKI各組的骨小梁數量明顯增多,而且骨小梁聯系緊密,骨小梁更粗。骨微觀參數更加明確的表明PTH+KKI組有最高的BV/TV、Tb.Th、Tb.N、Conn.D和最低Tb.Sp,而OVX組有最高的Tb.Sp和最低BV/TV、Tb.Th、Tb.N、Conn.D。和OVX組比較,KKI、PTH、PTH+KKI各組骨微觀參數有明顯的統計學意義(P<0.05),從結果可以發現相對于單獨使用PTH和KKI,聯合使用兩者對去卵巢大鼠股骨骨量提高更明顯。
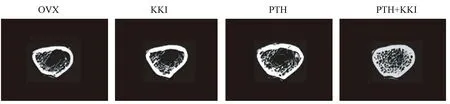
圖1 藥物治療12 w時各組大鼠股骨干骺端Micro-CT三維重建結果Fig.1 3D reconstruction of micro-CT images in the metaphysis of the left femurs of the rats in each group after 12-week treatment
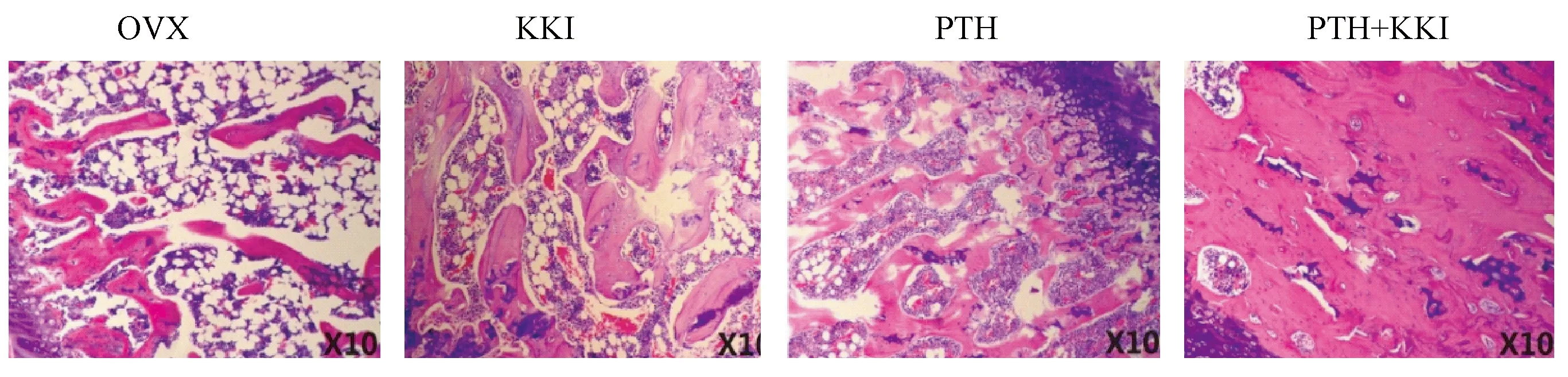
圖2 藥物治療12 w時各組大鼠股骨干骺端HE組織切片結果Fig.2 The results of HE staining of the histological slices in the metaphysis of the left femurs of the rats in each group after 12-week treatment
2.4 HE組織切片結果
大鼠左側股骨切片經過HE染色結果如圖2所示,結果表明KKI、PTH、PTH+KKI各組干骺端的骨量遠遠大于OVX組,且骨小梁之間聯系緊密,排列有規律;而OVX組骨小梁稀疏,且骨小梁纖細,部分骨小梁出現斷裂,這表明KKI和PTH明顯增加股骨干骺端骨量,HE切片的觀察結果進一步證實Micro-CT的結果。
2.5 骨生物力學結果
股骨三點彎曲試驗中,KKI、PTH、PTH+KKI組最大載荷、剛度均高于OVX組PTH+KKI組有著最大的載荷、剛度值,且各組之間比較有明顯的統計學意義(P<0.05),見表2。

表2 藥物治療12 w時各組大鼠股骨(右)三點彎曲試驗的結果Table 2 The 3-point bending test results of the right femurs of the rats in each group after 12-week treatment
注:與OVX組比較,*P<0.05;與SIM組比較,#P<0.05;與PTH組比較,&:P<0.05
3 討論
本次實驗中使用雌性SD大鼠經過去卵巢12 w來建立骨質疏松模型,經過全身使用PTH及KKI來改變去卵巢大鼠的骨代謝,藥物治療12 w后處死大鼠取下雙側股骨行Micro-CT、HE切片及骨生物力學檢測,實驗的結果表明相對于單獨使用PTH及KKI,聯合使用兩者可以明顯增加股骨BMD,提高股骨干骺端微觀參數,保護骨小梁的質和量,增加股骨最大載荷及剛度;這暗示聯合使用PTH及KKI對骨質疏松的治療有疊加作用。
骨質疏松癥是一種以骨量降低,骨組織顯微結構發生退變,導致骨脆性增加,骨強度下降,易導致骨折的骨骼疾病[6]。隨著世界老年化進展,骨質疏松的患病率越來越高,骨質疏松相關骨折已經成為很大的世界性難題,防治骨質疏松對臨床醫生來說是一項巨大的挑戰[7]。雖然雙膦酸鹽類、地諾單抗、雌激素在治療骨質疏松都有不錯的療效,但是常常會出現一些不利因素影響其臨床應用,如雙膦酸鹽類人體吸收率低,不適用于有血栓栓塞性疾病或腎功能不全者[8];地諾單抗使用時出現下頜骨壞死率[9];雌激素會加大婦科腫瘤的發病率。其嚴重后果是發生骨折及骨折后難以愈合, 嚴重影響患者的生活質量。為了取得最大療效, 人們尋求聯合治療或序貫治療的方法防治骨質疏松癥。間歇性小劑量使用PTH具有促進骨合成代謝作用,并可改善骨微結構,增加骨量。本研究表明間歇性小劑量使用PTH確實具有提高骨質疏松狀態下骨密度,增加骨量。
本實驗中使用KKI是一種四烯甲萘醌合成物,它可以有效抑制組織蛋白酶K形成,促進骨形成作用,同時抑制破骨形成,可以有效提高血清骨鈣素濃度[10]。我們發現聯合使用PTH和KKI可以明顯的增加股骨骨量及骨強度,這說明它們同時使用有互相促進作用。具體的機制尚不清楚,這可能和兩者的促進骨形成的機制有關。PTH具有強烈的促進成骨作用和破骨細胞有偶聯系性,而KKI抑制破骨細胞的作用并不影響PTH成骨作用,這與PTH和雙膦酸鹽類聯合使用不同,雙膦酸鹽類抑制破骨細胞的活性的同時也會影響到PTH的成骨效果;而KKI抑制骨吸收且不影響到破骨細胞的數目,增加骨形成[11,12],因此并不會影響PTH的作用,這種結果導致兩者聯合使用有疊加作用。
本次試驗也有其局限性,首先實驗大鼠數量有限,且時間較短,12w之后動物骨質疏松的具體情況不知。我們沒有進一步進行機制探索,但是這次試驗從體外很好的證實 PTH 聯合 KKI可以協同防治骨質疏松,為其在臨床藥物方面提供了可能性。但目前動物實驗中用于治療骨質疏松藥物的效果較好,但是在人體這個復雜環境,且聯合使用PTH 和KKI治療骨質疏松會進一步增加治療成本,臨床上具體實施仍需進一步研究。

