日本鰻鱺的C-型和G-型溶菌酶研究
楊 勇黃 貝黃文樹段明珠張芳芳聶 品
(1.集美大學水產學院, 廈門 361021; 2.中國科學院水生生物研究所淡水生態與生物技術國家重點實驗室, 武漢 430072)
日本鰻鱺的C-型和G-型溶菌酶研究
楊 勇1,2黃 貝1黃文樹1段明珠1張芳芳1聶 品2
(1.集美大學水產學院, 廈門 361021; 2.中國科學院水生生物研究所淡水生態與生物技術國家重點實驗室, 武漢 430072)
研究以日本鰻鱺(Anguilla japonica Temminck et Schlegel)為研究對象, 根據其基因組數據庫, 預測并擴增出2類, 共5個溶菌酶基因, 包括1個C-型溶菌酶和4個G-型溶菌酶, 分別命名為AJLysC、AJLysG1、AJLysG2、AJLysG3和AJLysG4。它們的cDNA全長分別為811、749、1352、1175和733 bp, 編碼143、193、185、185和187個氨基酸。SignalP預測表明, AJLysC和AJLysG1的N-端分別包括15和19氨基酸的信號肽, 另外3種溶菌酶沒有信號肽。基因組分析顯示, AJLysC、AJLysG2、AJLysG3和AJLysG4的基因結構與其他魚類的同類溶菌酶的基因結構相似, C-型溶菌酶具有4個外顯子, G-型則具有5個。但是, AJLysG1的基因結構與其他魚類G-型溶菌酶不同, 具有6個外顯子, 與其他魚類溶菌酶的蛋白序列比較, 發現AJLysG1缺失其他G-型溶菌酶存在的第2個酶活性位點氨基酸, 即天冬氨酸Asp。AJLysC與其他很多物種的C-型溶菌酶具有較高的同一性, 如與牙鲆的同一性為72.7%。G-型溶菌酶中AJLysG2、AJLysG3、AJLysG4彼此之間以及與其他物種G-型溶菌酶的同一性相對較高; 而AJLysG1與其他物種以及與其他3種G-型溶菌酶的同一性均不高, 且都在50%以下。組織表達分析顯示, 所有5個溶菌酶基因在12種檢測的組織中均有表達。C-型溶菌酶在胃及免疫相關組織的表達量較高; G-型溶菌酶在各組織/器官中的表達則差異較大, AJLysG1在皮膚和肌肉中的表達量最高, AJLysG2在免疫組織/器官如血液、頭腎、體腎和鰓中表達量較高。經遲緩愛德華氏菌(Edwardsiella tarda)刺激48h后, 這5個溶菌酶基因在組織/器官中的表達量均有上調, 其中在血液、腸道和頭腎等的上調較為顯著。此外, 研究嘗試重組表達這些抗菌肽, 獲得了AJLysG2、AJLysG3和AJLysG4基因在鯉上皮瘤細胞(Epithelioma papulosum cyprinid, EPC)細胞中的表達, 重組蛋白表現出對溶壁微球菌(Micrococcus lysodeikticus)生長的明顯抑制作用。文章較全面地研究了日本鰻鱺溶菌酶基因的組成和類型及其表達變化, 并重組表達了部分基因, 這為進一步研究這些溶菌酶的功能, 特別是對病原微生物的作用奠定了基礎。
日本鰻鱺; 溶菌酶; 表達; 重組蛋白; 抑菌活性
溶菌酶廣泛存在于有機體, 能水解細菌的細胞壁肽聚糖中由N-乙酰葡萄糖胺(N-acetylglucosamine)和N-乙酰胞壁酸(N-acetylmuramic acid)形成的β-1,4糖苷鍵, 造成細胞壁裂解, 引起細菌死亡, 從而在機體的防御系統中起著重要作用[1]。脊椎動物中有C-型(Chicken-type)和G-型(Goose-type)兩種溶菌酶[2,3]。C-型溶菌酶是最早發現并且研究最多的一類溶菌酶。最早被測序的雞蛋蛋白溶菌酶和人的溶菌酶都是C-型溶菌酶, 它們也是應用較廣的溶菌酶[4—6]。魚類C-型溶菌酶的研究涉及許多種類,包括一些重要的經濟種類和模式種類, 如羅非魚(Oreochromis niloticus Linnaeus)、虹鱒(Oncorhynchus mykiss Walbaum)、牙鲆(Paralichthys olivaceus Temminck et Schlegel)、鯉(Cyprinus carpio L.)、紅鰭東方鲀(Fugu rubripes Temminck et Schlegel)、斑馬魚(Danio rerio Buchanan-Hamilton)等[7—11]。所有已發現的C-型溶菌酶均含有2個酶活性位點, 即第35個氨基酸谷氨酸(Glu)和第52個氨基酸天冬氨酸(Asp); 同時也存在8個保守的半胱氨酸(Cys), 這些半胱氨酸能形成4個二硫鍵, 維持蛋白結構的穩定[12,13]。C-型溶菌酶的基因結構較為保守, 脊椎動物中已報道的C-型溶菌酶基因均為4個外顯子和3個內含子的結構, 其中第一個外顯子編碼的蛋白質含有信號肽[14]。
G-型溶菌酶最初由Canfield等[15]于1967年在鵝蛋蛋白中發現, 因此命名為G-型溶菌酶。之后, 在很多其他鳥類中也報道了G-型溶菌酶, 如鴕鳥(Struthio camelus L.)、黑天鵝(Cygnus atratus L.)和雞(Gallus domesticus L.)等[16—19]。然而, 直到2001年才在魚類中報道了G-型溶菌酶[2]。目前, 已在很多魚類中發現了G-型溶菌酶的存在, 包括斜帶石斑魚(Epinephelus coioides Temminck et Schlegel)、鱖(Siniperca chuatsi Basilewsky)、大西洋鮭(Salmo salar L.)、大西洋鱈(Gadus morhua L.)等[20—23]。目前, 對于哺乳動物G-型溶菌酶的研究相對較少。2003年, Irwin等[24]通過對基因組的分析, 首次在人(Homo sapiens L.)、鼠(Mus musculus L.)等物種中發現了G-型溶菌酶基因。在不同物種中, G-型溶菌酶外顯子的數目差異較大。人的G-型溶菌酶基因有7個外顯子[24]; 其他哺乳動物以及鳥類的G-型溶菌酶均為6個外顯子, 這些溶菌酶均含有信號肽[24,25]。在魚類中, 已經報道的G型溶菌酶基因均為5個外顯子, 并且很多魚類的G-型溶菌酶沒有信號肽, 因此曾認為魚類G-型溶菌酶基因較少的外顯子數目是造成魚類溶菌酶中沒有信號肽的原因[24]。然而, 在大西洋鮭和大西洋鱈中的G-型溶菌酶盡管只有5個外顯子, 但經過變換轉錄起始位點(Transcription start site)可以影響其是否分泌到胞外[22,23]。
魚類C-型溶菌酶和G-型溶菌酶在魚體的所有組織/器官中都有表達, 如草魚(Ctenopharyngodon idella Valenciennes)[26]和菱鲆(Scophthalmus rhombus L.)[12]的肝臟、頭腎、腎、脾、皮膚、肌肉、心臟、腦、腸道和鰓等組織/器官中均有溶菌酶基因的表達。經過病原或病原相關分子刺激后, 這兩類溶菌酶基因在檢測的組織/器官中出現上調表達[12,26]。已有的研究顯示, 魚類的溶菌酶對一些病原細菌具有明顯的抑制作用。例如, 草魚的C-型溶菌酶和G-型溶菌酶蛋白對溶壁微球菌(Micrococcus lysodeikticus)、大腸桿菌(Escherichia coli)及嗜水氣單胞菌(Aeromonas hydrophila)、副溶血弧菌(Vibrio parahaemolyticus)、遲緩愛德華氏菌(Edwardsiella tarda)、銅綠假單胞菌(Pseudomonas aeruginosa)等細菌均表現出溶菌活性[26]。重組的鱖G-型溶菌酶對溶壁微球菌的生長有明顯的抑制作用[21]。斜帶石斑魚的G-型溶菌酶對大腸桿菌、溶藻弧菌(V.alginolyticus)、創傷弧菌(V.vulnificus)、副溶血弧菌、嗜水氣單胞菌、熒光假單胞菌(P.fluorescens)等多種病原菌均有溶菌活性[20]。
日本鰻鱺(Anguilla japonica)屬于鰻鱺目(Anguilliformes)、鰻鱺科(Anguillidae), 是重要的經濟種類, 也是我國重要的水產養殖對象[27]。目前, 我國東南沿海分布的日本鰻鱺的苗種捕撈量逐年降低, 資源量不斷減少, 無法滿足養殖生產需求[28]。在日本, 日本鰻鱺已被列為國際瀕危物種紅色目錄(IUCN Red List of Threatened Species)[29]。我國鰻鱺養殖業也曾一度依賴進口的歐洲鰻鱺(Anguilla anguilla L.), 但其也被列為國際瀕危物種紅色目錄,其苗種的出口受到了嚴格限制[30]。因此, 研究日本鰻鱺的生物學和養殖對于其種質資源保護、養殖生產和相關產業的發展都有重要意義。本研究通過分析日本鰻鱺的基因組數據庫, 發現了5個溶菌酶基因, 在此基礎上克隆了它們的基因序列, 揭示了它們的表達變化規律, 并在魚類細胞系中表達了其中的3個溶菌酶基因, 為進一步研究這些溶菌酶的功能奠定了基礎。
1 材料與方法
1.1 目的基因的部分序列
根據日本鰻鱺基因組數據, 以其他魚類的C-型和G-型溶菌酶基因作為參照, 用Blast軟件進行分析, 獲得日本鰻鱺可能的C-型和G-型溶菌酶基因的部分序列。
1.2 擴增目的基因cDNA全長
為確認預測的目的基因是否正確以及獲得目的基因完整的cDNA全長序列, 本研究根據SMARTTMRACE cDNA Amplification Kit (Clontech)的說明,以預測的基因序列為模板設計并合成引物, 并對目的基因的3′及5′端分別進行擴增。實驗用魚取自于集美大學海水養殖場, 體重約250 g。經暫養后, 采集頭腎及肝臟, 采用Trizol?Reagent (Invitrogen)提取總RNA, 然后采用SMARTTMRACE cDNA Amplification Kit合成模板。基因的擴增采用槽式PCR,即第一輪采用降落PCR (Touchdown PCR)經UPM (Universal Primer Mix)和外引物進行擴增; 第二輪采用常規PCR經NUP (Nested Universal Primer)和內引物進行擴增。其中, AJLysC、AJLysG2、AJLysG3和AJLysG4使用Ex taq (TaKaRa)進行擴增; AJLysG1采用擴增性能較好的Advantage 2(Clontech)進行實驗。PCR擴增產物經1%瓊脂糖凝膠電泳后切膠回收。回收產物連接至pMD19-T (TaKaRa), 然后轉化至大腸桿菌(Escherichia coli)TOP10感受態細胞;轉化細菌的陽性克隆被送測序公司(金斯瑞生物科技或生工生物)進行測序。將5′-RACE和3′-RACE測序結果拼接, 即獲得cDNA序列全長。本研究所有使用的引物見表 1。
1.3 目的基因DNA的擴增
為研究分析目的基因, 根據所獲得的cDNA序列設計并合成了擴增DNA全長的引物(表 1)。采用QIAamp DNA Mini Kit (QIAGEN)從肌肉組織中純化DNA, 目的基因DNA使用LA Taq (TaKaRa)進行擴增, 經測序獲DNA序列。
1.4 生物信息學分析
目的基因的預測采用本地Blast (blast-2.2.22)。引物的設計采用Primer Premier 5.0和6.0。序列經查找重疊區域而拼接完整后采用ORF Finder (http:// www.ncbi.nlm.nih.gov/gorf/gorf.htmL)查找開放閱讀框。使用ExPASy網站(http://www.expasy.org)中的Translate軟件推導氨基酸序列。信號肽的分析采用SignalP 4.1 Server (http://www.cbs.dtu.dk/services/SignalP/)。推導出的蛋白的參數分析采用Ex-PASy網站中ProtParam tool軟件進行分析。序列同源性比對分析采用軟件MatGat 2.02[31]。蛋白質二硫鍵的預測采用Predict Protein (https://www.predictprotein.org/)。進化樹使用MEGA 5.2經鄰接法(Neighbor-Joining, NJ)構建, bootstraps設置為1000。基因結構采用Spidey (http://www.ncbi.nlm.nih.gov/IEB/Research/Ostell/Spidey/spideyweb.cgi)進行分析。
1.5 溶菌酶基因在正常魚和受病原刺激魚體的表達分析
使用大豆酪蛋白消化液培養基(Tryptic soytone broth medium, TSB), 30℃培養遲緩愛德華氏菌, 待菌液渾濁后, 測定OD540值(Spectrumlab 721N型, 上海精密科學儀器有限公司)。按照比例使用TSB將E.tarda梯度稀釋, 將稀釋后的菌液涂布在大豆瓊脂培養基(Tryptic soy agar, TSA)平板上, 生化培養箱中30℃培養過夜, 第2天對菌落進行計數。經計數分析顯示, 當OD540為0.5時, 每毫升菌液對應的細菌菌落總數約為2.5×108。2200×g離心15min回收菌體, 棄培養基后用合適體積的PBS緩沖液(Phosphate buffer saline, pH 7.4)懸浮菌體; 將菌體再次2200×g離心15min, 更換PBS, 將菌液濃度調節至1.0×107cfu/mL用于感染魚體。

表 1 本研究使用的引物Tab.1 Primers used in the current study
將經過暫養2周的日本鰻鱺(購自廣東省江門市, 個體體質量約為500 g)隨機分成4組: 空白組、對照組和兩個刺激組, 每組均為4條魚。空白組不注射, 對照組每條魚腹腔注射1.0 mL滅菌后的PBS緩沖液; 刺激組每條魚注射1 mL濃度調節至1.0×107cfu/mL的遲緩愛德華氏菌菌液。對照組在注射PBS緩沖液后24h采樣, 刺激組分別在注射菌液24h和48h后采樣。采樣時, 將日本鰻鱺經丁香酚醇溶液麻醉, 分別采集血液、腸道、頭腎、體腎、胃、肝、脾、鰓、腦、心、皮膚和肌肉, 共計12個組織/器官。然后, 將樣品浸入冰上預冷的1 mL Trizol?Reagent中, 提取樣品總RNA或者將樣品保存于超低溫冰箱中備用。
提取總RNA后, 用Nano Drop 2000(Thermo)測定濃度, 取總RNA 500—1000 ng使用DNaseⅠ(Thermo)處理, 然后用M-MuLV酶逆轉錄試劑盒(Thermo)合成cDNA。為降低或消除定量分析時提取總RNA過程中殘留的基因組DNA的影響, 實驗引物采用跨內含子的方法設計, 采用定量分析引物(表 1)擴增目的基因, 連接至pMD18-T, 然后測序確認。將測序正確的克隆擴大培養, 提取質粒(Plasmid Mini Kit, Omega), 使用分光光度計(NanoDrop 2000, Thermo)測定質粒的濃度。質粒拷貝數的計算參照已報道的方法[32]。將測定濃度后的質粒按照10倍梯度稀釋, 然后使用Bio-rad公司定量PCR系統(CFX96TMReal-Time System)構建標準曲線。實時熒光定量分析(Real-time quantitative reverse transcription-PCR, rt-qPCR)的反應體系為20 μL, 包括iQTM SYBR Green Super Mix (2×) 10 μL, 正向引物(10 μmol/L) 1 μL, 反向引物(10 μmol/L) 1 μL, 模板1 μL, 和ddH2O 7 μL。rt-qPCR的程序如下: 預變性95℃ 3min; 95℃變性10s, 60℃退火20s, 72℃延伸20s, 80℃讀板5s, 共41個循環。

1.6 溶菌酶基因的重組表達與重組蛋白的活性分析
分別使用EcoRⅠ/BamHⅠ和BamHⅠ/Hind Ⅲ酶切位點將AJLysG2、AJLysG3和AJLysG4的開放閱讀框序列(去掉終止密碼子及信號肽編碼序列)連入pcDNATM3.1/myc-His(-) A (Invitrogen)真核表達質粒。
采用鯉上皮瘤細胞(Epithelioma papulosum cyprinid, EPC)進行重組表達。利用M199培養基+ 10%胎牛血清(Fetal bovine serum, FBS), 于28℃在CO2培養箱培養。將構建成功的pcDNA3.1-AJLysG2、-AJLysG3、-AJLysG4以及pcDNA3.1空載體質粒分別使用Lipofectamine 2000(Invitrogen)轉染75 cm2培養瓶中的EPC細胞。轉染24h后, 去掉上清培養基并用含有蛋白酶抑制劑cocktail (Roche)的RIPA細胞裂解液裂解細胞。裂解產物經12000×g, 4℃離心10min, 獲取上清液用于后續實驗。
轉染后的EPC細胞裂解產物上清液經SDSPAGE電泳后轉PVDF膜(孔徑0.2 μm), 用含有3%脫脂奶粉的TBS緩沖液常溫封閉1h, 然后使用含鼠抗Myc單抗(Sigma, 1鯰2000)及1.5%脫脂牛奶的TBS緩沖液4℃孵育過夜。洗膜后, 二抗(羊抗鼠IgG-HP多抗, Pierce, 1鯰5000)孵育1h。TBST緩沖液洗膜后, 在化學發光儀(Bio-Rad)中顯色和拍照。根據蛋白標準品(MagicMarkTMXP Western Protein Standard, Novex)估測目的蛋白濃度。
溶菌酶抑菌實驗參照Hikima等[2]以及Sun等[21]的方法進行。磷酸鹽緩沖液(pH 6.5)、TSB培養基和瓊脂粉, 以100鯰3鯰1 (v鯰w鯰w)比例混合滅菌。滅菌后, 固體培養基在50℃水浴保溫。TSB液體培養基培養溶壁微球菌, 當菌液OD600為0.4時, 以1鯰200 (v鯰v)的比例將菌液混入50℃固體培養基中, 倒在9 cm平板上。培養基凝固后打孔并分別加入轉染pcDNA3.1-AJLysG2、-AJLysG3、-AJLysG4和pcDNA3.1空載體質粒的EPC細胞裂解產物上清液以及雞蛋蛋白溶菌酶(Hen egg white lysozyme, HEWL)。然后將平板置于28℃培養約18h。觀察樣品在平板上產生的溶菌環的大小并拍照記錄。
2 結果
2.1 C-型和G-型溶菌酶基因的cDNA和DNA序列分析
通過分析基因組數據庫以及PCR擴增, 鑒定了日本鰻鱺的1個C-型和4個G-型溶菌酶基因, 將它們分別命名為AJLysC、AJLysG1、AJLysG2、AJLysG3和AJLysG4。它們的cDNA全長分別為811、749、1352、1175和733 bp, 編碼143、193、185、185和187個氨基酸。SignalP預測表明, AJLysC和AJLysG1的N-端含有信號肽, 成熟肽分別為128和174氨基酸; 另外3種溶菌酶沒有信號肽(表 2)。在這些基因的3′端非編碼區, 其cDNA序列均有多腺苷酸化信號(AATAAA), 其中AJLysG1和AJLysG2在ploy A之前分別含有1和4個不穩定信號(ATTTA)(未顯示, 可見GenBank序列)。
氨基酸序列比對結果顯示, AJLysC與菱鲆的同一性最高, 為76.9%, 其次是牙鲆、紅鰭東方鲀和塞內加爾鰨, 分別為72.7%、69.2%和67.8%, 與鯉和草魚的比較低, 只有38.6%和37.4%。G-型溶菌酶中AJLysG2、AJLysG3和AJLysG4之間的同一性相對較高, 在50%以上; 而AJLysG1與其他溶菌酶的則較低, 均在50%以下(表 3)。與其他魚類的相對應的溶菌酶序列比較發現, 日本鰻鱺的C-型溶菌酶和其他魚類的C-型溶菌酶都有信號肽, 有8個保守的半胱氨酸和2個保守的催化殘基Glu35和Asp52; 這8個半胱氨酸能形成4個二硫鍵(圖 1)。日本鰻鱺的G-型溶菌酶AJLysG2、AJLysG3和AJLysG4均具有3個保守的催化殘基, 即Glu73、Asp86和Asp97, 但AJLysG1的第二個催化殘基, 即Asp86缺失(圖 2)。此外, AJLysG1存在2個半胱氨酸, 但預測結果顯示,這2個半胱氨酸并不形成二硫鍵(圖中未顯示)。
本研究采用鄰接法構建了系統進化樹(圖 3)。從圖中可以看出, 日本鰻鱺的AJLysC與其他脊椎動物的C-型溶菌酶聚為一大支。魚類的G-型溶菌酶聚為一大支, 而日本鰻鱺的AJLysG2、AJLysG3、AJLysG4與其他硬骨魚類G-型溶菌酶聚為一支, 再與AJLysG1聚在一起。
2.2 C-型和G-型溶菌酶的基因結構
日本鰻鱺的5個溶菌酶基因的基因組結構信息見圖 4。這5個溶菌酶基因的基因組結構均符合經典的剪切模式(GT/內含子/AG)。AJLysC基因組為1878 bp, 含有4個外顯子和3個內含子。AJLysG1基因組長3733 bp, 含有6個外顯子, 5個內含子。AJLys-G2、AJLysG3和AJLysG4的基因組長度分別為2357、2108和2725 bp, 這3個G-型溶菌酶基因和其他魚類同類溶菌酶基因一樣, 均含5個外顯子和4個內含子,并且對應的外顯子堿基數目接近, 特別是AJLysG3和AJLysG4, 其對應的外顯子的數目完全相同。
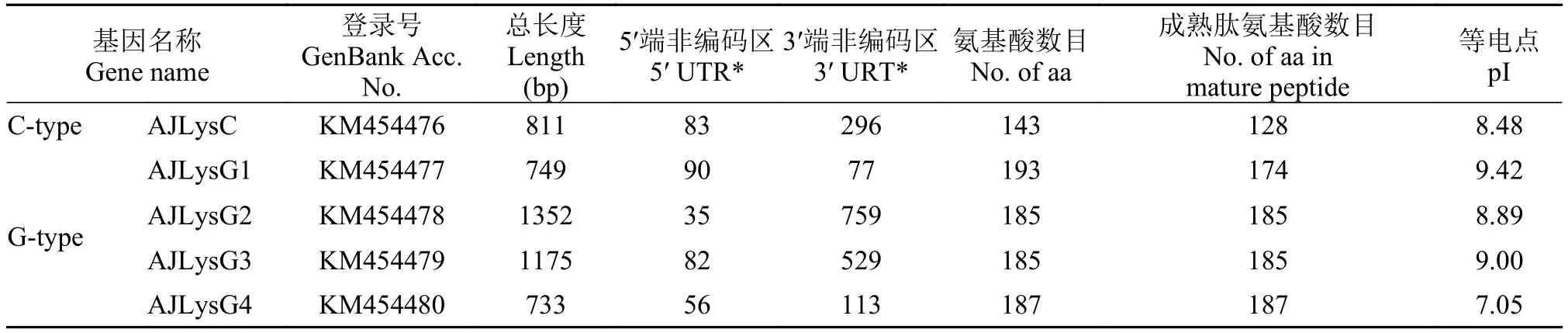
表 2 日本鰻鱺溶菌酶基因cDNA序列及其氨基酸序列Tab.2 The cDNA sequences and deduced amino acids of lysozyme genes in the Japanese eel
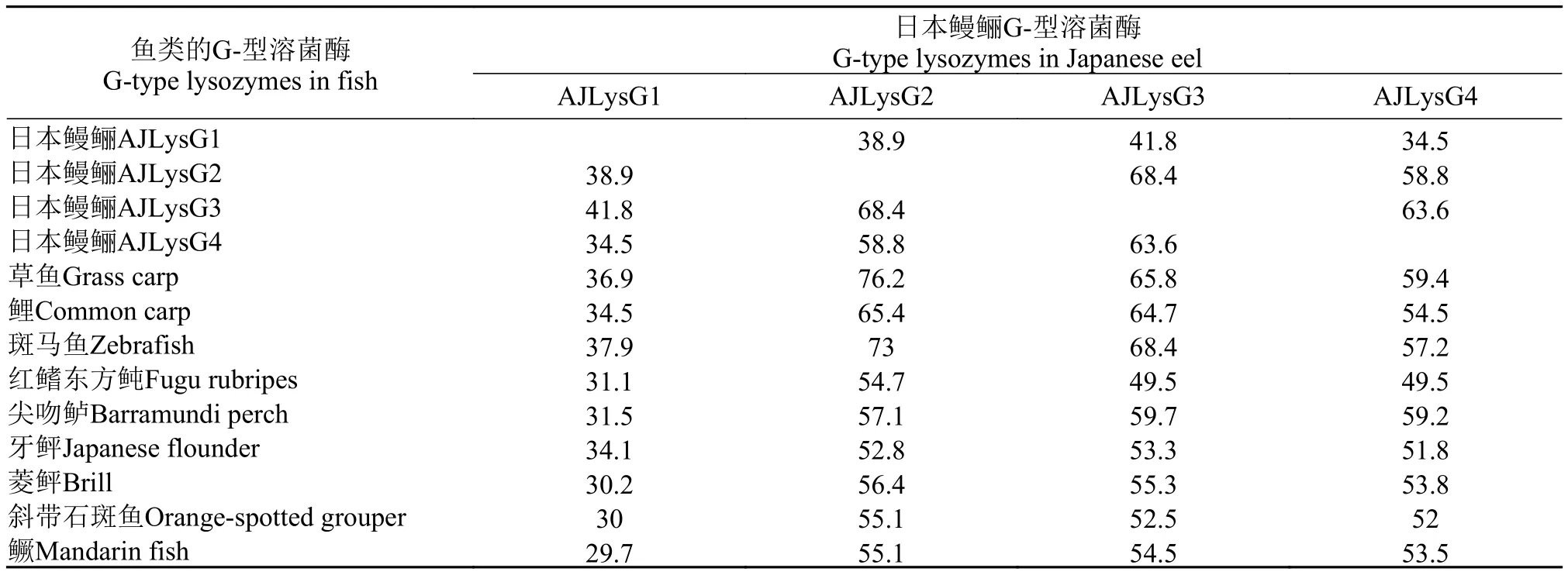
表 3 日本鰻鱺G-型溶菌酶之間以及與其他魚類G-型溶菌酶的同一性分析Tab.3 Comparison among G-type lysozymes of the Japanese eel and other species of fish

圖 1 日本鰻鱺C-型溶菌酶AJLysC和其他魚類C-型溶菌酶的氨基酸序列比較Fig.1 Comparison of deduced amino acid sequence of C-type lysozyme, AJLysC of the Japanese eel with homologues of other species of fish

圖 2 日本鰻鱺G-型溶菌酶和其他魚類G-型溶菌酶氨基酸序列的比較Fig.2 Comparison of deduced amino acid sequences of G-type lysozymes of the Japanese eel with homologues of other species of fish
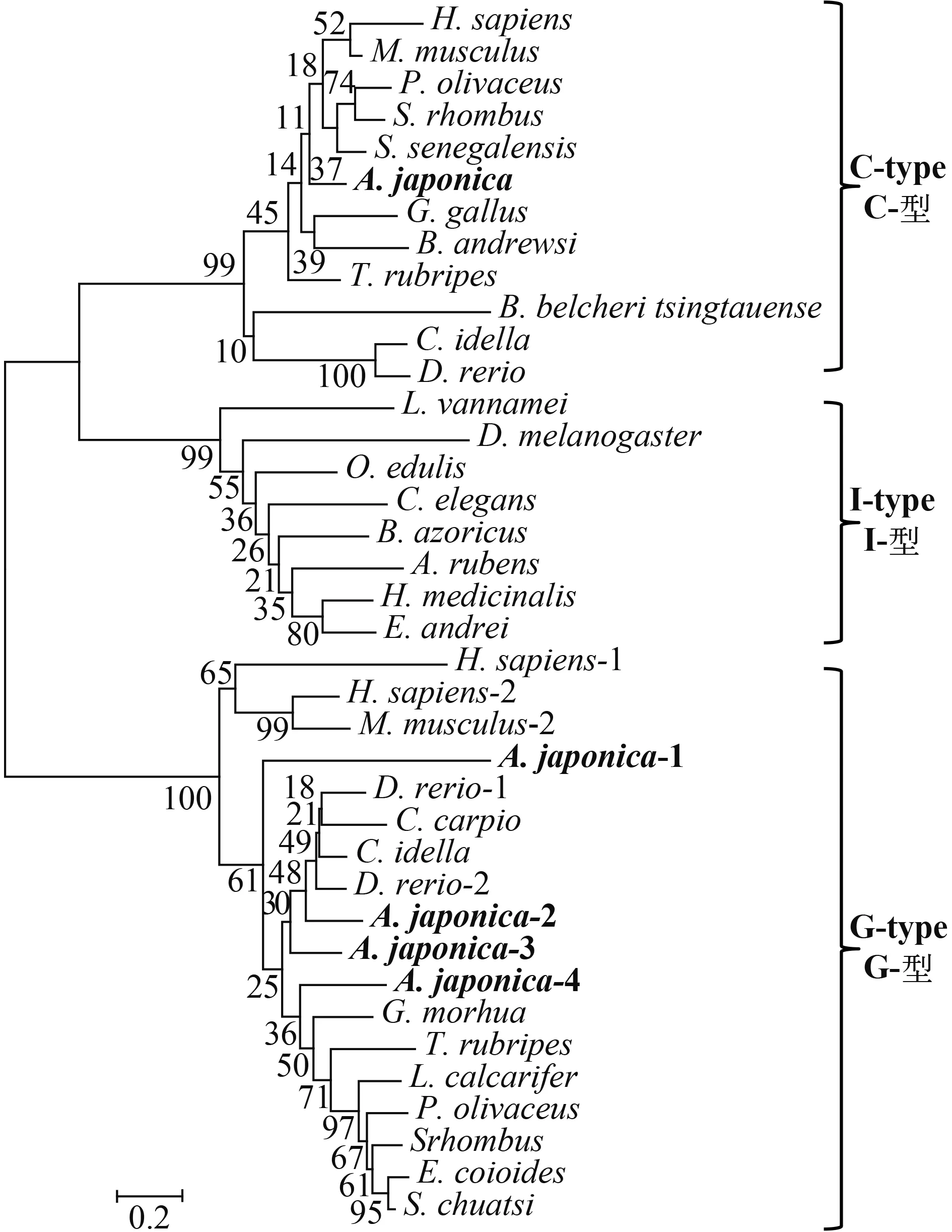
圖 3 鄰接法構建的日本鰻鱺與其他物種的溶菌酶的系統進化樹Fig.3 Phylogenetic analysis of lysozymes of the Japanese eel and other vertebrates

圖 4 日本鰻鱺的1個C-型(AJLysC)和4個G-型(AJLysG1-4)溶菌酶基因結構圖Fig.4 Gene organization of the C-type (AJLysC) and four G-type (AJLysG1-4) lysozymes of the Japanese eel
2.3 C-型和G-型溶菌酶基因在健康魚體組織/器官的表達
熒光定量PCR分析顯示, 克隆到的1個C-型溶菌酶和4個G-型溶菌酶基因在健康魚體的組織/器官都有表達(圖 5、圖6)。然而, 這5個溶菌酶基因的表達水平及其在不同組織/器官的表達似乎都不一樣。C-型溶菌酶在所有組織/器官中的表達量都比相對應的組織/器官中G-型溶菌酶的表達量高, C-型溶菌酶在胃中的表達量最高, 是β-actin表達量的30倍; 在腸和脾中的表達量也很高, 分別是βactin表達量的14和2倍(圖 5)。G-型溶菌酶基因在所有組織/器官中的表達都較低。AJLysG1在各組織/器官中的表達差異很大, 在皮膚的表達量最高,卻只有β-actin表達量的0.011倍, 在頭腎、肝和脾等免疫器官中幾乎不表達。AJLysG2基因在各組織/器官中的表達差異較小, 在鰓中表達量最高, 為βactin表達量的0.023倍; 在血液、頭腎、鰓和體腎中的表達量相對較高。AJLysG3基因在鰓中的表達量最高, 為β-actin表達量的0.017倍。AJLysG4基因在在肌肉中的表達水平最高, 在其他組織/器官中的表達普遍較低。
2.4 C-型和G-型溶菌酶基因在遲緩愛德華氏菌感染后的表達變化
經定量分析顯示, 遲緩愛德華氏菌刺激后, 溶菌酶基因在組織/器官中均有明顯的上調表達。刺激后, AJLysC在各組織/器官中的表達均上調,24h后在脾和腦中表達量上調25和22倍(圖 6A)。AJLysG1在刺激48h后上調更明顯, 其表達量在胃、腸和頭腎中上調倍數分別為50、45和41(圖 6B)。AJLysG2在刺激48h后表達上調更明顯, 在腸道、胃和血液中的上調倍數分別為18、17和13(圖 6C)。與AJLysG1和AJLysG1相似, AJLysG3在刺激后48h上調較為明顯, 如血液中表達上調27倍(圖 6D)。AJLysG4的表達量在刺激后24h和48h均有較明顯的上調, 在肝臟中分別上調了67和50倍(圖 6E)。刺激后, 目的基因在部分組織中表達量也存在下調的現象, 如AJLysG1在刺激24h后, 其在鰓和心臟中的表達量分別下調了3和3.4倍。
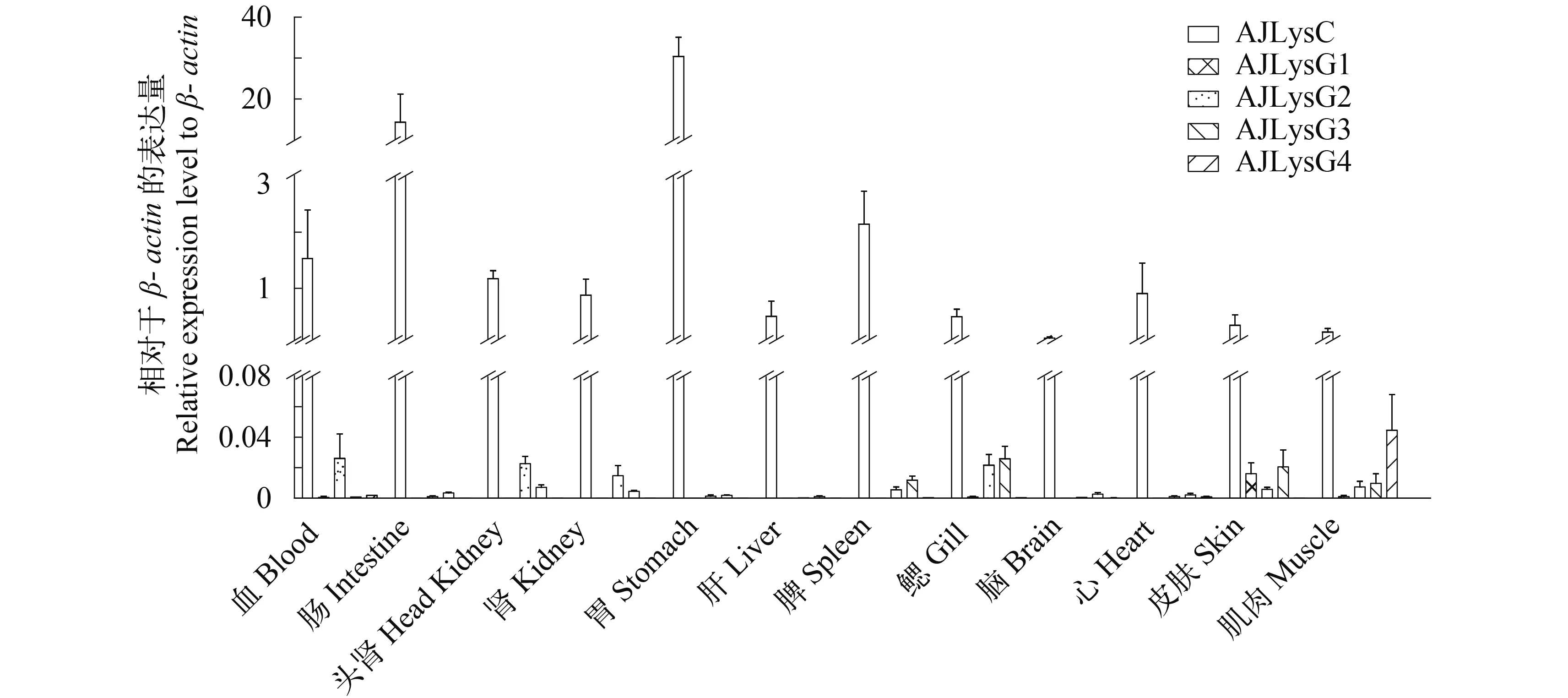
圖 5 日本鰻鱺的1個C-型(AJLysC)和4個G-型(AJLysG1-4)溶菌酶基因在健康魚體組織/器官的表達分布Fig.5 The expression of the C-type (AJLysC) and four G-type (AJLysG1-4) lysozyme genes in different tissues/organs of the Japanese eel
2.5 溶菌酶重組蛋白表達及活性分析
使用生物軟件分析顯示, AJLysG2、AJLysG3、AJLysG4蛋白分子量分別為20.7、20.4和20.7 kD;加上真核表達載體上Myc、His標簽以及多克隆位點等堿基表達的肽鏈, 這3個重組蛋白的分子量分別為26.3、26.0和26.3 kD, 目的條帶分子量與預測的分子量基本相符(圖 7)。
參考Hikima等[2]和Sun等[21]的實驗, 本實驗使用溶壁微球菌為底物進行溶菌酶重組蛋白對細菌生長抑制作用的檢測。實驗結果表明, 這3個重組蛋白對溶壁微球菌的生長均有明顯的抑制作用, 抑制作用與雞蛋白溶菌酶的作用基本一致(圖 7B)。
3 討論
多種溶菌酶基因在同一物種中同時存在的現象極其普遍, 如雞, 除了是最早發現具有C-型溶菌酶的物種外, 還具有2個G-型溶菌酶基因[19]; 在一些哺乳類也具有類似的現象, 如人類、鼠等物種同時具有C-型和G-型溶菌酶基因[5,35,23]。目前研究過的大部分魚類均同時具有C-型和G-型溶菌酶基因, 如牙鲆、草魚、菱鲆等魚類[2,10,12,26]。經過將完整的cDNA序列在NCBI上進行Blast分析和構建進化樹,本研究成功地從日本鰻鱺克隆到了C-型和G-型兩類溶菌酶基因, 其中C-型溶菌酶基因1個, G-型溶菌酶基因4個。這4個G-型溶菌酶基因的結構極為相似, 這應該是基因倍化理論一個例證。
在同一物種中也有多個C-型溶菌酶基因的報道。反芻動物中有檢測到約10個C-型溶菌酶基因,并且這些基因在胃中大量表達[36—38]; 魚類中也有多個C-型溶菌酶基因的報道, 如羅非魚有3個C-型溶菌酶基因[8]。然而, 本研究只在日本鰻鱺的基因組數據庫中發現了一個C-型溶菌酶基因, 對其他鰻鱺種類的研究將有助于揭示鰻鱺這一類群中C-型溶菌酶基因的組成。
雞蛋蛋白溶菌酶具有2個酶活性位點, 即Glu35和Asp52[37]。目前, 所發現的C-型溶菌酶均具有這2個酶活性位點。鵝蛋蛋白溶菌酶(Goose egg-white lysozyme, GEWL)的酶活性位點為Glu73、Asp86和Asp97[1]。Weaver等[39]通過蛋白三維結構證實GEWL的Glu73和HEWL的Glu35對應; Kawamura等[40]以鴕鳥G-型溶菌酶為材料通過點突變證明Glu73是酶活性位點。Asp86和Asp97的作用尚未得到證明, 僅有部分實驗證明HEWL的Asp97可能與HEWL Asp52對應[11,41]。目前, 鯉、鼠[11,24]等物種和本研究所獲得的AJLysG1均出現第2個酶活性位點缺失或突變的現象。若能證實這些G-型溶菌酶具有酶活性, 這對于溶菌酶的研究將有重要的促進作用。
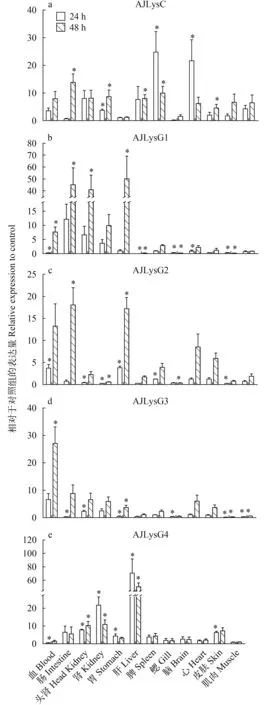
圖 6 日本鰻鱺的1個C-型(a)和4個G-型(b、c、d、e)溶菌酶基因在遲緩愛德華氏菌刺激后的表達變化(*P<0.05)Fig.6 The expression of the C-type (a) and four G-type (b, c, d, e) lysozyme genes in Japanese eel stimulated by Edwardsiella tarda

圖 7 日本鰻鱺三個G-型溶菌酶基因(AJLysG2—4)的重組表達(a)與抗菌活性檢測(b)Fig.7 Expression (a) and bacterial inhibition (b) of recombinant proteins of three G-type lysozymes from the Japanese eel
進化分析顯示, AJLysC與其他脊椎動物的C-型溶菌酶聚為一支, 所有AJLysG均和其他物種的G-型溶菌聚為一支。盡管本研究所發現的AJLysG1和另外3種AJLlysG以及其他魚類G-型溶菌酶聚在一起, 但自成一支。在基因結構上, AJLysG3和AJLysG4的外顯子數目完全相同, 但是進化樹的分析顯示AJLysG2和AJLysG3同源性較高, AJLysG4則與前兩者的同源性較低; AJLysG1則在基因組成和蛋白序列上有差異, 這也反映在它們之間的進化關系上。
目前所發現在脊椎動物C-型溶菌酶均為4個外顯子, 3個內含子結構, 基因結構很保守[14]。G-型溶菌酶的基因結構有所不同, 哺乳類和鳥類動物G-型溶菌酶有6個及更多外顯子[24,25]; 已報道的魚類G-型溶菌酶則只有5個外顯子。鳥類和哺乳類的G-型溶菌酶N-端均含有信號肽結構, 魚類則沒有, 故Irwin等[24]推測外顯子的數目與G-型溶菌酶是否分泌直接相關。而在大西洋鮭[22]和大西洋鱈[23]中的發現表明, G-型溶菌酶能否分泌似乎和外顯子的數目沒有直接的關系。本研究所獲得的AJLysG1含有6個外顯子, 經預測含有信號肽。這一發現部分證實了Irwin等[24]的推測。
C-型溶菌酶的作用主要是通過裂解細胞壁的組成成分肽聚糖, 而很多動物的C-型溶菌酶在一定程度上表現出適應性進化, 還具有消化等其他的功能。在反芻動物中胃中大量表達的C-型溶菌酶基因被認為具有消化的功能[36,37]; 魚類, 包括虹鱒、菱鲆等物種也在胃中檢測到C-型溶菌酶基因的表達。由此可見魚類的C-型溶菌酶也可能同時具有免疫和消化的功能。這些發現可以解釋日本鰻鱺AJLysC在胃中表達量最高, 同時在免疫組織中表達量也較高這一現象。G-型溶菌酶的功能主要表現在免疫方面。根據表達規律, 推測含有信號肽的AJLysG1可能是通過分泌到皮膚表面而發揮抵御外界病原入侵的作用; AJLysG2、AJLysG3和AJLysG4不具有信號肽, 應該屬于胞內蛋白, 它們在不同的組織/器官表達豐度不同, 表明它們可能在不同的組織/器官具有不同的作用, 這些都有待實驗的進一步證實。經病原菌刺激后, 魚類溶菌酶基因幾乎均呈上調表達。注射嗜水氣單胞菌后, 草魚C-和G-型溶菌酶基因表達量均有上調[26]; 人工感染溶藻弧菌72h后, 斜帶石斑魚胃、脾、腎等組織G-型溶菌酶基因的表達量均上調[20]。本實驗也得到了類似的結果, 人工感染遲緩愛德華氏菌后, 日本鰻鱺的溶菌酶基因都呈上調表達, 然而它們的不同的上調表達的差異可能表明它們在不同的組織/器官具有不同的作用, 這有待進一步的研究。
質粒pcDNATM3.1是一個非常完善的真核表達系統, 其人類的CMV啟動子使目的蛋白在細胞中能大量表達。而在魚類中, pcDNATM3.1表達系統也得到廣泛的應用。如劉穎等[42]曾用pcDNA3.1載體轉染至魚類細胞用于斑馬魚IFIT家族基因啟動子的分析, Zou等[43]曾將重組pcDNA3.1/myc-His(-) A轉染至EPC, 同樣取得了良好的實驗結果。本實驗采用pcDNATM3.1/myc-His(-) A為表達載體同樣也獲得了良好的結果, 3個溶菌酶基因均能重組表達, 而且重組蛋白對溶壁微球菌的生長具有抑制作用。然而, 本研究嘗試表達AJLysC和AJLysG1努力沒有成功(結果未顯示), 含有信號肽的AJLysC基因表達量非常低, AJLysG1的重組表達則沒有檢測到, 從而限制了這5種溶菌酶溶解細菌功能的比較研究, 這也有待今后的研究探討。
[1]Jollés P, Jollés J.What’s new in lysozyme research? Always a model system, today as yesterday [J].Molecular and Cellular Biochemistry, 1984, 63(2): 165—189
[2]Hikima Jun-ichi, Minagawa S, Hirono I, et al.Molecular cloning, expression and evolution of the Japanese flounder goose-type lysozyme gene, and the lytic activity of its recombinant protein [J].Biochimica et Biophysica Acta - Gene Structure and Expression, 2001, 1520(1): 35—44
[3]Thammasirirak S, Torikata T, Takami K, et al.The primary structure of cassowary (Casuarius casuarius) goose type lysozyme [J].Bioscience Biotechnology and Biochemistry, 2002, 66(1): 147—156
[4]Canfield R E.Amino acid sequence of egg white lysozyme [J].The Journal of Biological Chemistry, 1963, 238(8): 2698—2707
[5]Peters C W, Kruse U, Pollwein R, et al.The human lysozyme gene.Sequence organization and chromosomal localization [J].European Journal of Biochemistry, 1989, 182(3): 507—516
[6]Callewaert L, Michiels C W.Lysozymes in the animal kingdom [J].Journal of Bioscience and Bioengineering, 2010, 35(1): 127—160
[7]Liu F, Wen Z.Cloning and expression pattern of the lysozyme C gene in zebrafish [J].Mechanisms of Development, 2002, 113(1): 69—72
[8]Yu S G, Ye X, Zhang L L, et al.Molecular cloning and sequencing of three C-type lysozyme genes from Oreochromis aureus [J].Journal of Agricultural Biotechnology, 2010, 18(1): 66—74 [禹紹國, 葉星, 張莉莉, 等.奧利亞羅非魚3種C型溶菌酶基因的克隆和序列分析.農業生物技術學報, 2010, 18(1): 66—74]
[9]Dautigny A, Prager E M, Phamdinh D, et al.CDNA and amino-acid-sequences of rainbow trout (Oncorhynchusmykiss) lysozymes and their implications for the evolution of lysozyme and lactalbumin [J].Journal of Molecular Evolution, 1991, 32(2): 187—198
[10]Hikima J, Hirono I, Aoki T.Molecular cloning and novel repeated sequences of a C-type lysozyme gene in Japanese flounder (Paralichthys olivaceus) [J].Marine Biotechnology, 2000, 2(3): 241—247
[11]Fujiki K, Shin D H, Nakao M, et al.Molecular cloning of carp (Cyprinus carpio) leucocyte cell-derived chemotaxin 2, glia maturation factor β, CD45 and lysozyme C by use of suppression subtractive hybridization [J].Fish and Shellfish Immunology, 2000, 10(7): 643—650
[12]Jiménez-Cantizano R M, Infante C, Martin-Antonio B, et al.Molecular characterization, phylogeny, and expression of c-type and g-type lysozymes in brill (Scophthalmus rhombus) [J].Fish and Shellfish Immunology, 2008, 25(1-2): 57—65
[13]Ye X, Gao F Y, Zheng Q M.Cloning and characterization of the tiger shrimp lysozyme [J].Molecular Biology Reports, 2008, 36(6): 1239—1246
[14]Liu M, Zhang S, Liu Z, Li H, et al.Characterization, organization and expression of AmphiLysC, an acidic c-type lysozyme gene in amphioxus Branchiostoma belcheri tsingtauense [J].Gene, 2006, 367(15): 110—117
[15]Canfield R E, McMurry S.Purification and characterization of a lysozyme from goose egg white [J].Biochemical and Biophysical Research Communications, 1967, 26(1): 38—42
[16]Schoentgen F, Jolles J, Jolles P.Complete amino acid sequence of ostrich (Struthio camelus) egg-white lysozyme, a goose-type lysozyme [J].European Journal of Biochemistry, 1982, 123(3): 489—497
[17]Thammasirirak S, Torikata T, Takami K, et al.The primary structure of cassowary (Casuarius casuarius) goose type lysozyme [J].Bioscience, Biotechnology, and Biochemistry, 2002, 66(1): 147—156
[18]Pooart J, Torikata T, Araki T.The primary structure of a novel goose-type lysozyme from rhea egg white [J].Bioscience, Biotechnology, and Biochemistry, 2004, 68(1): 159—169
[19]Nile C J, Townes C L, Michailidis G, et al.Identification of chicken lysozyme g2 and its expression in the intestine [J].Cellular and Molecular Life Sciences, 2004, 61(21): 2760—2766
[20]Yin Z X, He J G, Deng W X, et al.Molecular cloning, expression of orange spotted grouper goose-type lysozyme cDNA, and lytic activity of its recombinant protein [J].Diseases of Aquatic Organisms, 2003, 55(2): 117—123
[21]Sun B J, Wang G L, Xie H X, et al.Gene structure of goose-type lysozyme in the mandarin fish Siniperca chuatsi with analysis on the lytic activity of its recombinant in Escherichia coli [J].Aquaculture, 2006, 252(2-4): 106—113
[22]Kyomuhendo P, Myrnes B, Nilsen I W.A cold-active salmon goose-type lysozyme with high heat tolerance [J].Cellular and Molecular Life Sciences, 2007, 64(21): 2841—2847
[23]Larsen A N, Solstad T, Svineng G, et al.Molecular characterisation of a goose-type lysozyme gene in Atlantic cod (Gadus morhua L.) [J].Fish and Shellfish Immunology, 2009, 26(1): 122—132
[24]Irwin D M, Gong Z.Molecular evolution of vertebrate goose-type lysozyme genes [J].Journal of Molecular Evolution, 2003, 56(2): 234—242
[25]Nakano T, Graf T.Goose-type lysozyme gene of the chicken: sequence, genomic organization and expression reveals major differences to chicken-type lysozyme gene [J].Biochimica et Biophysica Acta - Gene Structure and Expression, 1991, 1090(2): 273—276
[26]Ye X, Zhang L L, Tian Y Y, et al.Identification and expression analysis of the g-type and c-type lysozymes in grass carp Ctenopharyngodon idellus [J].Developmental and Comparative Immunology, 2010, 34(5): 501—509
[27]Hu Y, Zhou C S, Hu L H, et al.Comparative analysis of the nutritional composition in the muscles and skins of Anguilla japonica cultured in the seawater and freshwater [J].Acta Hydrobiologica Sinica, 2015, 39(4): 730—739 [胡園, 周朝生, 胡利華, 等.海、淡水養殖日本鰻鱺肌肉和魚皮營養分析比較.水生生物學報, 2015, 39(4): 730—739]
[28]Yu H Z, Li Q Y, Zhang K.Nutrition of eels, breeding status and the countermeasures [J].Journal of Anhui Agriculture Science, 2014, 42(20): 6632—6633, 6664 [于海振, 李秋云, 張坤.鰻鱺的營養成分·養殖現狀與對策.安徽農業科學, 2014, 42(20): 6632—6633, 6664]
[29]The IUCN Red List of Threatened Species [DB/OL].Version 2014.3.Available at: www.iucnredlist.org/details/ 166184/0
[30]The IUCN Red List of Threatened Species [DB/OL].Version 2014.3.Available at: www.iucnredlist.org/details/ 60344/0
[31]Campanella J J, Bitincka L, Smalley J.MatGAT: an application that generates similarity/identity matrices using protein or DNA sequences [J].BMC Bioinformatics, 2003, 4: 29
[32]Qi Z T, Nie P.Comparative study and expression analysis of the interferon gamma gene locus cytokines in Xenopus tropicalis [J].Immunogenetics, 2008, 60(11): 699—710
[33]Schmittgen D T, Livak J K.Analyzing real-time PCR data by the comparative CTmethod [J].Nature Protocols, 2008, 3(6): 1101—1108
[34]Bustin S A, Benes V, Garson A J, et al.The MIQE Guidelines: Minimum information for publication of quantitative real-time PCR experiments [J].Clinical Chemistry, 2009, 55(4): 1—12
[35]Yeh T C, Wilson A C, Irwin D M.Evolution of rodent lysozymes: isolation and sequence of the rat lysozyme genes [J].Molecular Phylogenetics and Evolution, 1993, 2(1): 65—75
[36]Irwin M D.Evolution of the bovine lysozyme gene gamily: Changes in gene expression and reversion of function [J].Journal of Molecular Evolution, 1995, 41(3): 299—312
[37]Irwin M D.Evolution of cow nonstomach lysozyme genes [J].Genome, 2004, 47(6): 1082—1090
[38]Cheetham J C, Artymiuk P J, Phillips D C.Refinement of an enzyme complex with inhibitor bound at partial occupancy [J].Journal of Molecular Biology, 1992, 224(3): 613—628
[39]Kawamura S, Ohno K, Ohkuma M, et al.Experimental verification of the crucial roles of Glu73 in the catalytic activity and structural stability of goose type lysozyme [J].Journal of Biochemistry, 2006, 140(1): 75—85
[40]Hirakawa H, Ochi A, Kawahara Y, et al.Catalytic reaction mechanism of goose egg white lysozyme by molecular modelling of enzyme-substrate complex [J].Journal of Biochemistry, 2008, 144(6): 753—761
[41]Helland R, Larsen R L, Finstad S, et al.Crystal structures of g-type lysozyme from Atlantic cod shed new light on substrate binding and the catalytic mechanism [J].Cellular and Molecular Life Sciences, 2009, 66(15): 2585—2598
[42]Liu Y, Zhang Y B, Liu K T, et al.Identification and promoter analysis of an IFIT family gene from zebrafish Danio rerio [J].Acta Hydrobiologica Sinica, 2012, 36(1): 1—8 [劉穎, 張義兵, 劉庭凱, 等.斑馬魚一個IFIT 家族基因的鑒定及啟動子分析.水生生物學報, 2012, 36(1): 1—8]
[43]Zou P F, Chang M X, Xue N N, et al.Melanoma differentiation-associated gene 5 in zebrafish provoking higher interferon-promoter activity through signalling enhancing of its shorter splicing variant [J].Immunology, 2013, 141(2): 192—202
CHICKEN- AND GOOSE- TYPE LYSOZYME GENES IN THE JAPANESE EEL ANGUILLA JAPONICA
YANG Yong1,2, HUANG Bei1, HUANG Wen-Shu1, DUAN Ming-Zhu1, ZHANG Fang-Fang1and NIE Pin2
(1.Fisheries College, Jimei University, Xiamen 361021, China; 2.State Key Laboratory of Freshwater Ecology and Biotechnology, Institute of Hydrobiology, Chinese Academy of Sciences, Wuhan 430072, China)
Based on genomic database of the Japanese eel (Anguilla japonica), two types of lysozyme genes including one C-type and four G-type lysozyme genes were found and named as AJLysC, AJLysG1, AJLysG2, AJLysG3, and AJLysG4, which consisted of 809, 732, 1352, 1177 and 731 nucleotides that encode 143, 193, 185, 185 and 187 amino acids, respectively.AJLysC and AJLysG1 have 15 and 19 amino acids signal peptides, respectively, but other three lysozymes have no signal peptide.The gene structure of AJLysC, AJLysG2, AJLysG3 and AJLysG4 is similar to their corresponding lysozyme genes in other species in terms of exon-intron organization, with 4 exons for the C-type and 5 exons for the G-type.However, the gene structure of AJLysG1 differed from other fishes, with 6 exons, representing the first report in fish.Compared with other species, second catalytic residue, Asp, in AJLysG1 is missing.AJLysC shares high identity with C-type lysozymes of other species, having 72.7% identity with Japanese flounder (Paralichthys olivaceus).AJLysG2, AJLysG3 and AJLysG4 share high identity with each other and with those in other species, while AJLysG1 does not share high identity with neither G-type lysozymes of other species nor the other three, with the identity lower than 50%.The real-time quantitative PCR analysis showed that all five genes were expressed in all examined organs/tissues of eels.The C-type lysozyme gene expressed highly in stomach and modestly in immune related tissues.The expression of the four G-type lysozymes was tissue-dependent.AJLysG1 highly expressed in skin and muscle, while AJLysG2 highly expressed in blood, head kidney, trunk kidney and gills.All five genes were up-regulated in many organs/tissues by Edwardsiella tarda infection, especially in blood, intestine and head kidney.In addition, the recombinant proteins of AJLysG2, AJLysG3 and AJLysG4 obviously repressed the growth of Micrococcus lysodeikticus, however, their roles in inhibiting pathogenic bacteria of the Japanese eel need further investigation.
Japanese eel; Lysozyme; Expression; Recombinant protein; Antimicrobial activity
Q344+.1
A
1000-3207(2017)04-0807-12
10.7541/2017.101
2016-03-12;
2016-12-28
國家自然科學基金(31402329); 海洋經濟發展區域示范項目(14PYY050SF03)資助 [Supported by the National Natural Science Foundation of China (31402329); the Regional Project of Marine Economic Development (14PYY050SF03)]
楊勇(1988—), 男, 湖北仙桃人; 碩士研究生; 研究方向為水產動物病害防治。E-mail: sterny@aliyun.com
聶品, 男, 研究員; E-mail: pinnie@ihb.ac.cn

