rhG-CSF包含體處理工藝改進
劉建飛+匡瑾瑾+傅暉
摘 要 通過使用管式離心機替代轉子離心機對rhG-CSF(賽格力)包含體處理工藝進行改進,使4個亞批次處理的包含體合并為1個批次進行處理,操作時間縮短4倍。通過改進前后的質量對比研究發現,本工序變性蛋白的純度、內毒素及殘余DNA與原工藝相比均無明顯差異,且符合企業質量要求,而人工和動力成本下降了75%。
關鍵詞 包含體 rhG-CSF 變性蛋白
中圖分類號:TQ464.7 文獻標識碼:A 文章編號:1006-1533(2017)15-0075-04
Process improvement of inclusion-body of rhG-CSF
LIU Jianfei*, KUANG Jinjin, FU Hui
(Shanghai Sunway Biotech Co., Ltd., Shanghai 201206, China)
ABSTRACT An improved process for the treatment of rhG-CSF inclusion body was established by using tubular centrifuge instead of rotor centrifuge, which could make 4 sub-batches treatment of inclusion bodies in the original process into only one and total operation time be reduced to one fourth. It was found that the purity of denatured protein and the contaimination of endotoxin and residual DNA in the improved process was comparable to those in the original process and the quality could meet the requirements of enterprises while the costs of labor and power could be reduced by 75%.
KEY WORDS inclusion body; rhG-CSF; denatured protein
人粒細胞集落刺激因子是一個小的弱酸性蛋白,分子量為18.8 kD。重組人粒細胞集落刺激因子(rhG-CSF)為利用基因重組技術通過工程菌的發酵生產的,與天然產品相比,生物活性在體內、外基本一致。rhG-CSF是調節骨髓中粒系造血的主要細胞因子之一,選擇性作用于粒系造血祖細胞,促進其增殖、分化,并可增加粒系終末分化細胞的功能[1]。它對于治療由腫瘤放化療、骨髓移植所引起的粒細胞減少癥具有顯著療效[2-4]
賽格力(SunGran)為我們公司生產的重組人粒細胞集落刺激因子注射液的商品名,是以大腸埃希氏菌為表達載體,表達的rhG-CSF以包含體[5]形式存在與大腸埃希氏菌細胞質中,須經細胞破碎后收集包含體,再經包含體處理、復性、純化,制備成賽格力原液[5-7]。
包含體處理一般采用多種緩沖液對其進行洗滌,最后用高濃度變性劑(6 mol/L鹽酸胍或8 mol/L尿素)對其進行溶解。由于包含體難溶解和密度的特異性,緩沖液洗滌后,都用離心機來進行固液分離,重新收集包含體[8-11]。目前廣泛運用的轉子離心機由于處理量小,效率較低。管式離心機利用連續離心的原理,可以在短時間內一次離心大量的液體。本研究利用管式離心機代替傳統的轉子離心機,對包含體處理工藝進行改進,實踐證明工藝改進后的產量和質量無明顯變化,而工作效率大大提高了。
1 材料與方法
1.1 材料
基因工程大腸埃希氏菌在發酵罐中進行高密度發酵[12-13],最終獲得50 L發酵液,離心收集到2 800 g菌體,收集的大腸埃希氏菌經超聲破碎、離心后獲得的固體物質約600 g。
脫氧膽酸鈉、十二烷基肌氨酸鈉、Acrylamide/bisacrylamide,30% solution(分析純,Sigma公司);二巰蘇糖醇、Tris(分析純,Promega公司);低分子量標準蛋白(marker,中國科學院上海生物化學研究所,分子量依次為97.4、66.2、43.0、31.0、20.1和14.4 kD);細菌內毒素工作標準品(10 EU/ml及1 000 EU/ml)、鱟試劑(湛江安度斯生物有限公司);鹽酸胍(分析純,英濰捷基上海貿易有限公司);DIG High Prime DNA Labeling and Detection Starter KIT(Roche公司);其他常用化學試劑為市售分析純或藥用輔料。
1.2 設備
GQ76管式離心機、GL-21M高速冷凍離心機(上海離心機研究所);PowerPac HV電泳儀、GelDocXR凝膠成像儀(Bio-Rad公司)。J98-Ⅲ DN型超聲儀(寧波新芝生物科技有限公司)。
1.3 方法
1.3.1 溶液制備
破菌緩沖液:20 mmol/L pH 8.0 Tris-EDTA-2Na鹽酸緩沖液;水溶性洗滌液(A液):1 mmol/L乙二胺四乙酸二鈉、0.1 mol/L氯化鈉;脂溶性洗滌液(B液):含1%脫氧膽酸鈉、5 mmol/L二巰蘇糖醇、5 mmol/L乙二胺四乙酸二鈉的50 mmol/L Tris-HCl緩沖液(pH 9.0);蛋白溶解液(C液):含2%十二烷基肌氨酸鈉、20 mmol/L硫酸銅的50 mmol/L Tris-HCl緩沖液(pH 8.0);變性液(D液):含6 mol/L鹽酸胍的40 mmol/L的HAc-NaAc緩沖液(pH 4.0)。
1.3.2 原工藝和改進后工藝
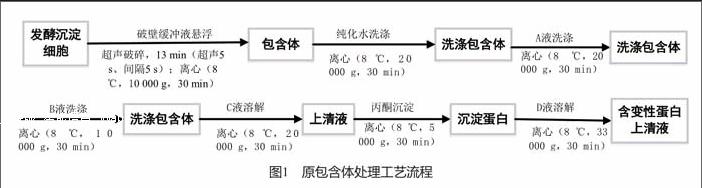
賽格力一批發酵所獲得的包含體分成4個亞批進行處理。首先,包含體分別經純化水、A液、B液洗滌,每次洗滌后均離心收集沉淀。B液洗滌后收集的沉淀,用C液溶解后,收集上清液,然后在上清液中加入冷凍后的丙酮(在冰浴條件下)進行攪拌離心,收集沉淀,最后用變性劑D液溶解,離心獲得含變性蛋白的上清液(圖1)。
改進后工藝流程和改進前一樣,只是前5步用管式離心機代替轉子離心機,但是考慮到安全原因,丙酮沉淀后的步驟還是保留使用轉子離心機。
1.4 檢測方法
內毒素檢測:按照《中國藥典》2015年版通則1143方法1 凝膠法進行檢測。
殘余DNA測定:按照《中國藥典》2015年版通則3407第一法 DNA探針雜交法進行檢測。
電泳方法:按照《中國藥典》2015年版通則0541第五法SDS-聚丙烯酰胺凝膠電泳法進行檢測。
2 結果與討論
2.1 產量比較
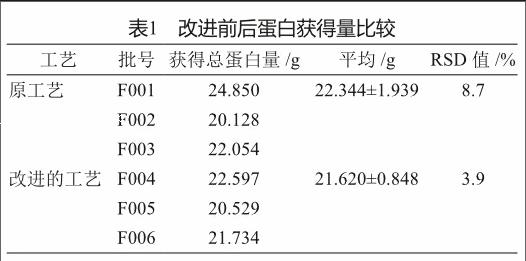
采用管式離心機勞動效率得到了大大提高,但是兩者所采用的離心模式以及離心力還是有所不同的。管式離心機是否能夠把洗滌液中的包含體全部離心收集起來,將是影響其產量的關鍵因素。分別選取了工藝改進前和后連續的3批包含體處理后所得到的蛋白量進行比較(表1)。結果表明,改進前后產量無明顯差異。同時改進后3批RSD為3.9%較改進前的8.7%有著更好的穩定性和重現性。
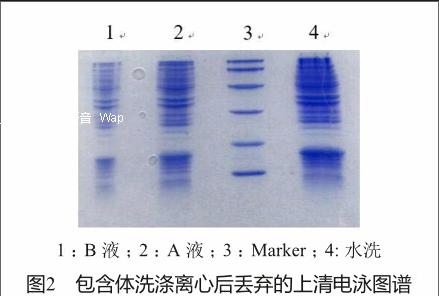
對采用改進工藝的F004處理時的純化水、A液、B液丟棄上清取樣,進行電泳檢測(圖2)。丟棄的上清中含有大量的雜質蛋白。對照rhG-CSF分子量為18.8 kD,在電泳的相應分子量位置未見有大量目標蛋白存在。經電泳圖譜掃描,損失蛋白大約在10%以下,與原有工藝基本持平。
2.2 質量對比
2.2.1 純度
包含體內除了含有目標蛋白外,還含有大量的宿主蛋白。利用包含體的不易溶解的特性,分別用不同的緩沖液來溶解大腸埃希氏菌本身的蛋白質,從而達到分離宿主蛋白的目的。圖3是工藝改進前后各1批處理后獲得變性蛋白的電泳圖譜。工藝改進前后的圖譜基本一致,改進后未見有新的雜蛋白產生。同時對電泳圖譜進行掃描,圖形基本一致(圖4)。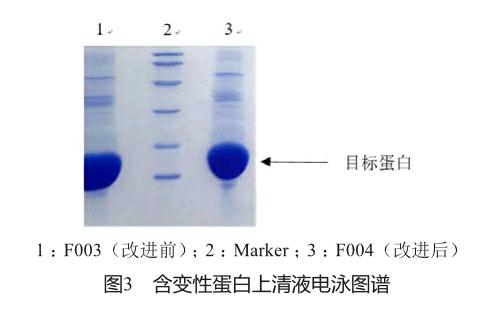
表3對工藝改進前后連續各3批變性蛋白的純度進行了統計與比較。工藝改進后純度均在80%以上,達到變性蛋白質量標準要求,并且RSD值為1.80%,說明改進工藝具有相當穩定的重現性。
2.2.2 內毒素
工程菌大腸埃希氏菌屬革蘭陰性菌,超聲破壁后收集包含體時,裂解液中也含有大量的細菌內毒素,須盡可能地去除掉。經我們檢測,未經處理的包含體,其細菌內毒素含量大于1 000萬EU/ml。檢測連續3批包含體處理后樣品的內毒素含量,值均在100~1 000 EU/ml之間,達到要求。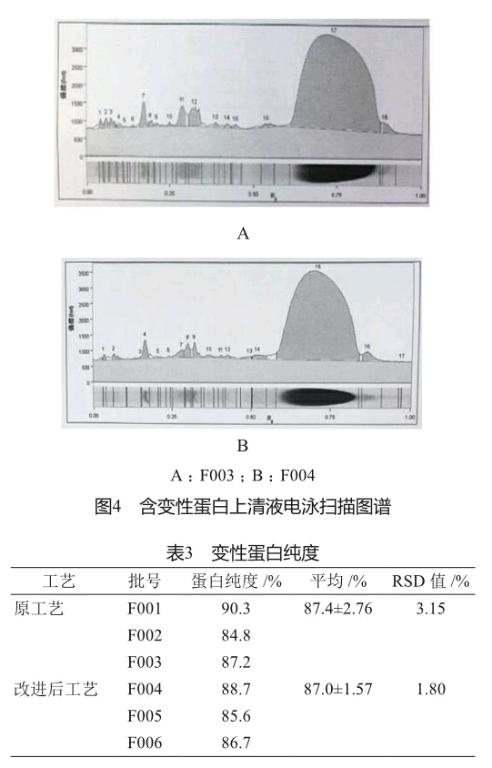
2.2.3 殘余DNA
隨著超聲破碎,大腸埃希氏菌的宿主DNA也與包含體粘連在一起。由于微生物來源的基因組DNA富含CpG和非甲基化序列,故殘余DNA增加了重組蛋白藥物在體內的免疫源性風險[14-15],一直是國內外藥品監管機構關注的重點。目前檢測的方法為半定量法,通過樣品與標準品顏色深淺的比較,來確定殘余宿主DNA含量的范圍。從圖5可以看出,工藝改進前后2批次的樣品F001和F004顏色深淺幾乎一樣,介于標準品100 ng和10 ng之間,滿足變性蛋白質量標準中殘余DNA≤100 ng/ml的要求。表4統計了連續3批工藝改進處理后最終樣品的殘余DNA含量,均小于100 ng/ml,達到要求。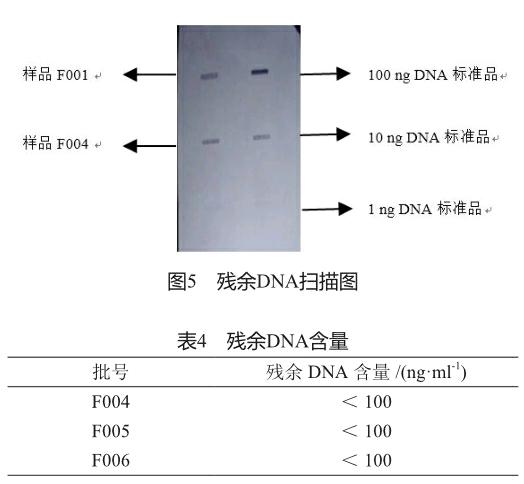
2.3 生產效率
用轉子離心機處理一批高密度發酵所獲得的包含體,必須分成4個亞批次進行處理。每個亞批次的時間為2個工作日,也就是處理完1批完整的包含體需要8個工作日。用管式離心代替轉子離心機可以一次性處理完整的一批包含體,并且只需要2個工作日。生產效率提高了4倍。節約了6 d操作時間。勞動效率的提升,帶來了生產成本的降低。1批發酵按照上海市人2017年人均工資計算,改進后節省人工成本1 740元,同時動力消耗也節省9 000元。
1批發酵獲得的包含體通過處理,一般可以獲得22 g蛋白。原工藝的人工和動力成本為14 320元,而改進后的成本為3 580元。獲得的粗蛋白的成本從651元/g下降到163元/g,成本下降了75%。
3 討論
從產量、蛋白純度、內毒素和殘余DNA幾個方面對賽格力包含體洗滌改進工藝與原工藝進行了比較,改進工藝在產量和質量上與原工藝基本持平,具有相當好的穩定性和重現性,同時大大提高了勞動效率,降低了生產成本,表明改進工藝在實際生產上是可行的。
參考文獻
[1] 李迎新. rhG-CSF粒細胞集落因子藥理學研究[D]. 哈爾濱:哈爾濱醫科大學, 1998.
[2] 張力, 李龍蕓, 林宏英, 等. 重組人粒細胞集落刺激因子對腫瘤患者白細胞的影響[J]. 中國臨床藥學雜志, 2001, 10(4): 207-210.
[3] 候梅, 鄢希, 石晶, 等. 國產重組人粒細胞集落刺激因子Ⅱ期臨床試驗[J]. 中國新藥雜志, 2001, 10(4): 279-281.
[4] 茅偉, 邱慧敏, 許德鳳. 賽格力和惠爾血防治腫瘤化療所致白細胞減少的觀察[J]. 同濟大學學報(醫學版), 2001, 22(3): 89-90.
[5] Palmer I, Wingfield PT. Preparation and extraction of insoluble(inclusion body) proteins from Escherichia coli[J/ OL]. Curr Protoc Protein Sci, 2012 [2017-05-31]. https:// www.ncbi.nlm.nih.gov/pmc/articles/PMC3809847/.
[6] 宋爽, 蔣文宏, 蔣永平. 新一代重組人粒細胞集落刺激因子的工業化發酵、復性和純化[J]. 中國生物醫學工程學報, 2012, 31(4): 552-557.
[7] 張兵, 鄒文藝, 戎隆富, 等. 重組人粒細胞集落刺激因子的表達、純化以及PEG修飾[J]. 生物學雜志, 2008, 25(2): 36-39.
[8] 鄺愛麗, 陳圓圓, 彭志峰, 等. 包涵體的形成原因及其處理方法[J]. 上海畜牧獸醫通訊, 2009(1): 62-63.
[9] 高永貴, 關怡新, 姚善涇. 包涵體蛋白的變復性研究[J].科技通報, 2003, 19(1): 10-15.
[10] 張婷婷, 葉波平. 包涵體蛋白質的復性研究進展[J]. 藥物生物技術, 2007, 14(4): 306-309.
[11] 羅惠霞, 李敏, 王玉炯. 包涵體蛋白復性的幾種方法[J].生物技術通訊, 2007(5): 96-98.
[12] 高麗華. rhG-CSF基因工程菌高密度發酵的研究[D]. 上海:華東理工大學, 2011.
[13] 岑仡, 童涌,楊峰. 溶氧濃度對rhG-CSF工程菌高密度發酵的影響[J]. 藥學實踐雜志, 2011, 29(3): 197-199.
[14] 王蘭, 王軍志. 關于生物制品殘余DNA質量控制問題[J].中國新藥雜志, 2011, 20(8): 678-683.
[15] 張昀, 陳興. 生物制劑中殘余DNA的潛在危害性及其檢測方法的研究進展[J]. 中國生物制品學雜志, 2014, 27(10): 1348-1353.

