苯那普利對糖尿病腎病大鼠腎臟結締組織生長因子表達的調節作用
劉楠楠 王立英 姜 晶 董志恒 李 才
(北華大學基礎醫學院病理教研室,吉林 吉林 132013)
苯那普利對糖尿病腎病大鼠腎臟結締組織生長因子表達的調節作用
劉楠楠 王立英1姜 晶2董志恒 李 才3
(北華大學基礎醫學院病理教研室,吉林 吉林 132013)
目的 研究苯那普利對糖尿病腎病(DN)大鼠腎臟結締組織生長因子(CTGF)表達的調節。方法 Wistar大鼠34只,隨機分為:對照組、DN、苯那普利組。DN組及苯那普利組大鼠經腹腔注射鏈脲佐菌素(STZ)建立DN模型。于實驗第12周末處死大鼠測量大鼠體質量、空腹血糖、腎功能、尿白蛋白排泄率(UAER)及24 h尿總蛋白。應用免疫組化方法檢測腎臟CTGF蛋白表達,并進行半定量分析。結果 與對照組相比,DN組大鼠空腹血糖、血尿素氮、血清肌酐、UAER 及24h尿總蛋白顯著升高(P<0.05或P<0.01);腎臟CTGF表達增加(P<0.05)。DN大鼠苯那普利組各項檢測指標均較模型組顯著改善(P<0.05或P<0.01)。結論 苯那普利可下調DN苯那普利腎組織CTGF的表達,降低蛋白尿,保護腎功能。
腎組織;苯那普利;結締組織生長因子;糖尿病腎病
糖尿病腎病(DN)是最常見的糖尿病微血管并發癥,其主要病理特征為腎小球系膜基質積聚、腎小球和腎小管基底膜增厚及腎間質纖維化,已成為終末期腎衰竭和糖尿病患者死亡的主要病因〔1〕。在DN導致腎小球硬化和腎小管間質纖維化的過程中,結締組織生長因子(CTGF)是關鍵性細胞因子之一,參與纖維化過程〔2〕。本研究建立鏈脲佐菌素(STZ)誘導的DN大鼠模型,觀察苯那普利對DN大鼠腎組織CTGF表達的影響。
1 材料與方法
1.1 動物 Wistar大鼠34只,體重197~255 g,雌雄各半,健康狀態良好,血糖正常,購自吉林省藥品檢驗實驗動物科。實驗期間所有動物自由飲水進食,保持室內通風、墊料干燥。
1.2 儀器、試劑及藥品 LD5- 2A醫用離心機,北京醫用離心機廠制造;日立7150型自動生化分析儀,日本生產;T1000電子天平,常熟雙杰測試儀器廠;血糖測定儀,三諾公司;Olympus 顯微鏡,日本。STZ購自美國Sigma公司;苯那普利,購自北京諾華公司;兔抗人CTGF多克隆抗體,購自上海穎心實驗設備有限公司;尿白蛋白酶免疫法試劑盒,購自上海德波生物技術公司;血糖高靈敏度試劑盒,購自匯力生物工程技術有限公司;尿葡萄糖檢測試紙片,購自桂林中輝生物技術有限公司。
1.3 實驗方法
1.3.1 分組與DN模型制備 Wistar大鼠34只,隨機分為對照組(n=10)、DN模型組(n=12)、苯那普利組(n=12)。給DN組及苯那普利組大鼠腹腔一次性注射STZ 60 mg/kg。給對照組腹腔注射不含STZ的同等體積的緩沖液。72 h后由尾尖靜脈采血測量空腹血糖,當空腹血糖≥16.7 mmol/L,3 w后檢測24 h尿蛋白定量,當其>30 mg時,為DN模型建立成功。隨后將造模成功的大鼠分為DN組及苯那普利組。穩定1 w后,給DN組大鼠每日灌服苯那普利10 mg·kg-1·d-1。對照組及DN組給予等量生理鹽水灌服,連續灌服12 w。實驗期間所有大鼠未給胰島素及其他降糖藥物。給實驗大鼠腹腔注射STZ后,其多飲、多食及多尿表現顯明。但DN組有4只死亡,而苯那普利組有3只死亡。
1.3.2 標本留取 實驗第12周時,給各組大鼠稱重,并經尾靜脈采血測量空腹血糖,并用代謝籠收集大鼠24 h尿樣,記錄尿量,離心除掉沉渣,-20℃保存待測尿白蛋白。給所有動物乙醚麻醉,處死動物,眶后靜脈采血,肝素抗凝,分離血清(2 000 r/min,10 min),保存于-74℃冰箱。剖開腹腔,取出腎臟,用生理鹽水清洗,去掉包膜,使用精密天平稱重,經腎門冠狀面取腎組織,置入10%中性福爾馬林液固定待作免疫組化檢查。
1.3.3 生化指標測定 尿白蛋白排泄率(UAER)、尿素氮、空腹血糖、血肌酐采用全自動生化分析儀測定。尿總白蛋白采用雙縮脲法測定。
1.3.4 免疫組化測定 將已用10%福爾馬林液固定的腎組織,石蠟包埋,制片4 μm厚,二甲苯脫蠟,酒精脫水,滴加3%甲醛H2O2封閉內源性過氧化物酶,滴加兔抗人CTGF多克隆抗體(1∶100)工作液,室溫孵育60 min,此后加入生物素標記山羊抗兔IgG,室溫孵育20 min,再加入鏈霉素生物素辣根過氧化物酶工作液,室溫孵育30 min,二氨基聯苯胺(DAB)顯色,蘇木素復染,常規脫水,透明,樹膠封片,磷酸鹽緩沖液(PBS)替代Ⅰ抗作陰性對照。對圖像進行分析應用Image- pro plus圖像分析系統,隨機選取8個不重疊視野(×400),測定陽性染色部位的積分光密度值為半定量分析值。
1.4 統計學方法 應用SPSS17.0軟件進行t檢驗。
2 結 果
2.1 體質量、腎質量及腎質量/體質量狀況 實驗前各組大鼠體質量均無明顯不同。成模后在實驗第12周時,DN組及苯那普利組大鼠體質量減輕,與對照組比較有統計學差異(P<0.01或P<0.05)。苯那普利組成模后至12 w末時體質量較DN組明顯增加(P<0.05)。但苯那普利組腎質量/體質量與DN組比較顯著降低(P<0.01),見表1。
2.2 生化指標 實驗前各組大鼠血糖比較均無明顯差異。12 w末時,苯那普利組與DN組空腹血糖較對照組顯著增高(P<0.01),苯那普利組與DN組顯著降低(P<0.01)。腎功能指標,DN組大鼠UAER、尿總蛋白、尿素氮、血肌酐較對照組顯著升高(P<0.01),與DN組比較,苯那普利組UAER、尿總蛋白、血肌酐及尿素氮均明顯下降(P<0.01),見表2。
2.3 腎組織CTGF的表達 免疫組化結果顯示,CTGF在腎小球系膜細胞、上皮細胞及系膜區的陽性表達呈棕黃色顆粒。CTGF在對照組大鼠腎小球內表達微弱(呈輕微著色,僅見少量淺淡黃色顆粒);DN組大鼠CTGF表達明顯增強(著色加深,呈棕黃色);苯那普利組大鼠CTGF表達較DN組減輕(著色變淺,呈淺黃色)。見圖1。半定量結果表明,DN組(0.50±0.09)較對照組(0.31±0.05,P<0.05)顯著增強;苯那普利組(0.38±0.07)較DN組顯著降低(P<0.05)。
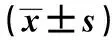
表1 各組大鼠體質量、腎質量、腎質量/體質量比較
與對照組比較:1)P<0.01,2)P<0.05;與DN組比較:3)P<0.05,4)P<0.01
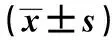
表2 各組相關指標比較
與對照組比較:1)P<0.01;與模型組比較:2)P<0.01

圖1 腎組織CTGF免疫組化染色結果(DAB,×400)
3 討 論
DN的明確發病機制并不十分清楚,目前認為多種因素可能與DN的發生有關。但在DN機制中CTGF的作用越來越受到廣泛關注。CTGF屬于即刻早期基因CCN家族成員之一。近年研究發現,CTGF與包括血管、心臟、腎臟、胰腺、肺及肝臟等在內的許多組織器官纖維化發生發展密切相關〔3~5〕。正常情況下,體內的CTGF表達很低或無表達,但在腎等器官病理狀態下,便會出現CTGF過度表達〔6〕。初步研究表明,在腎臟疾病時,CTGF主要表達于腎臟中起源于中胚層的固有細胞,如臟層上皮細胞、壁層上皮細胞、系膜細胞〔7〕。Ren等〔8〕在研究中發現,在糖尿病狀態下,腎臟分泌或產生更多的轉化生長因子β(TGF- β),進而促進CTGF等細胞因子的作用。但從DN早期開始系膜細胞與腎小球足細胞的CTGF表達呈顯著升高〔9〕。
正常狀態下,CTGF的含量很低,高血糖、晚期糖基化終末產物(AGEs)、血管緊張素Ⅱ(AngⅡ)及機械應力等作用可以使CTGF過度表達,結果引起細胞外基質(ECM)成分,如纖維連接蛋白(FN),膠原等的增多,并參與DN發生〔10〕。研究提示,CTGF可能是TGF- β1促纖維化活性的下游信號介質,在刺激細胞增殖及ECM的形成、促進組織器官纖維化方面起重要作用〔11〕。AGEs是高血糖環境中糖與蛋白質上的游離氨基酸、脂肪及核酸之間反應形成,當AGEs同特異受體結合影響生長因子及細胞因子如CTGF與TGF- β的表達,導致ECM的合成和降解失衡,引發腎纖維〔12〕。高血糖狀態下,腎組織CTGF產生增多,可能是由于糖尿病糖代謝紊亂所致。因此控制高血糖,減少AGEs的形成,也是防止糖尿病發展為DN的重要措施。
本研究結果提示,應用苯那普利對DN大鼠進行干預,可明顯減輕其腎臟的病理性損傷,其作用機制很可能與苯那普利下調DN大鼠腎組織中CTGF的表達有關。已有研究證實,在DN早期即有血、尿及腎組織中CTGF水平增高〔13〕。尿中CTGF濃度與DN的嚴重程度,即UAER和腎小球濾過率呈正相關〔10〕。尿蛋白增多不僅是DN損害的表現,而且也是腎病和心血管病進展的重要因素〔14〕,說明腎組織中CTGF表達水平的變化通常與DN的嚴重程度密切相關。本實驗結果提示,苯那普利通過抑制DN大鼠腎組織中CTGF的表達,而發揮其保護腎功能的作用機制。
1 Dronavalli S,Duka I,Bakris GL.The pathogenesis of diabetic nephropathy 〔J〕.Nat Clin Pract Endocrinol Met,2008;4(8):444- 52.
2 王 俏,杜 勤,雷 鏡.糖尿病腎病大鼠CTGF異常表達及藥物干預研究〔J〕.上海交通大學學報(醫學版),2008;28(5):536- 9.
3 Kiran G,Nandini CD,Ramesh HP,etal.Progression of early phase diabetic nephropathy in streptozotocin- induced diabetic rats:evaluation of various kidney- related parameters 〔J〕.Indian J Exp Biol,2012;50(2):133- 40.
4 Tundemir M,Oztürk M,Histochem A.The effects of angiotensin- Ⅱ receptor blockers on podocyte damage and glomerular apoptosis in a rat model of experimental streptozotocin- induced diabetic nephropathy 〔J〕.Acta Histochem,2011;113(8):826- 32.
5 Yao L,Wang J,Mao Y,etal.Different expressions of protein kinase C- alpha,beta Ⅰ and beta Ⅱ in glomeruli of diabetic nephropathy patients〔J〕.J Huazhong Univ Sci Technolog Med Sci,2006;26(6):651- 3.
6 Kapoor M,Liu S,Huh K,etal.Connective tissue growth factor promoter activity in normal and wounded skin〔J〕.Fibrogenesis Tissue Repair,2008;1(1):3- 11.
7 Ruiz- Ortega M,Rupérez M,Esteban V,etal.Angiotensin Ⅱ:a key factor in the inflammatory and fibrotic response in kidney diseases 〔J〕.Nephrol Dial Transplant,2006;21(1):16- 20.
8 Ren X,Guan G,Liu G,etal.Irbesartan ameliorates diabetic nephropathy by reducing the expression of connective tissue growth factor and alpha- smooth- muscle actin in the tubulointerstitium of diabetic rats〔J〕.Pharmacology,2009;83(2):80- 7.
9 Wahab NA,Schaefer L,Weston BS,etal.Glomerular expression of thrombospondin- 1,transforming growth factor beta and connective tissue growth factor at different stages of diabetic nephropathy and their interdependent roles in mesangial response to diabetic stimuli〔J〕.Diabetologia,2005;48(12):2650- 60.
10 Nguyen TQ,Tarnow L,Andersen S,etal.Urinary connective tissue growth factor excretion correlates with clinical markers of renal disease in a large population of type 1 diabetic patients with diabetic nephropathy〔J〕.Diabetes Care,2006;29(1):83- 8.
11 聶 興,劉 暢,宛 月.厄貝沙坦對糖尿病腎病大鼠腎臟結締組織生長因子及纖維連接蛋白表達的影響〔J〕.廣西醫科大學學報,2013;30(4):526- 30.
12 董 明,王秋月.結締組織生長因子:糖尿病腎病治療的新靶點〔J〕.國際內科學雜志,2008;35(8):456- 9.
13 Roestenberg P,van Nieuwenhoven FA,Joles JA,etal.Temporal expression profile and distribution pattern indicate a role of connective tissue growth factor (CTGF/CCN- 2) in diabetic nephropathy in mice 〔J〕.Am J Physiol Renal Physiol,2006;290(6):F1344- 54.
14 Jefferson JA,Shankland SJ,Pichler RH.Proteinuria in diabetic kidney disease:a mechanistic viewpoint 〔J〕.Kidney Int,2008;74(1):22- 36.
〔2016- 01- 28修回〕
(編輯 苑云杰/曹夢園)
劉楠楠 (1976- ),女,醫學博士,副教授, 主要從事糖尿病腎病及腫瘤分子病理研究。
R587.2
A
1005- 9202(2017)15- 3659- 03;
10.3969/j.issn.1005- 9202.2017.15.008
1 北華大學基礎醫學院生理教研室 2 北華大學附屬醫院病理科 3 吉林大學再生醫學科學研究所

