LED藍光治療創傷性感染傷口的療效觀察
羅 梅,王秀薇,胡 盼,向 勤,胡艷紅
·經驗交流·
LED藍光治療創傷性感染傷口的療效觀察
Effct of LED blue light in the treatment of traumatic wound infection
羅 梅,王秀薇,胡 盼,向 勤,胡艷紅
研究LED藍光治療創傷性感染傷口的療效。在常規清創換藥治療的基礎上,采用藍光照射治療10d為1個療程,照射1~2個療程。照射1個療程后,觀察組轉陰率明顯升高,并隨著干預時間的延長而增加,效果明顯;傷口面積縮小,傷口愈合時間平均縮短6~7d,所有病例未出現傷口局部及全身的不良反應,值得推廣。
創傷感染;傷口;LED藍光;治療
創傷是當今危害人類健康的重大疾患,在全球居第4位,創傷傷口感染是影響患者生存和生活質量的主要因素之一,但過度使用抗菌藥物將增加內源性機會性感染的危險已成共識[1]。近年來,光動力治療廣泛應用于臨床,有報道波長為405~470mm的藍光具有廣譜的抗菌作用,同時也能促進傷口愈合[2]。為此,大坪醫院門診傷口護理中心自2015年10月-2016年4月采用藍光治療創傷性感染傷口,效果滿意。
臨床資料
1 一般資料 入選患者41例(1例因治療不足1周失訪剔除),其中男性24例,女性16例;年齡25~64歲,平均45歲。傷口持續時間(從出現傷口到入選本研究的時間)25~56d,其中物理性創傷傷口28例(包括皮膚挫裂傷、燙傷和皮膚放射性損傷共24例,擠壓傷1例和切割傷3例)稱為A型,生物性創傷傷口12例(包括狗咬傷3例、蚊蟲咬傷4例、貓咬傷2例、人咬傷3例) 稱為B型, 傷口大小初診時測量2.5cm×2.0cm~9.0cm×5.0cm。按首次換藥的先后順序編號后用電腦隨機分為觀察組和對照組,每組20例。兩組患者的性別、年齡、傷口情況比較差異無統計學意義(P>0.05),具有可比性,見表1。
入選標準:按照創傷的定義[3]和創傷性傷口的分類[3]選擇門診傷口護理中心常見的物理性創傷傷口(如皮膚挫裂傷、機械切割傷口、擠壓傷、燙傷、放射性損傷等),生物性傷口(動物或生物咬傷傷后),傷口深度至真皮層或以下,不及肌肉及骨骼、神經和肌腱組織,傷口面積≥2cm2,經細菌培養均存在不同程度感染,經常規清創、抗炎治療3周以上未愈者,健康情況良好,無基礎病。
排除標準:年齡<16歲或>75歲;嚴重的肝腎功能不全;有惡性腫瘤、免疫性疾病、糖尿病、低蛋白血癥(血清白蛋白<30g/L);妊娠、哺乳期婦女,特異性感染傷口(結核、破傷風、真菌等)、動脈潰瘍、不能按規定療程接受治療者。本研究獲得醫院倫理委員會授權批準,向患者解釋研究目的取得同意并簽署知情同意書。
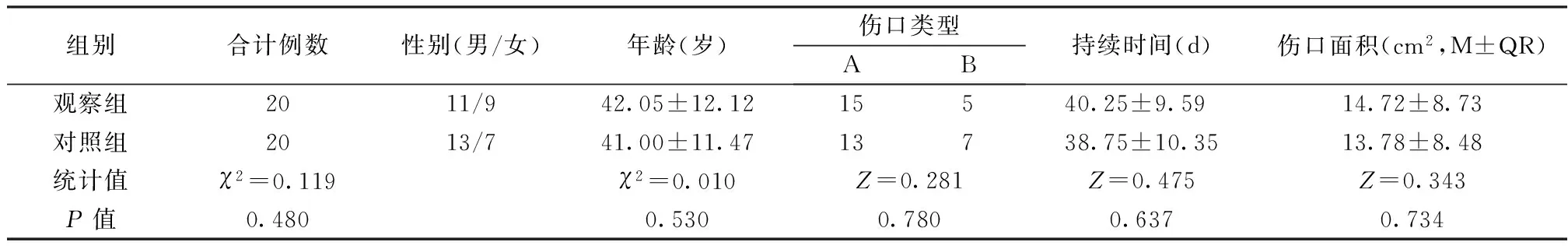
表1 兩組患者的基本情況比較
2 傷口的局部治療 傷口清創,剪去失活、壞死組織,生理鹽水反復清洗傷口,并取傷口基底部組織做細菌培養;清創后傷口顏色為紅色期予以照射干預。觀察組采用藍光治療儀(型號GF-RB43-A,武漢光福生物醫學工程有限公司生產) 照射傷口,藍光波長465nm,光斑面積260cm2,照射時藍光照射頭與傷口垂直,距離10cm,照射時間20min,每日1次,光照中患者佩戴專門的護目鏡。具體流程:安置舒適體位暴露傷口,揭開敷料即刻測量傷口面積與深度,生理鹽水沖洗傷口,行傷口分泌物細菌培養,生理鹽水再次沖洗傷口,干紗布拭干創面藍光照射20min。移去光源, 根據傷口滲液量、組織顏色、氣味和疼痛程度選擇敷料,如傷口組織灰暗伴有大量滲液和異味,選用含銀敷料抑制細菌生長和控制炎癥反應;如傷口組織紅潤,滲液量少,無異味,則選用促進肉芽生長的敷料;設定10d為一療程,照射1~2個療程。對照組除不用藍光照射外,換藥方法同觀察組直至傷口愈合。
3 觀察指標
3.1 傷口分泌物細菌培養及鑒定 每組傷口在干預的第4、6、8、10天采用無菌技術用無菌旋渦式沖洗傷口或用無菌棉簽清洗傷口后,去除表面腐肉或壞死組織,再用無菌棉簽按“Z”字法從傷口一端至另一端均勻涂抹傷口基底滲液,進行細菌培養,依據分泌物細菌培養結果,比較兩組患者治療第4、6、8、10天的細菌轉陰率。細菌轉陰率=(初次細菌陽性例數-治療后細菌陽性例數)/初次細菌陽性例數×100%。
3.2 傷口面積縮小率 每組傷口予干預的第4、6、8、10天采用直接測量技術測量傷口長和寬(cm)計算面積(cm2)和傷口面積縮小率。傷口面積縮小率=(初始面積-現有面積)/初始面積×100%。
3.3 傷口愈合時間 以傷口完全上皮組織覆蓋,3%雙氧水涂抹局部無氧化反應(陰性結果)為治愈標準,計算從入組第1天至傷口完全上皮化的時間。
3.4 不良反應 觀察患者照射后局部皮膚有無瘙癢、皮疹、色素沉著等不適反應;眼睛是否干澀等不適現象。
4 統計學分析 采用SPSS 18.0統計軟件進行分析,計量資料進行正態性檢驗和方差齊性檢驗,滿足正態性者根據滿足方差齊性與否使用獨立樣本t檢驗或t2檢驗,不滿足正態性者使用秩和檢驗;計數資料及率的比較采用χ2檢驗,檢驗水準a=0.05。P<0.05為差異有統計學意義。
5 結果
5.1 兩組傷口細菌轉陰率比較 治療前兩組陽性率比較,差異無統計學意義(P>0.05);治療第4、6、8、10天,兩組轉陰率比較差異明顯,具有統計學意義(P<0.05),見表2。
5.2 兩組患者各時間點創面面積縮小率比較 用創面面積縮小率來代替創面面積縮小情況,在第4、6、8、10天,兩組創面面積縮小百分比差異有統計學意義(P<0.01),從表3可以看出,觀察組傷口面積縮小率明顯高于對照組(干預主效應P<0.01),表明LED藍光照射觀察組能有效促進創面縮小,隨著時間的變化,組內面積縮小百分比率差異有統計學意義,干預因素和時間因素之間存在交互作用,見表3。
5.3 兩組患者創面完全愈合時間比較 觀察組患者創面完全愈合時間為(16.3±3.6)d,與對照組(23.5±4.05)d相比,差異有統計學意義(P<0.05)。
5.4 安全性評價 在干預期間,所有病例未出現傷口局部及全身的不良反應。
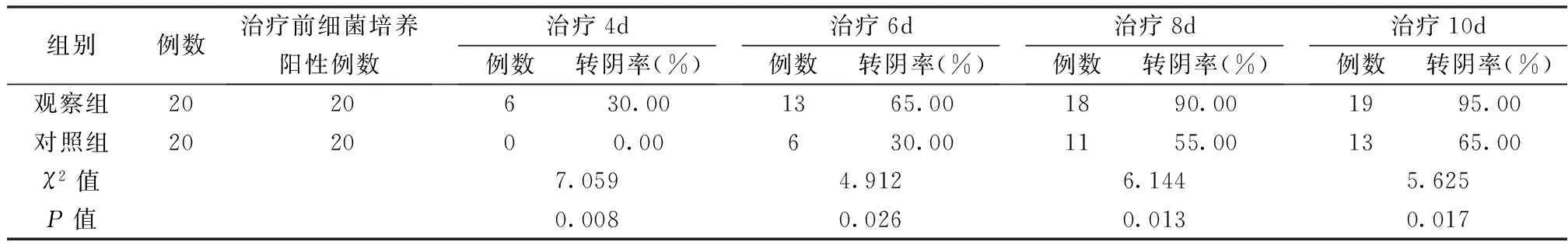
表2 兩組傷口細菌轉陰率比較
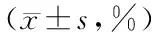
表3 兩組患者各時間點創面面積縮小率比較
兩組比較干預主效應F=77.788,P=0.000;時間主效應F=886.836,P=0.000;交互效應F=48.946,P=0.000;與對照組比較:aP<0.01
討 論
創傷性感染傷口為難治性傷口,傷口細菌的定值和感染是影響傷口愈合的重要因素之一,由于抗生素的篩選作用,傷口多合并多重耐藥菌感染,感染難以控制,愈合時間長,長期換藥給患者帶來身體和精神上的痛苦,如何有效干預是傷口處理中亟待解決的問題,尋找特定情景下的抗生素替代療法具有重要意義。
LED藍光是波長405~470nm的可見光,能直接將電能轉化為光能的光源,藍光殺菌機制與激活細菌內源生成的光敏卟啉有關[4]。 Hamblin等[5]用藍光照射幽門螺旋桿菌的7個菌株,殺菌率為99.9%,藍光還廣泛應用于痤瘡和新生兒黃疸的治療。Maclean等[6]的研究發現藍光能殺滅革蘭氏陽性和革蘭氏陰性菌。本研究對藍光對細菌轉陰率的影響進行了觀察,研究結果顯示,觀察組用藍光干預第4天,有6例轉陰,轉陰率為30.0%,而對照組轉陰率為0,并隨著干預時間的延長,藍光對細菌生長的抑制作用逐漸增強,觀察組轉陰率明顯升高,第10天達到95%,兩組比較差異有統計學意義(P<0.05)。由此可見,藍光可有效殺滅創傷性感染傷口細菌,且殺菌局限在細菌感染區域,不會影響其他的非感染部位。藍光的輻射強度可以很好地調整和監控,相對于抗生素來說,有很好的安全性[7]。光抗菌機制有別于紫外線,對正常組織細胞幾乎無毒性[8]。劉娜等[9]用藍光照射對健康人體晝夜節律的影響,同時評價其安全性,發現藍光對健康受試者生物節律的影響有效且安全。
藍光照射可以促進傷口愈合[7]。萬睿等[10]采用波長465nm的藍光對11例MRAS(耐藥金黃色葡萄糖球菌)感染的難愈性創面患者進行照射,結果11例患者創面均完全愈合。本研究采用隨機對照的方法,觀測藍光對創傷性感染傷口的影響,結果顯示,觀察組在藍光干預的不同時間段傷口面積縮小率明顯高于對照組(干預主效應P<0.01),并隨著治療時間的延長,傷口面積縮小率明顯增加,可推測與藍光的殺菌與抑菌有關。兩組愈合時間相比,觀察組比對照組提前6~7d,傷口愈合速度較對照組明顯加快(P<0.05),這與其他研究[11]結果相似,分析原因可能因為藍光殺滅了傷口定植菌,傷口局部炎癥反應減輕,白細胞及細菌對上皮細胞的破壞作用減少,間接促進了傷口愈合。
總之,LED藍光治療創傷性感染傷口是一種可行而有效的新方法,照射治療安全、無毒副作用,且能減少抗生素使用,防止耐藥菌產生,并能促進傷口愈合。但是,由于病種分布局限,樣本偏少,對細菌學研究不夠深入,未來需要擴大樣本量進一步研究藍光殺菌效果及促進傷口愈合的作用機制。
[1] Lazarus HM,Fox J,Lloyd JF,et al.A six-year descriptive study of hospital-associated infection in trauma patients:demographics,injury fetures,and infection pattems[J].Surg Infect,2007,8(4):463-473.
[2] Adamskaya N,Dungel P,Mittermayr R,et al.Light therapy by blue LED improves wound healing in an excision model in rats[J]. Injury,2011,42(9):917-921.
[3] 蔣琪霞,李曉華,彭青,等.三乙醇胺濕敷創傷性傷口的減痛效果研究[J].醫學研究生學報,2012,25(1):64-66.
[4] Nitzan Y,Kauffman M.Endogenous porphyrin production in bacteria by aminolaevulinic acid and subsequent bacterial photoeradication[J].Lasers Med Sci,1999,14(4):269-277.
[5] Hamblin MR,Viveiro SJ,Yan GC,et al.Helicobacter pylori accumulates photoactive porphyrins and is killed by visible light[J].Antimicrob Agents Chemother,2005,49(7):2822-2877.
[6] Maclean M, MacGregor SJ,Anderaon JG,et al.Inactivation of bacterial pathogens following exposure to light form a 405-nanometer light-emitting diode array[J]. Appl Environ Microbiol,2009,75(7):1932-1937.
[7] Fuku TM,Yoshiok AM,Satomur AK,et al.Specific-wavelength visible light irradiation inhibits bacterial growth of porpbyromonas gingiralis[J].J Periodontal Res,2008,43(2):174-178.
[8] Dai T,Gupta A,Murray CK,et al.Blue light for infectious diseases: propionibacterium acnes,helicobactepylori,and beyond[J].Drug Resist Updat,2013,15(4):223-236.
[9] 劉娜,張楠,文冰亭,等.單色LED藍光照射對健康人體晝夜節律的影響[J].中國組織工程研究與臨床康復,2009,13(30):5923-5926.
[10] Dai T,Gupta A,Murrag CK,et al.Blue light for infectious diseases: propionibacteriuma,Helicobacterpylori,and beyond[J].Drug Resistance Updates,2012,15(4):223-236.
[11] 萬睿,龐星原,歐陽山蓓,等.LED藍光照射治療MRSA感染創面的臨床研究[J].中國美容醫學,2014,23(7):554-555.
(本文編輯:郭 衛)
1009-4237(2017)09-0629-03
400042 重慶,第三軍醫大學大坪醫院野戰外科研究所門診傷口護理中心
王秀薇:Email:papaioy@126.com
R 63
B
10.3969/j.issn.1009-4237.2017.08.022
2016-04-29;
2017-05-25)

