銀鯽卵母細胞體外誘導成熟技術的建立
李 志 汪 洋 周 莉 李熙銀 張曉娟 周 劍 桂建芳
(中國科學院水生生物研究所淡水生態與生物技術國家重點實驗室, 武漢 430072)
銀鯽卵母細胞體外誘導成熟技術的建立
李 志 汪 洋 周 莉 李熙銀 張曉娟 周 劍 桂建芳
(中國科學院水生生物研究所淡水生態與生物技術國家重點實驗室, 武漢 430072)
研究以銀鯽為材料, 根據銀鯽(Carassius auratus gibelio)卵母細胞生發泡(Germinal vesicle, GV)邊移程度及剝離GV中減數分裂前期染色體的凝集狀態, 將銀鯽Ⅳ時相的卵母細胞分為GV0、GV1、GV2和GV3四個時期; 并進一步比較了分別處于這4個時期銀鯽卵母細胞體外誘導培養的成熟率、卵裂率和孵化率。結果表明, GV1期之后的卵母細胞均可有效進行體外誘導成熟, 可正常受精發育, 由于GV1期卵母細胞有較長時間用于顯微操作, 因此GV1期卵母細胞被選為進行體外誘導的最早時期的卵母細胞。以GV1期卵母細胞為研究材料, 摸索了銀鯽卵母細胞體外誘導成熟的適宜條件: 取GV1期的Ⅳ時相卵母細胞, 放置于pH 8.5、加有1 μg/mL孕酮激素(17α, 20β-dihydroxy-4-pregnen-3-one, DHP)的格氏平衡鹽溶液(Gey’s balanced salt solution, GBSS)中, 在23℃培養箱中體外誘導12h后, 將濾泡膜剝離后再進行人工體外授精, 其所獲胚胎的孵化率可達55.5%。此外, 將體外轉錄合成的帶GFP標簽的h2af1o mRNA注射到GV1期卵母細胞, 發現經顯微操作和體外誘導后不僅可以通過GFP綠色熒光信號活體觀察GVBD、受精、卵裂和早期胚胎發育的全過程, 而且誘導成熟的卵子仍可正常受精和胚胎發育。研究建立的銀鯽卵母細胞體外誘導成熟技術為銀鯽和其他魚類卵母細胞發育過程研究及其相關基因和細胞顯微操作提供了技術平臺。
銀鯽; 卵母細胞成熟; 體外誘導; 生發泡; 顯微注射
卵母細胞是高度分化的細胞, 它的發育、成熟和受精是生命發生的開端[1,2]。對其母源關鍵因子的研究將揭示調控這些生命發生基本過程的分子機制, 但由于這些母源因子是在卵母細胞體內成熟階段發揮作用, 因此對它們的研究需要突破卵母細胞體外成熟技術。在大多數脊椎動物中, 卵母細胞在進入減數分裂期, 會停滯于第一次減數分裂期的雙線期, 此時細胞核明顯變大, 稱為“生發泡Germinal vesicle, GV)期”[3]。在促性腺激素作用下, 卵母細胞可恢復第一次減數分裂, 發生生發泡破裂(Germinal vesicle broken down, GVBD)而成熟[5,6]。卵母細胞的體外成熟(in vitro maturation, IVM), 是指將卵巢中處于未成熟的生發泡期或生發泡破裂前期的卵母細胞, 在體外加入誘導物質經過適宜的條件培養, 促使它們完成減數分裂, 人工誘導成熟,并具備受精及胚胎發育的能力[7,8]。此項技術在哺乳動物中的研究較為多見, 是卵母細胞減數分裂、成熟、受精和早期胚胎發育研究的重要技術之一。在斑馬魚、鰻、泥鰍等少數魚類中也開展了相關研究[8—10], 結果均表明孕酮激素(17α, 20β-dihydroxy-4-pregnen-3-one, DHP)是體外誘導成熟最有效的荷爾蒙激素, 而且不同魚類卵母細胞的最適宜的體外誘導成熟系統存在差異[11—13]。譬如, 斑馬魚卵母細胞最適宜的誘導系統是在90%Leibovitz L-15(L-15)培養基(含0.5 mg/L的BSA, pH 9.0)中培養270min[8]; 鰻卵母細胞的體外培養液是格氏培養體系(pH 8.2), 不加BSA, 并在體外培養成熟前3—6h加入了前列腺素2a (PGF2a)[9]; 泥鰍卵母細胞是在75%L-15培養基(pH 9.0)中加入20%鯉卵巢液和人絨毛膜促性腺激素(Human Chorionic Gonadotropin, HCG)處理[10]。在上述研究中, 體外培養的卵母細胞的成熟度都是以其大小達到一定尺寸為標準[13], 均沒有從卵母細胞的生發泡和染色體的狀態進行評判。
銀鯽(Carassius auratus gibelio)是一種廣泛分布于亞歐大陸的多倍體魚類[14,15], 被證明經歷了兩輪連續的多倍化歷程[16], 且具有雌核生殖、兩性生殖和類雜種生殖等多重生殖方式[17,18]。這些特性使其成為一種開展發育遺傳學研究的獨特對象[19,20]。本實驗室已鑒定出一批與銀鯽卵子發生、卵母細胞成熟、受精和早期胚胎發育相關的重要基因, 并進行了表達特征研究和初步的功能分析, 為研究脊椎動物生殖方式及其調控機制提供了重要線索[21—27],但一些涉及卵母細胞早期發育的相關基因的功能研究需要在卵母細胞減數成熟前進行顯微操作, 并體外誘導成熟, 進行授精和發育。因此, 迫切需要建立適宜的銀鯽卵母細胞顯微注射和體外誘導成熟技術。目前, 有關銀鯽卵母細胞體外培養技術的研究報道較少, 且僅僅培養到GVBD期, 僅以第一極體排出作為卵母細胞成熟的形態學標志[28—30]。因此, 目前已報道的銀鯽卵母細胞體外培養技術還不足以進行母源因子及胚胎早期發育相關基因的功能研究, 仍然存在著很多技術問題需要解決。譬如, 如何解決平行實驗中選擇卵母細胞發育時相一致性; 進行顯微操作后的卵母細胞能否體外誘導成熟、能否受精和孵化。
本研究借鑒其他魚類體外成熟的培養系統, 并根據銀鯽卵母細胞自身的特點, 利用前期在實驗室建立的生發泡剝離技術, 建立了一種適合銀鯽卵母細胞顯微操作和體外誘導成熟技術。首先, 參照Lodde等[31]的研究將銀鯽IV時相的卵母細胞細分為GV0、GV1、GV2和GV3四個發育時期, 并對每個時期的卵母細胞進行體外培養的成熟率、卵裂率和孵化率的比較, 確定了可以進行體外誘導成熟的最早卵母細胞的發育時期為GV1期; 接著, 通過對不同培養條件下GV1期的卵母細胞的卵裂率和孵化率的分析, 確定了體外誘導銀鯽卵母細胞最適合的培養條件。此外, 對GV1期卵母細胞顯微注射GFP-zfh2af1o mRNA后, 在適宜體外培養條件下, 進行體外誘導成熟、授精, 并通過熒光示蹤觀察外源基因的表達情況。本研究建立的方法可為銀鯽卵母細胞減數分裂和成熟相關基因的功能研究提供技術支撐。
1 材料與方法
1.1 實驗材料
銀鯽雌性個體取自中國科學院水生生物研究所官橋實驗基地。在3月上旬到4月下旬之間的繁殖季節, 選取不同發育程度的雌性個體的卵巢用于分離卵母細胞。體外誘導卵母細胞成熟后, 選取成熟的興國紅鯉(Cyprinus carpio var. Singuonensis)為雄性親本, 每次采集新鮮的精液用于授精。
1.2 主要試劑及培養液配制
卵母細胞培養液格氏平衡鹽溶液(Gey’s balanced salt solution, GBSS)[29](7.25 g NaCl、0.41 g NaH2PO4、0.38 g KCl、0.95 g HEPES、1.0 g葡萄糖、0.147 g CaCl2、0.23 g MgSO4、0.1 g 1000 U青霉素、0.1 g硫酸鏈霉素, 配制1 L)分別配置成pH為7.5、8.0、8.5、9.0和9.5的梯度, 過濾除菌, 放置4℃冰箱備用。其中CaCl2和MgSO4需要配置母液, 按照MgSO4、CaCl2的順序依次往卵母細胞培養液格氏平衡鹽溶液中滴加, 以免產生沉淀。90%的L-15培養液按照Seki等[8]描述配置。每種培養液中均加入1 μg/mL孕酮激素。
1.3 適合體外誘導的銀鯽Ⅳ時相卵母細胞發育階段的篩選
在繁殖季節, 多數銀鯽卵母細胞處于Ⅳ時相,此時相的卵母細胞直徑在1—1.2 mm左右。為了細分銀鯽Ⅳ時相卵母細胞發育階段, 我們首先在無菌條件下用鑷子將銀鯽不同個體的卵巢取出后, 分別轉移至預熱至23℃的GBSS和L-15卵母細胞培養液中, 接著從中分離10顆左右的卵母細胞, 用透明液(甲醇∶乙酸=3∶1)在解剖鏡下檢查核(生發泡)的邊移情況。根據生發泡的位置將把銀鯽Ⅳ時相卵母細胞分為GV0、GV1、GV2和GV3四個時期[31],同時利用本實驗室已建立的生發泡剝離技術, 取對應時期卵母細胞的生發泡, 參照Zhang等[18,32]描述的方法對染色體進行DAPI染色, 并在激光共聚焦顯微鏡(Zeiss LSM710, 德國)下進行觀察和拍照。由于來自銀鯽同一個體的卵母細胞發育程度均一,因此我們可以根據上述分析結果獲得具有活性的、發育一致的分別處于GV0、GV1、GV2和GV3時相的卵母細胞。接著, 利用實驗室前期的銀鯽卵母細胞的體外誘導方法[30]對4個時期的卵母細胞分別進行誘導培養, 并統計成熟率, 每4h統計一次。
1.4 銀鯽卵母細胞體外誘導成熟條件的優化
選取處于GV1期的卵母細胞, 放置于6 mL的GBSS和L-15培養液的平皿(直徑30 mm、高度0.17 mm)中進行培養, 以每毫升培養10顆卵母細胞為宜。分別配制pH為7.5、8.0、8.5、9.0和9.5五個梯度, 每種梯度都加入1 μg/mL的DHP, 23℃培養誘導卵母細胞體外成熟。在體外誘導8h后開始每隔1 h進行成熟率的統計。
1.5 體外誘導卵母細胞卵裂率和孵化率的統計
卵母細胞經體外誘導后, 選透明的卵母細胞用尖鑷子剝去濾泡膜(圖 1)。連續在誘導培養液中剝離50顆卵母細胞后, 參照干法授精[33]完成體外受精;待受精卵發育至二胞期, 選分裂比較均勻的卵子統計卵裂率, 并追蹤至出苗期統計孵化率。誘導16h后停止每組的成熟統計和授精工作。
1.6 GV1期卵母細胞的顯微注射、體外誘導成熟和人工授精
首先按照本實驗室已報道的方法體外轉錄合成了帶GFP標簽的h2af1o mRNA[25,34], 接著按照每顆卵1—2 nL的劑量, 將GFP-zfh2af1o mRNA顯微注射到處于GV1期的卵母細胞中。注射針尖開口小于0.5 μm[35]。處于GV1期的卵母細胞膜薄而透明,核膨大明顯可見, 可以精確地注射到核的區域或附近。注射后的卵母細胞放置在pH為8.5加有1 μg/mL DHP的卵母細胞培養液GBSS中, 在23℃培養箱中體外誘導12h后, 剝離濾泡膜, 進行人工授精。其受精卵完全脫膜[35]后直接在熒光顯微鏡下追蹤, 觀察并拍照。
1.7 數據統計分析
成熟率=透明的卵母細胞數/體外誘導的總卵母細胞數×100%; 卵裂率=觀察到分裂均勻二胞的胚胎/經過人工授精的總胚胎數×100%; 孵化率=孵出的魚苗數/經過人工授精的總胚胎數×100%; 3次實驗數據采用SPSS軟件進行單因素方差分析, 數據間比較用Tukey’s法進行, 并利用GraphPad Prism 6作圖軟件繪制曲線或柱狀圖來顯示, 取P<0.05為差異顯著。
2 結果
2.1 不同發育階段Ⅳ時相卵母細胞體外誘導成熟的比較
為了確定可以進行體外誘導成熟的銀鯽卵母細胞的發育時期, 我們首先根據生發泡向受精孔遷移的位置和減數分裂前期染色體的凝集狀態, 將銀鯽Ⅳ時相卵母細胞分為GV0、GV1、GV2和GV3期; 接著我們將分別處于4個時期的卵母細胞按照孫敏等[30]描述的方法進行體外誘導培養, 統計卵母細胞的成熟率、卵裂率和孵化率。如圖 2所示, 處于GV0期的卵母細胞, 生發泡位于卵母細胞中部或稍邊移(圖 2A, GV0), 減數分裂前期染色體處于未凝聚狀態(圖 2B, GV0); 體外誘導培養8h成熟率為零, 培養10h開始發生GVBD, 培養到12h有14.3%的卵母細胞成熟, 但進行人工授精的胚胎卵裂率較低(<10%), 當增加培養時間至16h, 成熟率可達到63.16%, 卵裂率有37.5%, 繼續培養到24h, 成熟率和分裂率已有所下降, 均沒有胚胎能正常孵化出膜(圖 2C, GV0)。處于GV1期的銀鯽卵母細胞, 生發泡開始膨大, 明顯邊移(圖 2A, GV1), 減數分裂前期染色體開始濃縮變粗(圖 2B, GV1); 體外誘導4h開始發生GVBD, 成熟率約有64.5%, 卵裂率約有30%, 但求未見可孵化的胚胎, 隨著培養時間增加,成熟率和卵裂率也不斷提高, 培養到8h, 開始出現有少量孵化胚胎, 其孵化率約3%, 體外誘導培養12h后有大約30.6%的胚胎可以孵化出膜, 繼續培養到16h, 成熟率和分裂率也開始下降, 孵化率僅有7.8%(圖 2C, GV1)。當銀鯽卵母細胞發育到GV2期, 生發泡更靠近卵孔(圖 2A, GV2), 減數分裂前期染色體進一步的凝聚變粗(圖 2B, GV2); 體外誘導成熟時間有所縮短, 成熟率、卵裂率和孵化率都有所提高(圖 2C, GV2)。處于GV3期的卵母細胞的生發泡已靠近受精孔, 核膜已融合(圖 2A, GV3),減數分裂前期染色體濃縮的更粗更短(圖 2B, GV3); 卵母細胞發育越靠后, 到GVBD時期所用的時間越短, 卵裂率和孵化率越高。以培養12h為例,在GV3期的卵母細胞成熟率、卵裂率、孵化率分別提高到88.5%、68.7%和42.5%(圖 2C, GV3)。上述結果表明, GV1期之后的卵母細胞均可以有效進行體外誘導成熟, 并可正常受精發育, 孵化出苗; 由于GV1期在體外時間較長, 有利操作, 我們一般選GV1期作為體外誘導的最佳時期的卵母細胞。
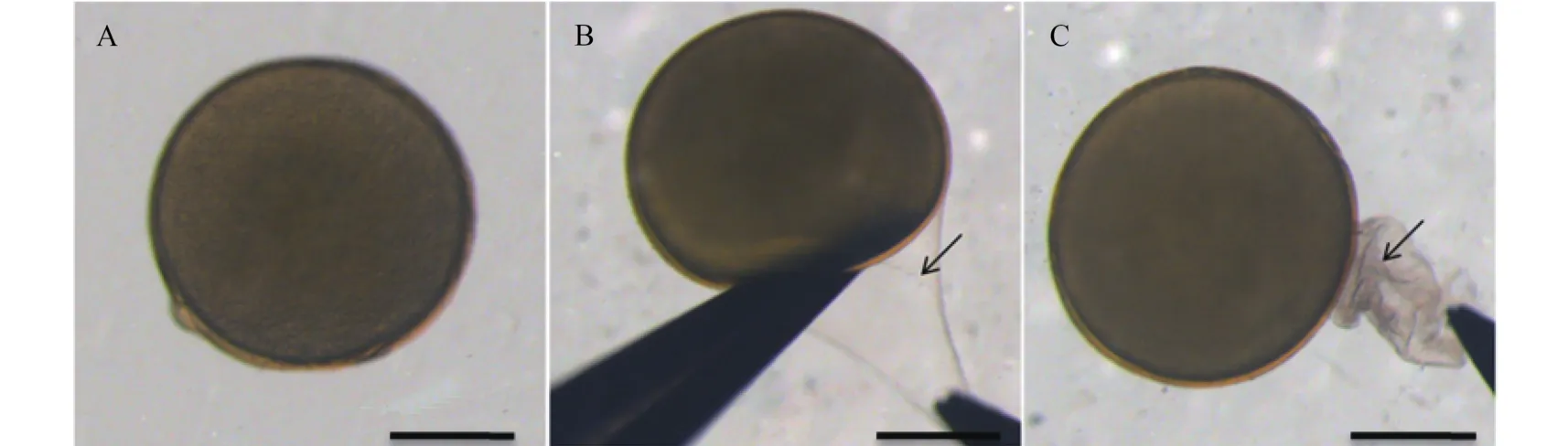
圖 1 體外誘導成熟銀鯽卵母細胞在解剖鏡下剝離濾泡膜的過程
2.2 最佳培養液和最佳誘導時間的確定
為了篩選適合銀鯽卵母細胞體外誘導的培養液, 我們配制了pH分別為7.5、8.0、8.5、9.0和9.5的GBSS和L-15培養液, 對GV1期銀鯽卵母細胞進行體外誘導, 并對誘導成熟的卵母細胞進行授精和胚胎發育狀態觀察。誘導13h后的結果表明, 在pH 8.5的GBSS培養液中, 銀鯽GV1期卵母細胞的平均成熟率、卵裂率和孵化率分別為91.3%、74.6%和42.5%, 均高于其他pH梯度的GBSS培養液中的結果(圖 3A)。在pH 9.0的L-15培養液中, 銀鯽GV1期卵母細胞的平均成熟率、卵裂率和孵化率分別為89.3%、71.0%和25.3%, 均高于其他pH梯度的結果(圖 3B)。對這2種不同培養液之間的比較表明, pH 8.5的GBSS培養液更適合銀鯽卵母細胞體外誘導, 其誘導成熟率和卵裂率略高于pH 9.0的L-15培養液的結果, 且孵化率顯著高于pH 9.0的L-15培養液的結果(P<0.05)。

圖 2 銀鯽Ⅳ時相卵母細胞不同發育階段(GV0、GV1、GV2和GV3)生發泡偏移情況(A)、減數分裂前期染色體狀態(B)和其體外誘導的成熟、卵裂和孵化能力(C)Fig. 2 Germinal vesicle (GV) migration (A), DAPI-stained premeiotic chromosome spread (B) and the in vitro abilities to induce maturation, fertilization and hatching (C) of gibel carp oocytes at GV0, GV1, GV2 and GV3 stagesA. 白色星號指示生發泡, 黑色箭頭指向卵孔; 比例尺=0.5 mm; B. 比例尺=20 μm。C. 橫坐標為體外誘導時間A. Germinal vesicle (GV) and micropyle are indicated by white asterisks and black arrows, respectively. Scale bar=0.5 mm; B. Scale bar =20 μm; C. Abscissa denotes in vitro induction time
接著, 我們選擇pH 8.5的GBSS培養液, 對銀鯽GV1期卵母細胞進行體外誘導成熟, 觀察并統計不同誘導時間后銀鯽卵母細胞的平均成熟率、卵裂率和孵化率。如圖 4所示, 在體外誘導4.5h后, 生發泡開始破裂, 卵母細胞開始透明; 誘導8h后, 超過90%的卵母細胞的生發泡都已破裂。3次重復實驗結果表明, 誘導8h至16h之間的成熟率沒有顯著性差異, 均高達90%; 但不同誘導時間的卵裂率和孵化率差異顯著, 誘導12h后卵裂率和孵化率均是最高的, 分別為81.2%和55.5%。誘導8h后的卵裂率僅有4.4%, 孵化率為0; 誘導16h后卵裂率為26.5%, 孵化率為3.4% (圖 4)。以上結果表明, 銀鯽GV1期卵母細胞體外誘導成熟的適宜條件是在pH 8.5的GBSS培養液中誘導12h。
2.3 體外誘導卵母細胞的顯微操作及其發育過程的示蹤觀察
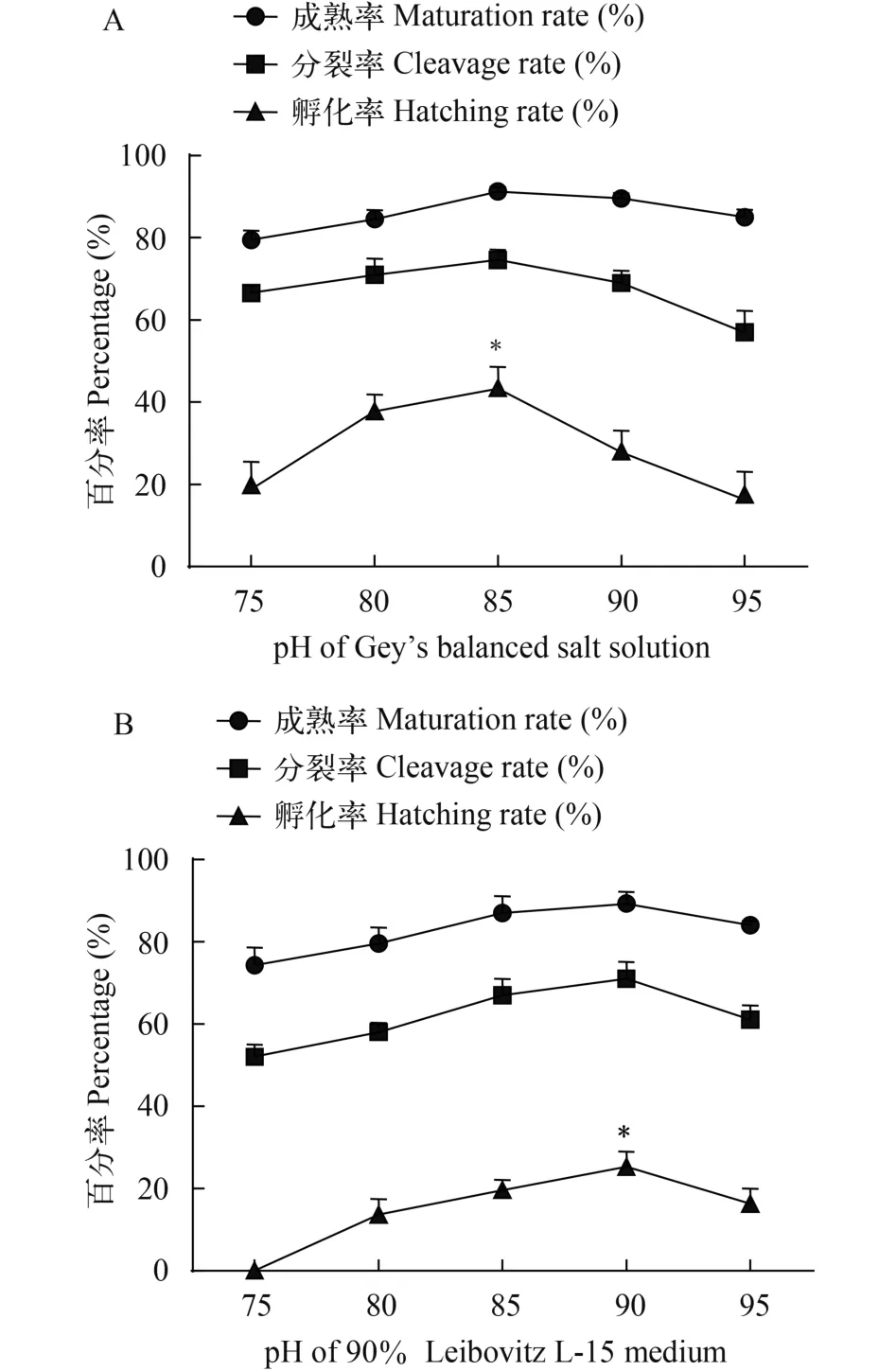
圖 3 處于GV1期的銀鯽卵母細胞在不同pH(pH 7.5—9.5)的GBSS培養液(A)和L-15培養液(B)中體外誘導的成熟率、卵裂率和孵化率的比較結果(*P<0.05)Fig. 3 The maturation rate (%), cleavage rate (%) and hatching rate (%) of gibel carp GV1 oocytes in vitro in GBSS cell-culture medium (A) and L-15 (B) cell-culture medium with different pH 7.5—9.0 (*P<0.05)
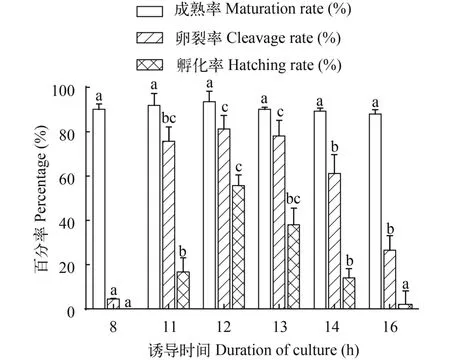
圖 4 銀鯽GV1期卵母細胞在GBSS培養液(pH 8.5)中體外誘導不同時間的成熟、分裂及孵化能力的比較Fig. 4 The ability of gibel carp GV1 oocytes to mature, fertilize, and hatch after cultured in GBSS medium (pH 8.5) for 8—16h相同顏色柱子上不同的字母表示差異顯著(P<0.05)Values with different subscripts within the same color criterion were significantly different (P<0.05)
為了進一步評價銀鯽卵母細胞體外誘導成熟的顯微操作能力及其相關技術, 我們將體外轉錄合成的帶GFP標簽的h2af1o mRNA[23,25]注射到GV1期卵母細胞, 然后在GBSS培養液(pH 8.5, 含1 μg/mL DHP)中體外誘導成熟, 經授精直到胚胎發育, 利用其表達產物定位于染色質可示蹤細胞核的特性[23,25],用其綠色熒光來示蹤評價顯微操作效果及其發育全過程。如圖 5所示, 在顯微注射后(圖 5A)體外誘導2h時, 核區開始出現綠色熒光信號(圖 5B); 誘導4h后, 胚泡破裂, 綠色熒光信號擴散到動物極(圖 5C);誘導12h后, 剝離濾泡膜進行人工授精, 待發育至一胞期時, 綠色熒光信號開始集中于細胞核(圖 5D);由于綠色熒光標示出細胞核, 發育至二胞期(圖 5E)、八胞期(圖 5F)、256胞期(圖 5G)、以致囊胚期(圖 5H)的胚胎清晰可辨。上述結果表明, 體外誘導的卵母細胞不僅可以通過熒光信號活體觀察GVBD、受精、卵裂和早期胚胎發育的全過程, 而且經過顯微操作后的卵母細胞, 仍可以正常被誘導減數分裂成熟以及正常受精和胚胎發育。
3 討論
卵母細胞成熟是相當復雜的生理過程, 包括細胞核和細胞質成熟, 但在體外誘導成熟過程中, 卵母細胞的發育程度和培養條件都可能造成細胞核和細胞質發育不同步而使卵母細胞的成熟受到影響[5—8]。在適宜培養條件下, 只有具備恢復減數分裂能力的卵母細胞才能夠成熟[4,5], 因此, 選擇合適發育程度的卵母細胞和適宜培養條件非常重要。
目前, 關于銀鯽卵母細胞體外誘導培養的報道不多。Wang等[28]報道在GBSS培養液加入0 .5 μg/mL的DHP, 24℃培養20h可以誘導66.7%的銀鯽卵母細胞發生GVBD。而孫敏等[30]將分離的銀鯽Ⅳ期卵母細胞在GBSS培養液(pH 7.4—7.7, 含1 μg/mL的DHP)中, 22—23℃體外培養6h后有90%的銀鯽卵母細胞發生GVBD。由此可見在這些銀鯽卵母細胞體外誘導成熟的報道中, 基于卵母細胞大小選擇IV時相卵母細胞進行體外誘導到GVBD的時間存在較大的差異[28—30], 這可能跟所選擇的IV時相卵母細胞本身發育階段不同有關。而且, 誘導減數分裂成熟的判斷是基于細胞學觀察GVBD的發生[36], 并沒有進行受精和孵化能力的驗證[8,28—30]。為了建立可重復的適合銀鯽卵母細胞顯微操作和體外誘導成熟的技術, 本研究首先通過卵母細胞的GV邊移程度和減數分裂前期染色體凝集狀態之間的關系, 將銀鯽IV時相卵母細胞進一步分為GV0、GV1、GV2和GV3四個時期。在此基礎上, 對每個時期的卵母細胞分別進行體外培養, 結果表明GV1期之后的卵母細胞均可以有效進行體外誘導成熟和受精, 且發育越靠后的卵母細胞, 到GVBD時所用的時間越短, 卵裂率和孵化率越高。因此, 卵母細胞發育程度是卵母細胞體外誘導獲得高成熟率、高卵裂率和高孵化率的重要條件之一[10]。該研究為銀鯽卵母細胞選擇上提供了依據, 增加了實驗的可重復性。
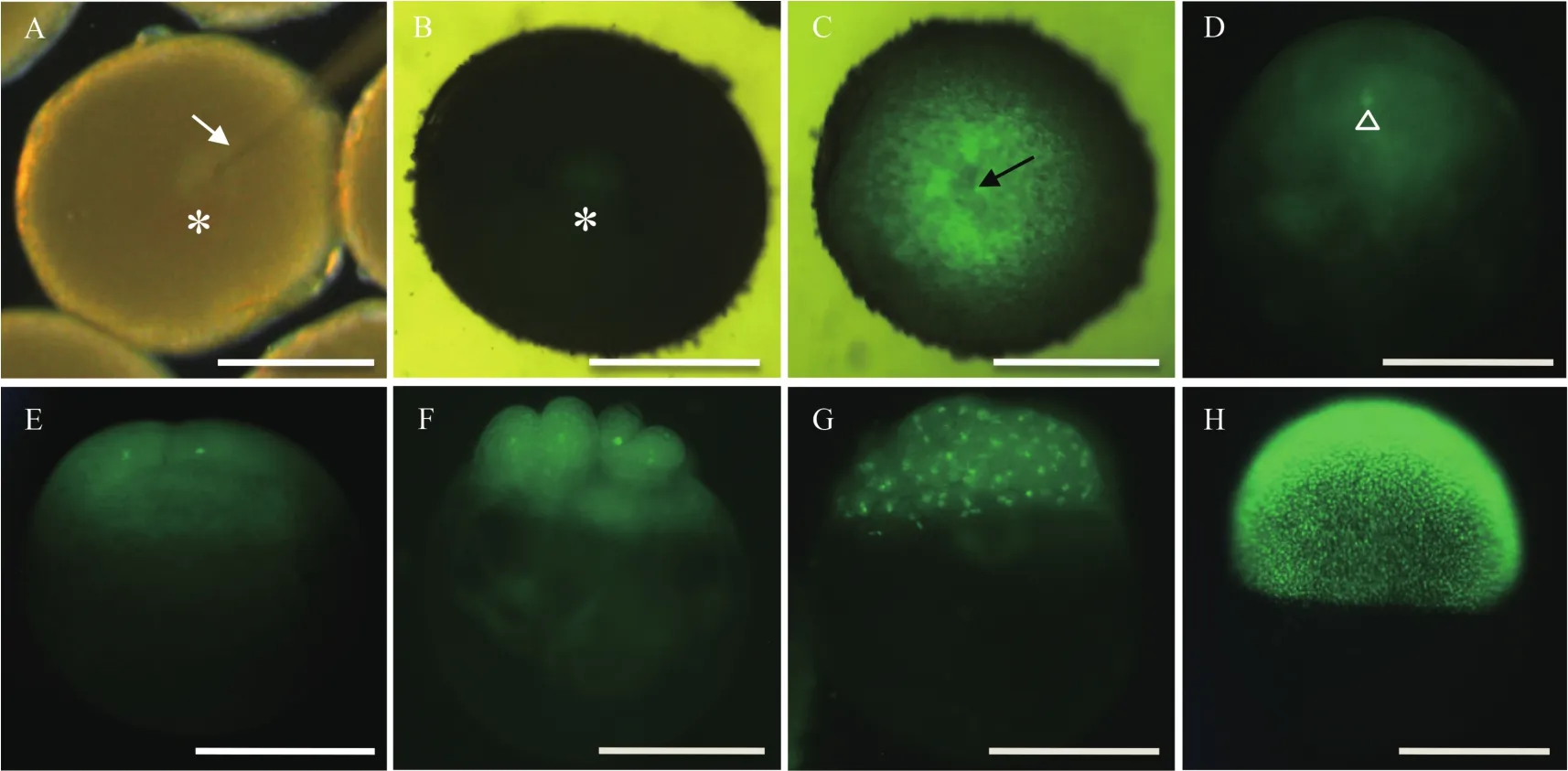
圖 5 GFP-zfh2af1o mRNA顯微注射到GV1期卵母細胞體外誘導成熟, 受精和胚胎發育的熒光示蹤
體外誘導卵母細胞減數分裂成熟后, 不僅需要通過GVBD來判斷卵母細胞是否成熟[28—30], 更重要的是需要驗證這些體外誘導成熟的卵母細胞是否具有受精能力和孵化出苗的能力[8]。在本實驗中,通過統計卵母細胞體外誘導成熟率、卵裂率和孵化率發現, 在GBSS(pH 8.5)培養液中誘導8—16h成熟率無顯著性差異, 但不同誘導時間的卵裂率和孵化率差異顯著, 其中誘導12h后卵裂率和孵化率均是最高的, 表明該誘導時間是卵母細胞體外誘導核質同步成熟的最佳時間點。在該時間點之前卵母細胞雖然已經透明但未達到核質同步成熟, 誘導時間太長可能導致卵子過熟, 從而影響受精能力和孵化能力。因此, 本研究在卵母細胞體外誘導成熟的判斷標準上, 不僅通過GVBD的發生來判斷卵母細胞的成熟, 又進一步通過受精和孵化能力的比較建立了判斷銀鯽卵母細胞體外誘導核質同步成熟的時間和條件。
本研究建立了銀鯽卵母細胞體外誘導成熟的適宜條件: 分離處于GV1期的卵母細胞, 對其顯微注射后放置于加有1 μg/mL DHP的GBSS溶液(pH 8.5)中, 在23℃培養箱中體外誘導12h, 即可獲得核質同步成熟的銀鯽卵母細胞。本研究可為分析魚類卵母細胞早期發育相關基因的功能提供技術平臺。
參考文獻:
[1]Gui J F. Roles of oocytes in studies on cell cycle regulation [J]. Bulletin of National Natural Science Foundation of China, 1996, 3: 173—178 [桂建芳. 卵母細胞在細胞周期調控研究中的貢獻. 中國科學基金, 1996, 3: 173—178]
[2]Xu H Y, Li M Y, Gui J F, et al. Fish germ cells [J]. Science China Life Science, 2010, 42(2): 124—138 [徐紅艷,李名友, 桂建芳, 等. 魚類生殖細胞. 中國科學生命科學, 2010, 42(2): 124—138]
[3]Chen D Y. Fertilization Biology [M]. Beijing: Science Press. 2000, 316—317 [陳大元. 受精生物學. 北京: 科學出版社. 2000, 316—317]
[4]Metz C B, Monroy A. Biology of Fertilization [A]. In: Masui Y (Eds.), Meiotic arrest in animal oocytes [C]. Florida: Academic Press. 1985, 189—219
[5]Judith K, Susan S. The C. elegans Research Community [A]. In: Greenstein D, (Eds.), Control of Oocyte Meioticmaturation and Fertilization [C]. WormBook. 2005, 1—12
[6]Skoblina M N. In vitro stimulation of oocyte ovulation in teleosts by gonadotropic and steroid hormones [J]. Ontogenez, 2009, 40(4): 245—253
[7]Nagahama Y, Yamashita M. Regulation of oocyte maturation in fish[J], Development Growth & Differentiation. 2008, 50(1): 195—219
[8]Seki S, Kouya T, Tsuchiya R, et al. Development of a reliable in vitro maturation system for zebrafish oocytes [J]. Reproduction, 2008, 135(3): 285—292
[9]Abe T, Ijiri S, Adachi S, et al. Development of an in vitro culture system for producing eel larvae from immature ovarian follicles in Japanese eel Anguilla japonica [J]. Fisheries Science, 2010, 76(2): 257—265
[10]Skoblina M N, Minin A A. Hormonal induction of in vitro maturation and ovulation of loach oocytes and obtaining egg cells capable of fertilization and development [J]. Russian Journal of Developmental Biology, 2015, 46(3): 159—167
[11]Zuberi A, Naeem M, Jalali S, et al. Relative in vitro effectiveness of several gonadal steroids on oocyte maturation in freshwater teleost Barilius vagra [J]. African Journal of Biotechnology, 2011, 10(55): 11772—11777
[12]Skoblina M N. In vitro stimulation of oocyte ovulation in teleostsby gonadotropic and steroid hormones [J]. Ontogenez, 2009, 40(4): 245—253
[13]Pang Y F, Ge W. Gonadotropin and activin enhance maturational competence of oocytesin the zebrafish (Danio rerio) [J]. Biology of Reproduction, 2002, 66(2): 259—265
[14]Jiang F F, Wang Z W, Zhou L, et al. High male incidence and evolutionary implications of triploid form in northeast Asia Carassius auratus complex [J]. Molecular Phylogenetics and Evolution, 2013, 66(1): 350—359
[15]Ivan J, Gui J F. Recent invasion and low level of divergence between diploid and triploid forms of Carassius auratus complex in Croatia [J]. Genetica, 2011, 139(6): 789—804
[16]Li X Y, Zhang X J, Li Z, et al. Evolutionary history of two divergent Dmrt1 genes reveals two rounds of polyploidy origins in gibel carp [J]. Molecular Phylogenetics and Evolution, 2014, 78: 96—104
[17]Gui J F, Zhou L. Genetic basis and breeding application of clonal diversity and dual reproduction modes in polyploidy Carassius auratus gibelio [J]. Science China Life Science, 2010, 40(2): 97—103 [桂建芳, 周莉. 多倍體銀鯽克隆多樣性和雙重生殖方式的遺傳基礎和育種應用.中國科學生命科學, 2010, 40(2): 97—103]
[18]Zhang J, Sun M, Zhou L, et al. Meiosis completion and various sperm responses lead to unisexual and sexual reproduction modes in one clone of ployploid Carassius gibelio [J]. Scientific Reports, 2015, 5: 10898
[19]Gui J F, Zhu Z Y. Molecular basis and genetic improvement of economically important traits in aquaculture animals (review) [J]. Chinese Science Bulletin, 2012, 57(19): 1719—1729 [桂建芳, 朱作言. 水產動物重要經濟性狀的分子基礎及其遺傳改良. 科學通報, 2012, 57(19): 1719—1729]
[20]Gui J F. Animal reproduction and physiology: from basis to application [J]. Science China Life Science, 2010, 40(2): 95—96 [桂建芳. 動物生殖與生理研究: 從基礎到應用. 中國科學生命科學, 2010, 40(2): 95—96]
[21]Dong C H, Yang S T, Yang Z A, et al. A C-type lection associated and translocated with cortical granules during oocyte maturation and egg fertilization in fish [J]. Developmental Biology, 2004, 265(2): 341—354
[22]Peng J X, Xie J L, Zhou L, et al. Evolutionary conservation of dazl genomic organization and its continuous and dynamic distribution throughout germline development in gynogenetic gibel carp [J]. Journal of Experimental Zoology Part B-Molecular and Developmental Evolution, 2009, 312(2): 855—871
[23]Wu N, Yue H M, Chen B, et al. Histone H2A has a novel variant in fish oocytes [J]. Biology of Reproduction, 2009, 81(2): 275—283
[24]Mei J, Chen B, Yue H M, et al. Identification of a C1q family member associated with cortical granules and follicular cell apoptosis in Carassius auratus gibelio [J]. Molecular and Cellular Endocrinology, 2008, 289(1—2): 67—76
[25]Yue H M, Li Z, Wu N, et al. Oocyte-Specific H2A variant H2af1o is required for cell synchrony before midblastula transition in early zebrafish Embryos [J]. Biology of Reproduction, 2013, 89(4): 82
[26]Sun M, Li Z, Gui J F. Dynamic distribution of Spindlin in nucleoli, nucleoplasm and spindle from primary oocytes to mature eggs and its critical function for oocyte-to-embryo transition in gibel carp [J]. Journal of Experimental Zoology, Part A, Ecological Genetics and Physiology, 2010, 313(8): 461—473
[27]Liu W, Li S Z, Li Z, et al. Complete depletion of primor-dial germ cells in an all-female fish leads to sex-biased gene expression alteration and sterile all-male occurrence [J]. BMC Genomics, 2015, 16: 971
[28]Wang Y F, Yang Z A, Yang S T, et al. Comparative studies on the changes in cyclin synthesis and MPF activity during oocyte maturation in vitro in gynogenetic and amphimicti ccrucian carps [J]. Acta Zoologica Sinica, 2000, 46(1): 71—80 [王玉鳳, 楊仲安, 楊書婷, 等. 在雌核發育和兩性生殖鯽魚體外培養的卵母細胞成熟過程中MPF周期合成中的變化和活性比較. 動物學報, 2000, 46(1): 71—80]
[29]Ding J, Jiang Y G. The preliminapy observation on inducing crcian carp carassius auratus gibello oocyte maturation in vitro [J]. Journal of Fisheries of China, 1994, 18(1): 60—71 [丁軍, 蔣一珪. 銀鯽卵母細胞體外誘導成熟的初步觀察. 水產學報, 1994, 18(1): 60—71]
[30]Sun M, Wang L, Gui J F. Expression characterization and functional analysis of oocyte-specific splindlin in gibel carp [J]. Acta Hydrobiologica Sinica, 2012, 36(4): 593—599 [孫敏, 王蘭, 桂建芳. 銀鯽Spindlin的功能分析和銀鯽雙重生殖方式的調控機制研究. 水生生物學報, 2012, 36(4): 593—599]
[31]Lodde V, Modina S, Galbusera C, et al. Large-scale chromation remodeling in germinal vesicle bovine oocytes: interplay with gap junction functionality and developmental competence [J]. Molecular Reproduction and Development, 2007, 74(4): 740—749
[32]Lutes A A, Neaves W B, Baumann D P, et al. Sister chromosome pairing maintains heterozygosity in parthenogenetic lizards [J]. Nature, 2010, 464(7286): 283—286
[33]Gui J F, Si Y D, Zhou L. Practical Breeding Technology of Allogynogenetic Gibel Carp [M]. Beijing: Jindun Publishing House, 2003 [桂建芳, 司亞東, 周莉. 異育銀鯽養殖技術. 北京: 金盾出版社. 2003]
[34]Zhong J X, Zhou L, Li Z, et al. Zebrafish Noxa promotes mitosis in early embryonic development and regulates apoptosis in subsequent embryogenesis [J]. Cell Death and Differentiation, 2014, 21(6): 1013—1024
[35]Li Z, Zhou L, Zhang J, et al. A fast and efficient microinjection method in the fertilized eggs of teleost fish with adhesive eggs [J]. Acta Hydrobiologica Sinica, 2016, 40(1): 67—82 [李志, 周莉, 張君, 等. 黏性卵魚類受精卵一種快速高效的顯微注射方法. 水生生物學報, 2016, 40(1): 67—82]
[36]Wu Q J, Gui J F. Fish Genetic Breeding Engineering [M]. Shanghai: Shanghai Scientific & Technical Publishers. 1999, 43—44 [吳清江, 桂建芳. 魚類遺傳育種工程. 上海: 上海科學技術出版社. 1999, 43—44]
DEVELOPMENT OF IN VITRO MATURATION TECHNOLOGY FOR GIBEL CARP OOCYTES
LI Zhi, WANG Yang, ZHOU Li, LI Xi-Yin, ZHANG Xiao-Juan, ZHOU Jian and GUI Jian-Fang
(State Key Laboratory of Freshwater Ecology and Biotechnology, Institute of Hydrobiology, Chinese Academy of Sciences, Wuhan 430072, China)
In vitro oocytes maturation is a key and efficient technology for gene and cellular micromanipulation in oocytes of fish. In this study, we used gibel carp oocytes as studying materials to develop an efficient in vitro induction maturation technology. Based on previously established germinal vesicle (GV) isolation and premeiotic chromosome preparation methods , four different stage oocytes including GV0, GV1, GV2 and GV3 were firstly distinguished by GV migration and premeiotic chromosome condensation status, and the maturation rate (%), cleavage rate (%) and hatching rate (%) were analyzed. GV1, GV2 and GV3 oocytes had the capacity for in vitro induction maturation, and GV1 oocytes were the optimal stage oocytes because they have longer time for micromanipulation. We found that the optimal induction conditions for GV1 oocytes in vitro were 12 hours at 23℃ in pH 8.5 Gey’s balanced salt solution(GBSS) with 1 μg/ml DHP (17α, 20β-dihydroxy-4-pregne-3-one), by which up to 55.5% hatching rate was reached from these stripped follicle membrane oocytes. Moreover, we injected the GFP-zfh2af1o mRNA into the GV1 oocytes, and found that the whole process of in vitro maturation, fertilization and embryo development of the micromanipulated GV1 oocytes could be tracked by the expression of GFP, and normal fertilization and embryo development could be produced from the induced mature eggs. Therefore, we established an efficient platform for studying oocyte development and gene and cellular micromanipulation in this fish.
Gibel carp; Oocyte; In vitro maturation; Germinal vesicle; Micromanipulation
Q-366
A
1000-3207(2017)05-0984-08
10.7541/2017.123
2016-07-08;
2016-11-04
中國科學院戰略性先導科技專項(XDA08030201)資助 [Supported by the Strategic Priority Research Program of Sciences (XDA08030201)]
李志(1980—), 女, 河南周口人; 實驗師; 主要從事魚類發育遺傳研究。E-mail: lizhi@ihb.ac.cn
桂建芳, E-mail: jfgui@ihb.ac.cn

