湛江沿海海洋微藻及其多糖、脂類和蛋白藻株多樣性研究
黃永梅楊曉紅蘭柳波詹靜婷羅 輝江黎明,
(1. 廣東醫科大學化學教研室, 湛江 524023; 2. 廣東醫科大學湛江市環北部灣海洋微生物研究開發重點實驗室, 湛江 524023; 3. 廣東醫科大學生物化學與分子生物學研究所, 湛江 524023)
湛江沿海海洋微藻及其多糖、脂類和蛋白藻株多樣性研究
黃永梅1,2楊曉紅1,2蘭柳波3詹靜婷1,2羅 輝1,2江黎明2,3
(1. 廣東醫科大學化學教研室, 湛江 524023; 2. 廣東醫科大學湛江市環北部灣海洋微生物研究開發重點實驗室, 湛江 524023; 3. 廣東醫科大學生物化學與分子生物學研究所, 湛江 524023)
從硇洲島和徐聞珊瑚礁自然保護區潮間帶采集的海水和沉積物樣品中分離培養海洋微藻, 篩選其中富含多糖、脂類或蛋白質的藻株。采用形態學觀察、18S rDNA序列比較及其系統發育分析法, 對分離培養的海洋微藻及其富含多糖、脂類或蛋白質的藻株進行分類鑒定和生物多樣性分析。分離、培養、鑒定并儲藏了189株海洋微藻, 歸屬于65個種, 分布于硅藻門(Bacillariophyta)、綠藻門(Chlorophyta)、定鞭藻門(Haptophyta)和紅藻門(Rhodophyta)的9綱、25目、30個科、38個屬; 其中多糖含量較高的46株海洋微藻, 分布于25個種, 20個屬; 脂類含量較高的46株海洋微藻, 分布于32個種, 15個屬; 蛋白含量較高的46株海洋微藻, 分布于28個種, 18個屬。結果表明硇洲島和徐聞珊瑚礁自然保護區潮間帶可培養的海洋微藻及其富含多糖、脂類和蛋白質藻株的物種多樣性豐富, 在新型藥物、活性天然產物、功能食品和飼料及其添加劑的發掘等方面具有良好前景。
硇洲島; 徐聞珊瑚礁自然保護區; 海洋微藻; 多糖; 脂類; 蛋白質; 多樣性
海洋微藻是生活在海洋環境中的一大類原核或真核微生物。它們可利用太陽能將水和CO2經光合作用轉變成多糖、蛋白質和脂類等生物大分子。已知的物種有30000多種, 據估算總數約為200000種[1]。一些在東亞和亞太部分地區長期食用的海洋微藻含有豐富的蛋白質[2]、脂類[3]和多糖[4]等營養物質, 已經或正在被廣泛用于新型保健食品、飼料、食品和飼料添加劑及生物能源等的產品的研究和開發[5,6]; 另有一些海洋微藻含有豐富的活性多肽、包括二十二碳六烯酸(DHA)和二十碳五烯酸(EPA)在內的多不飽和脂肪酸、硫酸酯多糖等活性次級代謝產物, 被認為在新型活性天然產物、藥物或藥物先導物、食品和飼料添加劑、化妝品等的發掘中有巨大潛力[7,8]。
微藻是單細胞或簡單的多細胞光合自養微生物, 只要是有陽光和少量營養鹽的地方就能夠生長繁殖, 可在海水、鹽田和營養貧瘠等不利環境下快速生長[9]。獲取適合當地環境和氣候條件的優良藻種是海洋微藻培養和使用的前提條件[10]。雖然國內外已建有了一些保存微藻種質資源的培養物保藏中心, 但目前公認的24000多種微藻物種中大約只有10%的微藻物種被成功地長期保存[8,11], 而許多自然環境中則存在著很多具有優良生物學特性的藻種有待發掘, 且使用當地藻種已被證明對當地環境和氣候條件等具有適應性強等明顯的優勢并可避免非當地物種入侵[12]。因此, 分析探討特定區域特定生態環境中海洋微藻, 尤其是富含多糖、脂類和蛋白質藻株的多樣性, 不僅有重要的生態學意義而且有良好的應用前景[6,8,13]。
硇洲島和徐聞珊瑚礁國家級自然保護區地處湛江沿海, 是目前國內受人類活動影響較小的熱帶、亞熱帶海島和珊瑚礁自然保護區, 其潮間帶蘊藏著豐富的海洋微生物資源[11,14]。研究的目的是篩選和分析硇洲島和徐聞珊瑚礁自然保護區潮間帶可培養的富含多糖、脂類或蛋白質的海洋藻微的多樣性, 為熱帶和亞熱帶海洋微藻資源的開發利用奠定基礎。
1 材料與方法
1.1 實驗材料
用于富含多糖、脂類和蛋白質藻株篩選及其物種多樣性分析的海洋微藻共189株, 其中118株為本研究組之前從徐聞珊瑚礁國家自然保護區(20°10′—20°27′N, 109°50′—109°24′E)潮間帶分離藻株(GenBank登錄號KU561102-KU561219)[11], 70株由本研究從徐聞珊瑚礁自然保護區和硇洲島(20°52′—20°56′N, 110°33′— 110°38′E)潮間帶采樣、分離和鑒定(GenBank登錄號為KY054925-KY054994), 紫球藻由廣東恒興飼料實業股份有限公司饋贈(GenBank登錄號為KY054995, 已在本地作為餌料養殖多年)。
1.2 研究方法
海洋微藻的富集、分離純化 采用本研究組之前報道的方法[11]進行。簡單說就是取2 g泥沙樣品懸浮于20 mL滅菌天然海水, 其上清液和海水樣品分別用100 μm的濾網過濾去除懸浮顆粒和浮游動物后, 取5 mL濾液轉移到裝有15 mL f/2-medium液體培養基[15](將f/2-medium營養液[15]與經0.45 μm濾膜過濾的自然海水1∶1000混合, 120℃, 20min高壓滅菌后冷卻至室溫)60 mL的錐形瓶中, 置于光照培養箱中, 在溫度(25±2)℃、光照強度3000 lx、光暗比12h∶12h條件下富集培養約7—10d。
富集培養液經細胞計數后分別稀釋成1個活細胞/μL, 取1 μL置于96孔培養板各孔的中央, 在倒置顯微鏡(10×10倍)下觀察, 找出并標記僅含有一個藻細胞的孔; 向含2個或2個以上藻細胞的孔中滴加10 μL f/2-medium液體培養基[15], 用微吸管將多余的細胞剔除或轉移到無細胞的小孔并標記為僅含1個藻細胞的孔; 各孔加入200 μL f/2-medium液體培養基[15]后, 將96孔板放置于光照培養箱中培養, 溫度為(25±2)℃, 光照強度3000 lx, 光暗比12h∶12h條件下培養約1周; 鏡檢確認單一藻細胞生長的孔, 并將孔中藻液轉移至裝有40 mL f/2-medium液體培養基[15]的100 mL錐形瓶中, 置入光照培養搖床, 在溫度(25±2)℃、光照強度3000 lx、光暗比12h∶12h、搖床轉速130 r/min的條件下培養7—10d。
微藻保存 取f/2-medium海水固體培養基[15]倒成試管斜面, 再向斜面內加入f/2-medium海水液體培養基[15](每1000 mL加入2.5 mL的2 mL 8萬單位的硫酸慶大霉素注射液), 使其漫過固體斜面形成固液雙相斜面培養基。取擴大培養約7d的藻種樣品, 8000×g離心5min棄上清, 將沉淀的藻細胞用少量液體培養基吹打均勻, 轉移至固液雙相斜面培養基中, 于光照培養箱中培養7—10d, 待長成一定量后放入4℃冰箱保存。4℃冰箱要定期開弱光以保證在低溫弱光的條件, 半年復蘇繼代一次[11]。
富含多糖藻株的篩選 采用硫酸蒽酮法[16],以葡萄糖為標準, 以已知多糖含量為12.55%的NZmm2w1藻株為陽性對照, 對所獲得的海洋微藻的多糖進行定量分析。取50 μL的新鮮藻液, 加入到96孔板中, 測定OD680值, 然后加入150 μL的0.2%硫酸蒽酮試劑, 在沸水浴中加熱3min, 冷卻到室溫, 用酶標儀在630 nm處測定OD值, 根據標以葡萄糖標準液制作的準曲線計算出多糖的相對濃度。
富含脂類藻株的篩選 采用一種基于96孔板的尼羅紅染色法進行。8000×g離心10min收集處于對數生長中晚期的海洋微藻, 用生理鹽水洗3次后再懸浮于生理鹽水; 測OD680后將微藻懸液調整至A680=0.8; 取各種微藻懸液100 μL, 一式3份, 加入到96孔板的孔中與400 μL 20% DMSO混勻; 各孔加入12 μL 100 μg/mL尼羅紅丙酮溶液, 混勻后置暗處35℃溫育6min; 微藻細胞中被尼羅紅染色的脂質可采用倒置熒光顯微鏡(Nikon eclipse TE2000-E inverted microscope)進行觀察并攝影記錄; 各孔的熒光強度采用酶標儀(Varioskan Flash Multimode Reader; Thermo-Fisher, USA), 選用530 nm激發波長和590 nm發射波長進行測定。
富含蛋白藻株的篩選 準確稱取2 mg冷凍干燥的微藻藻粉, 于玻璃勻漿器中, 加入100 μL 0.1 mol/L的PBS, 充分研磨藻粉, 使其細胞壁破碎完全后, 吸出置于2 mLEP管, 用900 μL 0.1 mol/L的PBS分3次洗滌玻璃勻漿器, 并吸出置于上述的EP管。在5000 r/min轉速下離心10min, 上清液按照BCA法蛋白定量試劑盒的說明進行蛋白質定量分析; 在562 nm波長下用紫外分光光度計測其吸光度值, 并根據標準曲線換算蛋白質的含量[13]。
微藻種屬鑒定及多樣性分析 取少量藻液滴于載波片并用盧戈式碘液固定, 于50i智能型正置顯微鏡上用100倍油鏡觀察微藻細胞的形態學特征并拍照記錄。
收集100 mg濕重對數生長中晚期的微藻, 用植物基因組DNA提取試劑盒提取基因組DNA作為模板, 用微藻18S rDNA特異性通用PCR引物對[17]擴增藻株18S rDNA序列, 擴增產物經1.5%瓊脂糖凝膠電泳分離后送至上海生工生物工程股份有限公司測序, 測序結果提交GenBank; 采用ClustalW2對測序結果進行兩兩比對, 排除相同序列; 采用Blast搜索軟件(http://www.ncbi.nlm.nih.gov/BLAST/)從GenBank公共數據庫中搜索出18S rDNA序列一致性最大的物種從而對藻株做出初步的鑒定; 用MEGA5.10軟件按照鄰接法聚類法[18](選擇Bootstrap檢驗值≥50%, 1000次重復) 構建藻株18S rDNA序列系統發育樹[11]。
2 結果
2.1 海洋微藻的分離純化
之前研究組已從徐聞珊瑚礁自然保護區潮間帶分離鑒定了118株海洋微藻[11], 本研究從徐文珊瑚礁自然保護區采集的樣品中分離出了56株微藻,從硇洲島分離的樣品中分離出了14株海洋微藻, 共分離、鑒定和收藏了188株海洋微藻, 加上紫球藻,共收藏了189株海洋微藻。
2.2 海洋微藻的鑒定及多樣性分析
各藻株的18S rDNA序列分析比對的結果顯示:獲得的189株海洋微藻歸屬微藻的4門, 9綱, 25目, 30科, 38屬, 65種; 優勢屬為雙眉藻屬(Amphora), 含39株, 占被分離藻種的20.6%, 與研究組之前的報道[11]一致; 其次為褶盤藻屬(Entomoneis), 含22株,占被分離藻株的11.6%(表 1)。微藻硅藻門(Bacillariophyta)海洋微藻共有154株45種22屬; 其中歸屬硅藻綱(Bacillariophyceae)的微藻134株, 占分離培養微藻的70.9%, 中鼓藻綱(Mediophyceae)微藻19株, 約占10.1%。綠藻門(Chlorophyta)海洋微藻共有29株15種12屬; 其中, 歸屬共球藻綱(Trebouxiophyceae)的微藻22株, 約占11.6%。定鞭藻門(Haptophyta) 海洋微藻共有5株4種3屬。紅藻門(Rhodophyta)只有1株(表 1)。65種海洋微藻的代表株在100倍油鏡下形態觀察見圖 1。
2.3 富含多糖海洋微藻分類及多樣性
采用硫酸蒽酮法[16]對獲得的藻株多糖含量進行分析和對藻株18S rDNA序列進行比對分析及系統進化樹構建(圖 2)的結果顯示: 189株海洋微藻中多糖含量較高(高于作為陽性對照的微擬球藻NZmm2W1的總糖量, 即高于藻體干重的12.55%,相當于0.45 μg/104cells)的46株高產多糖藻株(表1)歸屬25種, 分布于硅藻門(Bacillariophyta)、綠藻門(Chlorophyta)、定鞭藻門(Haptophyta)和紅藻門(Rhodophyta)的6綱、14目、16科、20屬; 其中優勢屬為褶盤藻/翼繭形藻屬(Entomoneis), 共8株, 占高產多糖藻株的17.4%; 其次為雙眉藻屬(Amphora),共7株, 占高產多糖藻株的15.2%。
多糖含量最高的3株微藻為Xmm16W4(克里格輻節藻: Stauroneis kriegeri)、Xmm16S2(小頭端菱形藻: Nitzschia capitellata)和DHmm1S3(俄克拉何馬綠藻: Picochlorum oklahomensis), 多糖含量依次為(2.57±0.01)、(1.94±0.03)和(1.59±0.03) μg/104cells。
2.4 富含脂類海洋微藻的分類及多樣性
采用基于96孔板的尼羅紅染色法對獲得的藻株脂類含量進行分析和對藻株18S rDNA序列進行比較及系統進化樹構建(圖 3)的分析結果顯示: 在189株海洋微藻中, 中性脂含量較高(高于作為陽性對照的小球藻NZmm3W1的脂含量, 即GC-MS測定值為藻體干重的11.74%, 相當于0.72 μg/104cells)的46株高產脂類藻株(表 1)歸屬32個種, 分布于硅藻門(Bacillariophyta)、綠藻門(Chlorophyta)和定鞭藻門(Haptophyta)的5綱,14目,11科,15個屬; 優勢屬為雙眉藻屬(Amphora), 含10株, 占富脂藻株的21.7%。
中性脂含量最高的8株微藻為Xmm16W4、Xmm19W1、Xmm10S2(克里格輻節藻: Stauroneis kriegeri)、Xmm19W2(劍形輻節藻: Stauroneis anceps)、Xmm20S4(纖細輻節藻: Stauroneis gracilior)、 Xmm18W1(新月細柱藻; Cylindrotheca closterium)、Xmm37W1(–: Nanochlorum eucaryotum)和Xmm16W1(–: Dickieia ulvacea)、中性脂含量為(2.11±0.01)—(3.61±0.03) μg/104cells。
2.5 富含蛋白海洋微藻分類及多樣性
采用BCA蛋白定量法[13]對獲得的藻株蛋白含量進行定量和對藻株18S rDNA序列進行比較及系統進化樹構建(圖 4)的分析結果顯示: 189株海洋微藻中蛋白含量較高(高于作為陽性對照的微擬球藻NZmm2W1的蛋白含量, 即高于藻體干重的10%)的46株高產蛋白藻株(表 1)歸屬于28個種, 分布于硅藻門(Bacillariophyta)、綠藻門(Chlorophyta)、定鞭藻門(Haptophyta)和紅藻門(Rhodophyta)的6綱,14目,15科,18個屬; 優勢屬為雙眉藻屬(Amphora), 含10株, 占富蛋白質藻株的21.7%。
蛋白含量最高的3株微藻為DHmm1W2(新月細柱藻; Cylindrotheca closterium)、Xmm30W2和DHmm2S4(咖啡型雙眉藻; Amphora coffeaeformis),蛋白含量依次為藻體干重的(20.47±0.41)%、(20.38±0.14)%和(19.82±0.20)%。
2.6 富含多糖、脂類和蛋白的海洋微藻
所獲得的189株海洋微藻中, 多糖、脂類物質和蛋白質含量相對都較高(同一藻株的多糖、脂肪酸和蛋白質分別高于藻體干重的12.55%、11.74%和10%)的藻株有8株(表 2); 舟形藻屬(Navicula)海洋微藻3株, 菱形藻屬(Nitzschia)海洋微藻有2株, 輻節藻屬(Stauroneis)、微眼藻屬(Minutocellus)和-(Nanochlorum)屬海洋微藻各1株(表 2)。其中, 藻株
Xmm16W4(克里格輻節藻: Stauroneis kriegeri)不僅蛋白質含量相對較高, 而且多糖和脂類的含量是所獲得的微藻中最高的。
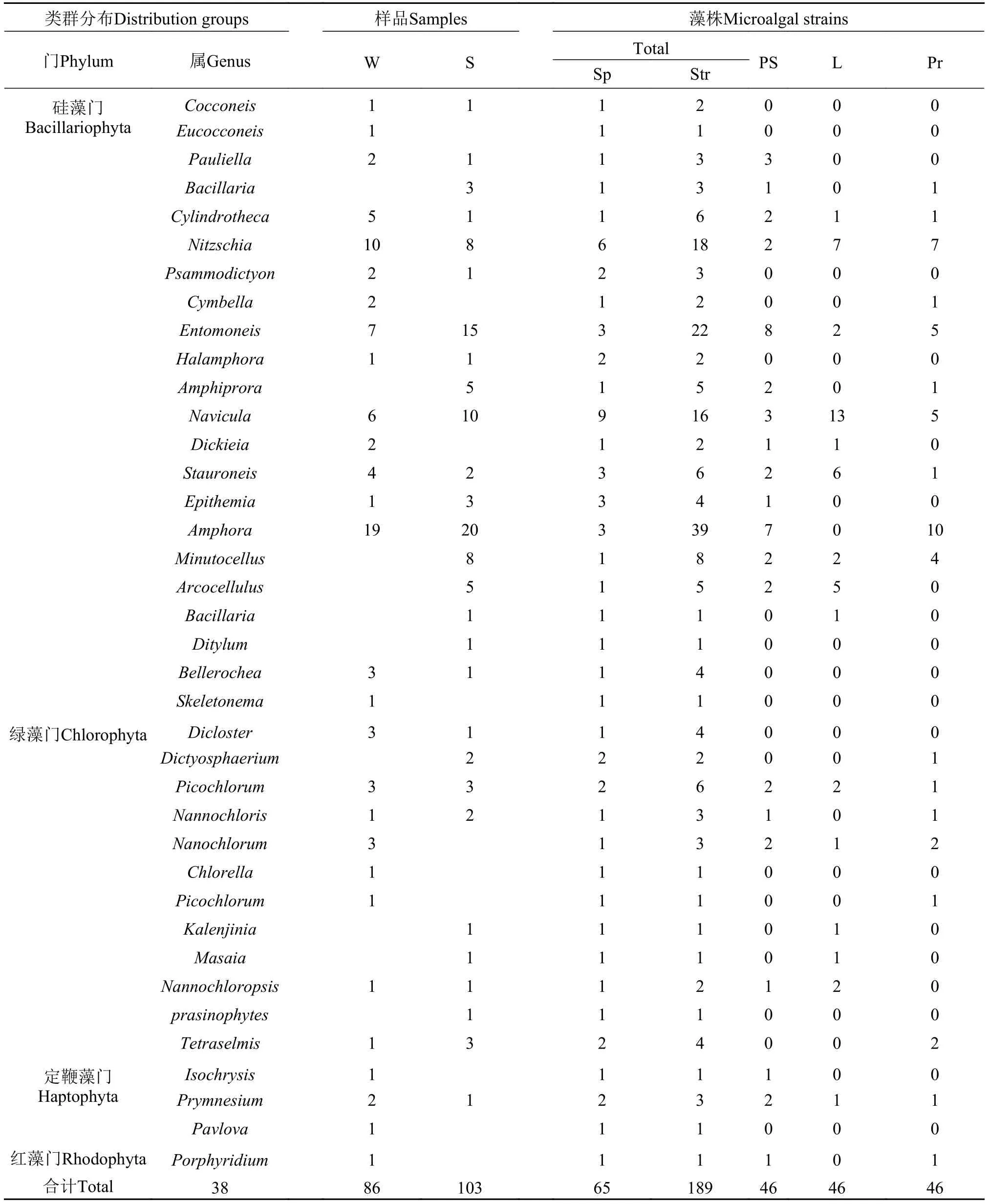
表 1 硇洲島和徐文珊瑚礁自然保護區可培養海洋微藻及其高糖、脂和蛋白藻株的類群分布Tab. 1 Groups distribution of the cultivated marine microalgae and the strains with higher polysaccharide, lipid and protein from Nao Zhou Island and Xuwen coral reef nature reserve

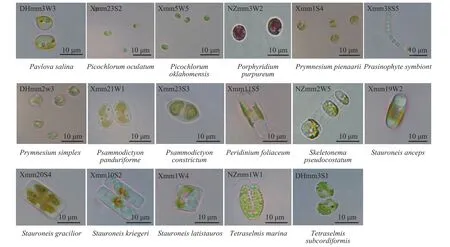
圖 1 湛江沿海潮間帶可培養海洋微藻Fig. 1 Light microscopic images of the marine microalgae from the intertidal zone along Zhanjiang coast
3 討論
湛江地區地處熱帶亞熱帶地區, 全年日照充足、氣溫適宜, 并擁有大量的灘涂濕地和適合海洋微藻生長的海水, 具備開展大規模培養海洋微藻進而研發微藻餌料和飼料、保健食品、飼料和食品添加劑、活性天然產物和藥物或藥物先導物、化妝品及生物燃料等的良好環境。研究表明, 獲取適合當地環境和氣候條件的優良藻種是海洋微藻培養和使用的前提條件之一[10]。本研究通過分析源自硇洲島和徐聞珊瑚礁自然保護區潮間帶的189株可培養的海洋微藻及其中富含多糖、脂類和蛋白質藻株的多樣性, 篩選出了一批富含多糖、脂類和蛋白的海洋微藻。在篩選出多糖含量最高的3株海洋微藻中, 克里格輻節藻(Stauroneis kriegeri)為輻節藻屬(Stauroneis)硅藻, 該屬已知藻種或藻株的適鹽性和適溫性都比較高, 多為能生長在鹽度和溫度變化幅度較大的高中潮區的底棲種類, 已有從中找到一些富含多糖和蛋白聚糖的藻種或藻株的報道[19]; 小頭端菱形藻(Nitzschia capitellata)為菱形藻屬(Nitzschia)硅藻, 一些藻株已被作為水產養殖的優質餌料使用, 或作為生物能源生產資源的候選藻種加以研發[4]; 俄克拉何馬綠藻 (Picochlorum oklahomensis)是一種適鹽性很強的單細胞綠藻, 最早是從美國俄克拉何馬州西北部的鹽平原國家野生動物保護區淺蒸發池的高鹽及營養貧瘠的環境分離得到[20], 后來發現一些藻株不僅包括多不飽和脂肪酸在內的脂類和蛋白含量較高, 而且生長快產量高, 已被用于生物能源和其他海洋微藻生物產品的研發[10]。大量研究表明, 海洋微藻多糖具有免疫增強和抗腫瘤、抗病毒、抗凝血、抗衰老、抗輻射及等多生物活性[4]。因此, 分離、培養、鑒定和貯藏這些適鹽性和適溫性都比較高的富糖海洋微藻, 預期在新型多糖類功能食品、藥品和抗輻射化妝品領域都有很好的應用前景。
其次, 在篩選出脂類含量最高的8株海洋微藻中, 3株克里格輻節藻(Stauroneis kriegeri)不僅脂類含量高, 多糖和蛋白質的含量也比較高; 新月細柱藻(Cylindrotheca closterium)是一種底棲硅藻, 其中一些藻株因被發現富含多糖, 包括胞外多糖和胞內多糖而被選用于海洋微藻多糖產品的研發[21,22], 但迄今未見有富脂新月細柱藻藻株的文獻報道; 劍形輻節藻(Stauroneis anceps)、纖細輻節藻(Stauroneis gracilior)和Dickieia ulvacea藻也都是硅藻, 但及至投稿前我們都沒能檢索到有關它們的文獻報道。目前, DHA和EPA等ω-3多不飽和脂肪酸已被世界各國批準作為飲料和食品添加劑、功能食品和藥物而廣泛用于預防和治療一些慢性疾病[8], 而富脂海洋微藻不僅被普遍認為是替代魚油作為ω-3多不飽和脂肪酸生產的理想資源, 而且也是替代油料植物用于生物燃料生產的重要資源。
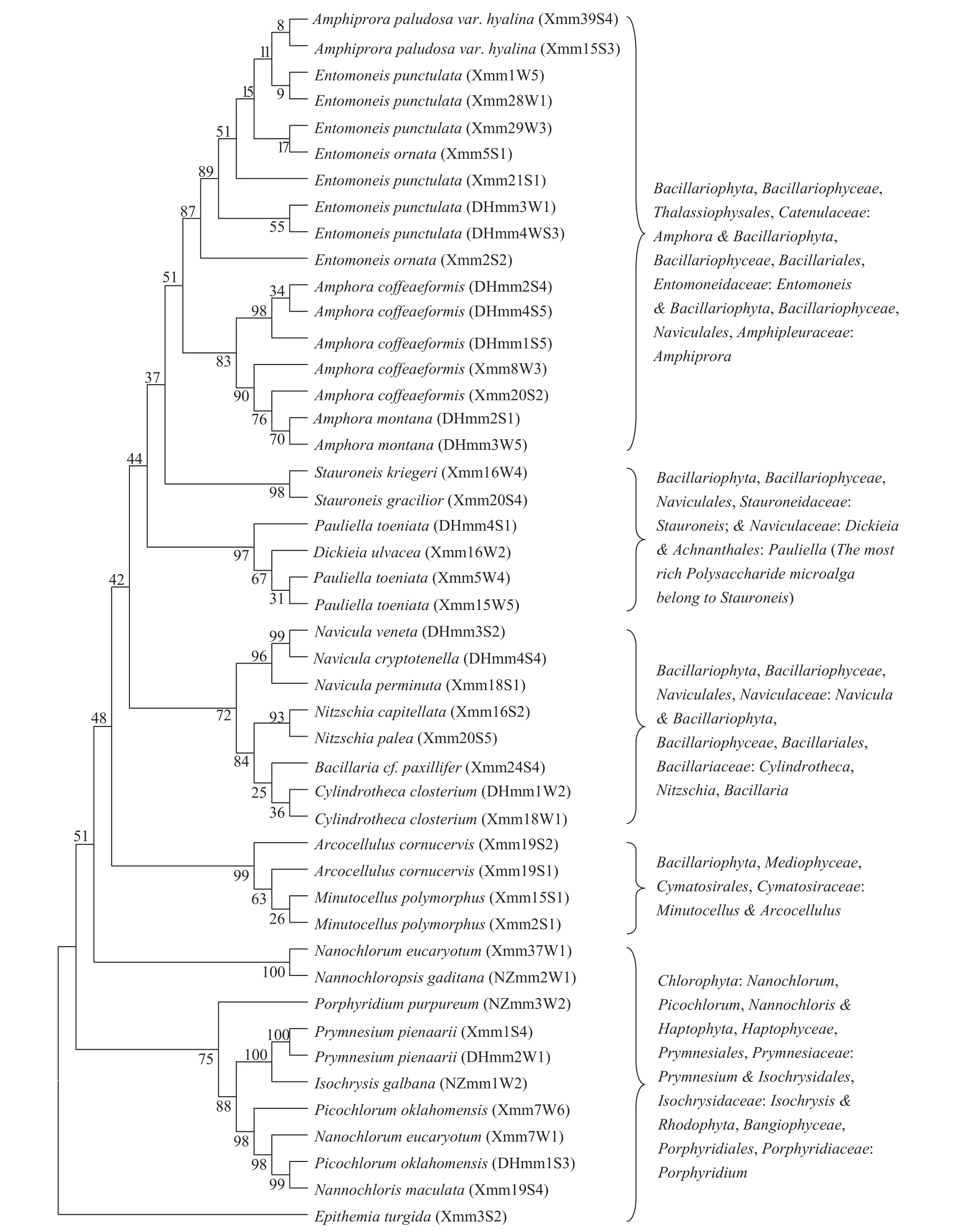
圖 2 高產多糖藻株與GenBank數據庫中相應藻種的18S rDNA序列系統進化樹
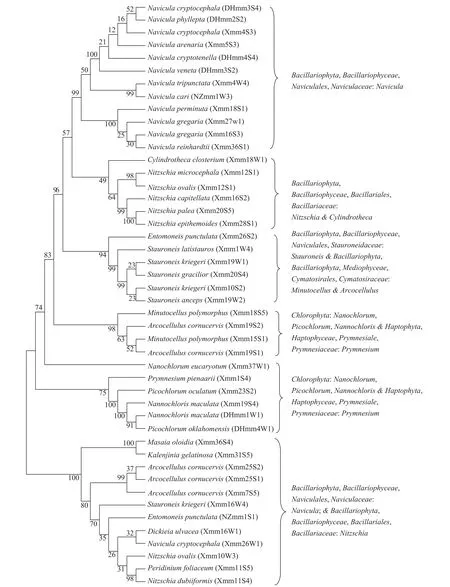
圖 3 富含脂藻株與GenBank數據庫中相應藻種的18S rDNA序列系統進化樹
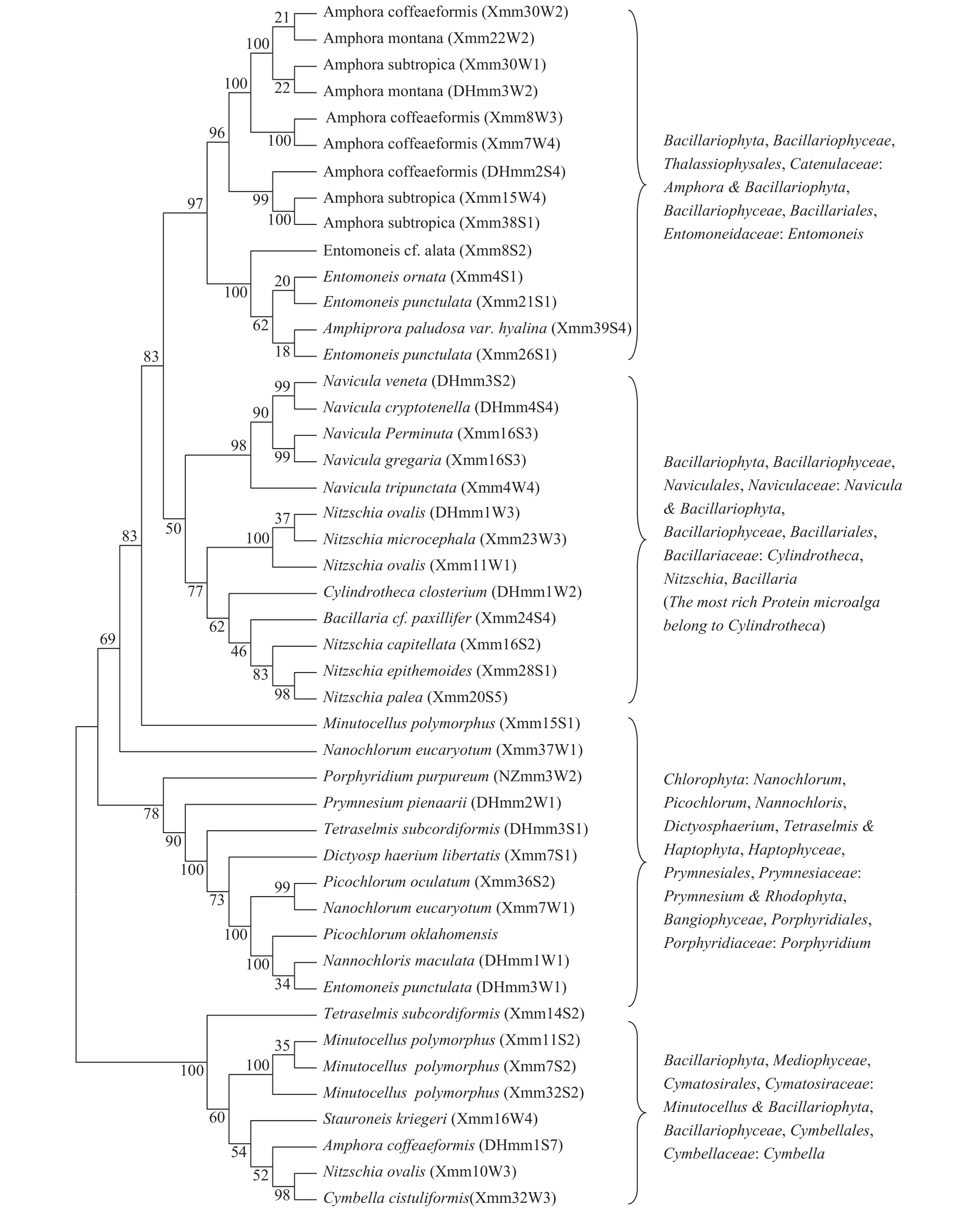
圖 4 富含蛋白藻株與GenBank數據庫中相應藻種的18S rDNA序列系統進化樹
此外, 在篩選出蛋白含量最高的3株海洋微藻中, 除新月細柱藻(Cylindrotheca closterium)外, 2株咖啡型雙眉藻(Amphora coffeaeformis)為雙眉藻屬(Amphora)硅藻, 已發現該屬的一些藻種或藻株富含脂類物質, 已被作為熱帶海參餌料而展開培養技術和營養價值分析, 另一些則作為抗氧化劑活性天然產物資源開展研究[23]。在篩選出多糖、脂類物質和蛋白質含量相對都較高的8株微藻中, 除克里格輻節藻(Stauroneis kriegeri)和小頭端菱形藻(Nitzschia capitellata)外, 舟形藻屬(Navicula)海洋微藻中的一些藻種或藻株, 如薩利娜舟形藻(Navicula salinarum), 有被作為海洋微藻多糖和抗氧化劑活性天然產物資源研究的報道[4,22,23]; 微眼藻屬(Minutocellus)微藻是在渤海海域褐潮期分離到的微型浮游生物之一, 也是在藻類毒性試驗中常使用的一種硅藻, 并有作為抗氧化劑活性天然產物資源研究的報道[24]; Nanochlorum eucaryotum藻是19世紀80年代發現的, 在海洋綠藻綱中少見并具有最小真核生物特性的球菌樣的物種, 在氮缺乏條件下通氣培養可檢測到類胡蘿卜素、角黃素和蝦青素[25]。本研究分離、培養、鑒定和貯藏的這類海洋微藻, 預期不僅可以作用海水水產養殖的優質餌料和飼料添加劑, 而且還可能在功能食品、食品和飼料添加劑、抗氧化劑活性等活性天然產物研發領域有良好的應用前景。
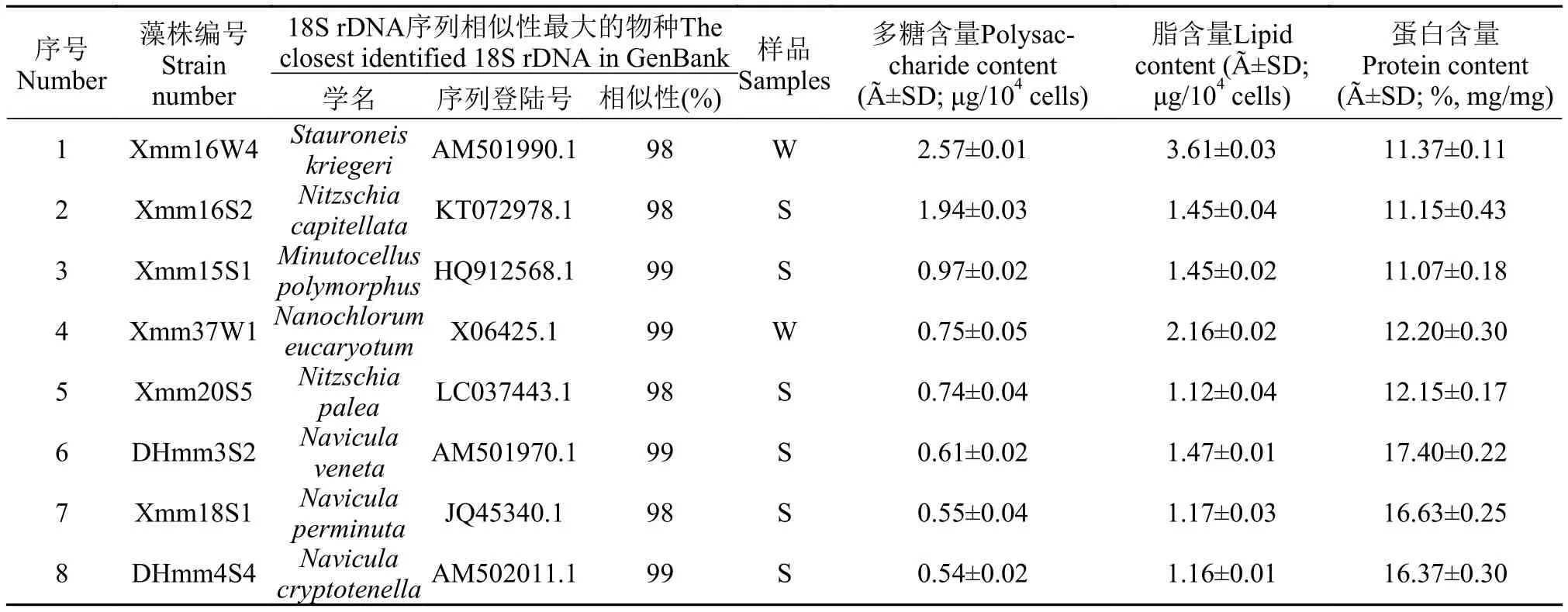
表 2 多糖、脂類和蛋白質含量都較高的海洋微藻藻株Tab. 2 The isolated microalgal strains with higher contents of polysaccharide, lipid and protein
[1]Barra L, Chandrasekaran R, Corato F, et al. The challenge of ecophysiological biodiversity for biotechnological applications of marine microalgae [J]. Marine Drugs, 2014, 12(3): 1641—1675
[2]Samarakoon K, Jeon Y J. Bio-functionalities of proteins derived from marine algae: A review [J]. Food Research International, 2012, 48(2): 948—960
[3]D’Alessandro E B, Antoniosi Filho N R. Concepts and studies on lipid and pigments of microalgae: A review [J]. Renewable and Sustainable Energy Reviews, 2016, 58(11): 832—841
[4]Raposo M F, de Morais R M, Bernardo de Morais A M. Bioactivity and applications of sulphated polysaccharides from marine microalgae [J]. Marine Drugs, 2013, 11(1): 233—252
[5]Suganya T, Varman M, Masjuki H H, et al. Macroalgae and microalgae as a potential source for commercial applications along with biofuels production: A biorefinery approach [J]. Renewable and Sustainable Energy Reviews, 2016, 55(2): 909—941
[6]Pulz O, Gross W. Valuable products from biotechnology of microalgae [J]. Applied Microbiology and Biotechnology, 2004, 65(6): 635—648
[7]Lauritano C, Andersen J H, Hansen E, et al. Bioactivity screening of microalgae for antioxidant, anti-inflammatory, anticancer, anti-diabetes, and antibacterial activities [J]. Frontiers in Marine Science, 2016, 68(3): 68—79
[8]Varfolomeev S D, Wasserman L A. Microalgae as source of biofuel, food, fodder, and medicines [J]. Applied Biochemistry and Microbiology, 2011, 47(9): 789—807
[9]Acreman J. Algae and cyanobacteria: isolation, culture and long-term maintenance [J]. Journal of Industrial Microbiology, 1994, 13(3): 193—194
[10]Zhu Y, Dunford N T. Growth and biomass characteristics of Picochlorum oklahomensis and Nannochloropsis oculata [J]. Journal of the American Oil Chemists’ Society, 2013, 90(6): 841—849
[11]Yiao X H, Huang Y M, Lan L B, et al. The biodiversity of culturable lipid-rich microalgae from Xuwen coral reef nature reserve [J]. Ecological Science, 2016, 35(4): 52—61 [楊曉紅, 黃永梅, 蘭柳波, 等. 徐聞珊瑚礁自然保護區可培養富脂海洋微藻的生物多樣性. 生態科學, 2016, 35(4): 52—61]
[12]Mata T M, Martins A A, Caetano N S. Microalgae for biodiesel production and other applications: A review [J]. Renewable and Sustainable Energy Reviews, 2010, 14(1): 217—232
[13]Duong V T, Ahmed F, Thomas-Hall S R, et al. High protein-and high lipid-producing microalgae from northern australia as potential feedstock for animal feed and biodiesel [J]. Frontiers in Bioengineering and Biotechnology, 2015, 53(3): 1—10
[14]Cui L J, W J, Lü Y N, et al. Biodiversity analysis of marine fungi producing extracellular fibrinolytic activity enzymes from the intertidal zone along Zhanjiang coast [J]. Microbiology China, 2016, 43(7): 1448—1461 [崔麗嬌,王潔, 呂應年, 等. 湛江沿海潮間帶產胞外纖溶活性酶類海洋真菌的生物多樣性分析. 微生物學通報, 2016, 43(7): 1448—1461]
[15]Harrison P J, Berges J A. Marine Culture Media [M]. In: Andersen R A (Eds.), Algal Culture Techniques. London: Elsevier Academic Press. 2005, 21—34
[16]Leyva A, Quintana A, Sanchez M, et al. Rapid and sensitive anthrone-sulfuric acid assay in microplate format to quantify carbohydrate in biopharmaceutical products: method development and validation [J]. Journal of the International Association of Biological Standardization, 2008, 36(2): 134—141
[17]Zhang S, Liu P H, Yang X, et al. Isolation and identification by 18S rDNA sequence of high lipid potential microalgal species for fuel production in Hainan Dao [J]. Biomass and Bioenergy, 2014, 66(7): 197—203
[18]Saitou N, Nei A M. The neighbor-joining method: a new method for reconstructing phylogenetic trees [J]. Molecular Biology and Evolution, 1987, 4(4): 406—425
[19]McConville M J, Wetherbee R, Bacic A. Subcellular location and composition of the wall and secreted extracellular sulphated polysaccharides/proteoglycans of the diatom Stauroneis amphioxys Gregory [J]. Protoplasma, 1999, 206(1—3): 188—200
[20]Annan J N. Growth and photosynthesis response of the green alga, Picochlorum oklahomensis to iron limitation and salinity stress [J]. International Journal of Plant Physiology and Biochemistry, 2014, 6(1): 7—18
[21]Staats N, Stal L J, Mur L R. Exopolysaccharide production by the epipelic diatom Cylindrotheca closterium: effects of nutrient conditions [J]. Journal of Experimental Marine Biology and Ecology, 2000, 249(1): 13—27
[22]Staats N, De Winder B, Stal L, et al. Isolation and characterization of extracellular polysaccharides from the epipelic diatoms Cylindrotheca closterium and Navicula salinarum [J]. European Journal of Phycology, 1999, 34(2): 161—169
[23]Lee S H, Karawita R, Affan A, et al. Potential of benthic diatoms Achnanthes longipes, Amphora coffeaeformis and Navicula sp. (Bacillariophyceae) as antioxidant sources [J]. Journal of Food Science and Nutrition, 2008, 13(3): 166—175
[24]Walsh G E, McLaughlin L L, Yoder M J, et al. Minutocellus polymorphus: A new marine diatom for use in algal toxicity tests [J]. Environmental Toxicology and Chemistry, 1988, 7(11): 925—929
[25]Geisert M, Rose T, Bauer W, et al. Occurrence of carotenoids and sporopollenin in Nanochlorum eucaryotum: a novel marine alga with unusual characteristics [J]. BioSystems, 1987, 20(2): 133—142
STUDIES ON THE DIVERSITY OF MARINE MICROALGAE AND THE STRAINS WITH HIGH POLYSACCHARIDES, LIPIDS AND PROTEINS ALONG ZHANJIANG COASTAL AREAS
HUANG Yong-Mei1,2, YANG Xiao-Hong1,2, LAN Liu-Bo3, ZHAN Jing-Ting1,2, LUO Hui1,2and JIANG Li-Ming2,3
(1. Chemistry Teaching and Research Section, Guangdong Medical University, Zhanjiang 524023, China; 2. The Key Lab of Zhanjiang for R&D Marine Microbial Resources in the Beibu Gulf Rim, Zhanjiang 524023, China; 3. Institute of Biochemistry and Molecular Biology, Guangdong Medical University, Zhanjiang 524023, China)
Marine microalgae were isolated from seawater and sediment samples collected from the intertidal zone of NaoZhou Island and Xuwen Coral Reef Nature Reserve, and identification and diversity of their strains with high contents of polysaccharides, lipids and proteins were analyzed by microalgal morphological observation, and sequence comparison and phylogeny analysis based on microalgal 18S rDNA sequences. A total of 189 strains of marine microalgae were isolated, cultured and identified, which represent 66 species distributed in 38 genera, 30 families, 25 orders, 9 classes, and belong to Bacillariophyta, Chlorophyta, Haptophyta and Rhodophyta of microalgae. Amongst, 46 strains with higher polysaccharide content belong to 25 species, and 20 genera, and 46 strains with higher lipid content represent 32 species belonging to 15 genera; and another 46 strains with higher protein content represent 28 species from 18 genera. It is concluded that the diversity of cultivable marine microalgae species and their strains with high content of polysaccharides, lipids and proteins is high from NaoZhou Island and Xuwen Coral Reef Nature Reserve, which possessed huge potential for exploring new drug or active natural products, functional food and fodder, and additives for food and fodder.
Naozhou Island; Xuwen coral reef nature reserve; Marine microalgae; Polysaccharide; Lipid; Protein; Biodiversity
10.7541/2017.135
2016-10-25;
2017-04-16
湛江市環北部灣海岸特色微藻生物資源產品研發重點實驗室(2012E02)資助 [Supported by the Key Lab of Zhanjiang for R&D Marine Microbial Resources in the Beibu Gulf Rim (2012E02)]
黃永梅(1988—), 女, 廣東羅定人; 碩士研究生; 研究方向為海洋微藻的開發利用。E-mail: 727148105@qq.com
羅輝, 男, 教授, 研究方向為海洋微生物資源開發與利用。E-mail: gdmuluohui@139.com; 江黎明, 男, 主任技師; 研究方向為海洋微生物資源開發與利用; E-mail: lmjiang@gdmc.edu.cn
Q949.2
A
1000-3207(2017)05-1080-11

