苜蓿鐮刀菌根腐病病原菌的分離鑒定與致病性分析
叢麗麗, 康俊梅, 張鐵軍, 龍瑞才, 楊青川*
(1.中國農業科學院北京畜牧獸醫研究所, 北京 100193; 2.青島農業大學動物科技學院, 山東 青島 266109)
紫花苜蓿(MedicagosativaL.)是世界上分布最廣泛的多年生豆科牧草,由于較高的產量和優良的品質使之享有“牧草之王”的美譽[1]。它的另一優勢是一次種植可利用多年,但因利用年限較長,根腐病已成為產量下降和植株衰敗的一個極其重要的原因。該病害是世界性病害,幾乎在所有苜蓿產區都有發生,據估計,每年全世界由該病造成的產量損失在20% 左右,有些嚴重發生的地塊甚至達到40%[2-3]。隨著種植面積的增加和種植年限的延長,病害問題會越來越嚴重,不僅降低了苜蓿的產量,還降低了品質,有些甚至失去了加工和利用價值,同時也會給奶業帶來隱患,因為根腐病的主要致病菌如鐮刀菌屬(FusariumLink ex Fr.)的三線鐮孢菌(F.tritinctum)以及腐皮鐮孢菌(F.solani)等菌種可以產生毒素[2]。其中,玉米赤霉烯酮(zearalenone, ZEN)和脫氧雪腐鐮刀菌烯醇(deoxynivaleno, DON)是較為常見、影響較大的兩種毒素[5]。ZEN具有較強的生殖發育、免疫和細胞毒性,對腫瘤的產生也有一定影響[6];DON對人畜具有高度危害性,可致急性中毒癥狀[7]。如果牛羊等家畜采食了含有這些毒素的苜蓿飼料,不僅對家畜本身帶來了影響,而且也會間接對消費者帶來傷害。因此,苜蓿根腐病致病菌的分離鑒定對后續的防治及抗病品種的培育具有重要意義。
由鐮刀菌引起的苜蓿根腐病迄今已在加拿大、美國、新西蘭、日本、澳大利亞等許多國家有所報道[8-13]。該病對紫花苜蓿生長的各個時期均可造成嚴重危害。2003年,李敏權[14]等對甘肅定西苜蓿根腐病的病原研究中發現了3種鐮刀菌,即尖孢鐮刀菌(F.oxysporum)、銳頂鐮刀菌(F.acuminatum)和半裸鐮刀菌(F.semitectum),這是我國首次對該病病原系統的研究報道。
過去我國關于苜蓿根腐病的研究一直集中在田間癥狀、防治等方面,對病原系統的研究報道不多。另外,鐮刀菌是真菌中最難鑒定和最具經濟價值的屬之一,其形態復雜,又易受外界環境影響發生變異,通過形態學觀察很難準確鑒定到種。本試驗在形態學觀察的基礎上,結合分子生物學手段,確保致病菌鑒定的準確性。本研究擬通過對河北廊坊、內蒙古臨河和山西陽高縣栽培苜蓿的田間調查、致病菌的分離鑒定,確定苜蓿鐮刀菌根腐病的主要病原,為指導根腐病的田間防治提供依據。
1 材料與方法
1.1 材料來源與準備
對河北省廊坊市、內蒙古臨河和山西陽高縣栽培2年以上的苜蓿田定點調查,觀察根腐病的田間癥狀。采集具有典型癥狀的鐮刀菌根腐病病株標樣帶回實驗室分離鑒定。為了能分離優勢致病菌,采樣后迅速進行病原菌的分離和鑒定。
1.2 病原菌的分離純化
病斑處切取約5 mm×5 mm的小塊組織,用75%的酒精處理30 s,0.1%的升汞處理3 min,無菌水沖洗3~5次。PSA培養基上,25°C暗培養4 天,挑取菌絲于PSA培養基上純化3次。再經過MGA培養基純化3次后通過在水瓊脂(WA) 平板上單孢梯度稀釋分離法進一步純化到種。將單孢分離純化的鐮刀菌接到PSA的試管斜面培養基中4°C保存,每6個月轉管一次,用于后續的菌種鑒定。
1.3 病原菌形態學觀察
參考王拱辰的《常見鐮刀菌鑒定指南》以及Booth《鐮刀菌屬》的方法進行菌種鑒定[15-16]。25°C培養4 d后,依據PSA培養基上的培養性狀,包括菌落形態和色澤及菌落生長速度;由于部分鐮刀菌株在PSA培養基和MGA培養基很難長孢子,所以本試驗通過VBC[17]和SNA[18]限定營養缺乏培養基上對大、小分生孢子的有無,分生孢子的形態及產生方式,厚垣孢子的有無以及著生方式等特征進行形態鑒定。
1.4 分子生物學鑒定
為了鑒定的準確性,在形態學特征鑒定的基礎上對分離菌株的核糖體基因內轉錄間隔區域 (rDNA-ITS)和翻譯延長因子1α基因(TEF-1α)序列進行擴增。取PSA培養基培養10 d的氣生菌絲,根據Simon G. Edwards[19]的方法提取基因組DNA。RDNA-ITS區域采用通用引物ITSl (5’-TCCGTAGGTGAACCTGCGG-3’) 和ITS4 (5’-TCCTCCGCTTATTGATAT- GC- 3’)PCR擴增。TEF-1α序列采用通用引物ef1(5’-ATGGGTAAGGAGGACAAGAC-3’)和ef2(5’-GGAAG TACCAGTGATCATGTT-3’)進行擴增。擴增產物回收純化,連接到pEASY-T1載體中并轉化大腸桿菌DH5α,陽性克隆送交上海英俊生物技術公司測序。DNAMAN軟件對測序結果進行剪切分析,剪切后在線比對分析。
1.5 進化樹的構建
獲得的RDNA-ITS序列和TEF-1α的序列分別與GenBank數據庫(http://www.ncbi.nlm.nih.gov/blast)和鑒定鐮刀菌的數據庫FUSARIUM-ID[20](http://isolate.fusariumdb.org/) 中的鐮刀菌的rDNA-RDNA-ITS和TEF-1α序列進行比較, 利用MEGA 5軟件進行聚類分析,構建系統發育樹。
1.6 致病性鑒定
參照Wang等[21]的接種方法,6個錐形瓶中分別放置200粒大小均勻的燕麥種子,加水浸泡過夜,除去多余水分,高壓滅菌2次。每個瓶中分別加入4個直徑1 cm的接種菌株的瓊脂塊。直到燕麥種子完全接種鐮刀菌后備用(約3周)。選擇飽滿健康的‘中苜2號’種子,75%的酒精消毒10 min,滅菌水洗5次后置于培養皿中催芽1天,播于直徑15 cm (高度13 cm)的盆中,營養土∶蛭石∶石英砂體積比為3∶1∶1,每盆15株,培養箱中培養(25℃光照/20℃黑暗,相對濕度80%)。待出苗10天后,每盆定苗10株,3個重復,每個重復30株。待植株培養40天后,將提前準備好的燕麥接種于植株地下1 cm 根頸處,每株接種2粒,不接菌的為對照。接種85 d后觀察病害情況。根據病斑占根系面積的百分比進行病害分級。分級標準為:0級,無癥狀;1級,根部輕度變色,根部壞死面積在1%~30%;2級,根部嚴重變黑褐色,壞死面積在30%~60%;3級,主根基本壞死,側根較少,壞死面積60%~100%。統計發病率(Disease incidence,DI)和病害嚴重指數(Disease severity index,DSI)。
DI(%)=(病株數/總株數)×100
DSI(%)= ∑(各級病株數×該級代表值)/(調查總株數×最重級別代表值)× 100
接種85 d后,切取5 mm×3 mm感病根組織,70%乙醇消毒1 min,無菌水漂洗3次后接種于PSA平板上進行分離和純化,并采用上述形態學觀察和分子鑒定的方法與最初的接種物進行比較和鑒定。
2 結果與分析
2.1 病原的分離純化
分離具有代表性鐮刀菌菌株6個,分別命名為C1,C2,C3,C4,C5和L1。其中河北廊坊分離的菌株為C1,內蒙古臨河分離的菌株為C2和C3,山西高陽縣的為C4,C5 和L1。
2.2 病原的形態學鑒定
C1,C2,C3,C4,C5和L1菌株根據在 PSA,MGA,VBC和SNA培養基上的形態特征,初步鑒定如下:
C1:PSA培養基上,氣生菌絲叢卷毛狀(圖1-A),培養基底部為青黑紅色,表面粉紅至白色,隨著生長天數的增加,變成棕色或紅棕色;氣生菌絲有隔,且具有側生分枝(圖1-E)。 在MGA培養基上呈白色絮狀菌落(圖1-B),不易產生小型分生孢子和大型分生孢子;SNA培養基上菌落不規則(圖1-C),產生大量的小型分生孢子(圖1-F),多呈長橢圓型,2.5~7.1 μm×1.7~3.5 μm;在VBC促孢培養基上,中心白色周圍黃色的特殊菌落(圖1-D),能產生大孢子(圖1-G),鐮狀至彎曲、紡錘形,1端銳尖,多為3隔,17.0~30.6 μm×3.0~5.0 μm。
C2:PSA培養基上氣生菌絲叢卷毛狀,培養基底部為深黑紅色,表面中心為黃棕色,向外為粉紅色至白色(圖2-A);在MGA培養基上呈白色絮狀菌落(圖2-B);菌絲少有隔,分支較多(圖2-E);SNA培養基表面呈粉紅色(圖2-C),可產生大量的小型分生孢子(圖2-F),小孢子長橢圓形或倒卵形,2.5~6.8 μm×1.7~3.2 μm,培養14天后可觀察到串生的厚垣孢子,球形或橢圓形(圖2-H);在VBC培養基上呈桃紅色(圖2-D),該培養基上大孢子稍彎曲或梨形,多為1隔(圖2-G),17.4~29.8 μm×3.5~5.0 μm。
C3:PSA培養基基部灰藍色至無色,周圍為白色,氣生菌絲絨毛狀(圖3-A),表面有明顯的環狀紋,氣生菌絲少隔,單軸分支(圖3-E);MGA培養基為白色菌落,棉絮狀(圖3-B);在VBC培養基上呈白色菌落(圖3-D),產生的大型分生孢子兩端較鈍圓,鐮狀或棒狀,1~3隔,16.4 ~30.7 μm × 3.2~4.8 μm(圖3-G);SNA培養基上菌落為白色,氣生菌絲稀疏(圖3-C),小型分生孢子長橢圓形或腎形,2.5~8.2 μm × 1.8~2.9 μm(圖 3-F)。
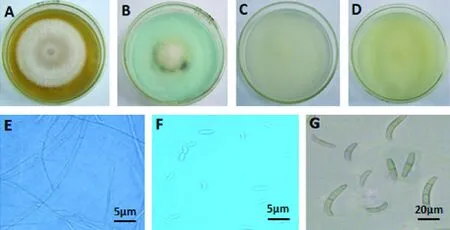
圖3 菌株C3的形態特征Fig.3 The morphological characteristics of strain C3
C4:PSA培養基菌落為白色,氣生菌絲較稀疏(圖4-A),菌絲有隔,單軸分支(圖4-E); MGA培養基上生長較慢,呈白色菌落(圖4-B);VBC培養基上呈不規則的白色菌落(圖4-D),大型分生孢子短而粗,腎形或棒狀(圖4-G),兩端較鈍圓,1隔,17.4~34.7 μm×3.2~5.8 μm;SNA培養基上表現為白色絮狀菌落(圖4-C),小型分生孢子長橢圓形、卵形,3.1~8.0 μm×1.6~3.8 μm(圖 4-F)。
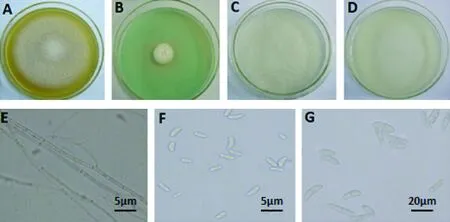
圖4 菌株C4的形態特征Fig.4 The morphological characteristics of strain C4
C5:PSA培養基上菌落呈白色,菌落基部培養基呈無色或乳黃色,氣生菌絲稀疏(圖5-A);菌絲多隔(圖5-E);MGA培養基上呈白色絮狀菌落(圖5-B);在VBC培養基上呈白色稀疏菌落(圖5-D),大型分生孢子鐮狀(圖5-G),1隔,14.4~25.7×3.4~5.5 μm;SNA培養基上呈白色菌落(圖5-C),產生的小型分生孢子橢圓形、卵形,大小差異較大,2.0~7.2 μm×1.6~3.8 μm(圖5-F)。
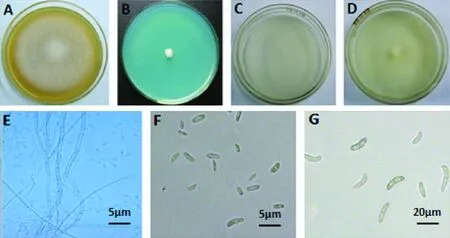
圖5 菌株C5的形態特征Fig.5 The morphological characteristics of strain C5
L1:PSA培養基上氣生菌絲白色,絨毛狀,邊緣整齊(圖6-A),菌落培養后期中央基部白色變為紫灰色;MGA培養基上白色菌落(圖6-B);SNA培養基上菌落為白色(圖6-C),產生的小型分生孢子無隔、棒狀、少數梨形,2.0~7.5×1.0~2.5 μm(圖6-F);菌絲有隔和分支(圖6-E);VBC培養基上菌落為白色(圖 6-D),大型分生孢子微彎,鐮刀形,2~5個隔膜(圖6-G),20~36.3×3.8~5.0 μm,以單瓶梗或復瓶梗假頭狀產孢(圖6-H)。
2.4 鐮刀菌的分子生物學鑒定
2.4.1分離鐮刀菌菌株rDNA-ITS和TEF-1α片段的克隆 6個菌株的rDNA-ITS序列大約為560 bp (圖 7-A),TEF-1α序列大小約為 700 bp (圖7-B)。將擴增產物純化后連接到T載體,經抗性篩選和菌液PCR鑒定(圖7-C,D),將陽性單克隆送交上海英俊生物公司測序。
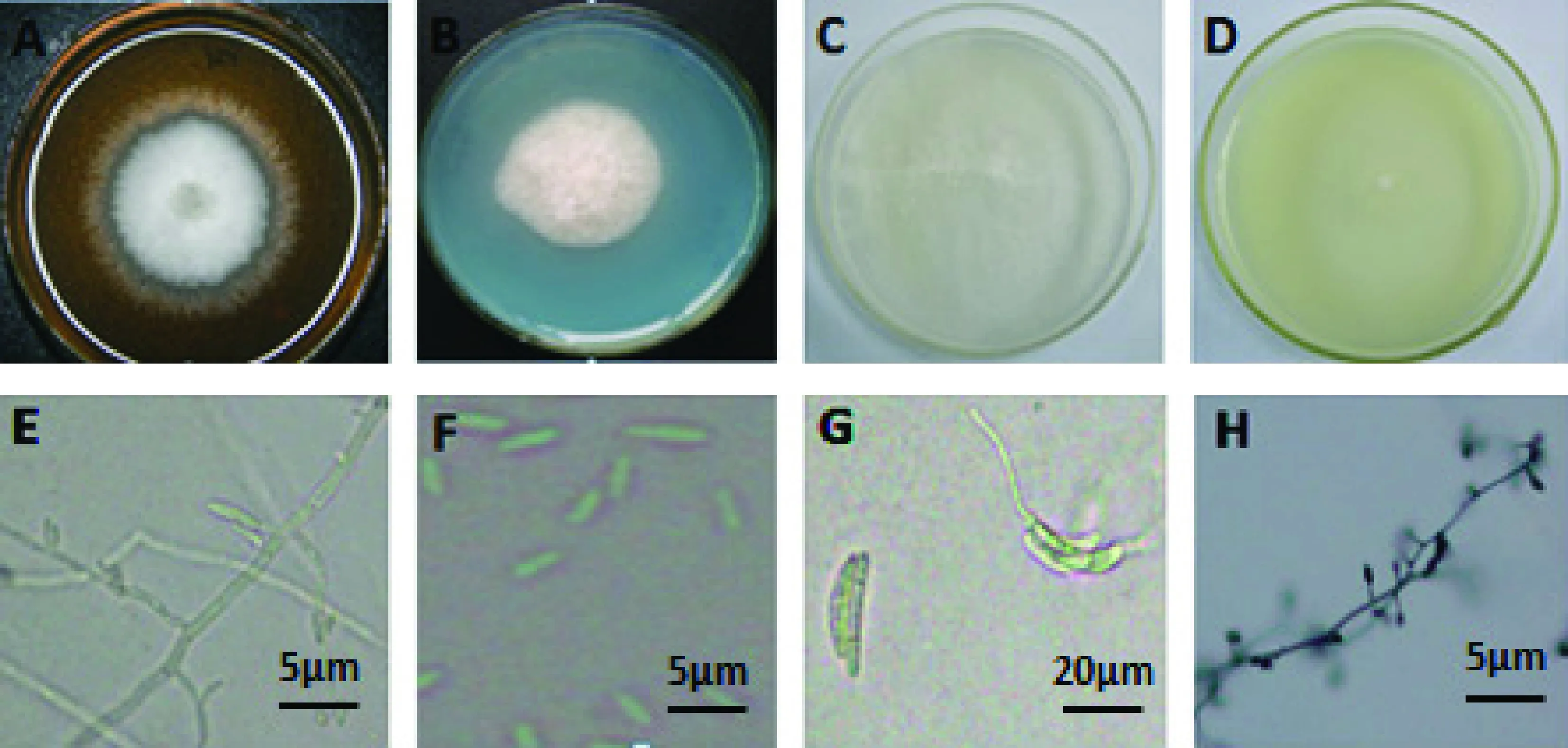
圖6 菌株L1的形態特征Fig.6 The morphological characteristics of strain L1
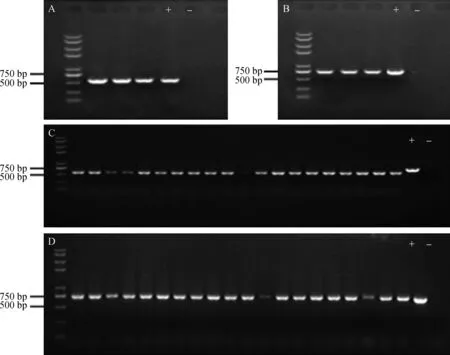
圖7 菌株rDNA-ITS片段和 TEF-1α片段的PCR擴增圖譜及菌液PCR鑒定圖譜 Fig. 7 Agarose gel electrophoretic analysis of rDNA-ITS and TEF-1α fragments
2.4.2rDNA-ITS和TEF-1α序列比對及分析 測序結果顯示,菌株間的rDNA-ITS和TEF-1α序列均有不同程度的變異。將序列提交到GenBank,登錄號見表1。所獲得的序列在NCBI和鐮刀菌Fusarium-ID數據庫進行比對,結果如表1所示,每個株系的rDNA-ITS區序列和TEF-1α序列的同源性均在99% ~100%之間,而且每個株系兩種序列的比對結果均為同一鐮刀菌種,進一步證明了分離純化的純度高和鑒定結果的可靠。
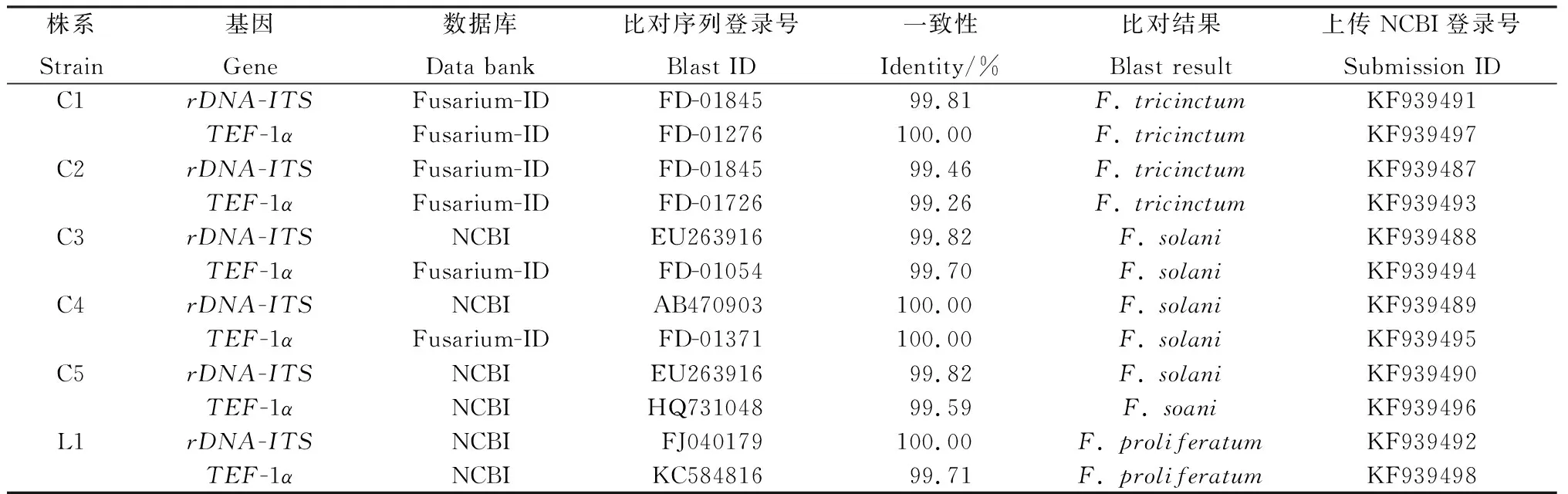
表1 rDNA-ITS 和 TEF-1α 序列比對及鑒定結果Table 1 Blast and identification results of rDNA-ITS and TEF-1α
2.5 系統發育樹的構建
2.5.1基于rDNA-ITS區序列構建系統發育樹 在基于rDNA-ITS序列構建的系統發育樹中(圖8),C1與C2菌株與NCBI和Fusarium-ID數據庫中的三線鐮刀菌(FJ233196,FD-01845,FD-01726)相聚于同一群,自舉值大于90%;C3,C4和C5與已上傳的腐皮鐮刀菌(AB470903,EU263916)聚為一類,其中C3與C5親緣關系較近;L1與層出鐮刀菌(FJ040179)聚一類,而與其他菌種距離較遠。
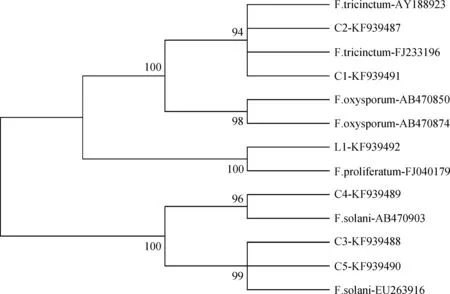
圖8 基于rDNA-ITS區序列構建的系統發育樹Fig.8 Phylogenetic tree constructed with the program Neighbor-Joining(NJ)based on rDNA-ITS sequences
2.5.2基于TEF-1α區序列構建系統發育樹 基于轉錄延伸因子TEF-1α序列構建的進化樹中(圖9),聚類結果與以rDNA-ITS序列構建的進化樹結果相似。C1和C2與NCBI(JX3978650.1,JX397855.1)和Fusarium-ID(FD-01726- EF-1α)數據庫的三線鐮刀菌聚為一類;菌株C3,C4和C5與數據庫中已上傳的腐皮鐮刀菌(FD-01371-EF-1α,FD-01054-EF-1α,HQ731048.1)聚為一類;L1單獨與層出鐮刀菌(KC584816.1)聚為一類。
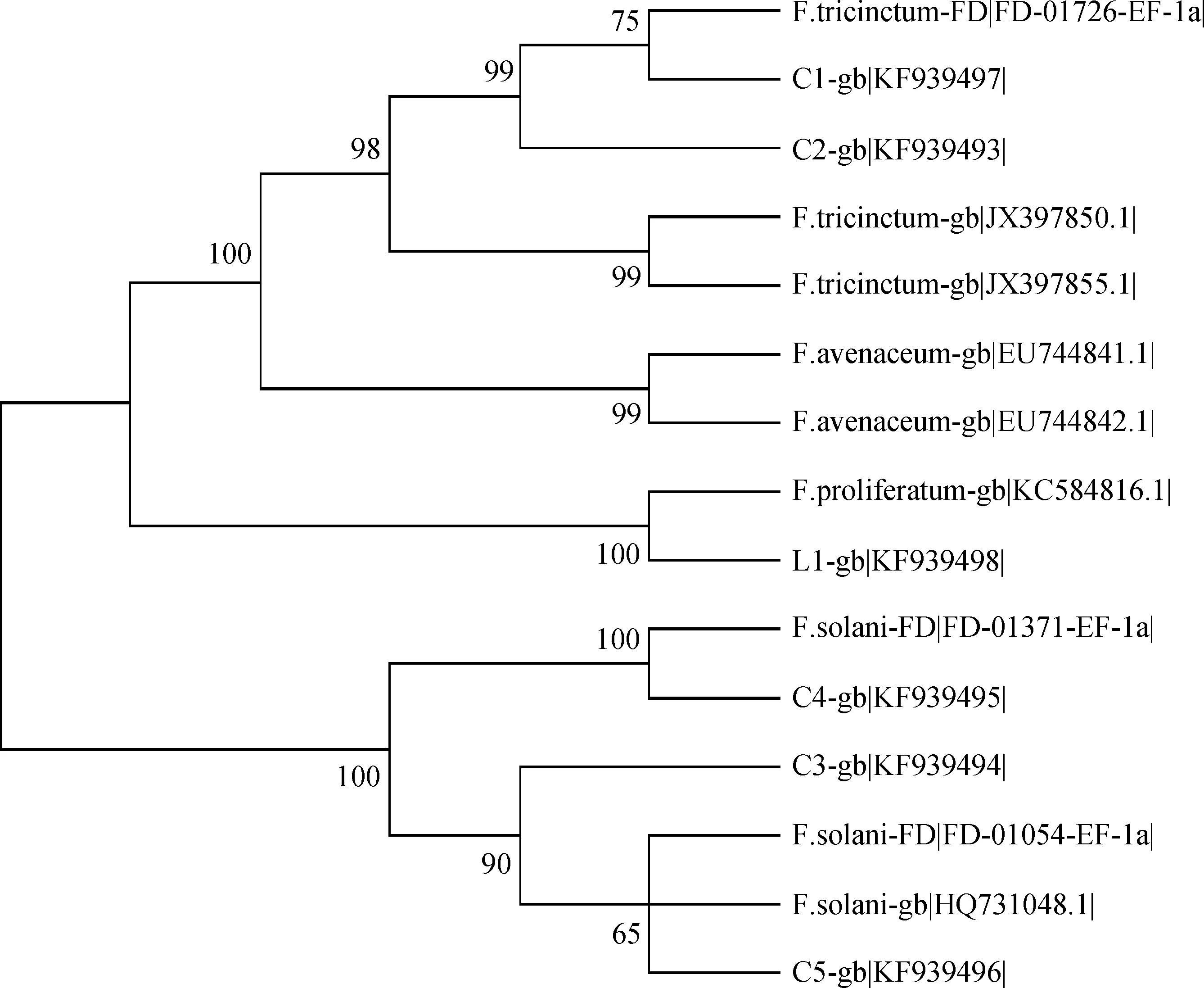
圖9 根據TEF-1α序列應用鄰接法(NJ)構建的系統發育樹Fig.9 Phylogenetic tree constructed with the program Neighbor-Joining(NJ)based on TEF-1α sequences
2.6 不同病原分離物的致病性分析
通過回接試驗,發病植株癥狀表現與田間的癥狀基本一致,經過形態觀察與分子鑒定確定從發病植株分離得到的鐮刀菌與用于接種的鐮刀菌相同,表明這6株鐮刀菌是苜蓿根腐病的致病菌。6個菌株的致病性有差異(表2),其中L1 菌株和C4菌株的致病性較強,發病率均大于80%,病害嚴重指數均約為60%。C2 株系致病性最弱(DI 54.44%,DSI 29.63%)。 C1、C3和C5 菌株的發病率和致病性均無顯著差異,發病率分別為66.66%,62.22%和65.55%;病害嚴重指數分別為42.59%,40.37%和38.89%。

表2 不同病原分離物的致病性Table 2 Variation in virulence among isolates of Fusarium spp.
3 討論
鐮刀菌是真菌中最難鑒定和最具經濟價值的屬之一,其形態復雜,又易受外界環境影響發生變異,通過形態學觀察很難準確鑒定到種。本研究在形態學鑒定的基礎上, 采用了rDNA-ITS和TEF-1α兩個基因進行分子生物學鑒定。其中rDNA-ITS是介于18S rDNA、5.8S rDNA 和28S rDNA 之間的區域,該區域進化速度較編碼區快,被普遍用來進行真菌種間或種內的遺傳相似性的分子系統研究[22-24]。而TEF-1α在鐮刀菌中為單一拷貝,在種內表現較高的保守性,TEF-1a已經成為鐮刀菌鑒定的有效工具。目前,已經通過該序列鑒定出禾谷鐮刀菌(F.graminearum)[22]、層出鐮刀菌[25]、串珠鐮刀菌(F.moniliforme)[22]、尖孢鐮刀菌(F.oxysporum)[26]等多個鐮刀菌種。因此,利用rDNA-ITS和TEF-1α序列對鐮刀菌種的鑒定,是對形態學鑒定的驗證和補充,避免因種間的高度相近帶來的鑒定錯誤。
通過了致病性鑒定試驗,明確了各菌株的致病性,特別是層出鐮刀菌株表現了高的致病能力。在之前的研究報道中,層出鐮刀菌多認為是弱致病菌,近幾年,層出鐮刀菌的致病性報道的越來越多,如引起番茄(Solanumlycopersicum)、豇豆 (Vignaunguiculata) 和藍莓 (SemenTrigonellae) 等植物的根部病害或葉部病害[27-29]。由此可見,不同層出鐮刀菌的株系或寄主都有可能影響其治病能力。
4 結論
根據形態學和分子生物學共同鑒定結果,C1和C2為三線鐮刀菌的不同變異種,C3、C4和C5為腐皮鐮刀菌的不同變異種,L1為層出鐮刀菌;河北廊坊苜蓿根腐病優勢致病菌為三線鐮刀菌;內蒙古臨河采樣區該病害優勢致病菌為三線鐮刀菌和腐皮鐮刀菌、山西陽高縣采樣區的優勢致病菌為腐皮鐮刀菌和層出鐮刀菌。其中,層出鐮刀菌是首次報道可引起我國苜蓿根腐病的病原菌。

