鋰電池發展淺談
張金龍,佟 微, 漆漢宏
(燕山大學電氣工程學院電力電子節能與傳動控制河北省重點實驗室,河北秦皇島066004)
鋰電池發展淺談
張金龍,佟 微, 漆漢宏
(燕山大學電氣工程學院電力電子節能與傳動控制河北省重點實驗室,河北秦皇島066004)
鋰具有比能量高,比體積小等優點,經過不斷的改善與發展,具有壽命長,安全性高,容量大,成本較低等特點的鋰電池已經成為當今的主流儲能設備。主要介紹了鋰電池的起源和發展歷程,重點通過對比鋰電池的正極,負極,電解質等部分材料組成,分析了鋰電池工作性能隨著電池材料的變化而產生的差異,討論了電池材料與鋰電池各項技術指標間的關系;并總結了目前鋰電池技術存在的問題和不足;此外,還對鋰電池的發展前景進行了展望。
鋰電池材料;電極;電解質;電池性能
Abstract:High specific energy and little specific volume were the advantages of lithium.After constant development,lithium battery,with high safety,large capacity and low cost,was the first choice for energy storage.The origin and development of lithium batteries were introduced first.Then by comparing the different material composition of anode,cathode and electrolyte respectively in lithium battery,the differences of battery working performance were analyzed.At the same time the relationship between technical indexes of lithium battery and battery materials were discussed.Also the disadvantages and defects of current lithium battery technology were briefly summarized.At last,the development prospect of lithium battery was also discussed.
Key words:lithium battery material;electrode;electrolyte;battery performance
伴隨著石油、煤炭等一次能源日益消耗,儲存量逐漸減少,可再生能源如風能、太陽能等二次能源將會逐步取代一次能源。但是,由于這些能源的不連續性,無法持續供應能量,故而需要一種能量儲存器,來輔助實現能量的連續供應。當前最常見的可再生能源利用方式就是將其轉化為電能來使用,即新能源發電技術,因為在當今世界,不管是工業生產還是社會生活,對電能的需求都是與日俱增。可見,必要的電能存儲裝置在新能源發電技術中起著舉足輕重的作用。眾所周知,應用最廣泛的儲能手段即蓄電池,而在眾多的蓄電池種類中,鋰電池因其壽命長、比能量高、放電性好、安全性高、體積小等優點,在儲能領域的應用日益廣泛,再加上政策扶持,鋰電池目前已經成為了蓄電池領域的主要發展方向。
1 鋰電池發展歷程
早在二百年前,意大利科學家伏打(Volta)發明了伏打電池,這是世界上第一塊能夠實際應用的電池,從此開啟了電池發展史。1895年法國科學家普蘭特(Plante)發明了世界上第一塊可充電的鉛酸蓄電池[1];20世紀50年代堿性鋅錳干電池問世;20世紀60年代燃料電池開發成功;20世紀70年代鋰電池研制成功。
雖然鋰電池在20世紀70年代實現了初步應用,但是鋰二次電池由于安全性問題等原因,一直未能推廣,發展處于停頓狀態。直到1991年,日本的索尼公司才推出第一塊商品化的可充電鋰電池,這也是電池產業的一次巨大革命。
鋰電池的研發成功,開啟了蓄電池的新時代。鋰是化學元素周期表中原子量最小的金屬元素 (6.94),也是密度最小(0.534 g/cm3,20℃)、電化學當量最小(0.26 g/Ah)及電極電勢最低(-3.045 V)的金屬[2]。具體來講,鋰電池具有以下優點:(1)比能量高。在質量比能量和體積比能量方面,鋰電池均比鉛酸蓄電池高出三倍以上。由此可以確定相同容量下,鋰電池具有更小的體積,更小的質量,適用范圍更加廣闊;(2)循環壽命長。錳酸鋰電池的循環次數在500次以上,而磷酸鐵鋰電池的循環次數在2000次以上,一般鉛酸蓄電池循環次數在400~600次左右,遠低于鋰電池;(3)充電功率范圍較寬。可以1C~3C進行快速充電,充電效率在85%以上,隨著控制電路的發展,這一技術將會得到進一步發展,具有更高的應用價值;(4)倍率放電性能好。鋰電池的倍率放電要高于鉛酸蓄電池,普通鋰電池可實現2C~3C放電,一些具有高倍率放電能力的鋰電池甚至可以實現20C~30C放電。這一特性對于電動汽車的智能控制技術非常有利。
以下論文將圍繞鋰電池結構,特別是電極與電解質材料與鋰電池性能間的關系展開分析與討論。
2 鋰電池的結構
普通電池的工作原理都是“氧化還原反應”,而鋰電池除此之外,還應用了“嵌入脫嵌反應”模型。如圖1所示,放電時,鋰離子在兩極電動勢的驅動下,由負極的空間夾層中穿過隔膜進入到正極空穴中,得到電子,變成鋰原子,而電子從外電路負極進入正極;充電時,在正極的空穴中失去電子變為鋰離子,穿過隔膜進入到負極的空間夾層中,在空間夾層處得到電子變為鋰原子,而電子從外電路正極進入到負極。由于此過程中,電極材料晶格結構未發生變化,且具有良好的可逆性,這使得鋰電池具有了其它高比能量電池所不具備的充放電的高循環性。
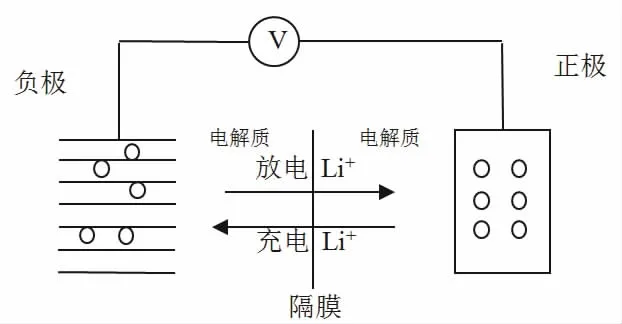
圖1 鋰電池基本結構
2.1 正極
目前,用于作為鋰電池正極材料的主要有磷酸鐵鋰、三元材料和錳酸鋰。國內企業多數以磷酸鐵鋰為主,如比亞迪等;而國外企業多數以三元材料和錳酸鋰為主,如日韓企業、美國Johnson Controls-Saft、EndDel等。如表1所示。采用三種正極材料的鋰電池性能比較見表2。
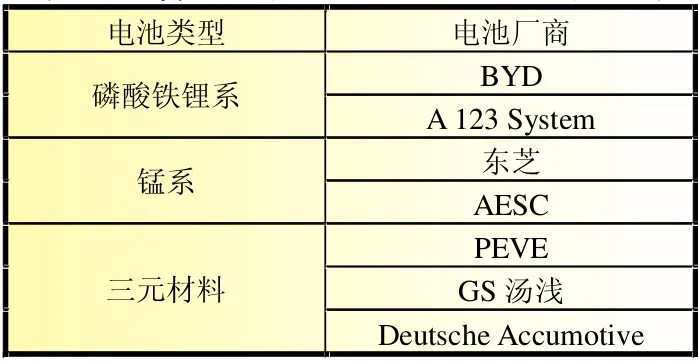
表1 部分動力鋰電池企業的技術路線
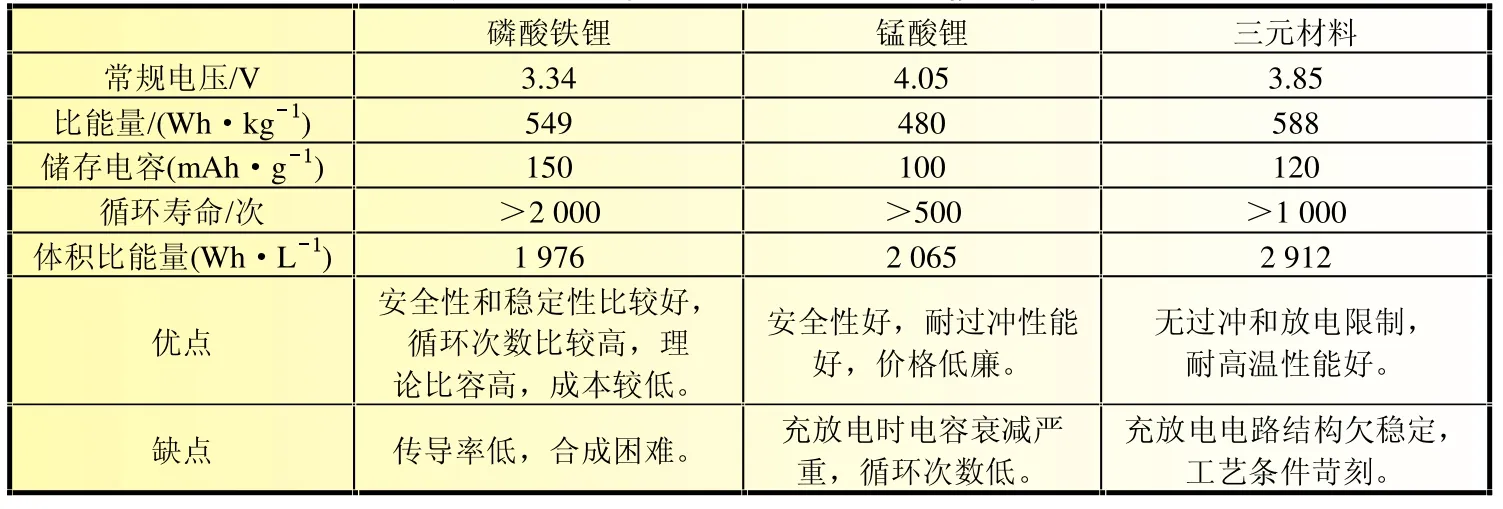
表2 三種技術路線鋰電池性能比較
當今,我國的鋰電池產業發展主要以磷酸鐵鋰為主,但兩項核心技術專利一個在美國,另一個在加拿大,因此我國的磷酸鐵鋰系鋰電池的發展存在知識產權隱患。除此之外,磷酸鐵鋰系電池也存在耐低溫性差,材料一致性控制困難等問題。在我國,另外一種技術路線是錳酸鋰系,雖然這種技術發展較早,技術比較成熟,但是電池壽命比較短,只能循環充電2000次左右,而且耐高溫性比較差[3]。
除上述主流正極材料外,現在鋰硫電池也逐漸成為研究熱點。單質硫(S8)的理論比容量為1675mAh/g,是較好的高比能量的電池材料。鋰硫電池主要分為有機硫材料和無機硫材料。有機硫化合物主要反應結構為S-S鍵,此結構與鋰配對的電池反應為:
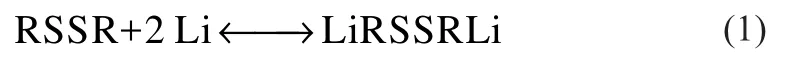
無機鋰硫電池形式同樣復雜多樣,具有體積小,質量輕,比能量大等優點,也是目前的研究熱點之一,主要反應為:
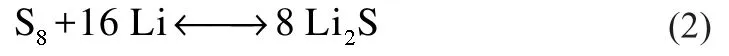
但是缺點同樣顯著[4]:硫的電絕緣性導致硫實際活性物質較少,利用率低;放電產物的中間體(Li2Sx)在電解液中溶解會導致陰極解體,而使容量迅速下降,進而使壽命較短;反應產物(Li2S)會聚集在陰極上,阻止電荷的傳輸與電極/電解液的界面狀態。這些都是制約鋰硫二次電池商品化發展的主要因素。
2.2 負極
鋰電池的負極材料主要以低電位的鑲嵌材料為主。而現在的主流鋰電池材料主要以C材料為主,因為C材料的結構較好,規則的C原子排布,不僅形成多個嵌鋰夾層,而且C材料還有較低的電位。目前C負極材料主要有:石墨,軟碳,硬碳等。
美國特斯拉公司在石墨中添加Si元素,使當前的電池容量上升了5%,這是鋰電池負極石墨材料的一個進步。商用鋰離子電池的負極一般由石墨制成,用硅作負極,其單位體積鋰離子容量可達到石墨的10倍左右。理論上,如果用硅大量取代石墨,就會使電極體積變小,從而使活性材料的空間變得更大。在鋰離子電池中,硅的質量不需太高,這也就意味著成本下降。這也是所有電池廠商的目標——提高產品質量,降低成本。但是把鋰和硅結合在一起的難點在于,最終出現的原子數量幾乎是初期的5倍,而這會引入其他復雜多樣的問題。
除此之外,合金材料也是研究的熱點,主要集中在納米結構、無定型化、多孔結構、薄膜材料等。合金材料的主要問題是首次充放電的效率問題,這也是限制合金材料發展的主要障礙。而且在納米合金中,雖然納米材料具有較大的反應面積、較短的反應路徑,但是由于其高活性,會導致材料表面形成不穩定的SEI膜,解決該問題的主要措施是在納米合金表面包覆非活性層,或者將納米材料包埋在穩定的基體中。而且合金材料在反復充放電過程中,體積膨脹,結構被破壞,壽命較短,這也是合金材料發展的主要障礙。
現在以鈦酸鋰為負極的鋰電池也逐漸發展起來,與石墨相比,鈦酸鋰為負極可使循環次數獲得極大的提升,例如用石墨的情況下,可循環兩千次以上,但是用鈦酸鋰后,循環次數可以提升至幾萬乃至幾十萬次[5]。但是,在提升循環次數的同時,鈦酸鋰不可避免地有電池比能量偏低的缺點,這也使鈦酸鋰電池的體積偏大。
2.3 電解質
電解質的研究主要以液態電解質和固態電解質為主。目前大多數電解質都為液態電解質,主要原因是合成成本較低,工藝簡單,具有良好的導電性;但是,采用液態電解質在充放電過程中會形成鋰枝晶,這會破壞正極結構,縮短電池壽命。而固態電解質則沒有這個缺點,不會形成鋰枝晶,但是由于工藝不夠成熟,具體物質尚未得到優化,故此仍然處于研究階段,不過,現在市場上已經出現了一些固態電解質的鋰電池。
鋰電池的液態電解質主要是以含磷的鋰離子化合物為主,目的是提高電解質的穩定性。目前液態電解質的主要研究焦點是功率提升和低溫穩定性的增強。值得指出的是,硼基化合物在新型溶劑[431,445,448,449]和鋰鹽[51,442,436]方面均有良好表現,如X.Q.Yang等將硼基Lewis酸作為電解液助劑,利用它對F-和O2-的鍵合作用,提高了難溶鋰鹽LiF和Li2O在PC+DMC和EC+DMC中的溶解度,使得LiF和Li2O能夠作為可溶性鋰鹽應用于電解液,且該電解液對LiFePO4和MCMB都表現出了相當好的性能[6]。
固態電解質則是目前研究探索的主流方向,可分為有機固態電解質和無機固態電解質。有些固態電解質具有接近、甚至超過熔鹽的高離子電導率和低電導激活能,其活躍度要超過液態電解液。由于固體鋰離子的擴散速率要低于液態,所以如何提高固體電解質鋰擴散速度的鋰離子電導率是目前的重要課題。有機固態電解質如PEO丙烯酸酯低聚物,纖維和全固態甲基丙酸烯基的固性聚合物,磷酸鋁鈦鋰(LATP),TMP(三甲基磷酸酯)都是目前的研究熱點。無機固態電解質可徹底解決因可燃性有機電解液泄露造成的安全性隱患問題。無機固態電解質應滿足以下要求[7]:在工作溫度下具有良好離子電導率,具有極小的或幾乎沒有晶界電阻;具有極低的電子電導率;在電池工作電壓范圍內有較高的電化學穩定性,一般要求電化學窗口高于5.0 V(vs.Li/Li+);化學穩定性好,與電極材料不發生化學反應。
目前關于無機固態電解質的研究主要集中在電解質的離子電導率的提高、電解質與電極相容性的提高以及電解質與電極界面阻抗的降低等幾個方面。
3 鋰電池發展現況與趨勢
鋰電池的整體發展趨勢主要分為兩個方向:小型化與大型化。小型化的主要發展方向為便攜式移動設備,如筆記本電腦,手機,相機等等,在這些設備中,鋰電池約占90%以上的市場份額,成為各類電子產品的主要能源,而且需求量也是在逐年增長。大型化的主要發展方向為動力電池組和大型儲能蓄電池,“十五”期間,國家設立了電動汽車專項課題,重點提出依靠能源控制系統、驅動電機控制系統和動力蓄電池管理系統來大力發展電動汽車[8]。此外,我國也對鋰電池的發展做出了相應的規劃,如國務院出臺的《產業結構調整指導目錄》和《汽車產業調整和振興規劃》等都對鋰電池及電動汽車行業的發展指明了方向。與此同時,我國的新能源汽車重大專項的實施也有力推動了我國鋰電池行業的發展,截至2014年9月底,中國已經累計生產新能源汽車27.4萬輛,其中,2013年生產1.7萬輛,與之前的四年產量總和相當;2014年生產8.4萬輛,同比增長4倍;今年前三季度生產15.6萬輛,同比增長2倍。
4 結束語
鋰電池的發展對于能源的利用,能源的儲備等具有重要意義,如何設計電池結構、材質,提高電池的比能量,獲得更大的容量、更長的壽命,是鋰電池的主要發展方向。雖然近幾十年來我國在鋰電池材料方面的發展取得了很大進步,但必須看到目前我國的鋰電池技術與國際先進技術相比還存在較大差距,具有自主知識產權的鋰電池核心技術仍然有待突破。
[1]閆俊美,楊金賢,賈永忠.鋰電池的發展與前景[J].鹽湖研究,2001,12(4):58-62.
[2]張勝利,余仲寶,韓周祥.鋰離子電池的研究與發展[J].電池工業,1999,4(l):26-28.
[3]唐鳳雄.我國鋰電池產業發展需要新思路[J].中國高新技術企業,2010,20(1):17-19.
[4]饒睦敏,耿秀玉.鋰電池單質硫/碳復合正極材料的研究進展[J].材料導報,2013,27(11):132-138.
[5]唐堃,金虹.鈦酸鋰電池技術及其產業發展現狀[J].新材料產業,2015,9(4):12-19.
[6]何向明.鋰離子電池發展的前瞻[J].電池,2008,38(4):222-224.
[7]劉嬌,懷永建,王海文.無機固態鋰離子電池電解質的研究進展[J].電源技術,2015,39(10):2308-2311.
[8]郎豐饒.鋰電池發展現狀及應用研究[J].統計與管理,2015,37(8):92-93.
Discussion of lithium battery development
ZHANG Jin-long,TONG Wei,QI Han-hong
(Key Lab of Power Electronics for Energy Conservation and Motor Drive of Hebei Province,Electrical Engineering College,Yanshan University,Qinhuangdao Hebei 066004,China)
TM 912
A
1002-087X(2017)09-1377-03
2017-02-15
河北省自然科學基金(E2014203198);國家自然科學基金(51477148)
張金龍(1983—),男,河北省人,博士,講師,主要研究方向為蓄電池管理技術及逆變器控制技術。

