金納米棒
——從可控制備與修飾到納米生物學與生物醫學應用
胡雪嬌 高冠斌 張明曦
(武漢理工大學,材料復合新技術國家重點實驗室,武漢 430070)
金納米棒
——從可控制備與修飾到納米生物學與生物醫學應用
胡雪嬌 高冠斌*張明曦*
(武漢理工大學,材料復合新技術國家重點實驗室,武漢 430070)
金納米棒因其獨特的光學活性(縱向和橫向兩個等離子體共振吸收峰, 可調范圍從可見光區到近紅外區)、長徑比可調,表面易于修飾,生物相容性良好而使得其在納米生物學和生物醫學等領域具有廣泛的應用前景。金納米棒的合成及表面修飾直接決定著其物理化學性質,進而影響其生物相容性及其在生物醫學中的應用。本文綜述了金納米棒的可控制備方法(包括模板法、電化學法、光化學法和晶種法)、表面可控修飾方法及其在納米生物學和生物醫學中的應用新進展,重點總結了金納米棒的表面可控修飾及其在分子探針、生物傳感、生物成像、藥物載體、基因載體和光熱療法的最新研究進展。最后針對金納米棒在生物應用過程中的一些瓶頸問題(如:特異性識別能力需要增強和熒光量子產率尚待提高等)提出了將手性分子或智能聚合物引入到金納米棒表面進行可控修飾,以期增強其特異性識別能力并提高熒光量子產率,為金納米棒的發展提供了新的思路。
金納米棒;可控制備;可控修飾;納米生物學應用;生物醫學應用
1 引 言
金納米材料因其獨特的表面等離子體共振效應、介電限域效應、小尺寸效應、量子隧道效應和光學效應等特殊效應1?3而使其產生電化學特性、吸附特性、熒光特性、超分子和分子識別等特性。并因此被廣泛應用于光電子學、催化、信息存儲、生物標記、生物傳感和表面增強拉曼等領域2?8。對金納米材料的研究,包括制備、性質和應用等一直都是材料科學的熱點。隨著技術的發展,研究者們已經制備出多種形貌各異的金納米材料9,10,包括金納米球、金納米星、金納米立方、金納米線、金納米棒等。
在這些形貌各異的金納米材料中,金納米棒的研究最為廣泛深入。這是由于金納米棒(gold nanorod,AuNRs/GNRs)制備簡單(如種子法11,12)、產率高13(可達 97%)、長徑比(aspect ratio,AR)可調(AR在1.5?20之間)14?17,且具有獨特的熒光性質2,4,18。因此金納米棒在納米生物學和生物醫學領域具有廣闊的應用前景。本文綜述了金納米棒的可控合成方法(包括模板法、電化學法、光化學法和晶種法等),可控表面修飾方法(包括配體置換法、無機物包覆法和多級修飾法等)及其在納米生物學(包括分子探針、生物傳感和生物成像等)及生物醫學(包括藥物載體、基因載體和光熱治療等)方面的最新應用。

2 金納米棒的可控制備
自1994年,Martin等19首次用模板法制備出金納米棒,經過近幾十年的發展,AuNRs已經發展出多種合成方法,其中可以較好地控制金納米棒長徑比的制備方法主要有以下四種:模板法19,電化學方法20,光化學方法21以及晶種生長方法22等。現簡要介紹如下:
2.1 模板法
模板法主要是利用多孔氧化鋁薄膜的孔道,在孔道內將金原子還原讓其受限沉積直至填滿孔道,然后用氫氧化鈉溶解掉氧化鋁薄膜并再用超聲得到分散性較好的AuNRs。1994年,Martin等19首次使用模板法合成出AuNRs。他們通過電化學沉積將 Au3+還原并沉積到多孔氧化鋁薄膜的孔道內,然后溶解掉多孔氧化鋁薄膜(模板)并去除反應過程中產生的雜質即得到AuNRs。在用模板法合成AuNRs的過程中,AuNRs的生長受到模板孔徑束縛,故而模板孔的尺寸直接決定了 AuNRs的直徑和長度,因此可以用不同的模板合成尺寸不同的AuNRs。模板法的優點是 AuNRs的長徑比可以通過孔徑大小、孔道長度、電化學沉積時間來調控。
2.2 電化學法
1997年,電化學法首次被Wang等20用來制備AuNRs,在該方法中用到了兩種表面活性劑:十六烷基三甲基溴化銨(CTAB)和四辛基溴化銨(TCAB)。
Wang等人構建了一個電解池,電解液為CTAB和TCAB,陰陽二極分別為鉑片和金片,在超聲的情況下電解。陽極的金原子失去電子變成金離子進入溶液中,溶液中金離子一部分被CTAB還原成中間體,另一部分在陽極的鉑片處得到電子被還原成金單質,在超聲的作用下,CTAB修飾的中間體在電解質溶液與鉑片界面上包裹陽極還原的金單質形成金納米棒。其中,CTAB不僅可以防止金納米粒子聚沉,而且還可以充當電解質。而TCAB同樣可以誘導形成AuNRs。AuNRs的長徑比可通過CTAB和TCAB的比例來控制。電化學法的優點是AuNRs的形貌易控且尺寸均勻。


2.3 光化學法
2002年,Franklin Kim等21率先采用光化學法來制備 AuNRs。該法首先準備 CTAB,四十二烷基胺和氯金酸(HAuCl4)模板劑水溶液體系,然后將適量丙酮和環己胺加入上述水溶液體系中,可使膠束結構散開,有利于形成AuNRs。然后再加適量硝酸銀(AgNO3)溶液,用紫外照射(254 nm)整個水溶液體系約30 h,在這個過程中利用紫外誘導激發,所制備的AuNRs分散性好,長徑比均勻。并且觀察到 Ag+的量越多,AuNRs的長徑比越大,而不加入 Ag+則不能生成 AuNRs。因此光化學法制備的AuNRs的長徑比可通過Ag+的量來調節。
2.4 晶種法
2001年 Murthy等22首次采用晶種法來制備AuNRs,該方法對環境和設備的要求低,制備過程簡單。Murphy課題組起初是在制備金納米粒子(AuNPs)時引入“seed”的概念,在CTAB溶液體系下研究尺寸可控的AuNPs。他們利用NaBH4制備出晶種,也就是尺寸較小的膠體金。然后將晶種加入到生長液中,生長液含弱還原劑和金屬鹽可避免二次成核。因此,反應只能在晶種表面進行,這種方法制備的AuNPs尺寸均一23。而且該課題組已能成功調控尺寸在5?40 nm的AuNPs。后來,Murphy課題組將晶種法引入到金納米棒的制備,得到不同長徑比的 AuNRs24。為提高金納米棒的產率,他們向反應液中加入銀離子溶液,但其產率仍然只有40%?50%22。2003年,El-Sayed課題組采用改進的晶種法制備出長徑比小于 5的金納米棒,其產率達 95%以上,他們主要調整了種子和銀的比例,并去掉反應液中的丙酮。該方法可用于大批量制備金納米棒16。此后金納米棒的制備方法大多以此為基礎,進行微量調整。據報道,目前有一種改進的晶種法來合成AuNRs,即:通過向對苯二酚(HQ)還原劑溶液中添加水楊酸(SA),可以制得 LSPR峰值波長更大(最高達到1273 nm),長徑比更大且單分散性更好的金納米棒25?29。總的來說,近十多年來金納米棒的種子合成法主要有兩大類:一類是Murphy課題組提出的“三步”晶種法;另一類是El-Sayed16課題組提出的“一步”銀離子介導晶種法30。晶種法經過持續的改進,目前已發展成為廣泛使用的制備金納米棒的方法。
3 金納米棒的可控修飾
金納米棒表面必須修飾一定數量的配體才能穩定存在,如果缺少表面配體,金納米棒將發生不可逆轉的聚集。CTAB是金納米棒上最為常見的表面配體,然而 He等31報道在 AuNRs溶液中的CTAB具有高毒性,吸附在AuNRs表面的CTAB會干擾生物過程,阻礙AuNRs與生物分子的偶聯32。因此發展不同配體修飾的金納米棒,即對金納米棒表面改性,對于擴展金納米棒在納米生物學和生物醫學中的應用有重要的意義。
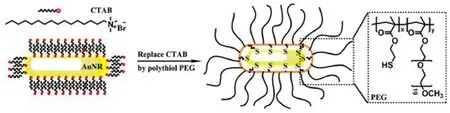
圖1 用PEG基共聚物置換AuNRs表面的CTAB的示意圖Fig.1 Schematic representation of surface modification of CTAB capped AuNRs with polythiol PEG based copolymer.
3.1 AuNRs的修飾方法
3.1.1 配體置換法
配體置換法是用配體將金納米棒表面的CTAB置換出來的一種方法,如 Shobhit小組33使用殼聚糖置換CTAB制成探針,可用于無創成像。Liu等34用聚乙二醇(PEG)替換金納米棒表面的CTAB,制成一種有效的近紅外光熱劑(如圖1),能消融體內腫瘤。常貫儒課題組35通過配體置換法制備出兩性離子半胱氨酸修飾的金納米棒(Cys-AuNRs)。L-半胱氨酸(Cysteine,Cys)是生命體中二十種天然 α-氨基酸之一,其可以通過分子中的巰基與金原子形成金硫鍵(Au―S)而被修飾到AuNRs表面,金硫鍵是一種較強的配位鍵,其穩定性遠大于 CTAB與Au原子之間的相互作用力。因此將L-半胱氨酸與CTAB修飾的金納米棒混合溶液在劇烈攪拌的條件下經過一段時間的配體交換,L-半胱氨酸可充分置換 AuNRs表面的CTAB。這種通過配體置換的方法得到的半胱氨酸修飾的AuNRs不僅可以保留原有的長徑比,而且其細胞毒性降低,生物相容性得以提高。更重要的是,由于含巰基的分子非常多,例如:十二硫醇、巰基丙酸、氨基硫醇、半胱氨酸衍生物、含半胱氨酸的二肽、三肽及多肽等,這些化合物未來都可以根據實際需要通過這種配體置換的方法修飾到不同長徑比的金納米棒表面,這將極大的拓展金納米棒的應用范圍。
3.1.2 無機物包覆
為了提高金納米棒的穩定性,使用無機材料如四氧化三鐵(Fe3O4)、氧化亞銅(Cu2O)和二氧化硅(SiO2)等包覆金納米棒是一種比較好的解決方案。其中SiO2包覆法因其良好的水溶性和生物相容性以及表面易修飾等優點而得到廣泛使用。
Rothberg課題組36首先使用 Nikoobakht和El-Sayed16所報道的種子生長法合成金納米棒,然后通過聚電解質在金納米棒的表面層層組裝,再由原硅酸四乙酯(TEOS)的水解和縮合而制得二氧化硅包裹的金納米棒(AuNRs@SiO2)。在此過程中,主要是通過靜電作用將聚苯乙烯磺酸鈉(PSS)、聚烯丙胺鹽酸鹽(PAH)、聚乙烯吡咯烷酮(PVP)等聚電解質分子逐層組裝在AuNRs的表面,隨后通過調節TEOS的用量來控制AuNRs表面包覆的SiO2厚度。透射電鏡顯示AuNRs表面包覆了厚度均勻的SiO2層,形成了明顯核-殼結構(圖2)。孫宏浩等37的紫外圖譜顯示 AuNRs在 SiO2包覆前后均有可見強吸收峰,表明SiO2包覆后的金納米棒的光學性質沒有改變。Gao等38報道AuNRs@SiO2的細胞毒性相比 CTAB修飾的AuNRs明顯降低,這些都表明AuNRs@SiO2在生物醫學領域有著良好的應用前景。包裹有SiO2的AuNRs如圖2b所示。
3.1.3 多級修飾
多級修飾就是在已經過修飾的金納米棒的表面繼續修飾的一種方法。Hyejin等39首先將巰基吡啶連接在AUNRs表面,然后用聚4-苯乙烯磺酸鈉對其進行處理使其表面帶負電,接著通過靜電相互作用將免疫球蛋白修飾到AUNRs表面,制成功能化的納米探針,用于癌細胞表面膜的高靈敏的特定標記和成像。佟倜等40通過在包覆了金納米棒的介孔硅表面修飾生物相容性的透明質酸,得到了具有腫瘤靶向性的多功能藥物載體,表現出對腫瘤細胞特異性殺傷作用,有望解決化療帶來的副作用以及耐藥性。Gao等38首先應用種子生長法合成出長徑比為3.5的同質AuNRs (40 ± 5)nm,然后由溶膠-凝膠的方法成功地合成 SiO2包覆的 AuNRs核殼結構。AuNRs@SiO2-NH2和AuNRs@SiO2-FA是通過在 AuNRs@SiO2表面分別修飾氨基和葉酸制得的,如圖 3所示。AuNRs@SiO2首先由氧等離子體凈化處理。接下來,凈化過的AuNRs@SiO2在混有氨丙基三甲氧基硅烷(APTS)的無水乙醇里再分散放置24 h。然后,將混合物放置在80 °C的烤箱反應2 h,以維持官能團的穩定。在60 °C的真空干燥箱干燥3 h后得到中間產物(GNRs@SiO2-NH2)。接下來,將AuNRs@SiO2-NH2加到三乙胺(TEA)和n[β-maleimidopropyloxy]琥珀酰亞胺酯(BMPS)中孵化30 min。洗滌干燥后,將底物加到葉酸半胱氨酸中反應 2?3 h,改性后就制得AuNRs@SiO2-FA。然后用聲波和離心法收集AuNRs@SiO2-FA樣本。

圖2 (a) CTAB包覆的金納米棒(b) SiO2包覆的金納米棒透射電鏡圖Fig.2 Transmission electron micrographs of (a) CTAB-coated gold nanorods and (b) silica-capped gold nanorods.
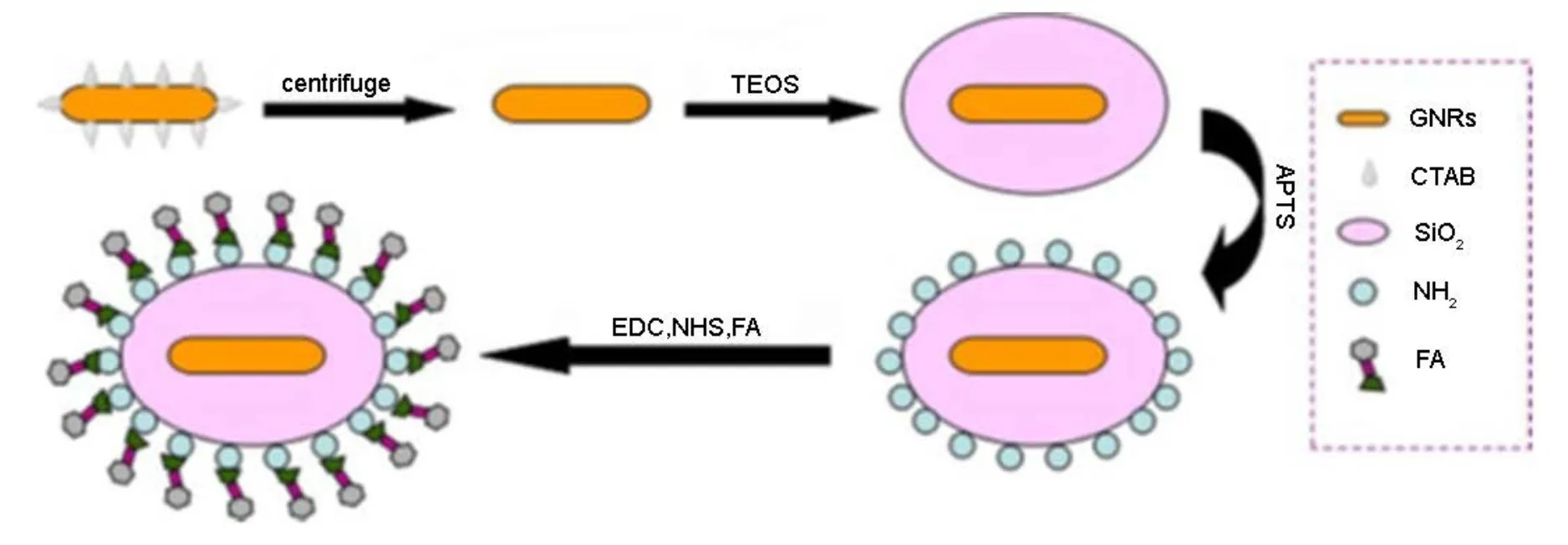
圖3 AuNRs@SiO2-FA的合成過程Fig.3 Procedure for the synthesis of AuNRs@SiO2-FA.
3.2 AuNRs的表面可控修飾
AuNRs常用雙層CTAB作表面活性劑穩定存在水溶液中43?45。金納米棒兩端的 CTAB密度比側面低,允許一些分子(如硫醇)在低濃度下選擇性取代金納米棒兩端的CTAB46,還可以通過控制條件在金納米棒的側面進行選擇性修飾。
Wang等46通過控制不同配體加入時間及濃度來選擇性修飾金納米棒的兩端和側面。起始時金納米棒在水溶液中和CTAB雙分子層穩定存在(圖4a)48,49由于金納米棒兩端曲率半徑較大,兩端連有的CTAB雙分子層少于端面50,51。原硅酸四乙酯(TEOS)的水解形成硅涂層。在路線1中,由于二氧化硅涂層動態可控,硅可以選擇性地包覆在金納米棒的兩端(圖4b),這是因為在金納米棒的兩端CTAB比較少,二氧化硅涂層只需要很少的能量就可以把兩端的CTAB分子移除。繼續加金鹽,隨后金屬就會在端面過度生長,形成兩端修飾有二氧化硅的金納米棒。在路線2中,金納米棒的側面包覆的是二氧化硅涂層。這種方法首先運用路線1中的方法將甲氧基聚乙二醇巰基(mPEG-SH)修飾到金納米棒的兩端,后續硅涂層選擇性地修飾在金納米棒的側面。在阻止金屬過度生長方面,硅涂層比mPEG-SH更強,在繼續加金鹽的條件下,金選擇性地沉積在金納米棒的兩端,就形成端面修飾有二氧化硅的金納米棒。
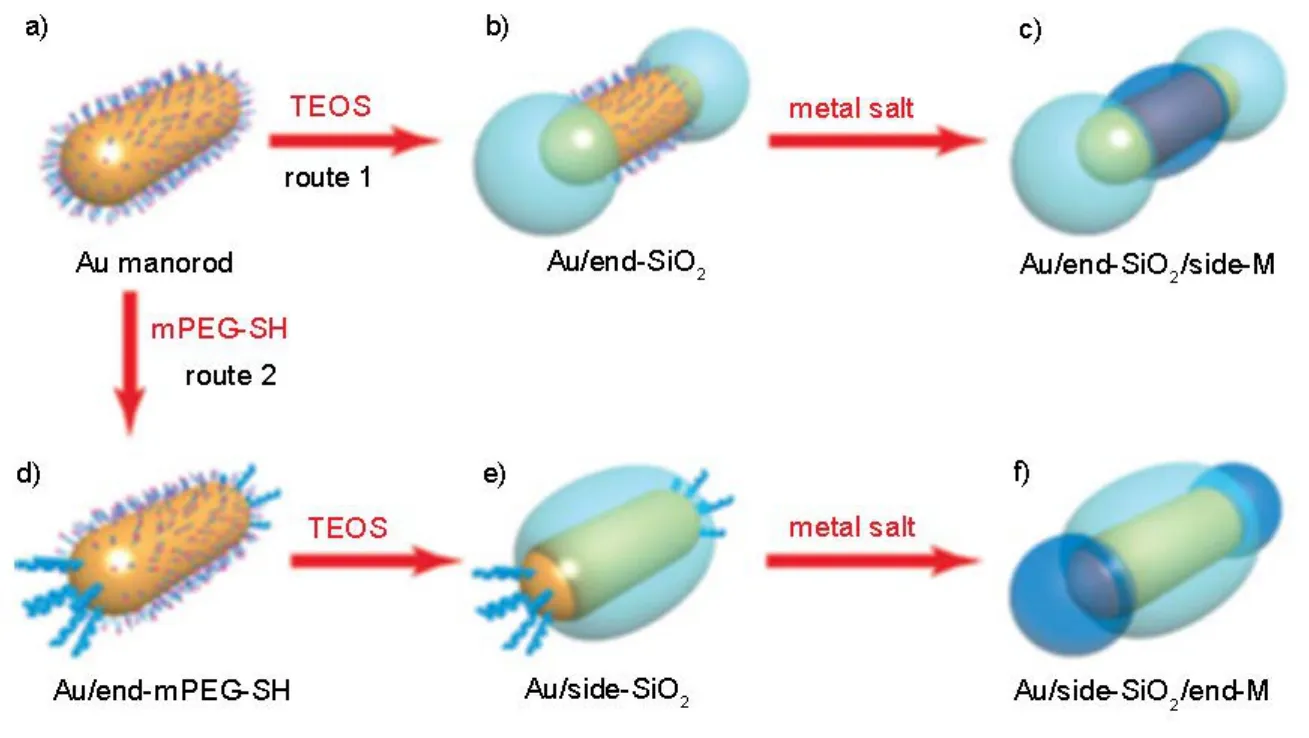
圖4 兩端和中間分別修飾有硅的金納米棒Fig.4 Nanorod coated with silica at the ends or on the side surface.
這些兩端或中間修飾有基團或聚合物的金納米棒還可以通過分子間特殊的相互作用組裝成有序的納米結構,比如end-to-end,side-by-side,甚至可以組裝成更高級的結構,實現多維組裝體。在某些方面,這些組裝成的結構比單個金納米棒性能更優,其性質是所有金納米棒之間光性質的加和,表現出更加優異的協同性質,擴大了金納米棒的使用范圍。
4 在納米生物學中的應用
AuNRs因其獨特的光學活性,使其在分子探針、生物傳感和細胞成像等納米生物學領域有著廣泛應用。
4.1 分子探針
AuNRs分子探針靈敏度較高,不同長徑比的AuNRs分子探針可將其表面微弱的折射率的變化轉化成可測量的波長偏移,對待測物的檢測極限可低至納摩爾級。胡家文課題組52將對巰基苯甲酸(MBA)連接在AuNRs表面,制成表面增強拉曼散射(SERS)標記的AuNRs探針,進行SERS免疫檢測研究,由于AuNRs的SPR峰位置可調,可通過激發光和SPR的共同作用來提高SERS信號,從而增強 SERS探針的靈敏度。Luong等53開發出一種新的用于DNA雜交的金納米棒靈敏探針,這種生物傳感器用于DNA雜交的濃度更低,而且反應也更快。Ye等54使用基于光度計和金納米探針的金屬波導毛細管(MWC)高度靈敏檢測凝血酶,金納米棒作為信號傳輸探針,圖 5為基于光度計的MWC原理圖。Ye課題組采用7 cm長的MWC,將最有可能的檢測極限提高了 68倍,以致低如0.02 nm的凝血酶也可被檢測到。此外,可通過流動注射模式減少樣品注射體積等方法提高分析性能。該課題組使用的光度計簡便且成本低,在生命科學和環境監測跟蹤分析方面可廣泛應用,它可能對生物發現過程的細胞和分子水平有巨大的影響。

圖5 基于光度計的MWC原理圖Fig.5 Schematic diagram of the MWC based photometer.
4.2 生物傳感
AuNRs因其獨特的表面等離子體共振特性,對溶液環境中的電介質非常敏感,AuNRs周圍電解質的微小改變會引起局部折射率的改變進而導致AuNRs等離子體共振頻率的改變,而這種改變可通過紫外吸收光譜檢測到,故而可利用這種特性將AuNRs用于生物傳感。何鑫等55利用金硫鍵構建了固相金納米棒免疫傳感器,其能夠通過表面等離子共振波峰的移動來檢測不同感染周期的日本血吸蟲循環抗原,并分析宿主體內抗體的消長變化。Jie等56用巰基十一烷酸(MUA)修飾金納米棒制成無標記的局部表面等離子體共振的生物傳感器,基于人類免疫球蛋白檢測反人類免疫球蛋白,并且可檢測到0.4 nmol·L?1的極限,可用于醫學,化學和生物化學等領域。
有數據顯示,在發展中國家和發達地區乳腺癌仍是女性最常見的癌癥57。目前正在大量研究乳腺癌的早期診斷和治療方法58。在2003年,美國國家綜合癌癥網確定穿刺活檢(NB)作為“首選”(一個手術切除乳房診斷)方案59,60。雖然NB擁有無痛、廉價和簡單的優勢,但提取分析樣本需要大量的手術經驗,嚴重限制了其應用61,62。
AuNRs可用于生物傳感器檢測人類乳腺癌MCF-7細胞。Li等63將金納米棒修飾后用于來檢測乳腺癌(圖6)。因AuNRs具有獨特的光學性質,可通過控制他們的形態,從可見到近紅外區方便地調節縱向等離子共振峰。由于近紅外(NIR)窗口的存在,AuNRs視為成像或體內治療潛在候選者,可達到深層滲透到軟組織的目的,更不要說細胞,這是Li等63目前的研究設計。已報道的夏團隊之前的工作提供了進一步的證據,金納米結構的LSPR屬性不會干擾細胞64。Li等63的假設結合了寡核苷酸適配子和金納米棒的優點,這個優點在MCF-7細胞的檢測可能蘊含著巨大的希望。據報道,粘蛋白-1蛋白(MUC-1)作為人類癌癥生物標志物,廣泛存在腫瘤細胞的表面,如乳腺癌、卵巢癌、肺癌和胰腺癌等,特別是初級和轉移性乳腺癌的特殊標志65。
2016年,Li小組63發現人類乳腺癌 MCF-7細胞上的MUC-1與寡核苷酸低聚糖4-16(5?-GCA GTT GAT CCT TTG GAT ACC CTG G-3?)之間存在特定的相互作用,而這種相互作用是可以被檢測到的。Li等63通過Au―S化學鍵將寡核苷酸低聚糖共價結合到AuNRs的表面,用來檢測乳腺癌細胞表面的 MUC-1,如圖 6,從檢測結果可以直接看到AuNRs的局部表面等離子體共振(LSPR),根據 MUC-1與寡核苷酸低聚糖之間特殊的相互作用可以檢測乳腺癌。總之,一種MUC-1適配子功能化的 AuNRs被開發和應用于人類乳腺癌MCF-7細胞的檢測。這種方法靈敏度高,穩定性好,操作簡單,成本低,并且這種生物傳感器可能闡明人類乳腺癌在早期臨床診斷中的應用,相信隨著醫學技術的發展,這種生物傳感技術可能應用于乳腺癌的主要診斷和治療,尤其是在 NB的應用上。
4.3 生物成像
AuNRs由于強的吸收信號,LSPR可調,無光漂白現象等能夠進行多功能成像技術,可精確地預測和診斷疾病。LSPR效應可使AuNRs表面的電場增強,再加上AuNRs之間的耦合電場強度,可得到遠大于入射光電場的電磁場(如表面增強熒光、表面增強吸收、表面增強瑞利散射和SERS等),通過提取增強的電磁場信號,可進行成像與分析檢測66。
Luo等67提出用硅包覆的吲哚菁綠色嵌入式的金納米棒進行雙模式CT和近紅外熒光成像。12小時瘤內后注射1.5 mg·mL?1的金納米棒改性液200 mL,CT掃描顯示,該方法可增強成像質量尤其是可提高對比度,而染料產生的近紅外熒光仍然存在。因此,金納米棒具有發展成為一種雙模式成像染色劑的潛力。Zhang等68首先用種子生長法合成金納米棒,然后將硫醇鹽甲氧基聚乙二醇(MeO-PEG-SH)和SiO2連接在AuNRs表面,用于細胞的多光子熒光成像,在生物成像方面的潛在應用可進一步探索,Joshi等69首先用甲氧基聚乙二醇巰基(mPEG-SH)替換AuNRs表面的CTAB雙分子層,然后使用配體交換法用硫醇鹽抗體分子置換mPEG-SH,再經過大多數抗體的交聯,二硫酚使抗體直接連接在金表面,如圖7所示,這種方法形成的生物軛合物既沒有聚合也無細胞毒性,合成的連有抗體的AuNRs軛合物可用于癌癥細胞培養模型里表皮生長因子受體(EGFR)分子的特定光學與光聲成像,在腫瘤成像方面具有潛在應用價值。
5 在生物醫學中的應用
AuNRs因其獨特的光學活性和良好的生物相容性,使其在藥物載體、基因載體、光熱療法等生物醫學領域有著廣泛應用。
5.1 藥物載體
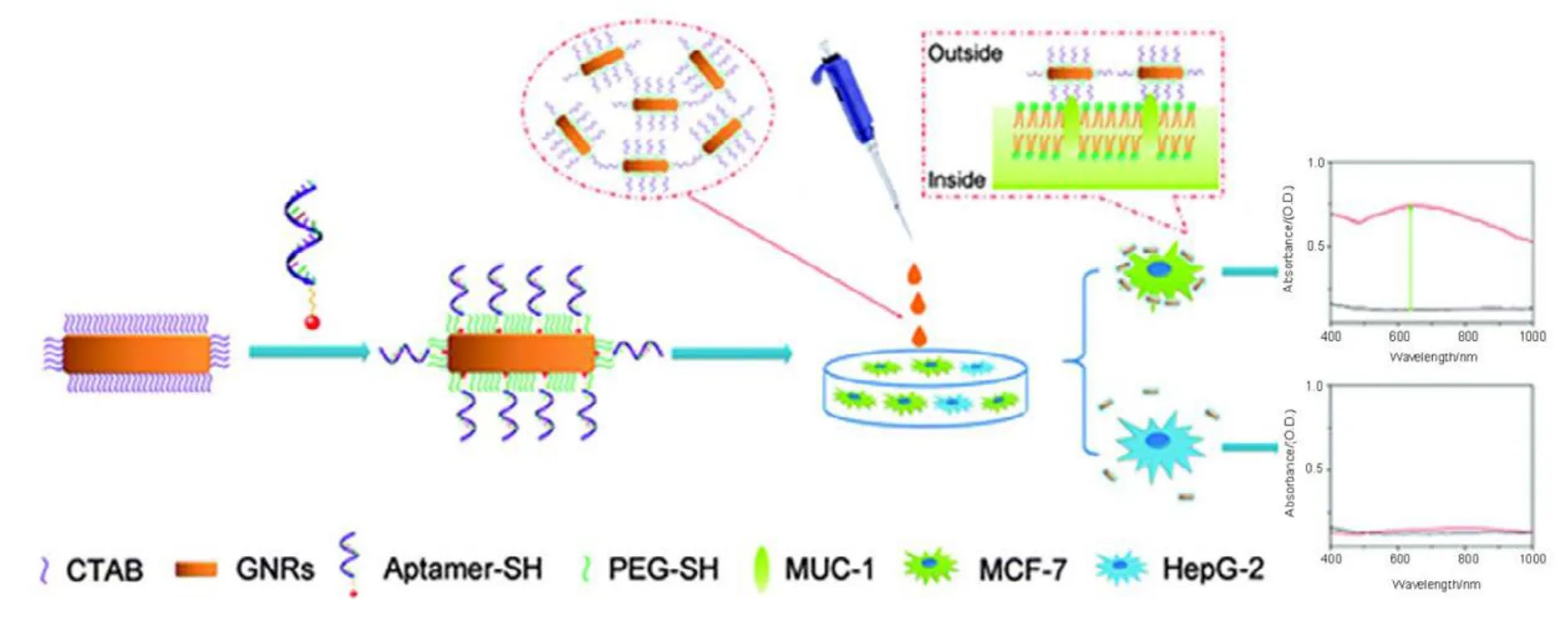
圖6 檢測機制的示意圖Fig.6 Schematic representation of the detection mechanism.
藥物控釋體系因其用藥量少、治療效果好、副作用小的優勢已成為藥劑學的研究熱點,具有控制藥物釋放的特點。如今,納米載藥系統越來越受到研究者的青睞。研究表明,可用物理吸附或化學鍵的方法將藥物裝載于AuNRs的表面,納米粒子所產熱量既能使周圍環境變化,又能使藥物釋放,使藥物能夠進入細胞內部70?73。用近紅外激光照射時,可使AuNRs產生表面等離子共振特性和光熱效應,從而達到遠程光控運載和釋放藥物的目的。
Park等74制備了一個可以生物相容性的藥物載體:微型有機凝膠通過使用植物油和自組裝凝膠因子纖維乳化制得。氟比洛芬封裝在金納米棒的微型有機凝膠里可緩慢釋放,當用近紅外熒光照射時,金納米棒周圍溫度升高,凝膠轉換為液體,釋放加速,這種系統可有效地用于多功能按需給藥體系。Ali等75將AuNRs與利福平(RF)共軛連接制成一個載藥體系治療結核病,其實驗結果表明AuNRs@RF有望在保證宿主細胞安全的情況下有效攻擊和殺死結核。
在過去的十年中,許多研究表明金納米棒在等離激元光熱治療(PPTT)中應用廣泛,特別是PPTT在抗擊癌癥方面有巨大的應用前景76?78。與金納米粒子相比,PPTT應用AuNRs獨特的物理化學特性78?80,即:AuNRs能吸收近紅外光并通過非放射過程(包括電子與電子和電子與光子之間的相互作用)將其迅速轉換成熱量81?84。因此,當AuNRs作用于癌細胞時,電磁輻射與光學激光產生足夠的熱量來選擇性地破壞癌細胞85?90。PPTT主要通過壞死和凋亡致癌細胞死亡91,92。但大劑量的納米顆粒或激光照射會導致過熱,易使細胞壞死,并可能誘發腫瘤轉移和生長93?95,也可能會損害臨近的健康細胞。因此,開發一種新的方法治療癌細胞至關重要。
研究表明,槲皮素(HSP70)可以直接通過阻止細胞色素c/dATP調解半胱天冬酶活性來抑制細胞凋亡96,并結合多個其他休克蛋白調節蛋白質重折疊97,Ali等98對多個細胞系進行了PPTT檢測,發現HSP70濃度與PPTT響應呈正相關關系。但當他們用siRNA移除HSP70觀察到PPTT的響應增強。Ali等98的測試結果表明可制造出新穎并具有AuNRs共軛作用的HSP70抑制劑,相比非共軛的 AuNRs,新的共軛抑制劑顯示防止熱阻的優越性能,導致更高比例的細胞凋亡。因此,AuNRs作為整體運載槲皮素到癌細胞與作為細胞凋亡的PPTT的誘導物一樣。
Ali等98在三個不同的細胞株HSC (人類鱗狀癌細胞),MCF-7 (乳腺癌細胞)和Huh7.5 (肝癌細胞)里進行PPTT檢測。觀察到初始HSP70濃度越少,應用PPTT后凋亡的細胞增多,在所有的細胞系被測試時減少HSP70蛋白濃度以增強細胞凋亡。Ali等98通過用熱休克蛋白抑制劑與AuNRs共軛作用來擴展這些結果,使敏感細胞進行PPTT,從而促進細胞作為非炎癥癌癥細胞死亡(圖8)。在成功地展示HSP70抑制劑與AuNRs接合后,這些新AuNRs增強癌細胞凋亡的能力會顯著增強。與直接添加HSP抑制劑到細胞中不同,Ali等98使用AuNRs作為藥物輸送系統,而AuNRs是一個高效的配送系統,可以將目標藥物直接運送到腫瘤細胞表面,而且HSP抑制劑的量很少可以消除HSP抑制,減少非癌細胞的副作用,這種方法大大促進了PPTT體外誘導細胞凋亡。如果將這些結果推廣到體內模型,則下一步可能以最小的副作用有效地切除腫瘤。
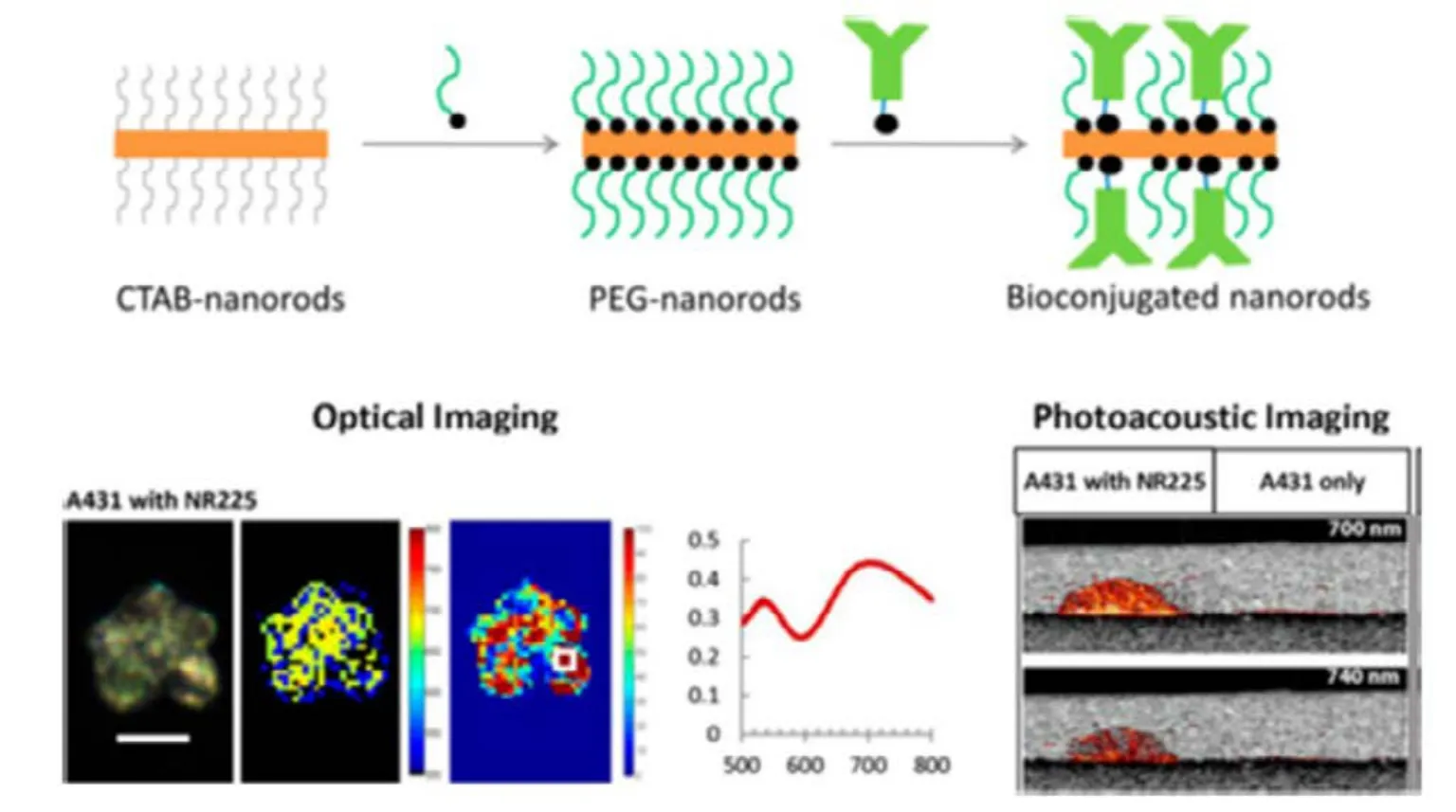
圖7 金納米棒的光學和光聲成像Fig.7 Optical and photoacoustic imaging of gold nanorods.
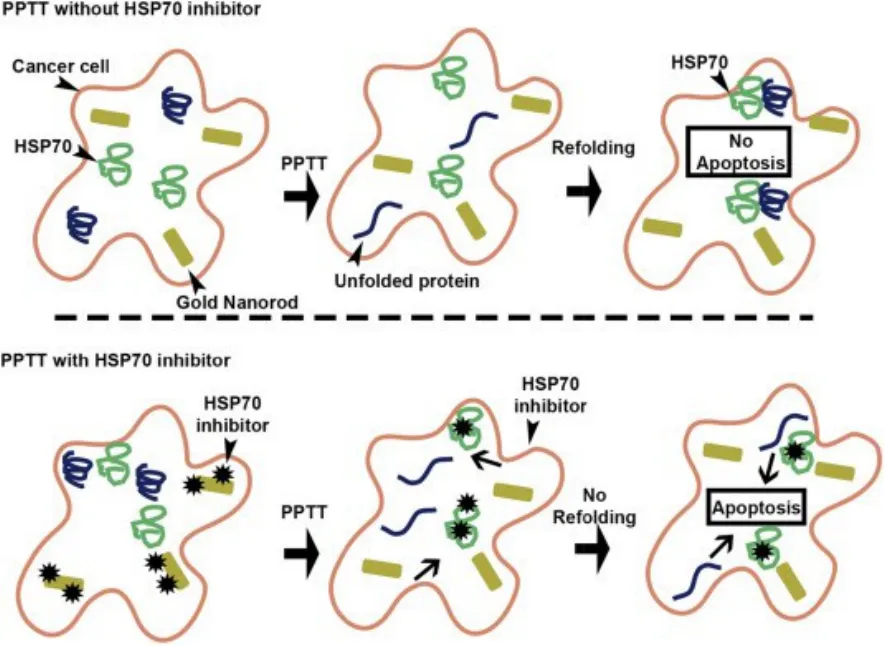
圖8 HSP70抑制劑優化PPTT的模型98Fig.8 A model for HSP70 inhibitor optimized PPTT98.
5.2 基因載體
基因療法由于彌補了蛋白治療的缺陷,能夠治療如傳染病、遺傳病、癌癥等多種疾病,因此成為一種新的治療方法,引起了多方關注,并在介入治療領域應用廣泛。但是,如何制備安全高效的基因載體成為基因治療的一個關鍵性要素。基因載體通常分為兩大類:病毒類和非病毒類。非病毒基因載體具有病毒載體無法比擬的優點,如低細胞毒性和低免疫原性、好的生物相容性、容易生物降解等,從而受到廣泛應用,非病毒基因載體有脂質體、陽離子聚合物和納米顆粒等99?103。金納米棒由于比表面積大及其獨特的光電性質104,以及化學性質穩定、合成方法簡單、毒性低、產率高等優點,在運載DNA、SiRNA方面,應用前景良好。AuNRs能充分吸收紅外光能量并使局部受熱,使蛋白質變性并殺死細胞,因此在治療疾病中展示出特殊的優越性 105?107。
聚乙烯亞胺(PEI) (陽離子聚合物)中的氨基能夠與DNA或SiRNA等生物分子通過靜電作用締合成復合物。其“質子海綿效應”可避免核酸酶降解DNA,促進與細胞的結合和攝取,在許多體內外基然PEI的毒性減弱,但轉染效率降低110,113?116。王倩等117致力于提高PEI轉染效率的同時降低其毒因轉染與治療研究中效果顯著108?112。但PEI對細胞毒性大,并且不可降解,而降低相對分子質量雖性,利用低分子量的PEI與AuNRs相結合。一方面利用 PEI的低分子量來降低陽離子聚合物對細胞的毒性,另一方面利用AuNRs的大比表面積擴大 PEI運載基因的能力,從而形成AuNRs/MUA/PEI (圖 9)。AuNRs/MUA/PEI既能夠降低陽離子聚合物對細胞的毒性,又能夠提高整體的轉染率。利用MTT法檢測AuNRs/MUA/PEI對 MCF-7細胞的毒性,實驗結果顯示AuNRs/MUA/PEI對細胞的毒性可以忽略不計,將加入的聚合物濃度增加,細胞存活率仍很高,而相同條件下的 PEI細胞存活率卻很低。由于AuNRs/MUA/PEI制備簡便,毒性低和表面積大,將作為高效的納米載體運送基因及藥物,在生物醫學領域展示出良好的應用前景。圖 9為AuNRs/MUA/PEI 納米載體的制備原理示意圖。
5.3 光熱療法
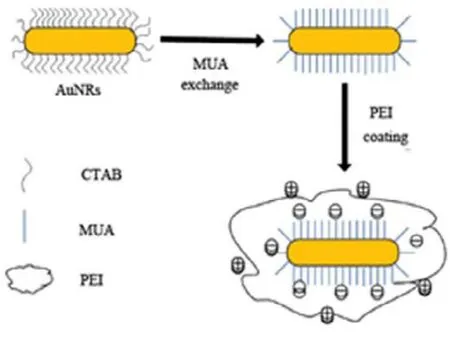
圖9 AuNRs/MUA/PEI納米載體的制備原理示意圖117Fig.9 Synthetic scheme of AuNRs/MUA/PEI117.
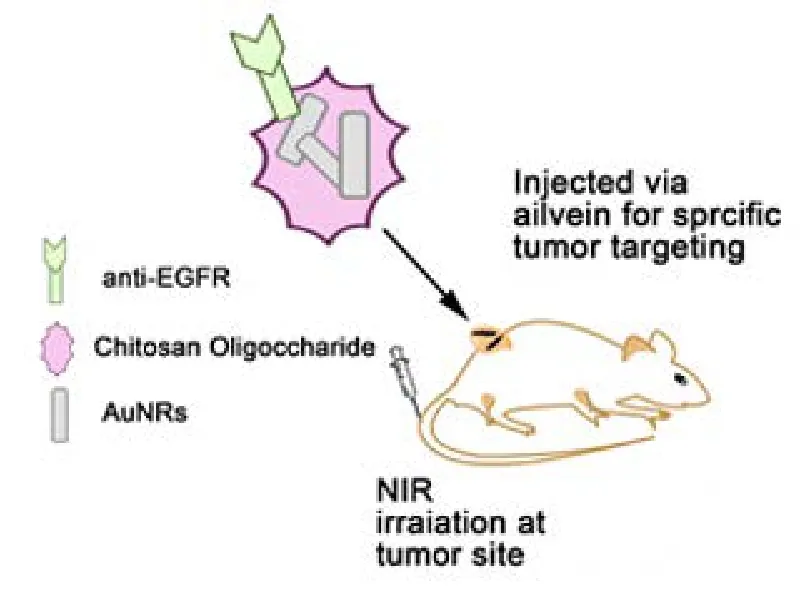
圖10 殼聚糖修飾的金納米棒用于癌癥的光熱治療Fig.10 Gold nanorods modified by Chitosan used in photothermal therapy for cancer.
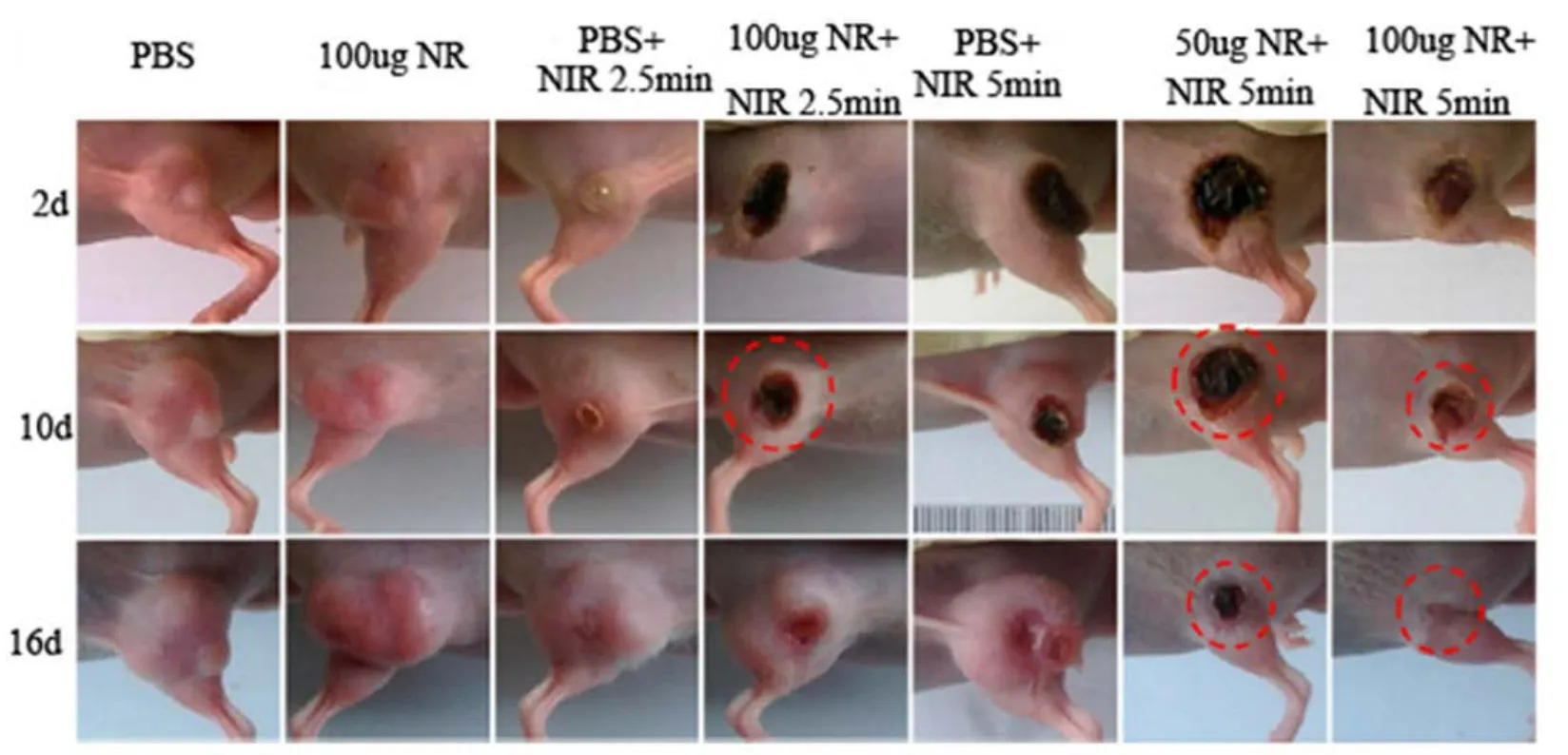
圖11 多齒PEG改性的金納米棒用于小鼠腫瘤的光熱療法Fig.11 Multidentate PEG modified AuNRs used in photothermal therapy for mice’s tumors.
近紅外激光具有穿透性好,對人體組織損傷輕的優點118。而金納米棒生物相容性好,毒性低,光穩定性好,光熱轉換功能高,還能吸收在700?1000 nm近紅外區的波長,這些優勢使金納米棒在光熱治療(photothermltherapy)方面可充當良好的介質119。近年來,在腫瘤及感染性疾病的治療中越來越多地應用金納米棒的光熱療法120。Charan小組33使用殼聚糖修飾金納米棒(圖10),制成生物相容性好、無毒的生物探針,使用光熱療法基于局部高熱可無創成像,為體內靶向治療提供了良好的前景。liu34等人用PEG改性金納米棒,可在體內進行光熱療法,能消融體內腫瘤。該小組設置如圖11所示的體內動力學實驗,用近紅外連續波激光發射器照射小鼠大腿部位的腫瘤,跟蹤腫瘤變化情況,結果表明:注入PEG改性的金納米棒進行光熱治療16 d后,腫瘤可被一次性徹底治愈不復發34。
隱球菌病是由于隱球菌侵染中樞神經而引起的一種深部真菌病121,這種疾病死亡率極高。通常使用兩性霉素進行治療,然而這種治療方式需鞘內輔助注射,且副作用大不能長期使用122。而氟康唑、伊曲康唑等抗真菌藥具有耐藥性,治療效果也不好123,124。肖琴等125用隱球菌的莢膜抗體特異性標記AuNRs,在體外接受近紅外激光照射進行介導光熱治療,發現抗體標記后的AuNRs可以明顯降低隱球菌的細胞活性。由于抗體對抗原的靶向性,抗體標記的AuNRs更易聚集在隱球菌感染的組織區域,這樣可以在集中殺死已感染的細胞的同時避免AuNRs在光熱治療時對周圍正常組織細胞的損傷和破壞。更重要的是該療法可以替代抗真菌藥物,從而避免過度使用抗真菌藥物而出現的副作用。雖然目前的實驗尚處于體外階段,但成功制備的 AuNRs-Ab對隱球菌的特異性靶向性及光熱效應,為光熱方法治療隱球菌感染提供一定的實驗基礎和新的思路。
6 結論與展望
經過近三十年的發展,金納米棒的合成方法已經非常成熟,其長徑比已經可以自由調控,且已陸續應用于生物感應、癌癥治療和藥物載體、基因載體和光熱療法等生物醫學領域。本文綜述了金納米棒的合成方法、表面改性及其在生物醫學中的應用新進展。重點闡述了金納米棒的可控修飾及其在生物感應、癌癥治療和藥物載體、基因載體和光熱療法等領域的最新進展。盡管金納米棒在生物醫學領域已經有了一些初步的應用,但仍然有許多問題需要研究者們繼續探索和研究。例如如何提高金納米棒的選擇性或特異性識別能力?如何解決金納米棒與無機納米載體在疾病治療中的瓶頸問題?如何解決金納米棒熒光量子產率低的問題?如何精確控制金納米棒表面的修飾?還有AuNRs的生長機理和不對稱修飾及其在生物活體內的應用等至今仍不清楚。這些問題都將成為未來幾年乃至幾十年的研究熱點。
針對上述問題,我們認為將分子手性或智能聚合物引入到金納米棒表面,制備出手性金納米棒或智能聚合物修飾的金納米棒,也許會成為一種新的思路。手性識別是生物分子之間的一種非常普遍而重要的識別途徑,因此越來越多的研究者將分子手性引入到納米材料表面得到手性納米材料。例如我們之前的工作將手性分子引入到金團簇的表面,得到手性金團簇可以作為一種新型近紅外熒光探針126,127。受此啟發,我們同樣可以將手性分子引入到金納米棒表面來制備手性金納米棒,這種具有潛在手性識別能力的金納米棒將在藥物載體和生物探針領域具有非常廣闊的應用前景。另一方面,智能聚合物是指可以對環境中力、熱、光、電、pH、溶劑等因素變化表現出響應性的一類大分子,如果可以將這類大分子修飾到金納米棒表面,那么這種兼具金納米棒獨特光學活性和智能聚合物智能響應性能力的新型金納米棒將在環境監控、污水檢測、大氣治理等領域有著非常廣闊的應用前景。
(1) Shen, L. M.; Yao, J. L.; Gu, R. A. Spectrosc. Spect Anal. 2005, 25,1998. [沈理明, 姚建林, 顧仁敖. 光譜學與光譜分析雜志, 2005,25, 1998.] doi: 10.3321/j.issn:1000-0593.2005.12.024
(2) Liu, M.; Yang, P. H.; Cai, J. Y. Prog. Biochem. Biophy. 2009, 11,1402. [劉 媚, 楊培慧, 蔡繼業. 生物化學與生物物理進展, 2009,11, 1402.] doi: 10.3724/SP.J.1206.2009.00194
(3) Ke, S. L.; Kan C. X.; Mo, B.; Cong, B.; Zhu, J. J. Acta Phys.-Chim.Sin. 2012, 28, 1275. [柯善林, 闞彩俠, 莫 博, 從 博, 朱杰君. 物理化學學報, 2012, 28, 1275.]doi: 10.3866/PKU.WHXB201203162
(4) Ma, Z. F.; Tian, L.; Di, J.; Ding, T. Prog. Chem. 2009, 21, 134. [馬占芳, 田 樂, 邸 靜, 丁 騰. 化學進展, 2009, 21, 134.]
(5) Dubertret, B.; Calame, M.; Libchaber, A . J. Nat. Biotechnol. 2001,19, 365. doi:10.1038/86762
(6) Imahori, H.; Fukuzumi, S. Adv. Mater. 2001, 13, 1197.doi: 10.1002/1521-4095(200108)13:15<1197::AID-ADMA1197>3.0.CO;2-4
(8) Nie, S.; Eniory, S. R. Science 1997, 275, 1102.doi: 10.1126/science.275.5303.1102
(9) Gao, G. B.; Zhang, M. X.; Gong, D. J.; Chen, R.; Hu, X. J.; Sun, T.L. Nanoscale 2017, 9, 4107. doi: 10.1039/c7nr00699c
(10) Thakor, A. S.; Jokerst, J.; Zavaleta, C.; Massoud, T. F.; Gambhir, S.S. Nano Lett. 2011, 11, 4029. doi: 10.1021/nl202559p
(11) Lu, W. S.; Wang, H. F.; Zhang, J. P.; Jiang, L. Prog. Chem. 2015, 27,785. [魯聞生, 王海飛, 張建平, 江 龍. 化學進展, 2015, 27, 785.]doi: 10.7536/PC150111
(12) Wang, P. B.; Song, Y. Z.; Du X. Y.; Liu, G. H. Rare Met. Mat. Eng.2010, 39, 1672. [王平波, 宋玉哲, 杜雪巖, 劉國漢. 稀有金屬材料與工程, 2010, 39, 1672.]
(13) Sau, T. K.; Murphy, C. J. Langmuir 2004, 20, 6414.doi: 10.1021/la049463z
(14) Lohse, S. E.; Murphy, C. J. Chem. Mater. 2013, 25, 1250.doi: 10.1021/cm303708p
(15) Zhou, H. Y.; Zhou, R.; Xiong, B.; He, Y. Chin. J. Anal. Chem. 2012,40, 1807. [周海英, 周 瑞, 熊 斌, 何 彥. 分析化學, 2012, 40,1807.] doi: 10.3724/SP.J.1096.2012.20793
(16) Nikoobakht, B.; El-Sayed, M. A. Chem. Mater. 2003, 15, 1957.doi: 10.1021/cm020732l
(17) Gao, Q.; Qian, Y.; Xia, Y.; Jiang, C. Y.; Qian, W. P. Acta Chim. Sin.2011, 69, 1617. [高 倩, 錢 勇, 夏 炎, 蔣彩云, 錢衛平. 化學學報. 2011, 69, 1617.]
(18) Luo, J. J.; Guo, Y. J.; Tang, Y. J.; Zhang, L.; Wang, J. H.; Yang, P. H.Chin. J. Anal. Chem. 2013, 41, 1413. [駱健俊, 郭顏杰, 唐艷娟,張 璐, 王錦慧, 楊培慧. 分析化學, 2013, 41, 1413.]doi: 10.3724/SP.J.1096.2013.30148
(19) Martin, C. R. Science 1994, 263, 1961.doi: 10.1126/science.266.5193.1961
(20) Yu, Y. Y.; Chang, S. S. Lee, C. L.; Wang, C. C. J. Phys. Chem. B.1997, 101, 6661. doi: 10.1021/jp971656q
(21) Kim, F.; Song, J. H.; Yang, P. D. J. Am. Chem. Soc. 2002, 124,14316. doi: 10.1002/chin.200313016
(22) Jana, N. R.; Gearheart, L.; Murphy, C. J. Adv. Mat. 2001, 13, 1389.doi: 10.1002/1521-4095(200109)13:18<1389::AID-ADMA1389>3.0.CO;2-F
(23) Jana, N. R.; Gearheart, L.; Murphy, C. J. Langmuir 2001, 17, 6782.doi: 10.1021/la0104323
(24) Jana, N. R.; Gearheart, L.; Murphy, C. J. J. Phys. Chem. B 2001,105, 4065.doi: 10.1021/jp0107964
(25) Nguyen, T. N.; Nguyen, T. L.; Luong, T. T. Adv. Nat. Sci. 2016, 7,015006. doi: 10.1088/2043~6262/7/1/015006
(26) Zhang, L.; Belova, V.; Wang, H. Q.; Dong, W. F.; Moehwald, H.Chem. Mater. 2014, 26, 2244. doi: 10.1021/cm404194n
(27) Vigderman, L.; Zubarev, E. R. Chem. Mater. 2013, 25, 1450.doi: 10.1021/cm303661d
(28) Wang, Y.; Wang, F. H.; Guo, Y.; Chen, R. J.; Shen, Y. Y.; Guo, A. J.;Liu, J. Y.; Zhang, X.; Zhou, D. J.; Guo S. R. J. Nanopart. Res. 2014,16, 2806. doi: 10.1007/s11051-041-2806-3
(29) Sirajuddin.; Mchler, A.; Torriero, A. A.; Nafady, A.; Lee, C. Y.;Bond, A. M.; Mullane, A. P.; Bhargava, S.K. Colloids Surf., A 2010,370, 35. doi: 10.1016/j.colsurfa.2010.08.041
(30) Lohse, S. E.; Murphy, C. J. Chem. Mater. 2013, 25, 1250. doi:10.1021/cm303708p
(31) Zhan, Q. Q.; Qian, J.; Li, X.; He, S. L. Nanotechnology 2010, 21,055704. doi: 10.1088/0957-4484/21/5/055704
(32) Connor, E. E.; Mwamuka, J.; Gole, A.; Murphy, C. J.; Wyatt, M. D.Small 2005, 1, 325. doi: 10.1002/smll.200400093
(33) Charan, S.; Sanjiv, K.; Singh, N.; Chien, F. C.; Chen, Y. F.; Nergui,N. N.; Huang, S. H.; Kuo, C. W.; Lee, T. C.; Chen, P. L.Bioconjugate Chem. 2012, 23, 2173. doi: 10.1021/bc3001276
(34) Liu, X. S.; Huang, N.; Li, H.; Wang, H. B.; Jin, Q.; Ji, J. ACS Appl.Mater. Interfaces 2014, 6, 5657. doi: 10.1021/am5001823
(35) Chang, G. R.; Lu, X. Y; Hu, F. K.; Chen, L.; Pan, C. Fine Chem.2016, 33 ,491. [常貫儒, 魯信勇, 胡逢愷, 陳 龍, 潘成兵. 精細化工, 2016, 33, 491.] doi:1 0.13550 /j. jxhg.2016.05.002
(36) Chang, C. S.; Rothberg, L. J. Chem. Mater. 2015, 27 , 3211.doi: 10.1021/cm504086z
(37) Wang, Y.; Zhou, F. Z.; Sun, H. H. New Chem. Mater. 2016, 44, 84.[王 怡, 周鳳珍, 孫宏浩. 化工新型材料, 2016, 44, 84.]
(38) Gao, B.; Xu, J.; He, K. W.; Shen, L.; Chen, H.; Yang, H. J.; Li, A.H.; Xiao, W. H. Mol. Imaging Biol. 2016, 18, 667.doi: 10.1007/s11307-016-0938-9
(39) Park, H.; Lee, S.; Chen, L.; Lee, E. K.; Shin, S. Y.; Lee, Y. H.; Son,S. W.; Oh, C. H.; Song, J. M.; Kang, S. H.; Choo, J. Phys. Chem.Chem. Phys. 2009, 11, 7444. doi: 10.1039/B904592A
(40) Jin, X. T.; Liu,G.; Li, J. Z.; Sun, L. L.; Wang, J. R.; Li, J. F.; Li, P.;Chen, W. Q.; Wang, Q.; Tong, T. Chem. J. Chin. Univ. 2016, 37,224. [金新天, 劉 剛, 李君哲, 孫麗麗, 王俊榮, 李俊鋒, 李 沛,陳文慶, 王 強, 佟 倜. 高等學校化學學報, 2016, 37, 224.]doi: 10.7503/cjcu20150662
(41) Tong, L.; He, W.; Zhang, Y. S.; Zheng, W.; Cheng, J. X. Langmuir 2009, 25, 12454. doi: 10.1021/la902992w
(42) Bickford, L.; Sun, J.; Fu, K.; Lewinski, N.; Nammalvar, V.; Chang,J.; Drezek, R. Nanotechnol 2008, 19, 315102. doi:10.1088/0957-4484/19/31/315102
(43) Liu, M. Z.; Guyot-Sionnest, P. J. Phys. Chem. B. 2005, 109, 22192.doi: 10.1021/jp054808n
(44) Johnson, C. J.; Dujardin, E.; Davis, S. A.; Murphy, C. J.; Mann, S.J. Mater. Chem. 2002, 12, 1765. doi: 10.1039/B200953F
(45) Nikoobakht, B.; El-Sayed, M. A. Langmuir 2001, 17, 6368.doi: 10.1021/la010530o
(46) Wang, Y. L.; DePrince, A. E., III; Gray, S. K.; Lin, X. M.; Pelton,M. J. Phys. Chem. Lett. 2010, 1, 2692. doi: 10.1021/jz1010048
(47) Wang, F.; Cheng, S.; Bao, Z. H.; Wang, J. F. Angew. Chem. Int. Ed.2013, 52, 10344. doi: 10.1002/anie.201304364
(48) Nikoobakht, B.; El-Sayed, M. A. Langmuir 2001, 17, 6368.doi: 10.1021/la010530o
(49) Lee, S.; Anderson, L. J. E.; Payne, C. M.; Hafner, J. H. Langmuir 2011, 27, 14748. doi: 10.1021/la202918n
(50) Kou, X. S.; Zhang, S. Z.; Yang, Z.; Tsung, C. K.; Stucky, G. D.;Sun, L. D.; Wang, J. F.; Yan, C. H. J. Am. Chem. Soc. 2007, 129,6402. doi: 10.1021/ja0710508
(51) Kou, X. S.; Sun, Z. H.; Yang, Z.; Chen, H. J. ; Wang, J. F.Langmuir 2009, 25, 1692. doi: 10.1021/la802883p
(52) Guo, H. Y.; Lu, L, H.; Wu, C.; Pan, J. G.; Hu, J. W. Acta Chim. Sin.2009, 67, 1603. [郭紅燕, 蘆玲慧, 吳 超, 潘建高, 胡家文. 化學學報, 2009, 67, 1603.] doi: 10.3724/SP.J.1096.2013.30148
(53) Li, C. Z.; Male, K. B.; Hrapovic, S.; Luong, J. H. Chem. Commun.2005, 31, 3924. doi: 10.1039/b504186d
(54) Ye, J. Q.; Zhang, Y.; Huang, H.; Wang, J.; Jiang, Z.; Bai, M. Sens.Actuators, B 2017, 243, 1255. doi: 10.1016/j.snb.2016.12.098
(55) He, X.; Wang, S. P.; Zhou, Y. F.; Huang, C. M.; Lyuqiu, S. J.; Ning,S. B. Chin. J. Zoonose 2016, 32, 315. [何 鑫, 汪世平, 周云飛, 黃成銘, 閭丘思嘉, 寧水兵. 中國人獸共患病學報, 2016, 32, 315.]doi: 10.3969/j.issn.1002-2694.2016.04.001
(56) Cao, J.; Galbraith, E. K.; Sun, T.; Grattan, K. T. Sens. Actuators, B 2012, 169, 360. doi: 10.1016/j.snb.2012.05.019
(57) Ferlay, J.; Shin, H. R.; Bray, F.; Forman, D.; Mathers, C.; Parkin, D.W. Int. J. Cancer. 2010, 127, 2893. doi: 10.1002/ijc.25516
(58) Stout, N. K.; Lee, S. J.; Schechter, C. B.; Kerlikowske, K.; Alagoz,O.; Berry, D.; Buist, D.S.; Cevik, M.; Chisholm, G.; de Koning, H.J.; Huang, H.; Hubbard, R. A.; Miglioretti, D. L.; Munsell, M. F.;Trentham-Dietz, A.; van Ravesteyn, N. T.; Tosteson, A. N.;Mandelblatt, J. S. J. Natl. Cancer. Inst. 2014, 106, 092.doi: 10.1093/jnci/dju092
(59) Bevers, T. B.; Anderson, B. O.; Bonaccio, E.; Buys, S.; Daly, M. B.;Dempsey, P.J.; Farrar, W. B.; Fleming, I.; Garber, J. E.; Harris, R.E.; Heerdt, A. S.; Helvie, M.; Huff, J.G.; Khakpour, N.; Khan, S. A.;Krontiras, H.; Lyman, G.; Rafferty, E.; Shaw, S.; Smith, M. L.;Tsangaris, T. N.; Williams, C.; Yankeelov, T. J. Natl. Compr. Cancer Network 2009, 7, 1060.
(60) Moran, M. S.; Kaufman, C.; Burgin, C.; Swain, S.; Granville, T.;Winchester, D. P. J. Oncol. Pract. 2013, 9, e62.doi: 10.1200/JOP.2012.000636
(61) Steve, H. P. Cancer 1994, 74, 256. doi: 10.1002/cncr.2820741309
(62) Calhoun, K. E.; Anderson, B. O. J. Clin. Oncol. 2014, 32, 2191.doi: 10.1200/JCO.2014.55.6324
(63) Li, Y.; Zhang, Y. L.; Zhao, M.; Zhou , Q. Q.; Wang, L. L.; Wang, H.Z.; Wang, X. H.; Zhan, L. S. R. Soc. Chem. 2016, 52, 3959.doi: 10.1039/C6CC01014H
(64) Cho, E. C.; Liu, Y.; Xia, Y. N. Angew. Chem. Int. Edit. 2010, 49,1976. doi: 10.1002/anie.200906584
(65) Yu, C. C.; Hu, Y.; Duan, J. H.; Yuan, W.; Wang, C.; Xu, H. Y.; Yang,X. D. Plos One 2011, 6 ,e24077. doi: 10.1371/journal.pone.0024077
(66) Yang, Y. D.; Liu, G, Z.; Li, D. Z.; Xu, J. H.; Yang, L. M. Chin. Sci.Bull. 2015, 60, 817. [楊玉東, 劉公召, 李冬至, 徐菁華, 楊林梅.科學通報, 2015, 60, 817] doi: 10.1360/N972014-00887
(67) Luo, T.; Huang, P.; Gao, G.; Shen, G.; Fu, S.; Cui, D.; Zhou, C.;Ren, Q. Opt. Express 2011, 19, 17030. doi: 10.1364/OE.19.017030
(68) Zhang, J. B.; Balla, N. K.; Gao, C.; Sheppard, C. J.; Yung, L. Y.;Rehman, S.; Teo, J. Y.; Kulkarni, S. R.; Fu, Y.H.; Yin, S. J. Aust. J.Chem. 2012, 65, 290. doi: 10.1071/CH12037
(69) Joshi, P. P.; Yoon, S. J.; Hardin, W. G.; Emelianov, S.; Sokolov, K.V. Bioconjugate Chem. 2013, 24, 878. doi: 10.1021/bc3004815
(70) Lajunen, T.; Viitala, L.; Kontturi, L.S.; Laaksonen, T.; Liang, H.;Vuorimaa-Laukkanen, E.; Viitala, T.; Le Guével, X.; Yliperttula, M.;Murtom?ki, L.; Urtti, A. J. Controlled Release 2015, 203, 85.
(71) Mayer, G.; Heckel, A. Angew. Chem., Int. Ed. Engl. 2006, 45, 4900.doi: 10.1002/anie.200600387
(72) Zhong, Y. N.; Wang, C.; Cheng, L.; Meng, F. H.; Zhong, Z. Y.; Liu,Z. Biomacromolecules 2013, 14, 2411. doi: 10.1021/bm400530d
(73) Wijaya, A.; Schaffer, S. B.; Pallares, I. G.; Hamad-Schifferli, K. .ACS Nano 2009, 3, 80. doi: 10.1021/nn800702n CCC: $40.75
(74) Park, H.; Yang, S.; Kang, J. Y.; Park, M. ACS Med. Chem. Lett.2016, 7, 1087. doi: 10.1021/acsmedchemlett.6b00293
(75) Ali,H. R.; Ali, M. R.; Wu, Y.; Selim, S. A.; Abdelaal, H. F.; Nasr, E.A.; El-Sayed, M. A. Bioconjugate Chem. 2016, 27, 2486.doi: 10.1021/acs.bioconjchem.6b00430
(76) Dickerson, E. B.; Dreaden, E. C.; Huang, X. H.; El-Sayed, I. H.;Chu, H. H.; Pushpanketh, S.; McDonald, J. F.; El-Sayed, M. A.Cancer Lett. 2008, 269, 57. doi: 10.1016/j.canlet.2008.04.026
(77) Li, W. Q.; Sun, C. Y.; Wang, F.; Wang, Y. C.; Zhai, Y. W.; Liang, M.;Liu, W. J.; Liu, Z. M.; Wang, J.; Sun, F. Nano Lett. 2013, 13, 2477.doi: 10.1021/nl400536d
(78) Bagley, A. F.; Hill, S.; Rogers, G. S.; Bhatia, S. N. ACS Nano 2013,7, 8089. doi: 10.1021/nn4033757
(79) Zhou, T.; Yu, M. F.; Zhang, B.; Wang, L. M.; Wu, X. C.; Zhou, H.J.; Du, Y. P.; Hao, J. F.; Tu, Y. P.; Chen, C. Y.; Wei, T. T. Adv. Funct.Mater. 2014, 24, 6922. doi: 10.1002/adfm.201401642
(80) Huang, X. H.; EI-Sayed, I. H.; EI-Sayed, M. A. Methods Mol. Biol.2010, 624, 343. doi: 10.1007/978-1-60761-609-2_23
(81) Alkilany, A. M.; Thompson, L. B.; Boulos, S. P.; Sisco, P. N.;Murphy, C. J. Adv. Drug Delivery Rev. 2012, 64, 190.doi: 10.1016/j.addr.2011.03.005
(82) Ali, M. R. K.; Snyder, B.; El-Sayed, M. A. Langmuir 2012, 28,9807. doi: 10.1021/la301387p
(83) Huang, X. H.; Neretina, S.; El-Sayed, M. A. Adv. Mater. 2009, 21,4880. doi: 10.1002/adma.200802789
(84) Shi, P.; Li, M.; Ren, J. S.; Qu, X. G. Adv. Funct. Mater. 2013, 23,5412. doi: 10.1002/adfm.201301015
(85) Sun, M. M.; Liu, F.; Zhu, Y. K.; Wang, W. S.; Hu, J.; Liu, J.; Dai, Z.F.; Wang, K.; Wei, Y.; Bai, J.; Gao, W. P. Nanoscale 2016, 8, 4452.doi: 10.1039/c6nr00056h
(86) Shen, J. L.; Kim, H. C.; Mu, C. F.; Gentile, E.; Mai, J. H.; Wolfram,J.; Ji, L. N.; Ferrari, M.; Mao, Z. W.; Shen, H. F. Adv. Healthc Mater. 2014, 3, 1629. doi: 10.1002/adhm.201400103
(87) Huang, X. H.; Kang, B.; Qian, W.; Mackey, M. A.; Chen, P. C.Oyelere, A. K.; El-Sayed, I. H.; El-Sayed, M. A. J. Biomed. Opt.2010, 15, 7. doi: 10.1117/1.3486538
(88) Yang, X. J.; Liu, X.; Liu, Z.; Pu, F.; Ren, J. S.; Qu, X. G. Adv Mater.2012, 24, 2890. doi: 10.1002/adma.201104797
(89) Zhu, Z. F.; Zou, Y. S.; Hu, W. D.; Li, Y. B.; Gu, Y.; Cao, B. Q.; Guo,N.; Wang, L.; Song, J. Z.; Zhang, S. L.; Gu, H. S.; Zeng, H.B. Adv.Funct. Mater. 2016, 26, 1793. doi: 10.1002/adfm.201504884
(90) Shao, J. X.; Xuan, M. J.; Dai, L. R.; Si, T. Y.; Li, J. B.; He, Q.Angew. Chem., Int, Edit, 2015, 54, 12782. doi:10.1002/anie.201506115
(91) Kannadorai, R. K.; Chiew, G. G. Y.; Luo, K. Q.; Liu, Q. Cancer Lett. 2015, 357, 152. doi: 10.1016/j.canlet.2014.11.022
(92) Perez-Hernandez, M.; del Pino, P.; Mitchell, S. G.; Moros, M.;Stepien, G.; Pelaz, B.; Parak, W. J.; Galvez, E. M.; Pardo, J.; de la Fuente, J. M. ACS Nano 2015, 9, 52. doi: 10.1021/nn505468v
(93) Orosz, P.; Echtenacher, B.; Falk, W.; Rüschoff, J.; Weber, D.;M?nnel, D. N. J. Exp. Med. 1993, 177, 1391. doi:10.1084/jem.177.5.1391
(94) Kudryavets, Y. I. Exp. Oncol. 1998, 20, 114.
(95) Bonfil, R. D.; Bustuoabad, O. D.; Ruggiero, R. A.; Meiss, R. P.;Pasqualini, C. D. Clin. Exp. Metastasis. 1988, 6, 121.doi: 10.1007/bf01784843
(96) Ali, M. R. K.; Panikkanvalappil, S. R.; El-Sayed, M. A. J. Am.Chem. Soc. 2014, 136, 4464. doi: 10.1021/ja4124412
(97) Miyako, E.; Deguchi, T.; Nakajima, Y.; Yudasaka, M.; Hagihara, Y.;Horie, M.; Shichiri, M.; Higuchi, Y.; Yamashita, F.; Hashida, M.;Shigeri, Y.; Yoshida, Y.; Iijima, S. Proc. Natl. Acad. Sci. U. S. A.2012, 109, 7523. doi: 10.1073/pnas.1204391109
(98) Ali, M. R. K.; Ali, H. R.; Rankin, C. R.; El-Sayed, M. A.Biomaterials 2016, 102, 1. doi: 10.1016/j.biomaterials.2016.06.017
(99) Zuckerman, J. E.; Choi, C. H. J.; Han, H.; Davis, M. E. Proc. Natl.Acad. Sci. U. S. A. 2012, 109, 3137. doi: 10.1073/pnas.1200718109
(100) Videira, M.; Arranja, A.; Rafael, D.; Gaspar, R.Nanomed-Nanotechnol. Biol. Med. 2014, 10, 689.doi: 10.1016/j.nano.2013.11.018
(101) Novo, L.; van Gaal, E. V. B.; Mastrobattista, E.; van Nostrum, C. F.;Hennink, W. E. J. Controlled Release. 2013, 169, 246.doi: 10.1016/j.jconrel.2013.03.035
(102) Kwok, A.; Hart, S. L. Nanomed-Nanotechnol. Biol. Med. 2011, 7,210. doi: 10.1016/j.nano.2010.07.005
(103) Novo, L.; Mastrobattista, E.; van Nostrum, C. F.; Hennink, W. E.Bioconjugate Chem. 2014, 25, 802. doi: 10.1021/bc500074a
(104) Yin, F.; Yang, C. B.; Wang, Q. Q.; Zeng, S. W.; Hu, R.; Lin, G. M.;Tian, J. L.; Hu, S. Y.; Lan, R. F.; Yoon, H. S.; Lu, F.; Wang, K.;Yong, K. T. Theranostics 2015, 5, 818. doi: 10.7150/thno.11335
(105) Sun, G. M.; Yang, P. H.; Sun, J. H.; Cai, J. Y. Chin. J. Lumin. 2011,32, 636. doi: 10.3788/fgxb20113206.0636
(106) Han, L.; Zhao, J.; Zhang, X.; Cao, W. P.; Hu, X. X.; Zou, G. Z.;Duan, X. L.; Liang, X. J. ACS nano. 2012, 6, 7340.doi: 10.1021/nn3024688
(107) Lee, S. K.; Han, M. S.; Asokan, S.; Tung, C. H. Small 2011, 7, 364.doi: 10.1002/smll.201001314
(108) Troiber, C.; Kasper, J. C.; Milani, S.; Scheible, M.; Martin, I.;Schaubhut, F.; Kuchler, S.; Radler, J.; Simmel, F. C.; Friess, W.;Wagner, E. Eur. J. Pharm. Biopharm. 2013, 84, 255.doi: 10.1016/j.ejpb.2012.08.014
(109) Xue, H. Y.; Wong, H. L. ACS Nano 2011, 5, 7034.doi: 10.1021/nn201659z
(110) Park, J. S.; Yang, H. N.; Woo, D. G.; Jeon, S. Y.; Do, H. J.; Lim, H.Y.; Kim, J. H.; Park, K. H. Biomaterials 2011, 32, 3679.doi: 10.1016/j.biomaterials.2011.01.063
(111) TrosdeIlarduya, C. T.; Sun, Y.; Duezguenes, N. Eur. J. Pharm. Sci.2010, 40, 159. doi: 10.1016/j.ejps.2010.03.019
(112) Lee, Y.; Miyata, K.; Oba, M.; Ishii, T.; Fukushima, S.; Han, M.;Koyama, H.; Nishiyama, N.; Kataoka, K. Angew. Chem. Int. Edit.2008, 47, 5163. doi: 10.1002/anie.200800963
(113) Tsai, L. R.; Chen, M. H.; Chien, C. T.; Chen, M. K.; Lin, F. S.; Lin,K. M. C.; Hwu, Y. K.; Yang, C. S.; Lin, S. Y. Biomaterials 2011, 32,3647. doi: 10.1016/j.biomaterials.2011.01.059
(114) Tang, G. P.; Guo, H. Y.; Alexis, F.; Wang, X.; Zeng, S.; Lim, T. M.;Ding, J.; Yang, Y. Y.; Wang, S. J. Gnne. Med. 2006, 8, 736.doi: 10.1002/jgm.874
(115) Goula, D.; Remy, J. S.; Erbacher, P.; Wasowicz, M.; Levi, G.;Abdallah, B.; Demeneix, B. A. Gene Ther. 1998, 5, 712.doi: 10.1038/sj.gt.3300635
(116) Vicennati, P.; Giuliano, A.; Ortaggi, G.; Masotti, A. Curr. Med.Chem. 2008, 15, 2826. doi:10.2174/092986708786242778
(117) Wang, Q.; Liu L. W.; Zhu, L. X.; Zou, P.; Hu, S. Y.; Bu, C. F. Chin.J. Lumin. 2015, 36, 1271. [王 倩, 劉麗煒, 朱伶西, 鄒 鵬, 胡思怡, 卜承飛. 發光學報, 2015, 36, 1271.]doi: 10.3788/fgxb20153611.1271
(118) Weissleder, R.; Ntziachristos, V. Nat. Med. 2003, 9, 123.doi: 10.1038/nm0103-123
(119) Naik, G. V.; Shalaev, V. M.; Boltasseva, A. Adv. Mater. 2013, 25,3264. doi: 10.1002/adma.201205076
(120) Jabeen, F.; Najam-ul-Haq, M.; Javeed, R.; Huck, C. W.; Bonn, G. K.Molecules 2014, 19, 20580. doi: 10.3390/molecules191220580
(121) Orsini, J.; Blaak, C.; Mahmoud, D.; Young-Gwang, J. J. Community Hosp. Intern. Med. Perspect. 2015, 5, 26098.doi: 10.3402/jchimp.v5.26098
(122) Ostrosky-Zeichner, L.; Marr, K. A.; Rex, J. H.; Cohen, S. H. Clin.Infect. Dis. 2003, 37, 415. doi: 10.1086/376634
(123) Arndt, C.; Walsh, T. J.; McCully, C. L.; Balis, F. M.; Pizzo, P. A.;Poplack, D. G. J. Infect. Dis. 1988, 157, 178. doi:https://doi.org/10.1093/infdis/157.1.178
(124) Van Peer, A.; Woestenborghs, R.; Heykants, J.; Gasparini, R.;Gauwenbergh, G. Eur. J. Clin. Pharmacol. 1989, 36, 423.doi: 10.1007/bf00558308
(125) Xiao, Q.; Chen, M.; Xu, N. Chin. J. Mycol. 2015, 10, 134. [肖 琴,陳 敏, 徐 楠. 中國真菌學雜志, 2015, 10, 134.]doi: 10.3969/j.issn.1673-3827.2015.03.003
(126) Gong, D. J.; Gao, G. B.; Zhang, M. X.; Sun, T. L. Prog. Chem.2016, Z2, 296. [龔德君, 高冠斌, 張明曦, 孫濤壘. 化學進展,2016, Z2, 296.] doi: 10.7536/PC150931
(127) Gao, G. B.; Gong, D. J.; Zhang, M. X.; Sun, T. L. Acta Chim. Sin.2016, 74, 363. [高冠斌, 龔德君, 張明曦, 孫濤壘. 化學學報,2016, 74, 363.] doi: 10.6023/A16010038
Gold Nanorods——from Controlled Synthesis and Modification to Nano-Biological and Biomedical Applications
HU Xue-Jiao GAO Guan-Bin* ZHANG Ming-Xi*
(State Key Laboratory of Advanced Technology for Materials Synthesis and Processing,Wuhan University of Technology, Wuhan 430070, P. R. China)
Gold nanorods (AuNRs) have been the focus of considerable attention in the nano-biotechnology and biomedicine fields because of their unique optical activities, adjustable aspect ratios, ease of surface modification, and good biocompatibility. AuNRs offer specific tunable surface plasmon resonance (SPR) effects (including TSPR and LSPR), which can tune their fluorescence-emission between the visible and near-infrared (NIR) zones. Controlled synthesis and surface modification determine the physical and chemical properties of AuNRs, which ultimately determine their biocompatibility and biomedical applicability. In this review, the four main types of controlled synthesis (template, electrochemical synthesis, photochemical synthesis, and seeded growth methods), controlled surface modification methods, as well as the nano-biological and biomedical applications of AuNRs, are summarized. The controlled surface modification methods of AuNRs and their application to molecular probes, bio-sensing, bio-imaging, gene carriers, pharmaceutical carriers,and cancer photothermal therapy are discussed in detail. Finally, we outline our personal perspectives on the main issue affecting AuNRs in biological applications. That is, chiral molecular and smart polymers can be introduced onto the surfaces of AuNRs to improve the specific recognition of tumor cells and to increase fluorescence quantum yields, thus providing a new direction for the development of AuNRs.
Gold nanorods; Controlled synthesis; Controlled modification; Nano-biological applications; Biomedical applications
January 3, 2017; Revised: March 13, 2017; Published online: April 11, 2017.
O648
10.1126/science.283.5408.1676
[Review]
10.3866/PKU.WHXB201704112 www.whxb.pku.edu.cn
*Corresponding authors. GAO Guan-Bin, Email: gbgao@whut.edu.cn; Tel: +86-15827567674. ZHANG Ming-Xi, Email: mxzhang@whut.edu.cn;Tel: +86-13476111239.
The project was supported by the National Natural Science Foundation of China (51533007, 51521001, 21404083).
國家自然科學基金(51533007, 51521001, 21404083)資助項目
? Editorial office of Acta Physico-Chimica Sinica
胡雪嬌,1993年生。2015畢業于沈陽化工大學高分子材料與工程專業,獲學士學位。2015年至今就讀于武漢理工大學材料工程專業。主要研究方向為金納米材料的制備與應用。
高冠斌,1987年生。2016年畢業于武漢理工大學材料物理與化學專業,獲博士學位。同年留校擔任材料復合新技術國家重點實驗室助理研究員。主要研究方向為智能納米材料、生物界面材料等。張明曦,1982年生。2010年畢業于武漢大學分析化學專業,獲博士學位。2010年起在武漢理工大學工作,2013年晉升副研究員。主要研究方向為納米生物技術、仿生復合材料、生物醫用材料等。

