糖尿病型牙周炎牙齦組織中炎癥因子表達及與細胞凋亡關系
陳鐵樓 張新海 徐爾理 唐大海 趙海軍 徐逸敏 張曉莉 欒瑋 劉進 陳駿 馬麗婷
糖尿病型牙周炎牙齦組織中炎癥因子表達及與細胞凋亡關系
陳鐵樓 張新海 徐爾理 唐大海 趙海軍 徐逸敏 張曉莉 欒瑋 劉進 陳駿 馬麗婷
目的探討糖尿病型牙周炎(diabetes associated periodontitis,DAP)牙齦組織中凋亡細胞發(fā)生及與IL-1β和TNFα表達的關系。方法納入DAP患者和健康齦(H)受試者各20 例,用HE染色和Tunnel法觀察牙齦細胞凋亡,透射電鏡觀察凋亡細胞超微結構;用免疫組化(IHC)檢測牙齦組織炎癥因子IL-1β和TNFα表達。結果DAP組牙齦上皮棘細胞層和基底細胞層見明顯細胞凋亡,固有層凋亡細胞較少;DAP組牙齦上皮棘細胞和基底細胞凋亡百分率高于H 組(P<0.01);IHC染色發(fā)現(xiàn)DAP組IL-1β和TNFα表達明顯高于H組,主要陽性表達細胞為巨噬細胞、漿細胞和淋巴細胞。結論DAP患者牙齦組織中IL-1β和TNFα在細胞凋亡中起重要作用。
細胞凋亡; 糖尿病型牙周炎(DAP); 炎癥因子; 機制
糖尿病型牙周炎(diabetes associated periodontitis,DAP)可因血糖升高和糖耐量降低引起機體對牙周局部刺激因子抵抗力降低,出現(xiàn)牙齦炎癥、牙槽骨吸收和組織愈合緩慢[1]。糖尿病患者發(fā)生牙周炎危險性比非糖尿病者高2.8~3.4 倍[2]。研究發(fā)現(xiàn),在糖尿病高糖狀態(tài)時可影響牙周炎凋亡相關蛋白表達,并可通過調(diào)節(jié)凋亡相關蛋白表達促進胰島細胞凋亡和胰島分泌功能,影響牙周炎發(fā)生和發(fā)展,老年患者牙周炎牙齦組織中凋亡細胞增加[3]。白細胞介素1β(IL-1β)可刺激人牙周韌帶細胞中膠原酶合成,誘導基質(zhì)金屬蛋白酶13(MMP-13)表達,調(diào)控人成骨細胞擴增和凋亡,MMP-13在牙周組織愈合和牙槽骨再生中起一定作用[4]。本文通過對DAP齦組織中IL-1β和TNFα分泌細胞、含量及與細胞凋亡和臨床指標關系分析,以探討IL-1β和TNFα與DAP牙齦細胞凋亡關系。
1 材料與方法
1.1 病例選擇
DAP組20 例,年齡55~76 歲,平均69.5 歲,男11 例,女9 例,要求患者附著喪失(attachment loss,AL)大于5 mm,牙槽骨吸收大于根長1/2;患者空腹血糖7.0 mmol/L,口服葡萄糖耐量2 h≥11.1 mmol/L[5];健康組(H組)20 例,年齡13~18 歲,平均15.2 歲,男12 例,女8 例,AL為0,為正畸拔除牙。受檢者無心血管疾病及遺傳病,就診前6 月內(nèi)未做牙周治療,3 個月內(nèi)未用抗生素及免疫抑制劑,婦女未妊娠。
1.2 主要試劑
兔抗IL-1β抗體和TNFα抗體(南京凱基生物科技有限公司),免疫組化(IHC)SABC試劑盒(武漢博士德生物工程有限公司),DAB顯色劑(北京中杉金橋生物技術有限公司)。
1.3 樣本采集
拔牙時,腭側取牙齦組織,一部分立即放入4%甲醛固定作HE染色、Tunul染色和IHC染色;另一部分用4%多聚甲醛固定制作電鏡標本。
1.4 指標測定
1.4.1 臨床指標測定 拔牙前測定SBI,GI,刻度探針測定PD和AL。
1.4.2 HE染色和TUNNEL染色法檢測凋亡細胞
取經(jīng)4%甲醛固定24 h牙齦組織,石蠟包埋切5 μm切片。①HE染色觀察牙齦上皮和固有層細胞凋亡情況;②Tunnel 染色觀察凋亡細胞比率,細胞凋亡陽性表達位于細胞核,陽性染色為棕黃色或褐色,每張切片陽性細胞計數(shù)標準相同。高倍鏡(×40)下,用10×10網(wǎng)格分別對牙齦上皮陽性細胞和視野下細胞總數(shù)計數(shù),每張切片觀察5 個視野,計算基底層和棘層凋亡陽性細胞表達百分率,PI=陽性細胞數(shù)/細胞總數(shù)×100%。
1.4.3 IL-1β和TNFα的IHC染色和顯微分光光度計定量 對固定包埋牙齦組織,5 μm連續(xù)切片,脫蠟,3%過氧化氫孵育,滴加山羊血清封閉非特異性抗體,加一抗(1∶100),4 ℃冰箱過夜。滴加生物素標記二抗、辣根酶標記鏈霉卵白素工作液,室溫孵育各15 min;DAB顯色,蘇木素復染,固定封片;以PBS代替一抗做空白對照。陽性細胞胞質(zhì)內(nèi)見黃褐色顆粒,高倍鏡下每切片選5 個視野,計數(shù)200 個細胞中陽性細胞數(shù),計算陽性細胞率=陽性細胞數(shù)/細胞總數(shù)×100%。
用MPV-3 型顯微分光光度計對IHC染色切片測定牙齦上皮層和固有層IL-1β和TNFα表達量,測定方法參照陳鐵樓[6]方法。
1.4.4 透射電鏡觀察[7]將4%多聚甲醛固定牙齦組織脫水和樹脂包埋,常規(guī)超薄切片,醋酸鈾、枸櫞酸鉛染色,透射電鏡觀察。
1.5 統(tǒng)計學處理
用SPSS 13.0軟件分析,2 組間比較采用兩樣本t檢驗和方差分析,P<0.05為有統(tǒng)計學意義。
2 結 果
2.1 牙周臨床指標
DAP組SBI,GI,PD,AL均高于H組(P<0.01,表 1)。
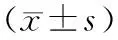
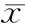

注: 與H組比, ①P<0.01
2.2 HE染色結果
DAP組牙齦上皮釘突增生并連接呈網(wǎng)狀,上皮層基底細胞和棘細胞凋亡細胞較多(圖 1A),固有層大量炎癥細胞浸潤,以巨噬細胞和淋巴細胞多見。膠原纖維排列紊亂,部分纖維斷裂、水腫變性,血管增生;H組牙齦上皮未見明顯細胞凋亡,固有層炎細胞少,膠原纖維排列整齊(圖 1B)。
2.3 超微結構變化
DAP組凋亡細胞核固縮與胞質(zhì)分離出現(xiàn)間隙,內(nèi)質(zhì)網(wǎng)疏松形成空泡,細胞質(zhì)濃縮,線粒體腫脹(圖 1C),嚴重時胞膜內(nèi)陷形成凋亡小體。H組膠原纖維排列整齊,成纖維細胞內(nèi)線粒體和內(nèi)質(zhì)網(wǎng)未見明顯水腫和變性,無明顯核固縮(圖 1D)。
2.4 TUNEL結果
DAP組陽性細胞位于基底細胞層和棘細胞層,染為強陽性(圖 1E),陽性細胞數(shù)明顯多于H組(圖 1F);DAP組牙齦上皮層凋亡細胞指數(shù)(57.9%)顯著高于H組(25.3%,表 2)。

圖 1 2 組牙齦組織中凋亡細胞 (A、D: ×400; C: ×600; F: ×200)
Fig 1 Cell apoptosis of human gingival tissue of the 2 groups (A,D: ×400; C: ×600; F: ×200)
表 2 2 組牙齦上皮層凋亡細胞率比較

Tab 2 Comparison of apoptosis cell ratio in gingival epithelium between 2 groups
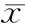
(±s,%)
注: ①與H組比,P<0.01

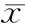

注: ①與H組比,P<0.01
2.5 IHC染色定量
DAP組牙齦固有層IL-1β和TNFα染色均顯示強陽性,陽性細胞為巨噬細胞、漿細胞和淋巴細胞(圖 2A~C),TNFα在上皮基底細胞層也有陽性細胞(圖 2C);H組炎細胞少,IHC染色IL-1β和TNFα呈陰性(圖 2D)或弱陽性。根據(jù)Lamber-Beer定律,組織中IL-1β和TNFα含量可用吸光度值來反映,DAP組牙齦組織中IL-1β和TNFα吸光度值明顯大于H組(表 3)。

圖 2 IHC染色測定2 組牙齦IL-1β和 TNFα表達 (×200)
Fig 2 IL-1β and TNFα expression in human gingival tissue examined by IHC staining (×200)
3 討 論
Kerr[8]于1972 年首次提出細胞凋亡為細胞收縮和核濃縮,伴有特異蛋白降解。據(jù)報道,伴放線放線桿菌可導致牙齦上皮細胞凋亡[9],牙齦卟啉菌產(chǎn)生蛋白酶可誘導牙齦成纖維細胞凋亡[10]。本研究發(fā)現(xiàn),DAP組牙齦上皮層基底細胞和棘細胞凋亡,牙齦組織凋亡細胞比率明顯大于對照組;電鏡發(fā)現(xiàn)凋亡細胞體積變小,線粒體腫脹,胞膜內(nèi)陷,核染色體固縮,表明DAP牙齦上皮細胞出現(xiàn)明顯凋亡。
Alikhani[11]報道,細菌脂多糖在TNFα作用下可增加Caspase-8活性,促進成纖維細胞凋亡。牙齦卟啉單胞菌侵入牙齦上皮2h時,凋亡促進蛋白Bax瞬時增加。牙周厭氧菌能激活人單核細胞產(chǎn)生IL-1β,刺激成纖維細胞產(chǎn)生膠原酶和前列腺素E2,誘導骨吸收。炎癥時中性粒細胞浸潤和激活,合成和釋放TNFα和IL-1β增多,促進炎癥反應。糖尿病長期高血糖導致活性氧族生成,直接損傷牙周組織或胰島β細胞,激活氧化應激敏感信號通路,包括NF-kB、蛋白激酶C(protein kinase C,PKC)等通路,導致TNFα等炎性細胞因子產(chǎn)生并激活膠原酶和破骨細胞引起牙周組織破壞[12]。本研究發(fā)現(xiàn)DAP牙齦固有層IL-1β和TNFα表達增強,主要陽性細胞為巨噬細胞、漿細胞、淋巴細胞;牙齦IL-1β和TNFα表達與SBI和GI顯著正相關。
我們知道,IL-1β和TNFα為炎癥細胞因子可促進炎細胞浸潤,正反饋調(diào)節(jié)炎癥因子加重牙周炎。He等[13]將牙眼葉啉單胞菌接種于糖尿病小鼠顱骨發(fā)現(xiàn)糖尿病組新骨形成被抑制。AI-Mashat等[14]報道,糖尿病可增加前凋亡基因表達和caspase活性,促進成纖維細胞和成骨細胞凋亡,引起DAP牙周組織破壞。DAP長期高血糖導致高級糖基化終產(chǎn)物增加,通過絲裂原活化蛋白激酶刺激細胞凋亡與細胞表面受體結合導致IL-1β和TNFα分泌,促進成纖維細胞凋亡,影響牙周組織修復[15]。本組資料表明DAP細胞凋亡和炎癥組織破壞與組織中IL-1β和TNFα過表達相關。
[1] Chen TL, Xu EL, Xu H, et al. The influence of diabetes enhanced inflammation on cell apoptosis and periodontitis[J]. Adv Biosci Biotechnol, 2012, 3(6): 712-719.
[2] 孟煥新. 牙周病學[M]. 4版. 北京: 人民衛(wèi)生出版社, 2013: 172-174.
[3] 吳嘉怡, 徐喆, 倪佳, 等. 牙周炎對Ⅱ型糖尿病大鼠胰島細胞凋亡相關蛋白表達的影響[J].實用口腔醫(yī)學雜志, 2014, 30(4): 464-468.
[4] Ozeki N, Kawai R, Yamaguchi H, et al. IL-1β-induced matrix metalloproteinase-13 is activated by a disintegrin and metalloprotease-28-regulated proliferation of human osteoblast-like cells[J]. Exp Cell Res, 2014, 323(1): 165-177.
[5] Expert committee on the diagnosis and classification of diabetes mellitus. Report of the expert committee on the diagnosis and classification of diabetes mellitus[C]. Diabetes Care, 2003, 26(Suppl 1): S5-S20.
[6] 陳鐵樓, 周以鈞, 吳織芬, 等. 牙周病患者牙齦組織中PGE2放免測定及免疫組化定量分析[J]. 牙體牙髓牙周病學雜志, 1995, 5(3): 141-143.
[7] 陳鐵樓, 劉景昌, 王曉熙, 等. 高壓氧對豚鼠實驗性牙周炎作用的組織病理學研究[J]. 實用口腔醫(yī)學雜志, 2002, 18(5): 418-420.
[8] Kerr JF, Wyllie AH, Currie AR. Apoptosis: A basic biological phenomenon with wide ranging implication in tissue kinetics[J]. Br J Cancer, 1972, 26(4): 239-257.
[9] Muro M, Koseki T, Akifusa S, et al. Role of CDl4 molecules in internalization of Actinobacillus actinomycetemcomitans by macrophages and subsequent induction of apoptosis[J]. Infect Immun, 1997, 65(4): 1147-1151.
[10] Wang PL, Shirasu S, Shinohara M, et al. Induction of apoptosis in human gingival fibroblasts by a Porphyromonas gingivalis protease preparation[J]. Arch Oral Biol, 1999, 44(4): 337-342.
[11]Alikhani M, Alikhani Z, Graves DT. Apoptotic effects of LPS on fibroblasts are indirectly mediated through TNFR1[J]. J Dent Res, 2004, 83(9): 671-676.
[12]趙海軍, 陳鐵樓, 張新海. 氧化應激誘發(fā)糖尿病性牙周炎作用及機制[J]. 口腔醫(yī)學, 2016, 36(3): 273-276.
[13]He H, Liu R, Desta T, et al. Diabetes causes decreased osteoclastogenesis, reduced bone formation, and enhanced apoptosis of osteoblastic cells in bacteria stimulated bone loss[J]. Endocrinology, 2004, 145(1): 447-452.
[14] Al-Mashat HA, Kandru S, Liu R, et al. Diabetes enhances mRNA levels of proapoptotic genes and caspase activity, which contribute to impaired healing[J]. Diabetes, 2006, 55(2): 487-495.
[15] Liu R, Bal HS, Desta T, et al. Diabetes enhances periodontal bone loss through enhanced resorption and diminished bone formation[J]. J Dent Res, 2006, 85(6): 510-514.
Therelationshipbetweeninflammatoryfactorexpressionandcellapoptosisingingivaltissueofthesubjectswithdiabetesassociatedperiodontitis
CHENTielou1,ZHANGXinhai1,XUErli2,TANGDahai3,ZHAOHaijun1,XUYimin1,ZHANGXiaoli4,LUANWei1,LIUJin1,CHENJun1,MALiting1.
1. 200081Shanghai,DepartmentofPeriodontal,OralResearchCenterofPLA, 2.DepartmentofEndocrinology, 3.DepartmentofMedicalLaboratory, 4.DepartmentofPathology,Hospital411ofPLA,China
Objective: To study the relationship between IL-1β and TNFα expression and cell apoptosis in gingival tissue of the subjects with diabetes associated periodontitis(DAP).Methods20 cases of DAP(group DAP) and 20 cases of health controls(group H) were included. The cell apoptosis and the ultrastructural changes in gingival tissue were observed by Tunnel staining and transmission electron microscope(TEM). IL-1β and TNFα expression in gingival tissue were detected by immunohistochemical staining. SBI, GI,PD and AL of the subjects were measured. The relationship between the level of IL-1β,TNFα and the cell appotosis was analyzed.ResultsApoptosis was obvious in prickle cells and basal cells of gingival tissue of DAP group. The percentage of apoptosis cells of DAP group was significantly higher than that of group H(P<0.01). The expression of IL-1β and TNFα in group DAP was significant higher than that of group H(P<0.01), and the mainly positive expression cells were macrophages, plasmocytes and lymphocytes.ConclusionIL-1β and TNFα play a role in cell apoptosis in the gingival tissue of the patients with DAP.
Cellapoptosis;Diabetesassociatedperiodontitis(DAP);Inflammatorycytokine;Mechanism
總后面上項目(編號: CHJ13J035); 上海市衛(wèi)計委項目(編號: 20134418); 上海市區(qū)重點課題(編號: 1002-04); 上海市區(qū)面上課題(編號: 1503-31)
200081 上海, 解放軍411醫(yī)院全軍口腔中心牙周科(陳鐵樓 張新海 趙海軍 徐逸敏 欒瑋 劉進 陳駿 馬麗婷), 內(nèi)分泌科(徐爾理), 醫(yī)學檢驗科(唐大海), 病理科(張曉莉)
陳鐵樓 021-81867179 E-mail: chentielou2010@sina.com
R780.2
A
10.3969/j.issn.1001-3733.2017.04.019
(收稿: 2016-10-12 修回: 2017-03-04)

