一種簡(jiǎn)便的環(huán)糊精超分子包結(jié)比測(cè)算新方法
張偉鋒 - 羅 新 王建輝 - 王 敏 劉 龍 王成峰 - 寧?kù)o恒 -
(長(zhǎng)沙理工大學(xué)化學(xué)與生物工程學(xué)院,湖南 長(zhǎng)沙 410114) (School of Chemical and Biological Engineering, Changsha University of Science & Technology, Changsha, Hunan 410114, China)
一種簡(jiǎn)便的環(huán)糊精超分子包結(jié)比測(cè)算新方法
張偉鋒ZHANGWei-feng羅 新LUOXin王建輝WANGJian-hui王 敏WANGMin劉 龍LIULong王成峰WANGCheng-feng寧?kù)o恒NINGJing-heng
(長(zhǎng)沙理工大學(xué)化學(xué)與生物工程學(xué)院,湖南 長(zhǎng)沙 410114) (SchoolofChemicalandBiologicalEngineering,ChangshaUniversityofScience&Technology,Changsha,Hunan410114,China)
利用紫外可見(jiàn)分光光度計(jì),通過(guò)測(cè)定β-環(huán)糊精-山梨酸超分子包合物的紫外吸光度,提出一種新的差量法用以測(cè)算該超分子的包結(jié)比,其值與經(jīng)典的摩爾比法及相溶解度法相同,均為1∶1,表明該類(lèi)超分子是由1分子主體分子(β-環(huán)糊精)包結(jié)1分子客體分子(山梨酸)而成。差量法為多次測(cè)量吸光度再取平均值進(jìn)行測(cè)算,其結(jié)果較摩爾比法更為準(zhǔn)確;其測(cè)算過(guò)程,不受外界因素干擾,無(wú)需繪制相圖,較相溶解度法更為簡(jiǎn)便。
包結(jié)比;差量法;環(huán)糊精;山梨酸
超分子又稱(chēng)主-客體化合物,是基于主客體分子間疏水、氫鍵等弱相互作用力所形成的分子聚集體[1]。環(huán)糊精作為一類(lèi)典型的主體分子,在超分子化學(xué)領(lǐng)域應(yīng)用極為廣泛[2-4]。其中,β-環(huán)糊精(β-Cyclodextrins,β-CD),由7個(gè)葡萄糖單元環(huán)合而成,具有內(nèi)腔疏水外壁親水的特殊結(jié)構(gòu),其空腔可包合疏水性有機(jī)物形成超分子從而改變后者的理化性質(zhì)[5-6]。環(huán)糊精包合物在食品工業(yè)的應(yīng)用很多,如Shao等[7]利用β-環(huán)糊精包結(jié)綠原酸形成籠狀超分子,可在保留原有綠原酸抗氧化性能的同時(shí)有效提高其穩(wěn)定性;G. Astray等[8]發(fā)現(xiàn)β-環(huán)糊精可包合肉桂醛、薄荷醇和檸檬醛等,對(duì)這些常見(jiàn)的食品香料起到保護(hù)和緩釋的作用。環(huán)糊精在食品工業(yè)中的這些應(yīng)用,都基于其對(duì)客體分子的包合作用有助于對(duì)客體分子理化性能的改善。因此,探討環(huán)糊精與客體分子之間的包合作用、包合方式、包合能力等系列機(jī)理問(wèn)題,既是環(huán)糊精超分子化學(xué)研究的核心內(nèi)容,也是拓寬環(huán)糊精應(yīng)用必須解決的關(guān)鍵問(wèn)題。
在超分子的包結(jié)機(jī)理研究中,包結(jié)比決定主、客體分子以何種比例進(jìn)行包合,是探討主客體分子包合方式的首要參數(shù)。常見(jiàn)包結(jié)比的測(cè)算方法有紫外分光光度法[9]、熒光光譜法[10]、核磁共振譜法[11]、差示掃描量熱法[12]及單晶X射線衍射法等[13-14]。其中,熒光光譜法易受其他離子干擾,核磁共振法樣品純度要求極高,差示掃描量熱法檢測(cè)時(shí)間長(zhǎng),單晶X射線衍射法不易制樣且譜圖解析難度大,此外,上述包結(jié)比的測(cè)算方法所需儀器都較昂貴,不便廣泛開(kāi)展。
基于此,利用常見(jiàn)的紫外可見(jiàn)分光光度計(jì),以實(shí)驗(yàn)室自制的β-環(huán)糊精-山梨酸包合物為例,提出一種新的測(cè)算包結(jié)比的方法——差量法。該法首先確定β-環(huán)糊精-山梨酸包合物的總質(zhì)量,利用紫外可見(jiàn)光光度計(jì),測(cè)定此質(zhì)量下β-環(huán)糊精-山梨酸包合物的吸光度值,依據(jù)紫外工作曲線計(jì)算包合物中山梨酸的質(zhì)量,則主體分子β-環(huán)糊精的質(zhì)量可由差量法計(jì)算確定(包合物總質(zhì)量減去山梨酸質(zhì)量),由此可得主客體分子的摩爾比亦即包合物的包結(jié)比。這一新的包結(jié)比測(cè)算方法,因其關(guān)鍵的吸光度數(shù)據(jù)是在多次測(cè)定后再取平均值,所以其計(jì)算結(jié)果將較經(jīng)典的摩爾比法準(zhǔn)確;同時(shí)其測(cè)算過(guò)程無(wú)需繪制復(fù)雜相圖,因此較經(jīng)典的相溶解度法將要簡(jiǎn)便得多。應(yīng)用新的差量法對(duì)β-環(huán)糊精與山梨酸的包結(jié)比進(jìn)行研究,有利于為深入研究此類(lèi)超分子的包結(jié)機(jī)理提供新的簡(jiǎn)便方法或途徑。
1 材料與方法
1.1 儀器與試劑
紫外可見(jiàn)分光光度計(jì):TU-1901型,北京普析通用公司;
β-環(huán)糊精:分析純,上海強(qiáng)順化學(xué)試劑有限公司;
山梨酸和無(wú)水乙醇:分析純,國(guó)藥集團(tuán)化學(xué)試劑有限公司;
去離子水:實(shí)驗(yàn)室自制;
其他試劑:均為分析純。
1.2 試驗(yàn)過(guò)程
1.2.1 包合物的制備 參照文獻(xiàn)[15]方法進(jìn)行改進(jìn)。準(zhǔn)確稱(chēng)取精制的β-環(huán)糊精1.135 0 g(0.001 0 mol)和山梨酸0.246 7 g(0.002 2 mol),分別溶于40 mL去離子水和2.5 mL 無(wú)水乙醇中,將溶液混合,一定溫度下超聲一定時(shí)長(zhǎng)使之反應(yīng)完全,保溫5 min后趁熱過(guò)濾,濾液自然冷卻至室溫再靜置,3 d后即可獲得較好晶體。
1.2.2 確認(rèn)紫外測(cè)量波長(zhǎng) 參照文獻(xiàn)[16]的方法進(jìn)行改進(jìn)。準(zhǔn)確稱(chēng)取山梨酸0.010 0 g(0.089 2 mmol),用少量無(wú)水乙醇溶解,轉(zhuǎn)移至100 mL容量瓶中定容,無(wú)水乙醇定容并搖勻,作為標(biāo)準(zhǔn)液備用。移取適量的標(biāo)準(zhǔn)液,置于25 mL容量瓶中,無(wú)水乙醇定容,以無(wú)水乙醇為參比,采用紫外可見(jiàn)分光光度計(jì)進(jìn)行測(cè)試,在200~400 nm內(nèi)掃描,確認(rèn)其最大吸收波長(zhǎng)λmax。
1.2.3 繪制工作曲線 參照文獻(xiàn)[17]的方法進(jìn)行改進(jìn)。準(zhǔn)確移取適量標(biāo)準(zhǔn)液,置于25 mL容量瓶中,加無(wú)水乙醇定容,以無(wú)水乙醇為參比,在最大吸收波長(zhǎng)處測(cè)量吸光度,以吸光度值(A)為橫坐標(biāo)、濃度(C)為縱坐標(biāo)作圖,繪制山梨酸的工作曲線。
1.2.4 待測(cè)樣品的測(cè)定 準(zhǔn)確移取適量待測(cè)液,置于25 mL容量瓶中,加無(wú)水乙醇定容,以無(wú)水乙醇為參比,在最大吸收波長(zhǎng)處測(cè)量吸光度,用標(biāo)準(zhǔn)工作曲線計(jì)算待測(cè)樣濃度。
2 結(jié)果與討論
2.1 最大吸收波長(zhǎng)λmax
圖1為山梨酸在波長(zhǎng)200~400 nm處的紫外吸收曲線。由圖1可知,在255 nm處吸收最強(qiáng),因此最大吸收波長(zhǎng)λmax=255 nm,即為后續(xù)試驗(yàn)中采用的紫外測(cè)量波長(zhǎng)。
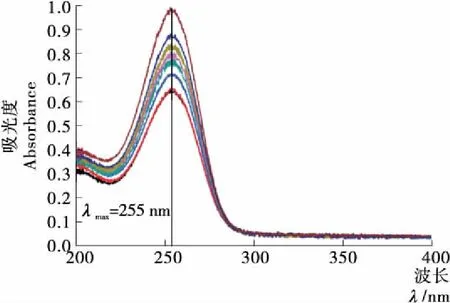
圖1 山梨酸紫外光譜Figure 1 UV-vis spectraof sorbic acid
2.2 工作曲線的繪制
圖2為山梨酸在最大吸收波長(zhǎng)λmax=255 nm處的工作曲線。由圖2可得,吸光度值與山梨酸濃度呈良好的線性關(guān)系。其線性回歸方程式為:A=1.083×105C+0.174 6,R2=0.998 5。
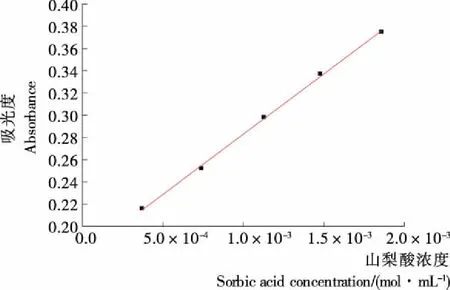
圖2 山梨酸的紫外工作曲線Figure 2 UV-viscalibration curve of sorbic acid
2.3 包結(jié)比的測(cè)算方法比較
2.3.1 差量法 利用紫外可見(jiàn)分光光度計(jì),通過(guò)測(cè)定β-環(huán)糊精-山梨酸超分子包合物的紫外吸光度值,提出一種新的測(cè)算包結(jié)比方法——差量法。首先準(zhǔn)確稱(chēng)量β-環(huán)糊精-山梨酸超分子包合物的總質(zhì)量,利用紫外可見(jiàn)分光光度計(jì),測(cè)定此質(zhì)量下包合物中山梨酸的質(zhì)量。根據(jù)差量法,得β-環(huán)糊精的質(zhì)量(包合物總質(zhì)量減去山梨酸質(zhì)量),進(jìn)而計(jì)算出主客體分子的摩爾數(shù)之比,即為包合物的包結(jié)比。
以實(shí)驗(yàn)室自制的β-環(huán)糊精-山梨酸包合物為例,差量法測(cè)算包合物包結(jié)比過(guò)程:
若β-環(huán)糊精-山梨酸包合物的總質(zhì)量為m包(g),定容后溶液體積為V定(mL),在λmax=255 nm處的吸光度值為A包,由于包合物中的主體分子環(huán)糊精無(wú)紫外吸收,可得A包=A山梨酸(山梨酸紫外吸光度值),代入上述線性回歸方程式中,得:
A包=1.083×105C山梨酸+0.174 6,R2=0.998 5。
(1)
由式(1)求得包合物中山梨酸摩爾濃度C山梨酸(mol/mL)為:
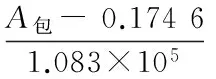
(2)
由式(2)可得包合物中山梨酸質(zhì)量為:
m山梨酸=C山梨酸V定M山梨酸。
(3)
則包合物中β-環(huán)糊精質(zhì)量為:
mβ-環(huán)糊精=m包-m山梨酸。
(4)
已知β-環(huán)糊精分子量為Mβ-環(huán)糊精,可得包合物中β-環(huán)糊精的摩爾數(shù)為:

(5)
同樣地,由山梨酸分子量M山梨酸可得包合物中山梨酸的摩爾數(shù)為:

(6)
由式(5)、(6)可知包結(jié)比R為:

(7)
將式(4)代入式(7),可得:
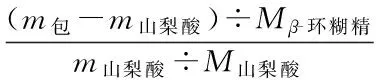
(8)
將式(2)、(3)代入式(8)可得:
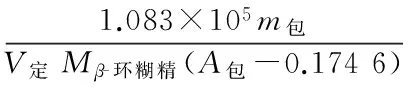
(9)
將M山梨酸=112.13,Mβ-環(huán)糊精=1 135代入式(9),可得包結(jié)比的計(jì)算公式為:

(10)
式中:
R——包結(jié)比;
m包——包合物的質(zhì)量,g;
V定——包合物溶液定容體積,mL;
A包——包合物吸光度。
由于m包和V定均為定值,所以由方程(10)可知,只要采用紫外分光光度計(jì)測(cè)定包合物的A包,即可算出其包結(jié)比。例如,分別準(zhǔn)確稱(chēng)量(m包)0.002 0,0.006 0,0.010 0 gβ-環(huán)糊精-山梨酸超分子包合物,置于50 mL容量瓶中,用去離子水定容,即V定=50 mL,在λmax=255 nm處測(cè)得吸光度A包,測(cè)量3次取平均值,按上述方法根據(jù)式(10)計(jì)算包結(jié)比,結(jié)果見(jiàn)表1。
由表1可知:多次測(cè)算包結(jié)比的結(jié)果均為1∶1,表明1分子β-環(huán)糊精與1分子山梨酸包結(jié)形成了超分子包合物。顯然,當(dāng)采用差量法確定其包結(jié)比時(shí),可準(zhǔn)確稱(chēng)取一定質(zhì)量的包合物(m包)配置一定體積的溶液(V定),然后只需采用紫外分光光度計(jì)測(cè)定溶液的吸光度值(A包),并經(jīng)多次測(cè)量取其平均值,即可由式(10)方便且準(zhǔn)確地計(jì)算出包結(jié)比。
2.3.2 經(jīng)典方法測(cè)算包合物包結(jié)比
(1) 摩爾比法:摩爾比法[18]也是采用紫外分光光度法測(cè)算包合物包結(jié)比的一種方法。其原理是固定一個(gè)組分的濃度和體積不變,改變另一組分的體積即改變其測(cè)試濃度,在最大吸收波長(zhǎng)處測(cè)定吸光度值,以摩爾比(即環(huán)糊精溶液與山梨酸溶液的體積比)為橫坐標(biāo)、吸光度值為縱坐標(biāo)作圖,圖中曲線轉(zhuǎn)折點(diǎn)對(duì)應(yīng)的摩爾比(體積比),即為該包合物的包結(jié)比。
表1差量法測(cè)算β-環(huán)糊精-山梨酸的包結(jié)比?
Table 1 Determination of the inclusion ratio ofβ-cyclodextrin-sorbic acid by subtraction method
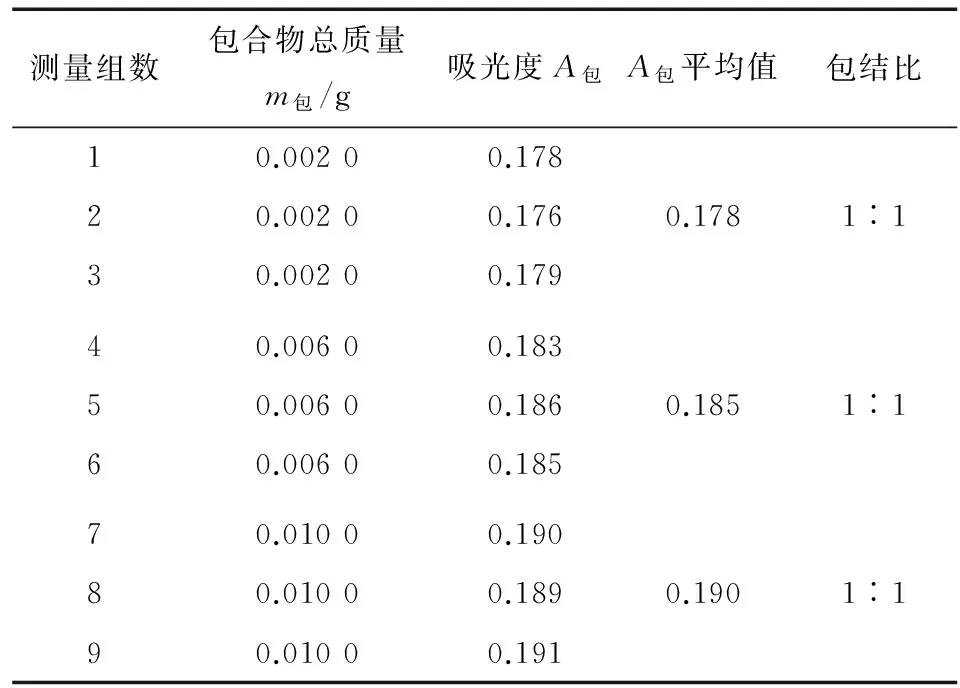
測(cè)量組數(shù)包合物總質(zhì)量m包/g吸光度A包A包平均值包結(jié)比10.00200.17820.00200.1760.1781︰130.00200.17940.00600.18350.00600.1860.1851︰160.00600.18570.01000.19080.01000.1890.1901︰190.01000.191
?V定均為50 mL。
圖3為β-環(huán)糊精與山梨酸溶液吸光度值隨摩爾比(體積比)變化曲線。β-環(huán)糊精水溶液的濃度為1×10-9mol/mL,山梨酸乙醇溶液的濃度為1×10-9mol/mL,山梨酸溶液體積為10 mL,β-環(huán)糊精體積分別為2,5,10,12,15,20 mL,在λmax=255 nm處分別測(cè)定,吸光度值,即可作圖3。由圖3可知,當(dāng)β-環(huán)糊精與山梨酸摩爾比(體積比)為1∶1時(shí),吸光度值發(fā)生明顯的變化,由此可以判定β-環(huán)糊精與山梨酸的包結(jié)比為1∶1,雖然摩爾比法比差量法簡(jiǎn)便,但溶液長(zhǎng)時(shí)間暴露在空氣中,易氧化變質(zhì),其計(jì)算結(jié)果的準(zhǔn)確性低于多次取平均值的差量法。
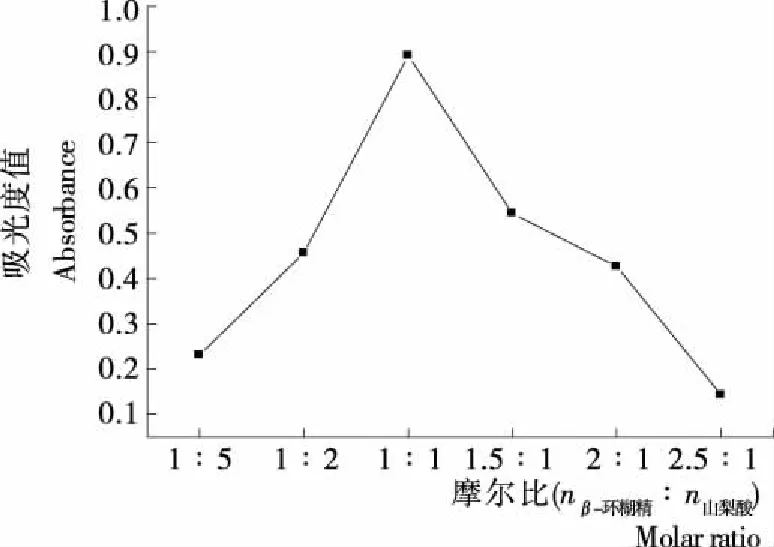
圖3 吸光度與摩爾比的關(guān)系變化圖Figure 3 The relationship between the absorbance and the molar ratio
(2) 相溶解度法:相溶解度法[19]是用于包合物包結(jié)機(jī)理研究的經(jīng)典方法,在測(cè)定包合常數(shù)的同時(shí)能獲得客體分子包合后溶解度行為的改變,繼而推斷出主客體分子的包結(jié)比。
圖4為包合物的相溶解度圖。如圖 4所示,根據(jù)Higuchi等[19]研究表明,超分子包合物相溶解等、溫線有5種類(lèi)型,AP、AL、AN、BS和BL。其中,AL類(lèi)型隨主體分子濃度增加,客體分子溶解度呈線性增加,表明形成包結(jié)比為1∶1的包合物;AP類(lèi)型包合物的溶解度較大;AN類(lèi)型包結(jié)行較為復(fù)雜;BS類(lèi)型為客體分子溶解度先隨主體分子濃度的增大而增大,而后逐漸析出包合物結(jié)晶;BL類(lèi)型表明形成包合物后,溶解度開(kāi)始下降。采用相溶解度法繪制β-環(huán)糊精-山梨酸包合物的相溶解度圖,隨著β-環(huán)糊精濃度的增加,山梨酸溶解度增加,二者呈線性關(guān)系,其相溶解度圖屬AL型,表明β-環(huán)糊精與山梨酸形成包結(jié)比為1∶1的包合物。相溶解度法雖然在測(cè)算包結(jié)比的同時(shí)可計(jì)算包合常數(shù),但易受外界因素(如溫度)干擾,作圖方法復(fù)雜,計(jì)算過(guò)程較差量法繁瑣。
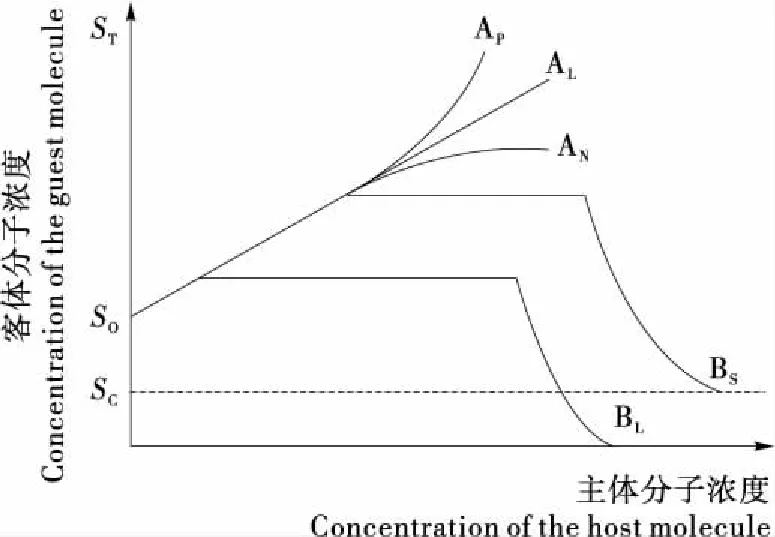
SO為無(wú)主體分子時(shí)客體的溶解度;ST為溶解客體分子的濃度;SC為溶解性差包合物的極限溶解度
圖4 相溶解度圖
Figure 4 Phase solubility isotherm types
3 結(jié)論
(1) 采用差量法成功測(cè)算了β-環(huán)糊精-山梨酸超分子包合物的包結(jié)比。此方法同經(jīng)典的摩爾法及相溶解度法相比,所得包結(jié)比均為1∶1,說(shuō)明1分子β-環(huán)糊精包結(jié)1分子山梨酸形成了超分子包合物。
(2) 差量法為本研究提出的一種新的、簡(jiǎn)便的包結(jié)比測(cè)算方法。只需利用紫外可見(jiàn)分光光度計(jì),測(cè)定一定質(zhì)量下包合物的吸光度值,根據(jù)客體分子工作曲線計(jì)算出該質(zhì)量下包合物中客體分子的質(zhì)量,根據(jù)差量法,得主體分子的質(zhì)量(包合物質(zhì)量減去客體分子質(zhì)量),進(jìn)而計(jì)算出主客體分子的摩爾數(shù)之比,即為包合物的包結(jié)比。此方法同經(jīng)典的摩爾法及相溶解度法相比,較前者準(zhǔn)確,較后者簡(jiǎn)單,為超分子包結(jié)比的確定提供一種新的簡(jiǎn)便且準(zhǔn)確的計(jì)算方法。
[1] SZEJTLI J. Introduction and general overview of cyclodextrin chemistry[J]. Chemical Reviews, 1998, 98(5): 1 743-1 753.
[2] VALLE E M M. Cyclodextrin their uses: A review[J]. Process Biochemistry, 2004, 39(9): 1 033-1 046.
[3] DAVIS M E, BREWSTER M E. Cyclodextrin-based pharmaceutics: Past, present and future[J]. Dressnature Reviews Drug Discovery, 2004, 3(12): 1 023-1 035.
[4] NING Jing-heng, WANG Yu-fang, WU Qi, et al. Novel supramolecular assemblies of repulsive DNA-anionic porphyrin complexes based on covalently modified multi-walled carbon nanotubes and cyclodextrins[J]. RSC Advances, 2015, 5(27): 21 153-21 160.
[5] LAKKAKULA J R, MA?EDO KRAUSE R W. A vision for cyclodextrin nanoparticles in drug delivery systems and pharmaceutical applications[J]. Nanomedicine, 2014, 9(6): 877-896.
[6] DENG Jie, LIU Xin-yue, MA Lang, et al. Heparin-mimicking multilayer coating on polymeric membrane via LbL assembly of cyclodextrin-based supramolecules[J]. Applied Materials & Interfaces, 2017, 6(23): 21 603-21 614.
[7] SHAO Ping, ZHANG Jia-feng, FANG Zhong-xian, et al. Complexing of chlorogenic acid withβ-cyclodextrins: Inclusion effects, antioxidative properties and potential application in grape juice[J]. Food Hydrocolloids, 2014, 41(6): 132-139.
[8] ASTRAY G, MEJUTO J C, MORALES J, et al. Factors controlling flavors binding constants to cyclodextrins and their applications in foods[J]. Food Research International, 2010, 43(4): 1 212-1 218.
[9] DANIEL K, BRINKER U H. Induced circular dichroism and UV-vis absorption spectroscopy of cyclodextrin inclusion complexes: Structural elucidation of supramolecular azi-adamantane (spiro[adamantane-2,3-diazirine])[J]. Journal of the American Chemical Society, 1998, 120(45): 11 627-11 632.
[10] AICART E, JUNQUERA E. Complex formation between purine derivatives and cyclodextrins: A fluorescence spectroscopy study[J]. Journal of Inclusion Phenomena and Macrocyclic Chemistry, 2003, 47(3): 161-165.
[11] SCHNEIDER H, FRANK HACKET A, RüDIGER V, et al. NMR studies of cyclodextrins and cyclodextrin complexes[J]. Chemical Reviews, 1998, 98(5): 1 755-1 786.
[12] FICARRA R, TOMMASINI S, RANERI D, et al. Study of flavonoids/β-cyclodextrins inclusion complexes by NMR, FT-IR, DSC, X-ray investigation[J]. Journal of Pharmaceutical & Biomedical Analysis, 2002, 29(6): 1 005-1 014.
[13] AIGNER Z, BERKESI O, FARKAS G, et al. DSC, X-ray and FTIR studies of a gemfibrozil/dimethyl-β-cyclodextrin inclusion complex produced by co-grinding[J]. Journal of Pharmaceutical & Biomedical Analysis, 2012, 57: 62-67.
[13] 劉彥利. 三種β-環(huán)糊精包結(jié)物的表征和晶體結(jié)構(gòu)解析[D]. 天津: 天津大學(xué), 2009: 58-64.
[15] 張清峰, 姜子濤, 占豪, 等. 紫外分光光度法研究β-環(huán)糊精與甲基橙的包結(jié)行為[J]. 光譜實(shí)驗(yàn)室, 2005, 22(5): 1 074-1 078.
[16] 羅見(jiàn)春, 陳學(xué)梁, 張景勍. 紫外分光光度法測(cè)定紫杉醇羥丙基-β-環(huán)糊精包合物的包合率[J]. 激光雜志, 2014(6): 66-67.
[17] 耿慶霞. 以瓜環(huán)為主體的超分子探針對(duì)金屬離子的識(shí)別作用[D]. 貴陽(yáng): 貴州大學(xué), 2016: 32-35.
[18] 李向軍, 連軍. 相溶解度法研究蘆薈大黃素和環(huán)糊精及其衍生物的包結(jié)作用[J]. 分析科學(xué)學(xué)報(bào), 1999(5): 368-371.
[19] HIGUCHI T, CONNORS K A. Phase solubility techniques[J]. Advances in Analytical Chemistry and Instrumentation, 1965(4): 117-212.
Anewandsimplemethodforcalculatingtheinclusionratioofcyclodextrinsupramolecules
Based on UV absorbance, a new and simple subtraction method was proposed for the calculation of the inclusion ratio, and it was proved to be equal in number to the classical molar ratio or phase solubility method. Using any kind of these three methods, the results always showed that the inclusion ratio of this complex was 1∶1, which indicated that this kind of supramolecular complex was formed through an inclusion interaction between 1 host molecule (β-cyclodextrin) and 1 guest molecule (sorbic acid). Sincethe subtraction methodadopted a repetitive measurement and took the averaged, its result was more accurate than the molar ratio method; meanwhile, due to the advantage of less interference factors and especiallyno need of drawing a complicated phase diagram, its calculation process was much simpler than the phase solubility method.
inclusion ratio; subtraction method; cyclodextrins; sorbicacid
國(guó)家自然科學(xué)基金(編號(hào):21505005);湖南省自然科學(xué)基金項(xiàng)目(編號(hào):2015JJ2011);湖南省教育廳項(xiàng)目(編號(hào):15C0023);湖南省電力與交通材料保護(hù)省重點(diǎn)實(shí)驗(yàn)室開(kāi)放基金(編號(hào):2017CL07);湖南省大學(xué)生研究性學(xué)習(xí)和創(chuàng)新性實(shí)驗(yàn)計(jì)劃(編號(hào):湘教通〔2016〕202號(hào))
張偉鋒,男,長(zhǎng)沙理工大學(xué)在讀碩士研究生。
寧?kù)o恒(1975—),女,長(zhǎng)沙理工大學(xué)副教授,博士。
E-mail: ningjingheng@126.com
2017—05—07
10.13652/j.issn.1003-5788.2017.09.002

