應用糖基化碳量子點研究甘露糖與致病菌之間的相互作用
趙 斌,崔飛云,徐 溢,張曉鳳,李澤全
(1.重慶大學 化學化工學院,重慶 400044;2.新型微納器件與系統技術重點學科實驗室,重慶 400044;3.重慶大學 光電工程學院微系統研究中心,重慶 400044;4.微納系統及新材料技術國際研發中心,重慶 400044;5.重慶理工大學 化學化工學院,重慶 400050)
應用糖基化碳量子點研究甘露糖與致病菌之間的相互作用
趙 斌1,2,4,崔飛云1,2,4,徐 溢2,3,4*,張曉鳳2,4,5,李澤全1*
(1.重慶大學 化學化工學院,重慶 400044;2.新型微納器件與系統技術重點學科實驗室,重慶 400044;3.重慶大學 光電工程學院微系統研究中心,重慶 400044;4.微納系統及新材料技術國際研發中心,重慶 400044;5.重慶理工大學 化學化工學院,重慶 400050)
以檸檬酸為碳源,通過水熱法制備得到熒光碳量子點(CQDs),基于其表面的—COOH,將4-氨基苯基-α-D-吡喃甘露糖苷以共價鍵的方式固定在CQDs表面,得到甘露糖基化碳量子點(Man-CQDs),并通過熒光競爭法,結合Scatchard方程計算了Man-CQDs與大腸桿菌JM109、大腸桿菌DH5a和沙門氏菌S.123443的結合常數Ka。實驗得到CQDs的粒徑為26 nm,最大發射波長為445 nm,熒光產率相較于54%硫酸奎寧為76%,Man-CQDs熒光強度與CQDs相比基本保持不變,通過苯酚-硫酸法計算得到Man-CQDs濃度為2.832 mmol/L,Man-CQDs納米顆粒中甘露糖含量約為40%。根據Man-CQDs、D-Mannose與致病菌競爭結合實驗,結合 Scatchard模型方程,計算得到Man-CQDs與大腸桿菌JM109的結合常數Ka=2.39×103L/mol,Man-CQDs與沙門氏菌S.123443的結合常數Ka=1.17×105L/mol,Man-CQDs與大腸桿菌DH5a無有效結合。研究結果顯示,該方法可用于甘露糖與致病菌非共價結合的結合常數測定,為研究糖與致病菌相互作用提供了參考。
甘露糖基化碳量子點(Man-CQDs);大腸桿菌JM109;大腸桿菌DH5a;沙門氏菌S.123443;結合常數;相互作用;熒光光譜
致病菌對宿主細胞的粘附主要通過致病菌菌毛/鞭毛末端的凝集素與宿主細胞表面聚糖發生選擇性識別結合完成,從而導致炎癥和痢疾等疾病[1]。在細胞水平上定量研究致病菌與糖的相互作用,以及在分子水平上研究凝集素與糖的相互作用,均能為致病菌粘附機制的研究、致病菌的特異性檢測提供新的策略。
目前,凝集素/細菌與糖相互作用的定量研究主要采用等溫滴定量熱法[2]、親和毛細管電泳法[3]、石英晶體微天平[4]、表面等離子體共振法[5]和熒光光譜法[6]等。熒光光譜法具有檢測靈敏度高、選擇性好、所需樣品量少以及方法簡便等優點,是目前采用較多的測試手段。如Wang等[7]基于熒光競爭性結合實驗研究了Man-Au與FITC-ConA的相互作用,FITC-ConA與Man-Au、D-Mannose競爭結合平衡后,根據Cheng-Prusoff方程計算得到Man-Au與ConA的解離常數在nmol級別。Okada等[8]在已修飾熒光染料的膠原蛋白肽的末端接枝甘露糖制備得到MPOG10復合物,采用熒光偏振結合非線性最小二乘法計算得到MPOG10與ConA的解離常數為1.9×10-5mol/L。然而,這些研究僅在分子水平上以凝集素替代致病菌菌毛/鞭毛末端的識別分子,難以真實地反映出致病菌與糖的相互作用,在細胞水平上對致病菌-糖相互作用的研究尚少。
本文以檸檬酸為碳源,采用水熱法制備得到熒光產率高、水溶性和生物相容性好的CQDs-COOH,利用羧基和氨基的酰胺化反應將修飾有氨基的甘露糖固定在CQDs表面,制備得到甘露糖基化碳量子點(Man-CQDs)。將Man-CQDs作為甘露糖與致病菌相互作用的熒光探針,以大腸桿菌K12變異型菌種JM109、大腸桿菌DH5a和沙門氏菌S.123443為研究對象,通過加入系列濃度的Man-CQDs,與固定濃度的D-Mannose競爭結合致病菌的結合位點,結合平衡后離心將Man-CQDs/致病菌復合物與殘余游離的Man-CQDs和D-Mannose分離,測試上清液的熒光光譜,結合Scatchard模型,計算得到Man-CQDs與大腸桿菌JM109/沙門氏菌S.123443 2種致病菌的結合常數。以期為糖與致病菌的相互作用的定量研究起到指導意義。
1 實驗部分
1.1 儀器與試劑
RF-5301熒光光譜儀、UV-2450紫外可見光分光光度計和IRprestige-21傅立葉紅外光譜儀(日本島津公司);JEM-1230透射電子顯微鏡(日本電子光學研究所)。LB培養基、營養瓊脂購自上海生工;檸檬酸、D-Mannose、4-氨基苯基-α-D-吡喃甘露糖苷(A-D-mannopyanoside)、1-(3-二甲氨基丙基)-3-乙基碳二亞胺鹽酸鹽(EDC)、奎寧均購自上海阿拉丁生化科技股份有限公司;乙二胺、N-羥基琥珀酰亞胺(NHS)等購自成都科龍化工試劑廠;所用試劑均為分析純;實驗用水為二次蒸餾水;實驗在常溫常壓下進行。
磷酸鹽緩沖溶液(PBS):精確稱取 0.24 g KH2PO4、1.44 g Na2HPO4、8 g NaCl、0.2 g KCl 溶于去離子水中,用0.1 mol/L的NaOH調至pH 7.4。
大腸桿菌JM109/大腸桿菌DH5a/沙門氏菌S.123443標本:菌種均由第三軍醫大學檢驗系提供,在LB培養基中37 ℃培養12~14 h;將原菌液以8 000 r/min離心3 min,去除上清液后重懸于PBS緩沖液中,重復離心2~3次,最后懸浮在PBS緩沖液中。
1.2 實驗方法
1.2.1Man-CQDs的制備參考Zhu等[9]的水熱法制備高熒光產率CQDs。將0.42 g檸檬酸和536 μL乙二胺溶解于10 mL去離子水中,轉移至聚四氟乙烯反應釜(30 mL)中,在200 ℃烘箱中反應5 h。自然冷卻至室溫后,避光透析(透析袋MW:3 500 Da)去除粒徑小的納米顆粒,得到粒徑均勻的CQDs,并置于4 ℃儲存。
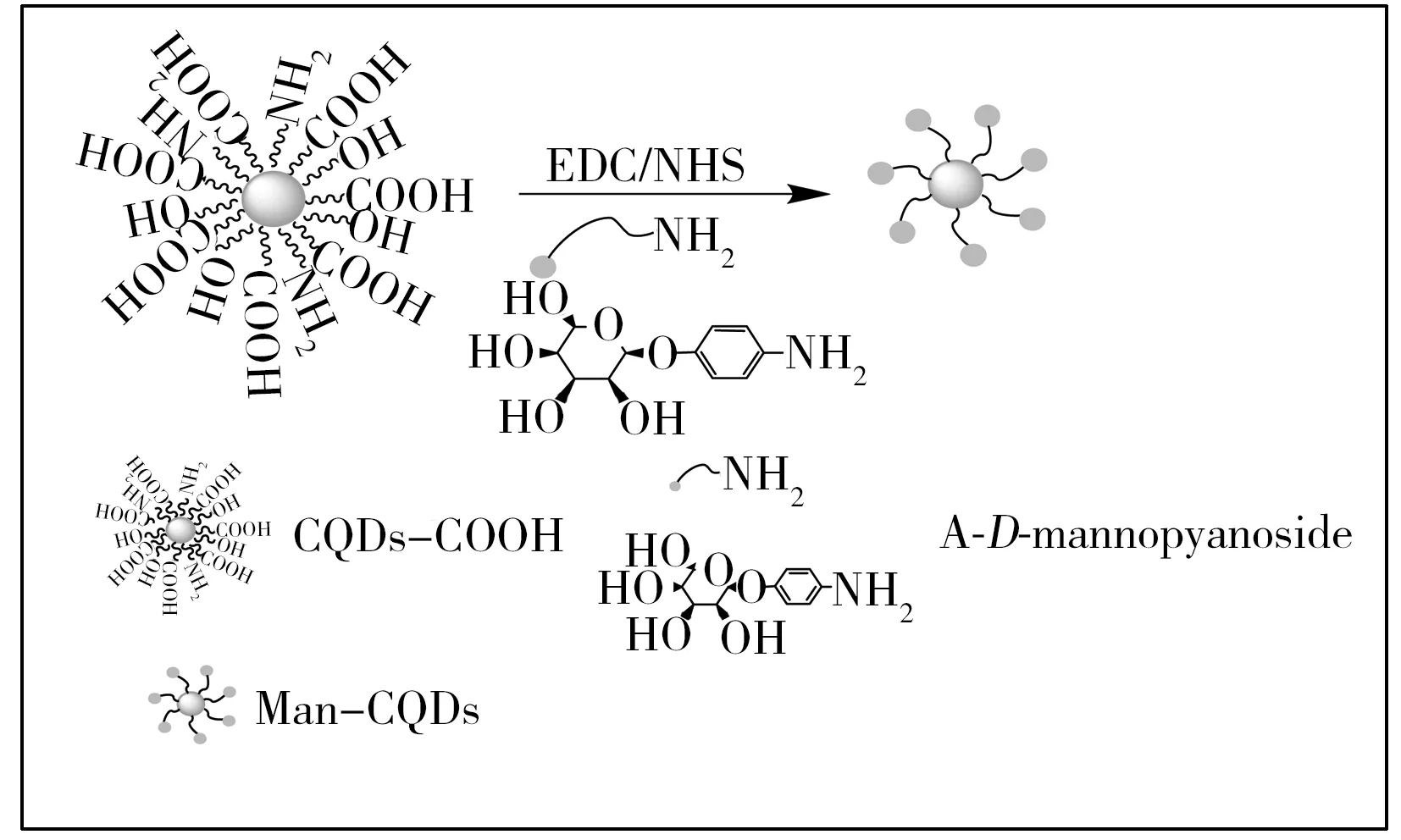
圖1 Man-CQDs制備原理圖Fig.1 Scheme of the coupling process of Man-CQDs
利用CQDs表面的—COOH,將氨基化的甘露糖通過酰胺鍵的方式固定在CQDs表面,制備得到Man-CQDs(如圖1)。取1 mL稀釋濃度[10]為1 mg/mL的CQDs,加入EDC(1 mL,60 mmol/L)和NHS(1 mL,30 mmol/L)于37 ℃活化30 min,隨后加入4-氨基苯基-α-D-吡喃甘露糖苷(1 mL,1 mg/mL),振搖120 min,加入Tris-HCl緩沖溶液封閉未反應的活性羧基,4 ℃條件下反應過夜,最后透析(透析袋MW:3 500 Da)去除多余的4-氨基苯基-α-D-吡喃甘露糖苷,制備得到Man-CQDs。
1.2.2Man-CQDs與致病菌的結合實驗將108cfu/mL的大腸桿菌JM109、沙門氏菌S.123443和大腸桿菌DH5a分別懸浮在pH 7.4的 PBS緩沖溶液中,加入1 mL 1 mmol/LD-Mannose溶液,隨后各自加入系列濃度(0.023 4~0.291 6 mmol/L)的Man-CQDs,用PBS緩沖溶液定容至3 mL,37 ℃孵育60 min,結合平衡后8 000 r/min離心3 min,獲得上清液測定其熒光光譜,記錄激發波長350 nm時發射波長在445 nm處的熒光強度。
2 結果與討論
2.1 CQDs及Man-CQDs表征結果
基于CQDs的熒光量子產率高、無毒、制備簡單等優點,研究者將生物分子如蛋白[11]、適配體[10]和抗生素[12]等修飾固定在CQDs表面,用于致病菌的相關研究。而將糖分子固定在CQDs表面制備糖基化碳量子點,用于致病菌選擇性識別的研究尚少。Huang等[13-14]將檸檬酸與甘露糖混溶后在高溫下碳化制備得到Man-CQDs,其熒光量子產率僅為9.8%;隨后通過包裹方式,在高溫下將甘露糖包裹在制備好的CQDs表面,熒光量子產率有小幅提高。但上述方法制備的Man-CQDs存在以下問題:高溫下甘露糖極易被碳化,結構被破壞;熒光量子產率不高,導致檢測靈敏度低。實驗采用水熱法制備得到的CQDs熒光量子產率較高,其表面還結合有豐富的活性官能團,如—OH、—COOH和—NH2等,可與甘露糖的衍生物共價結合,制備得到Man-CQDs,這個過程不會破壞甘露糖結構,同時還可以改善CQDs的生物相容性。圖2A顯示實驗制備得到粒徑范圍為2~6 nm,分布均勻,無團聚現象,水溶性好的CQDs,其紫外光譜測試結果顯示260 nm和350 nm處分別是碳核峰和表面分子的吸收峰[9];CQDs的熒光光譜測試結果顯示,激發波長(λex)為350 nm時,CQDs的最大發射波長(λem)為445 nm(圖2B)。根據熒光量子產率計算公式(式1)計算其熒光量子產率相較于54%硫酸奎寧約為76%;CQDs的FTIR測試結果(圖2C)顯示,3 401 cm-1附近為羥基伸縮振動峰,2 926 cm-1附近為氨基伸縮振動峰,1 656 cm-1附近為羧基伸縮振動峰,說明CQDs表面有—COOH、—OH和—NH2等功能基團,其中—COOH基團可與修飾有氨基的甘露糖進一步共價結合制備獲得Man-CQDs。
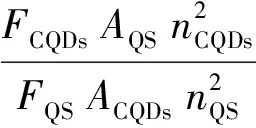
(1)
式中,YCQDs和YQS分別為CQDs與硫酸奎寧的熒光量子產率,FCQDs和FQS分別為CQDs與硫酸奎寧的積分熒光強度,ACQDs和AQS分別為CQDs與硫酸奎寧的吸光度值,nCQDs和nQS表示溶劑的折射率,對于CQDs溶液和硫酸奎寧溶液,兩者的折射率均為1.33。

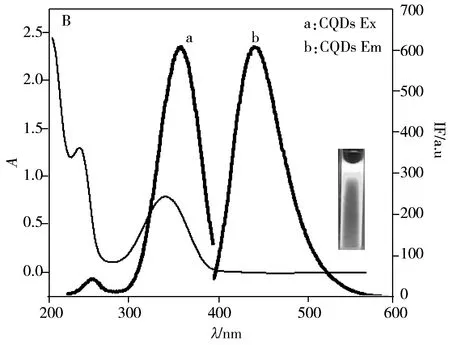
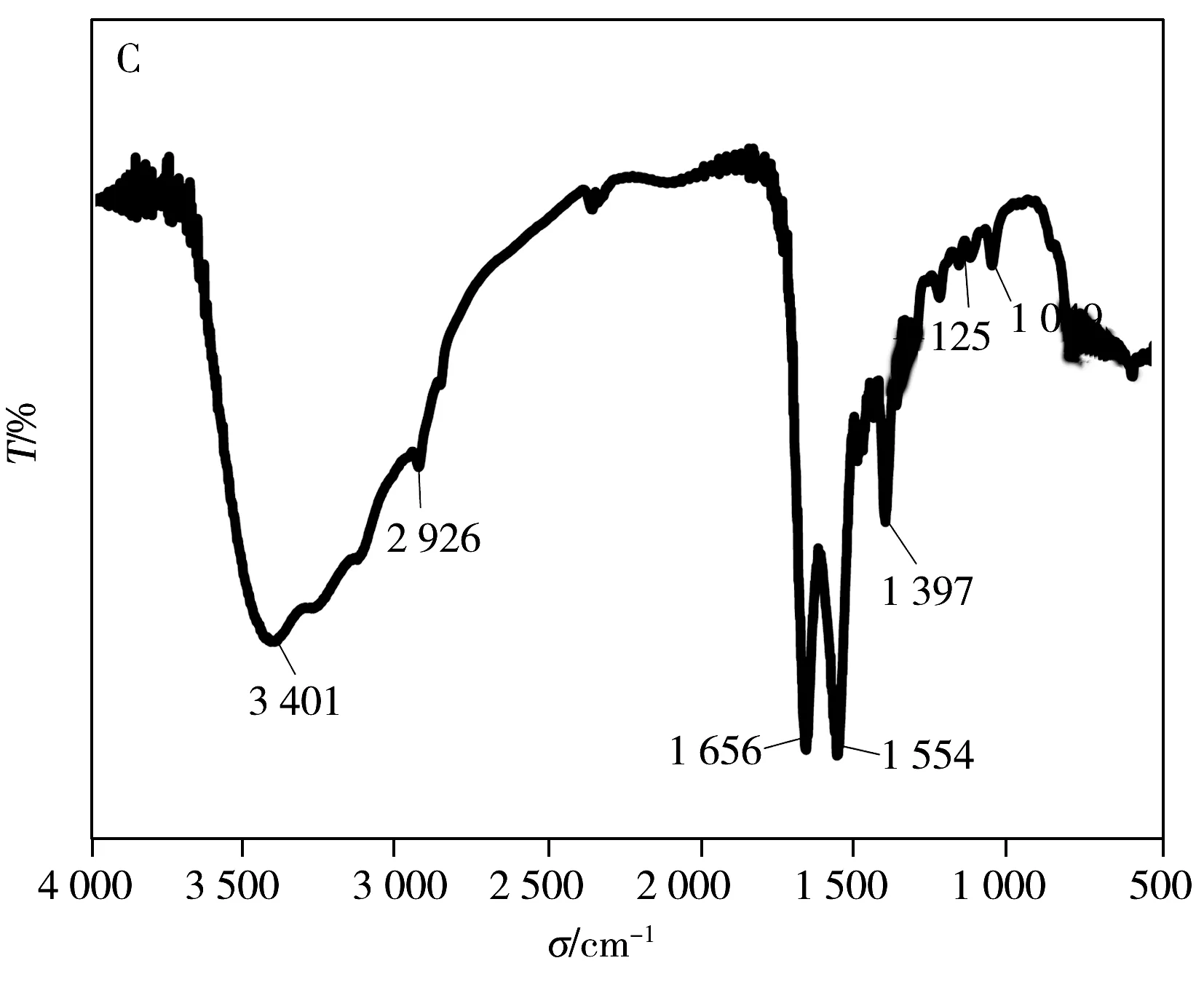
圖2 CQDs的透射電鏡圖(A)、紫外和熒光光譜圖(B)以及紅外光譜圖(C)Fig.2 TEM image(A),UV-Vis spectra and fluorescence spectra(B) and FTIR spectra(C)of CQDs
CQDs表面的—COOH官能團經EDC/NHS活化后,通過酰胺鍵將4-氨基苯基-α-D-吡喃甘露糖苷共價結合在CQDs表面。Man-CQDs的熒光光譜(圖3A)顯示最大發射波長仍為445 nm,熒光強度有較小的減弱;Man-CQDs的FTIR測試結果(圖3B)顯示,3 401~3 110 cm-1附近的羥基伸縮振動峰、2 964 cm-1和1 649 cm-1附近的氨基和羧基伸縮振動峰依然存在,1 649~1 406 cm-1附近的峰有明顯變化,顯示出苯環結構引入,推測甘露糖已被鏈接在CQDs表面;Man-CQDs的紫外光譜(圖3C)顯示除了230 nm和290 nm有CQDs的吸收峰,在288 nm處還有A-D-mannopyanoside的吸收峰,可進一步證實制備得到了Man-CQDs納米顆粒。
2.2 Man-CQDs制備條件優化
CQDs的表面有多個可與氨基化甘露糖鍵合的活性羧基,CQDs與A-D-mannopyanoside的不同配比也會影響鍵合效果。實驗設置了4組不同的配比(2∶1、1∶1、1∶5、1∶10),反應結束后,對制備得到的Man-CQDs進行熒光光譜測試。結果顯示,當CQDs與A-D-mannopyanoside的配比為1∶1時,Man-CQDs的熒光值最大,故選擇此條件為制備Man-CQDs的最優條件。
2.3Man-CQDs溶液中A-D-mannopyanoside含量的測定
Man-CQDs與致病菌的相互作用通過Man-CQDs表面接枝的甘露糖進行,因此,Man-CQDs表面接枝的甘露糖量對Man-CQDs與致病菌的識別和結合效果有很大影響。實驗通過用苯酚-硫酸[15]溶液處理系列濃度(0.01~ 4.5 mmol/L)的D-Mannose,測定其在490 nm處的吸光度,得到D-Mannose濃度與吸光度的標準曲線方程為IOA=0.148C-0.051 2,r2=0.961 7。Man-CQDs用相同的方法處理,測得其吸光度為0.368,代入線性方程,即可計算得到Man-CQDs溶液中接枝A-D-mannopyanoside的濃度為2.832 mmol/L,換算后即為0.768 mg/mL,且Man-CQDs的終濃度為1.919 mg/mL。經計算,Man-CQDs納米顆粒中的甘露糖含量約為40%。
2.4 Man-CQDs與致病菌結合時間的優化
Man-CQDs與致病菌的結合過程中,孵育時間是影響結合效率的關鍵因素。實驗以大腸桿菌JM109為樣本,考察了Man-CQDs與致病菌的不同孵育時間(15、30、45、60、90 min)。大腸桿菌JM109與250 μL 1 mg/mL Man-CQDs溶液孵育后,離心去除多余的Man-CQDs,將大腸桿菌JM109用PBS緩沖液重懸,測試標記后致病菌的熒光信號。結果顯示,在60 min內熒光強度隨時間的增加而增強,60 min后熒光強度基本保持不變。因此,選擇結合時間為60 min。
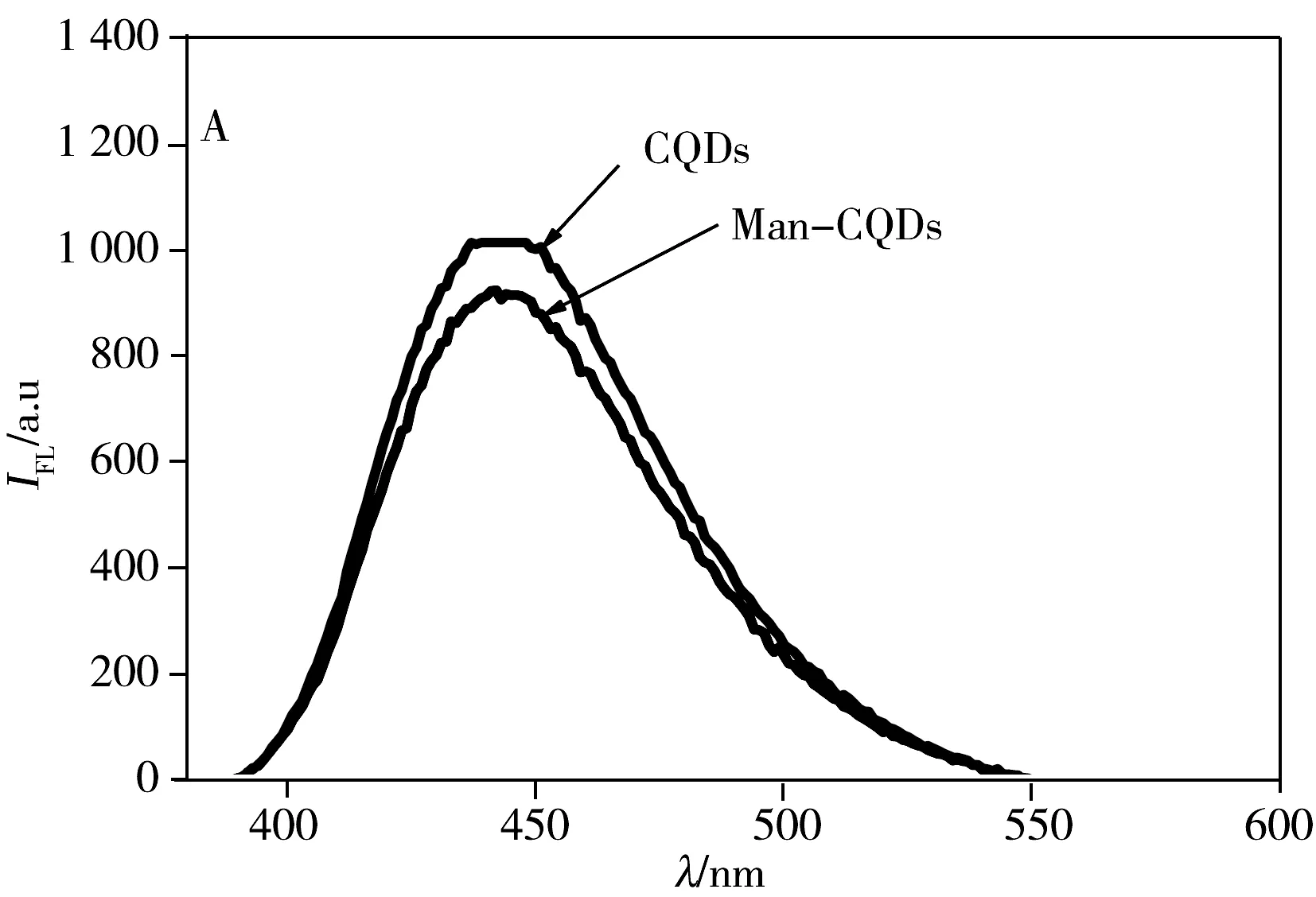
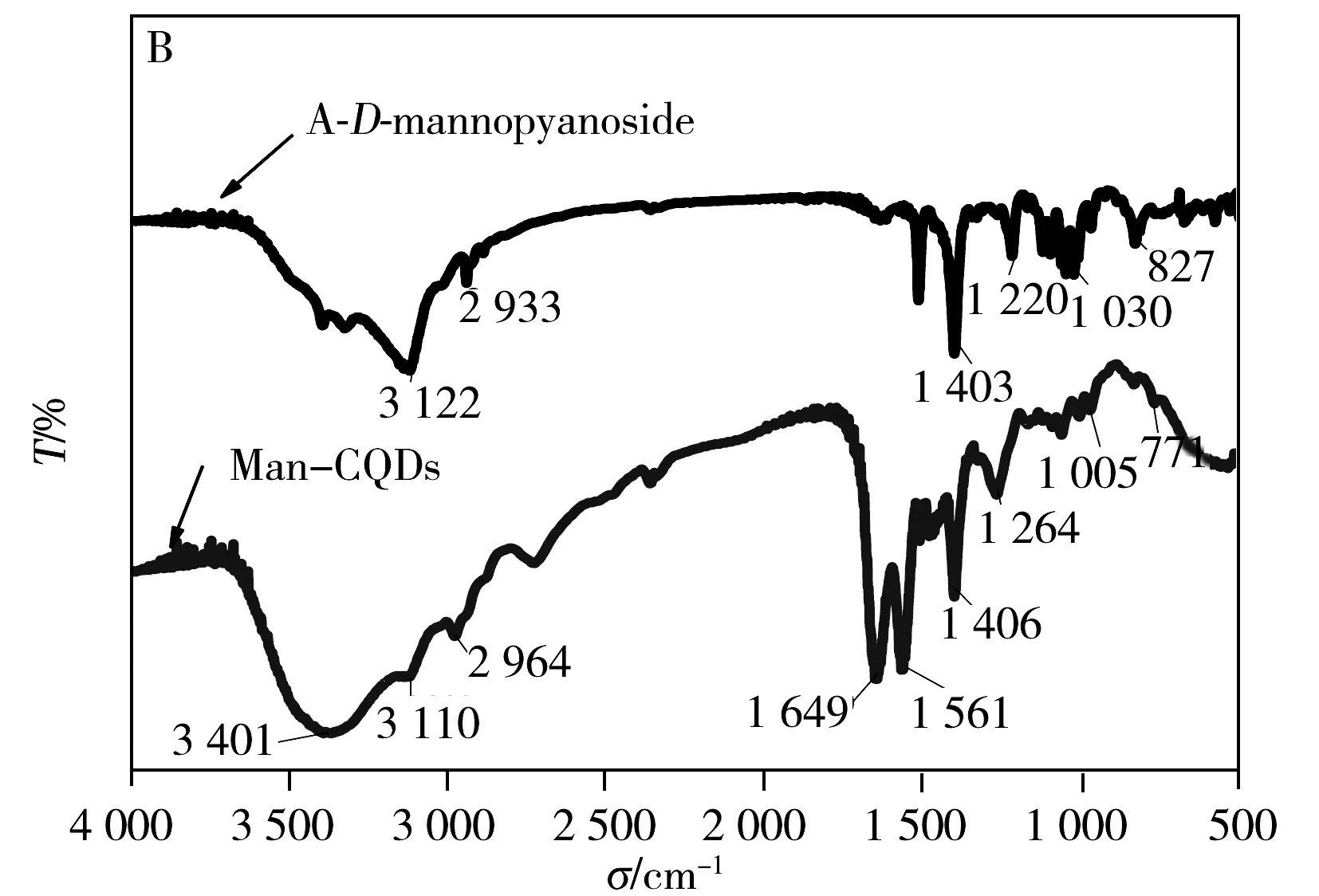
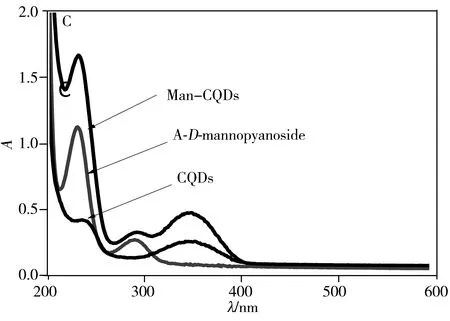
圖3 Man-CQDs的熒光光譜(A)、紅外光譜(B)與紫外光譜圖(C)Fig.3 Fluorescence spectra(A),FTIR spectra(B)and UV-Vis spectra(C) of Man-CQDs
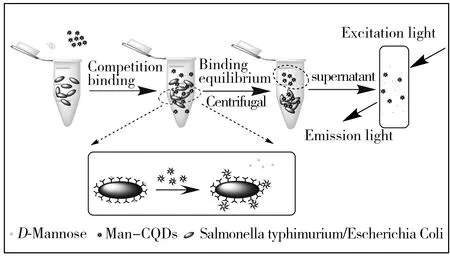
圖4 D-Mannose、Man-CQDs和細菌競爭結合原理圖Fig.4 Scheme of fluorescence-based competition binding assay between D-Mannose,Man-CQDs and bacteria
2.5 Man-CQDs與3種致病菌的相互作用
Man-CQDs與致病菌的相互作用采用競爭結合方式(圖4),首先加入D-Mannose與致病菌結合,再加入Man-CQDs競爭結合D-Mannose與致病菌已結合的位點,使D-Mannose脫離位點,Man-CQDs占據結合位點。熒光光譜(圖5A)測試結果顯示,與直接結合相比,競爭結合后的上清液熒光強度下降更多,說明Man-CQDs與致病菌結合更好。相較于D-Mannose單個結合位點,Man-CQDs表面有多個甘露糖位點,能夠有效地使D-Mannose與致病菌表面脫離,自身占據結合位點,能夠真實地反映Man-CQDs與致病菌結合的過程[16],避免和盡量減少非特異性結合。待Man-CQDs、D-Mannose與致病菌結合平衡后,通過離心將Man-CQDs/致病菌復合物與游離的Man-CQDs和D-Mannose分離,沉淀用PBS重懸,測試其熒光光譜并分析(CQDs作為對照組)。測試結果顯示,CQDs與致病菌不結合;Man-CQDs選擇性識別大腸桿菌JM109和沙門氏菌S.123443,不與大腸桿菌DH5a結合,且Man-CQDs與沙門氏菌S.123443的結合能力強于大腸桿菌JM109(圖5B,C,D)。結果表明,Man-CQDs能夠選擇性識別大腸桿菌JM109和沙門氏菌S.123443,而不是非特異性吸附。
2.6Man-CQDs與致病菌結合常數的計算
致病菌與糖非共價結合的機理研究,對致病菌的定量檢測和抑制粘附細胞均有重要意義,結合常數不僅是判定致病菌與糖作用強弱的參數,還是兩者結合方式和結合效果研究的基礎[17]。表達Ⅰ型菌毛的細菌如沙門氏菌、大腸桿菌和肺炎鏈球菌等能與甘露糖及其衍生物識別結合,其結合主要是與細菌菌毛/鞭毛末端的凝集素(蛋白)進行糖-蛋白識別[18-19]。Cecioni等[20]提出致病菌的每個菌毛/鞭毛末端只有1個結合位點,其結合方式為1∶1結合,因此可采用Scatchard方程計算得到甘露糖與致病菌的結合常數,以此評價兩者的親和作用強弱。假設致病菌菌毛/鞭毛有m個區域,每個區域有n個同等強度的結合位點,且相互獨立,可以結合n個Man-CQDs,則有Scatchard[21]方程:
μ/Cf=Ka(n-μ);μ=(Ct-Cf)/Cm
(2)
式中n、Ct、Cf、Ka、μ分別是結合位點數、加入Man-CQDs濃度、游離Man-CQDs濃度、結合常數和致病菌每個區域上結合Man-CQDs數量。Cf根據Man-CQDs濃度與其熒光強度的線性方程(IF=3 564C+41.09,r2=0.999 4)計算得到;根據細菌結合的Man-CQDs濃度與細菌濃度的比值,可計算得μ,由于致病菌為非均相溶液,濃度無法以摩爾濃度表示,通常以與致病菌結合最大的Man-CQDs濃度Cm替代。基于上述方程,以μ/Cf對μ線性回歸后可求出結合常數Ka。
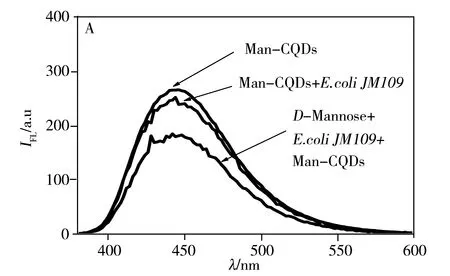

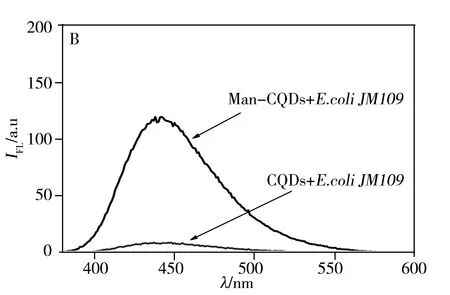
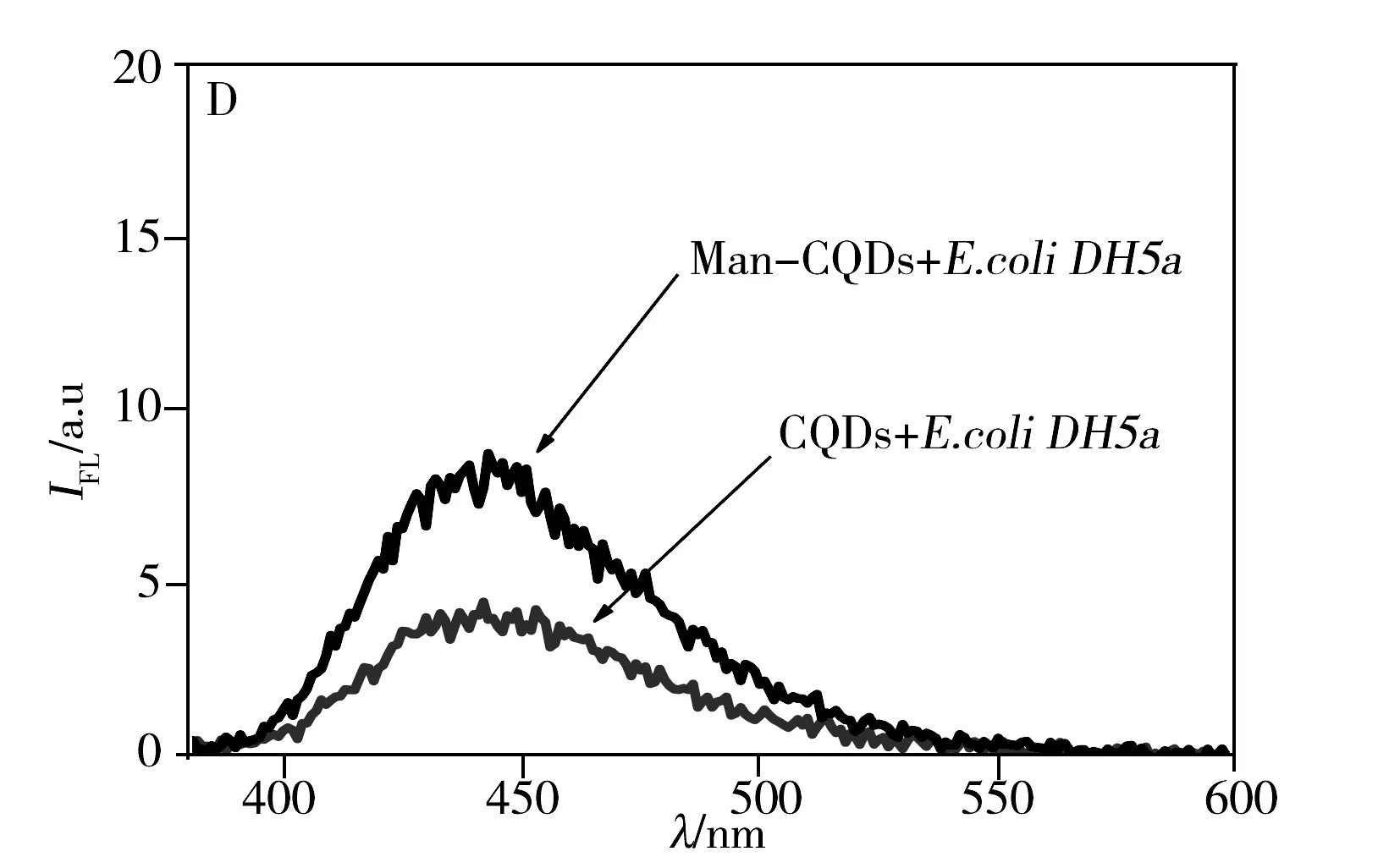
圖5 D-Mannose、Man-CQDs和細菌競爭結合后上清液的熒光光譜圖(A)以及細菌與Man-CQDs結合后的熒光光譜(B~D)Fig.5 Fluorescence spectra of the supernatant based on competition binding assay between D-Mannose,Man-CQDs (A)and bacteria,and fluorescence spectra of bacteria labeled Man-CQDs(B-D)B:E.coli JM109;C:typhimurium S.123443;D:E.coli DH5a

表1 Man-CQDs與細菌的結合常數Table 1 Binding constant of Man-CQDs and bacteria
3種致病菌與系列濃度(0.023 4~0.291 6 mmol/L)的Man-CQDs溶液結合后,其上清液的熒光光譜測試結果顯示,隨著Man-CQDs濃度的增加,上清液的熒光強度減弱,說明與致病菌結合的Man-CQDs也隨之增加。當Cf=1.06×10-4mol/L時,μ由迅速增加到逐漸平穩,說明Man-CQDs與致病菌結合達到最大,對應結合最大的濃度為1.94×10-4mol/L。然而大腸桿菌DH5a與Man-CQDs結合實驗中,隨著Man-CQDs濃度增加,上清液的熒光強度也隨之增加,并超出測試范圍,說明其未與Man-CQDs結合,與文獻[22]中甘露糖與大腸桿菌DH5a不結合是一致的。根據μ/Cf對μ線性回歸計算得到沙門氏菌與Man-CQDs的Ka=1.17×105L/mol,大腸桿菌JM109與Man-CQDs的Ka=2.39×103L/mol(表1),與文獻[17]中報道的糖與致病菌的結合常數同一數量級,Man-CQDs與這兩種致病菌有較強的親和作用,前者的Ka明顯比后者強,可能是兩者非共價結合的作用方式不同[17]所致。
3 結 論
本文以水熱法制備得到了水溶性好、熒光量子產率高、結構穩定的Man-CQDs,結合Scatchard線性分析,計算得到沙門氏菌、大腸桿菌JM109與Man-CQDs的結合常數。據此建立了一種新型的定量研究甘露糖與細菌選擇性識別結合的方法,該方法具有簡單、直接、靈敏度高及無毒的優點,為表達Ⅰ型菌毛的細菌與宿主細胞表面糖類分子選擇性識別結合的機理研究提供了理論基礎。同時,也擴展了CQDs在細菌領域的應用范圍,為后續細菌粘附宿主細胞機理的研究以及新型糖類抗菌藥的研發等提供了新的技術途徑。
[1] Ofek I,Hasty D L,Sharon N.FEMSImmunol.Med.Microbiol.,2003,3(38):181-191.
[2] Loka R S,McConnell M S,Nguyen H M.Biomacromolecules,2015,16(12):4013-4021.
[3] Hong M F,Cassely A,Mechref Y,Novotny M V.J.Chromatogr.B,2001,2(752):207-216.
[4] Coulibaly F S,Youan B B C.Biosens.Bioelectron.,2014,59:404-411.
[5] Smith E A,Thomas W D,Kiessling L L.J.Am.Chem.Soc.,2003,125(20):6140-6148.
[6] Ahmed K B A,Mohammed A S,Anbazhagan V.Spectrochim.Acta,A,2015,145:110-116.
[7] Wang X,Ramstro O,Yan M D.Anal.Chem.,2010,82(21):9082-9089.
[8] Okada T,Isobe C,Wada T,Ezaki S,Minourn N.BioconjugateChem.,2013,24(6):841-845.
[9] Zhu S J,Meng Q,Wang L,Zhang J H,Song Y B,Jin H,Zhang K,Sun H C,Wang H Y,Yang B.Angew.Chem.Int.Ed.,2013,52(14):3953-3957.
[10] Wang R J,Xu Y,Zhang T,Jiang Y.Anal.Methods,2015,7(5):1701-1706.
[11] Ma N,Jiang W T,Li T,Zhang Z Q,Qi H Z,Yang M H.Microchim.Acta,2015,182(1/2):443-447.
[12] Zhong D,Zhuo Y,Feng Y,Yang X M.Biosens.Bioelectron.,2015,74:546-553.
[13] Weng C I,Chang H T,Shen Y W,Unnikrishnan B,Li Y J,Huang C C.Biosens.Bioelectron.,2015,68:1-6.
[14] Lai I P J,Harroun S G,Chen S Y,Unnikrishnan B,Li Y J,Huang C C.Sens.ActuatorsB,2016,228:465-470.
[15] Dubois M,Gilles K A,Hamilton J K,Rebers P A,Smith F.Anal.Chem.,1956,28(3):350-356.
[16] Friguent B,Chaffatte A F,Djavadi-Ohaniance L,Goldberg M E.Immunol.Methods,1985,77(2):305-319.
[17] Abdelhamid H N,Wu H F.J.Mater.Chem.B,2013,1(44):6094-6106.
[18] Hartmann M,Lindhorst T K.Eur.J.Org.Chem.,2011,(20/21):3585-3609.
[19] Zeng X,Andrade C A S,Oliveira M D L,Sun X L.Anal.Bioanal.Chem.,2012,402(10):3161-3176.
[20] Cecioni S,Imberty A,Vidal S.Chem.Rev.,2015,115(1):525-561.
[21] Scatchard G,Ann N Y.Acad.Sci.,1949,51(4):660-672.
[22] Wang Y X,Ye Z Z,Si C Y,Ying Y B.FoodChem.,2013,136(3/4):1303-1308.
Study on Interaction between Mannose and Bacteria Using Glycosylated Carbon Quantum Dots
ZHAO Bin1,2,4,CUI Fei-yun1,2,4,XU Yi2,3,4*,ZHANG Xiao-feng2,4,5,LI Ze-quan1*
(1.School of Chemistry and Chemical Engineering,Chongqing University,Chongqing 400044,China;2.Key Disciplines Laboratory of Novel Micro-nano Devices and System Technology,Chongqing 400044,China;3.Microsystem Research Center,School of Optoelectronic Engineering,Chongqing University,Chongqing 400044,China;4.International R&D Center of Micro-nano Systems and New Materials Technology,Chongqing 400044,China;5.School of Chemistry and Chemical Engineering,Chongqing University of Technology,Chongqing 400050,China)
In this paper,citric acid was used as carbon source for preparing fluorescent carbon quantum dots(CQDs).Due to the obtained CQDs had carboxyl groups on their surfaces,Man-CQDs were synthesized by immobilizing 4-aminopheny-l-α-D-mannopyanoside on the surfaces of CQDs via covalent bond.Furthermore,the binding constants of Man-CQDs and Escherichia coliJM109/EscherichiaDH5a/SalmonellatyphimuriumS.123443 were obtained by fluorescent competition experiments.The results showed that the sizes of CQDs were approximately 26 nm,the maximum excitation wavelength for CQDs was 445 nm and the fluorescence yield was 76%in contrast to 54%quinine sulfate.Compared with the fluorescence intensity of CQDs,the prepared Man-CQDs remained unchanged in principle.By the Phenol-sulfate method,the concentration of Man-CQDs was calculated to be 2.832 mmol/L,and the content of mannose in Man-CQDs nanoparticles was approximately 40%.Based on competition binding experiments of Man-CQDs andD-mannose with bacteria,the binding constant of Man-CQDs and bacteria was calculated by Scatchard equation,namely the binding constants of Man-CQDs withEscherichiacoliJM109 andSalmonellatyphimuriumS.123443 were 2.39×103L/mol and 1.17×105L/mol,respectively.However,the reaction of Man-CQDs andEscherichiacoliDH5awas nonspecific binding.The results suggested that the proposed method was applicable for the determination of noncovalent binding constant between mannose and bacteria.Besides,it offered a valuable reference information for the research of interaction between carbohydrate and bacteria.
Man-CQDs;EscherichiacoliJM109;EscherichiacoliDH5a;SalmonellatyphimuriumS.123443;binding constant;interaction;fluorescence spectrum
2017-05-31;
2017-07-15
重慶市科學技術委員會社會民生科技創新一般項目(cstc2015shms zx00014);重慶市科學技術委員科技惠民計劃項目(cstc2015jcsf8001)
*
徐 溢,博士,教授,研究方向:分析化學、應用化學和微型集成生化分析系統,E-mail:18883724394@163.com 李澤全,博士,副教授,研究方向:熔鹽電化學、材料制備及性能、環境等,E-mail:lzq@cqu.edu.cn
10.3969/j.issn.1004-4957.2017.11.005
O433.4
A
1004-4957(2017)11-1318-07

