化學發光免疫分析技術在微生物檢測中的應用
李靜雯,劉清珺,杜美紅*,趙瑞雪,萬宇平,吳小勝,馮月君
(1.北京市理化分析測試中心 北京市食品安全分析測試工程技術研究中心,北京 100089;2.北京勤邦生物技術有限公司 北京市食品安全免疫快速檢測工程技術研究中心,北京 102206)
化學發光免疫分析技術在微生物檢測中的應用
李靜雯1,劉清珺1,杜美紅1*,趙瑞雪1,萬宇平2,吳小勝2,馮月君2
(1.北京市理化分析測試中心 北京市食品安全分析測試工程技術研究中心,北京 100089;2.北京勤邦生物技術有限公司 北京市食品安全免疫快速檢測工程技術研究中心,北京 102206)
化學發光免疫分析技術憑借其化學發光的高靈敏性和免疫反應的高特異性在微生物快速檢測中廣泛應用。該文著重敘述了化學發光免疫分析技術核心檢測體系在微生物檢測中的研究進展,并對其涉及到的樣品前處理和檢測新方法進行了綜述。化學發光免疫分析技術檢測微生物用時短、成本低,但特異性識別方法和檢測的靈敏度有待提升,新型的發光體系、發光放大方法、可替代抗體的識別分子以及相關的前處理技術是未來研究的重點。
化學發光免疫分析技術;微生物檢測;前處理;發光放大;識別分子
微生物檢測是食品安全、臨床診斷、環境監控、生物分析等領域的常見和必檢項目,全球的微生物檢測市場每年約有10億檢測量[1]。致病微生物的快速準確檢測對及時發現并合理控制污染和防止疾病的進一步傳播至關重要。因此,研發靈敏、快捷、成本低的微生物檢測新技術具有重要的現實意義和廣闊的應用前景。
目前微生物檢測采用國標方法,即平板培養法。該方法需經過前增菌、選擇性增菌、分離培養、生化鑒定等步驟,雖然結果較為準確,成本較低,但檢測過程繁瑣,一般需4~6 d的時間,不適用于致病微生物的快速篩查與污染控制。近年來,分子生物學和免疫學檢測技術的蓬勃發展,使得微生物的快速檢測方法不斷創新。分子生物學檢測技術,如聚合酶鏈式反應(Polymerase chain reaction,PCR)[2]、實時熒光定量PCR(Real-time quantitative PCR,qPCR)[3- 4]、環介導等溫擴增(Loop-mediated isothermal amplification,LAMP)[5-6]生物芯片[7-9],以及免疫分析技術,如酶聯免疫吸附測定(Enzyme linked immunosorbent assay,ELISA)[10-11]、化學發光免疫分析技術(Chemiluminescence immunoassay,CLIA)[12-13]、側流免疫層析技術(Lateral flow immunoassay,LFI)[14-15]、電化學免疫分析技術(Electrochemical immunosensor,ECIS)[16]等均被應用于食品、環境樣品的微生物快速檢測,檢出限達到100~104CFU/mL,檢測時間為0.5~5 h(表1)。這些快速檢測技術在縮短微生物檢測時間和降低檢出限等方面表現出巨大的優勢。分子生物學技術以檢測微生物的核酸(DNA和RNA)為特點,其靈敏度高、特異性好,但較難區別死、活菌,對檢測體系、檢測環境要求嚴格,檢測人員需要有較高的專業背景,而且檢測儀器昂貴,限制了其在基層部門微生物快速檢測中的應用。免疫學檢測技術以抗體特異性識別微生物細胞表面的抗原決定簇,成本低廉、特異性好,但是其檢測用抗體較難制備和保存,目前并不能對所有目標菌進行檢測,涉及的關鍵問題還需深入研究。化學發光免疫分析技術是近年來免疫分析技術中的研究熱點,該技術已成為真菌毒素、藥物、激素、腫瘤標志物等物質的重要檢測方法,并開發出多種檢測試劑盒[17]。化學發光免疫分析技術以其檢測用時短、靈敏度高、設備兼容性強的特點在微生物檢測中嶄露頭角,本文針對化學發光免疫分析技術在食品、環境等領域中微生物檢測的研究進展及應用進行闡述。
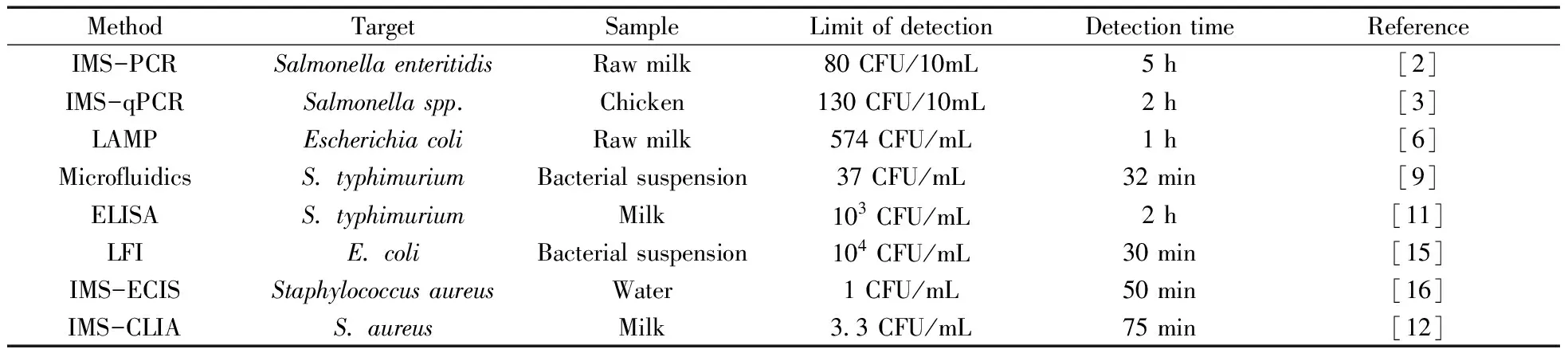
表1 常見的微生物快速檢測技術Table 1 Common rapid detection techniques of microbes
1 化學發光免疫分析技術檢測微生物的原理
1.1 檢測原理
1977年Halmann等[18]首先建立化學發光免疫分析技術,以參與化學發光反應的試劑(發光劑或催化劑)標記抗體,標記后的抗體與待測物經過抗原抗體反應和分離步驟,以化學發光的形式來定量反映待測物的含量。因為化學發光強度與化學發光反應速率相關,而反應速率由標記物的含量決定,所以化學發光強度可以作為定量依據[17]。相對于酶聯免疫以顏色深淺定量、放射免疫以放射強度定量,化學發光檢測具有靈敏度高、可檢測范圍大、檢測結果穩定和不易被干擾等突出優勢。化學發光免疫分析包括免疫反應系統和化學發光分析系統。免疫反應系統保證了檢測的準確性和特異性,化學發光分析系統決定了檢測的靈敏度。
1.2 免疫分析方法
化學發光免疫分析技術是一種利用抗原和抗體的特異性結合來選擇性識別和測定待測物的免疫分析方法,一般分為競爭法和雙抗夾心法。夾心法常用于大分子抗原的定量分析,微生物檢測多采用此法[19]:用免疫磁珠或包被了抗體的微孔板捕獲目標菌,加入標記抗體,形成夾心復合物;將游離標記抗體分離,再加入化學發光反應試劑,測定發光強度,目標菌濃度與發光強度成正比(圖1)。競爭法檢測微生物,將微生物的抗原決定簇包被在固相載體上,與目標菌競爭結合標記抗體,然后測定固相載體上標記物的含量,發光強度與目標菌濃度成反比(圖2)。由于夾心法涉及兩種抗體,檢測的特異性優于競爭法,測定結果更為準確。Gehring等[20]以特異性識別大腸桿菌O157∶H7的O抗原和H抗原的兩種抗體作為夾心雙抗,避免了其他大腸桿菌種屬的干擾,降低了檢測的假陽性率。Li等[21]通過電化學發光免疫分析技術采用競爭法和夾心法檢測大腸桿菌O157∶H7,并進行比較,發現夾心法的檢出限較低(1.2×102CFU/mL)且線性范圍更寬。
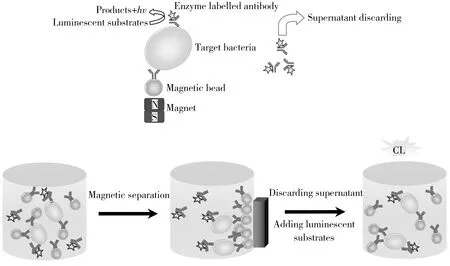
圖1 化學發光免疫分析技術檢測微生物的雙抗夾心法原理[12]Fig.1 Principle of sandwich immunoassay format in microbiological detection by chemiluminescence immunoassay
1.3 化學發光體系
以標記物區分,化學發光體系一般分為3類:酶促化學發光、非酶促化學發光和電化學發光。酶促化學發光體系以催化劑為標記物,靈敏度和穩定性均優于以發光劑為標記物,所以微生物檢測一般采用酶促化學發光體系。標記物多采用辣根過氧化物酶(Horseradish peroxidase,HRP)[13,19-20,22-25]和堿性磷酸酶(Alkaline phosphatase,ALP)[12,26]。Liu等[22]以HRP為標記物,催化魯米諾與H2O2進行化學發光反應,最強發光波長為425 nm,用雙抗夾心法對牛肉中的大腸桿菌O157∶H7進行檢測,檢出限為5.5×102CFU/mL,線性范圍為102~105CFU/mL。Gehring等[26]以ALP為標記物,二氧化吖啶二鈉鹽(APS-5)為發光底物,同樣利用雙抗夾心法對牛肉中的大腸桿菌O157∶H7進行檢測,檢出限為7.6×103CFU/mL。APS-5的穩定性較差,顯色溫度需低于20 ℃,保存溫度需低于-20 ℃,限制了其廣泛使用。目前,常用的ALP催化的化學發光底物為二氧雜環乙烷類物質,其中二氧環乙烷二鈉鹽(AMPPD)的應用最為成功[12],其在ALP催化下發生分解反應,脫去磷酸基團,產生477 nm的持續穩定的化學發光。AMPPD性質十分穩定,在無酶催化下水解速率非常慢,極具應用潛力。以酶為標記物的化學發光是化學發光免疫分析的主流,所占比例約為80%[17]。非酶促發光體系一般以化學發光試劑為標記物,如魯米諾、異魯米諾、吖啶酯,在過渡金屬離子、過氧化物酶等催化劑的作用下與H2O2反應,目前關于微生物檢測的報道較少。電化學發光是一類特殊的化學發光反應體系,一般以聯吡啶釕[Ru(bpy)3]2+為標記物,電極將其氧化為[Ru(bpy)3]3+,然后被電子載體N-羥基琥珀酰亞胺(N-Hydroxysuccinimide,NHS)還原,并釋放1個光子回到基態,在620 nm波長處檢測發光強度。[Ru(bpy)3]2+在化學發光反應過程中不消耗,兼具準確性和穩定性,便于開發全自動分析儀器,是近年來化學發光免疫分析技術的研究熱點之一[20,27-28]。Morel等[29]利用該方法檢測炭疽桿菌,檢出限為3×102CFU/mL,比酶促化學發光免疫分析技術表現出更高的靈敏度。
2 化學發光免疫分析技術在微生物檢測中的應用
2.1 樣品前處理策略
食品、環境和醫學微生物檢測的主要挑戰是樣品中痕量目標菌(<10 CFU/g)的檢測,和樣品基質對檢測的干擾。前處理過程能有效地從樣品顆粒、干擾物和抑制劑中分離、濃縮目標菌,有助于提高低水平或散發性污染樣品的檢測靈敏度和準確性,避免微生物分布不均勻導致的檢測結果代表性差的問題。此外,目標菌濃縮可以減少或消除對增菌步驟的需要。因此,前處理方法在微生物檢測中有舉足輕重的作用。目前,化學發光免疫分析技術常用的前處理方法有過濾、離心、免疫磁分離等(表2)。Wunderlich等[30]使用吸附過濾結合離心超濾的前處理方法,先將10 L樣品水通過單層過濾膜,并用20 mL洗脫液將吸附物完全洗脫下來,再離心濃縮至1 mL,整個前處理過程將水中微生物的密度提高10 000倍,省去了增菌步驟,嗜肺軍團菌的回收率達到99.8%。再利用微陣列化學發光芯片可檢出0.39 CFU/mL的目標菌,檢測全過程僅需90 min。過濾和離心等物理前處理方法可有效濃縮微生物,但無法實現目標菌的特異性分離,較適合液態、無較多顆粒干擾的檢測樣品。微生物過濾后需洗脫,面臨濃度降低和回收不完全的問題。
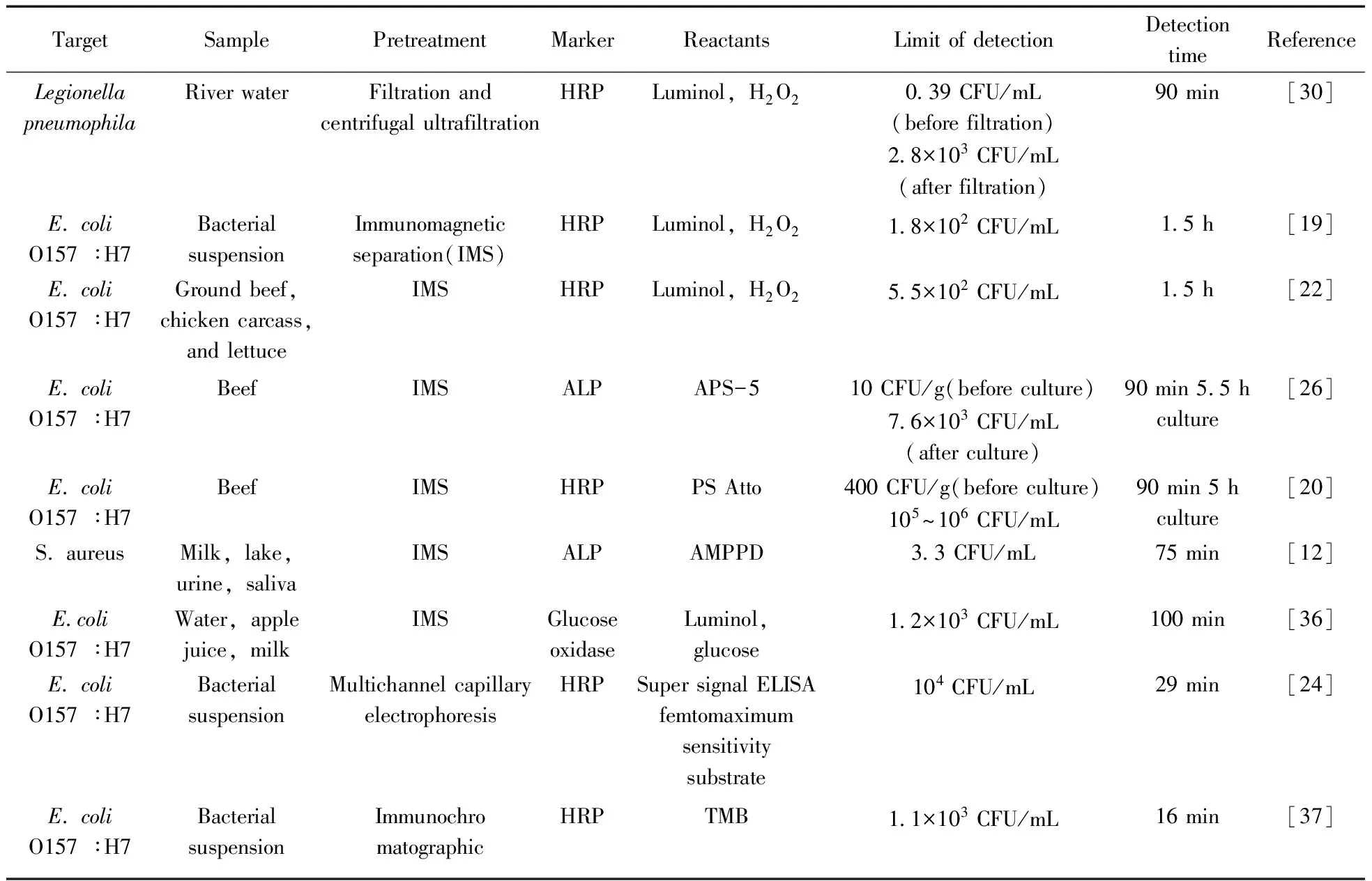
表2 化學發光免疫分析技術結合前處理技術在微生物檢測中的應用Table 2 Application of chemiluminescence immunoassay combined with pretreatment in microbiological detection
1979年免疫磁珠問世,磁性微粒表面偶聯著抗體等識別分子,可與目標菌特異性結合,通過外加磁場定向移動并聚集,達到特異性分離和濃縮的目的[31]。免疫磁珠分離能夠快速無損分離目標菌,不但排除了樣品基質對檢測的影響,還降低了其他種屬微生物對目標菌檢測的干擾,因此越來越多地應用于微生物檢測的前處理。高明遠課題組[32]以國產亞微米級的單分散磁性微球為基礎,制備出捕獲效率95%以上的免疫磁珠,用于沙門氏菌的富集分離。Du等[33-34]證實該納米級免疫磁珠的捕獲性能優于微米級免疫磁珠,利用該免疫磁珠對雞肉和牛奶樣品中100 CFU/mL的沙門氏菌免疫磁分離后進行了4 h增菌培養,即達到103CFU/mL以上,滿足化學發光免疫分析技術檢出限的需求。Yang等[12]利用萬古霉素標記的磁珠捕獲樣品中的目標菌,菌密度增加20倍,與標記ALP的金黃色葡萄球菌抗體形成夾心,ALP催化AMPPD進行化學發光反應檢測金黃色葡萄球菌,檢出限達3.3 CFU/mL。
將免疫色譜、毛細管電泳等新興的分離技術,與靈敏的化學發光結合,具有反應快,無需長時間溫浴,可以同時進行多組分檢測的優勢。Yacoub-George等[35]采用集成的毛細管芯片免疫反應器將含有菌毒素、病毒和細菌的樣品組分分離并同時檢測,分離檢測全過程僅需24 min,可檢測出105CFU/mL以上的大腸桿菌O157∶H7。
2.2 化學發光免疫分析技術中的特異性識別策略
免疫分析技術建立在免疫識別基礎上,識別分子保證了檢測的特異性和準確性。化學發光免疫分析技術檢測微生物的識別分子一般為抗體。多克隆抗體價格相對低廉,但需通過免疫動物獲得,雖然經過分離純化,但不可避免地與非目標菌存在交叉反應。單克隆抗體的特異性好,但雜交瘤技術非常昂貴且耗時[38]。此外,抗體活性易受環境、反應條件等多種因素的影響,制約了免疫分析技術的推廣普及。近年來,國內外學者嘗試使用新型識別分子代替抗體,適配體[39]、抗生素[12]、抗菌肽[21]、噬菌體[40]和分子印跡聚合物[41]等均在微生物特異性識別中得到應用(表3)。Kwun等[39]利用適配體作為識別分子偶聯1,1′-草酰二咪唑,競爭法檢測副溶血弧菌,目標菌與氧化石墨烯競爭結合適配體,檢出限為2.23×103CFU/mL。Li等[21]利用抗菌肽Magainin Ⅰ作為識別分子,通過電化學發光免疫分析技術檢測大腸桿菌O157∶H7,進一步降低了化學發光反應的本底值。Yue等[40]利用噬菌體作為識別分子,通過電化學發光免疫分析技術能檢測出56 CFU/mL以上的銅綠假單胞菌。這些新型識別分子制備過程相對簡單,制備成本低,在高溫下穩定性好,有更寬的pH值耐受范圍,而且應用靈活性強,容易標記各種酶分子或官能團。其中,對于微生物細胞這種大抗原,噬菌體和適配體是目前最有希望替代抗體的識別分子,但還需利用多種手段優化篩選方法以進一步提高識別分子與目標菌的親和性。抗生素和抗菌肽簡單易得,但特異性普遍較弱,一般用于初步捕獲,檢測需抗體配合。分子印跡聚合物較適合用于小抗原的識別,其制備常用本體聚合法,制備完成后存在模板分子難以去除導致實際產率低的問題[38]。

表3 新型識別分子特異性識別目標菌的作用機理Table 3 Mechanism of new recognition elements specific recognizing the target bacteria
2.3 化學發光免疫分析技術中的發光放大策略
靈敏度是微生物快速檢測技術的關鍵指標。特別在低水平污染的樣品中,靈敏度是決定微生物檢測時間和準確性的重要因素。因此,提高化學發光免疫分析技術的靈敏度具有重要的研究價值。將化學發光反應的發光放大是提高靈敏度的主要手段。利用微粒比表面積大的特點,在其表面結合大量的催化劑、發光劑等,使得與待檢物結合的標記物大大增加,靈敏度大幅提高,檢出限降低。Mun等[42]將HRP標記到免疫磁珠上用來捕獲沙門氏菌,利用100 nm免疫磁珠比沙門氏菌體積小很多的特點,用0.22 μm的過濾膜將免疫磁珠-沙門氏菌復合體與游離的免疫磁珠分離。由于免疫磁珠上可標記大量的HRP,所以檢出限顯著降低,10 CFU沙門氏菌即可檢出。Wang等[43]通過納米金顆粒輔助銀形成樹枝狀分布的Ag+,利用Ag+對K2S2O8-Mn2+-魯米諾反應體系顯著的催化作用,使得靈敏度提高2個數量級,實現了100 CFU/mL沙門氏菌不需經過增菌步驟的直接化學發光免疫分析檢測。
開發新的化學發光反應體系以提高檢測靈敏度是化學發光免疫分析技術的發展趨勢。Zhang等[36]以葡萄糖氧化酶作為標記物,催化葡萄糖和O2產生葡萄糖酸和H2O2,并利用漆酶在堿性環境下催化魯米諾與H2O2的化學發光反應起到二次放大的作用,增加了化學發光強度,檢出限為1.2×103CFU/mL。
2.4 化學發光免疫分析技術中固相材料的應用
固相材料用于固定抗體、酶、發光劑等物質,影響微生物檢測的靈敏性和穩定性。化學發光免疫分析技術中使用的固相材料有微孔板、磁性微粒和多孔材料等[17](表4)。Magliulo等[23]利用聚苯乙烯微孔板為固相材料,并在1個主孔中設置4個子孔分別包被大腸桿菌O157∶H7、鼠傷寒沙門氏菌、單核增生李斯特菌和小腸結腸炎耶爾森菌的單克隆抗體,利用HRP標記的多克隆抗體同時檢測這4種致病菌,檢出限為104CFU/mL。該方法使用極少量的抗體,實現了快速、高通量、低成本的微生物檢測。
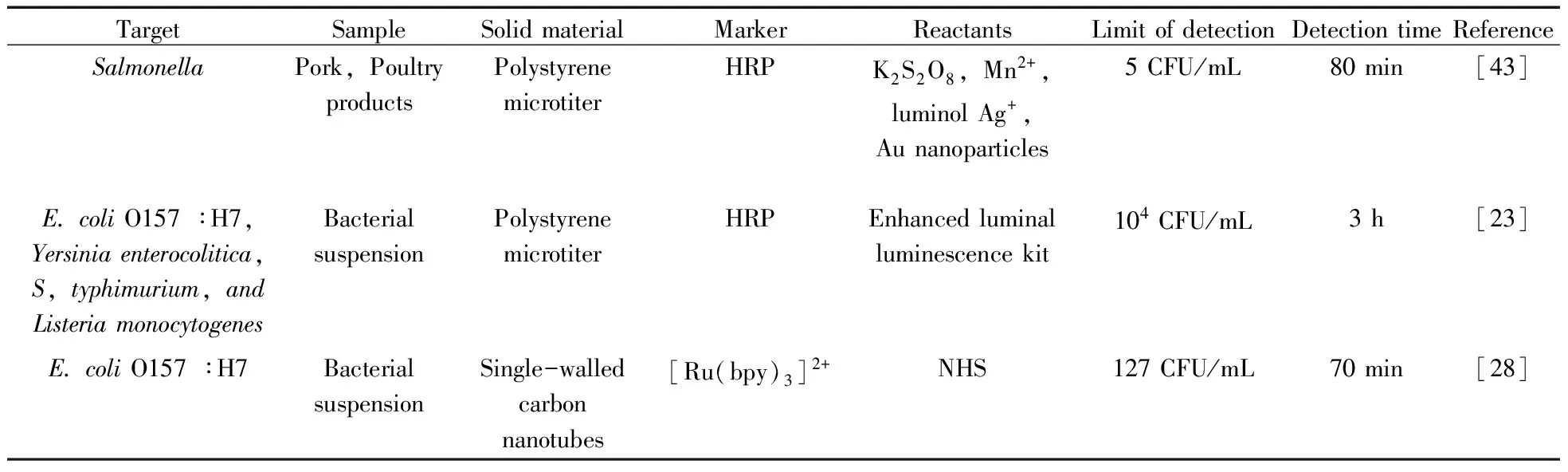
表4 固相材料在化學發光免疫分析技術檢測微生物中的應用Table 4 Application of solid materials in microbiological detection by chemiluminescence immunoassay
微粒形態的固相材料包被上抗原,模擬制成目標菌標準品,即可采用競爭法檢測微生物。Xiong等[13]將包被了葡萄球菌蛋白A的磁珠作為目標菌類似物,與金黃色葡萄球菌競爭結合HRP標記的抗體,檢出限達6 CFU/mL。此方法有較高的靈敏度和較寬的線性范圍,且抗原抗體一步孵育即可得出檢測結果,全部檢測過程僅需50 min,顯示出良好的應用前景。
固相材料還可用于合成人工模擬酶,比天然酶更易制備且性質穩定。Yang等[44]將脫氧核酶序列與適配體序列組成一個單鏈DNA探針,將探針包裹到單碳納米管上。其中適配體序列能特異性地與目標菌結合,導致脫氧核酶序列遠離單碳納米管與高鐵血紅素結合,形成HRP的模擬酶。該模擬酶能夠催化魯米諾-H2O2體系產生化學發光,可檢測出103CFU/mL的沙門氏菌。
3 總結與展望
微生物檢測技術,必須具備較高的靈敏度、顯著的特異性、獲得結果的快速性和檢測成本的低廉性。化學發光免疫分析方法的靈敏性和檢測范圍遠高于酶聯免疫等其他免疫分析技術,兼具操作簡便、檢測時間短等優勢,在微生物檢測方面發展迅速。靈敏度是微生物快速檢測技術的關鍵問題,化學發光體系中最成熟的是HRP-魯米諾-H2O2和ALP-ADPPM體系,目前靈敏度達到102~103CFU/mL。配合免疫磁分離、超濾等前處理方法,檢出限可降為10-1~100CFU/mL。新型的化學發光體系、納米顆粒和固相材料的應用能進一步增強發光信號,降低本底噪音,提高檢測的靈敏度。
免疫識別決定了化學發光免疫分析檢測微生物的特異性和穩定性。由于抗體難制備與不易保存的缺點,噬菌體、適配體等新型可替代抗體的識別分子的研發是今后化學發光免疫分析領域研究的重點,對該技術的推廣普及具有重要意義。微生物容易發生變異,一定程度上限制了免疫分析方法的穩定性,但這也是目前快速檢測方法普遍面臨的問題。必要時可結合生化鑒定、全基因組測序和基質輔助激光解吸電離飛行時間質譜等其他技術深入解析變異微生物,并進行鑒定和溯源。
食品行業的微生物監控,要求對樣品進行活菌檢測,但食品中活致病菌數量一般較少,直接進行化學發光免疫分析檢測難以達到目的。通過對樣品進行短暫增菌,使少量的活菌得到增殖,避免了檢測結果的假陰性;同時區分了死、活菌,避免了假陽性結果。因此針對不同性質的待測樣品開發成套的、結合前處理和增菌方案的化學發光免疫分析方法非常必要,可為該技術在微生物檢測領域的推廣普及奠定基礎。
[1] Wang Y,Salazar J K.Compr.Rev.FoodSci.Saf.,2016,15(1):183-205.
[2] Bai Y L,Song M H,Cui Y,Shi C L,Wang D P,Paoli G C,Shi X M.Anal.Chim.Acta,2013,787(13):93-101.
[3] Hyeon J Y,Deng X.FoodMicrobiol.,2017,63:111-116.
[4] Yang Y J,Xu F,Xu H Y,Aguilar Z P,Niu R J,Yuan Y,Sun J C,You X Y,Lai W H,Xiong Y H.FoodMicrobiol.,2013,34(2):418-424.
[5] Fan F X,Du P C,Kan B,Yan M Y.PLoSOne,2015,10(4):e0124507.doi:10.1371/journal.pone.0124507.
[6] Yang W T,Song X N,Wang J X,Li Z,Ji M J,Li Y F.Biosci.Trends,2014,8(6):316-321.
[7] Bang J,Beuchat L R,Song H,Gu M B,Chang H I,Kim H S,Ryu J H.Int.J.FoodMicrobiol.,2013,161(2):134-141.
[8] Goji N,Macmillan T,Amoako K K.J.Pathogens,2011,2012:627036.doi:10.1155/2012/627036.
[9] Wang R J,Ni Y N,Xu Y,Jiang Y,Dong C Y,Chuan N.Anal.Chim.Acta,2015,853(1):710-717.
[10] Cho I H,Irudayaraj J.Int.J.FoodMicrobiol.,2013,164(1):70-75.
[11] Wu W H,Li J,Pan D,Li J,Song S P,Rong M G,Li Z X,Gao J M,Lu J X.Acs.Appl.Mater.Interfaces,2014,6(19):16974-16981.
[12] Yang S J,Hui O Y,Su X X,Gao H F,Kong W J,Wang M Y,Shu Q,Fu Z F.Biosens.Bioelectron.,2016,78:174-180.
[13] Xiong J,Wang W W,Zhou Y L,Kong W J,Wang Z X,Fu Z F.Microchim.Acta,2016,183(4):1507-1512.
[14] Chaivisuthangkura P,Pengsuk C,Longyant S,Sithigorngul P.J.Microbiol.Methods,2013,95(2):304.
[15] Jin S,Dai M,Ye B C,Nugen S R.Microsyst.Technol.,2013,19(12):2011-2015.
[16] Abbaspour A,Norouz-Sarvestani F,Noori A,Soltani N.Biosens.Bioelectron.,2015,68:149-155.
[17] Lin J M,Zhao L X,Wang X.ChemiluminescenceImmunoassay.Beijing:Chemical Industry Press(林金明,趙利霞,王栩.化學發光免疫分析.北京:化學工業出版社),2008:1-9.
[18] Halmann M,Velan B,Sery T.Appl.Environ.Microbiol.,1977,34(5):473-477.
[19] Ye J,Liu Y,Li Y.Trans.Asae,2002,45(2):473-478.
[20] Gehring A G,Albin D M,Irwin P L,Reed S A,Tu S I.J.Microbiol.Methods,2006,67(3):527-533.
[21] Li Z J,Yang H Y,Sun L J,Qi H L,Gao Q,Zhang C X.Sens.ActuatorsB,2015,210:468-474.
[22] Liu Y C,Ye J M,Li Y B.J.FoodProt.,2003,66(3):512-517.
[23] Magliulo M,Simoni P,Guardigli M,Michelini E,Luciani M,Lelli R,Roda A.J.Agric.FoodChem.,2007,55(13):4933-4939.
[24] Yacoub-George E,Hell W,Meixner L,Wenninger F,Bock K,Lindner P,Wolf H,Kloth T,Feller K A.Biosens.Bioelectron.,2007,22(7):1368-1375.
[25] Karoonuthaisiri N,Charlermroj R,Uawisetwathana U,Luxananil P,Kirtikara K,Gajanandana O.Biosens.Bioelectron.,2009,24(6):1641-1648.
[26] Gehring A G,Irwin P L,Reed S A,Tu S I,Andreotti P E,Akhavan-Tafti H,Handley R S.J.Immunol.Methods,2004,293(1/2):97-106.
[27] Liao N.J.Instrum.Anal.(廖妮.分析測試學報),2016,35(7):832-838.
[28] Yang H Y,Wang Y Q,Qi H L,Gao Q,Zhang C X.Biosens.Bioelectron.,2012,35(1):376-381.
[29] Morel N,Volland H,Dano J,Lamourette P,Sylvestre P,Mock M,Créminon C.Appl.Environ.Microbiol.,2012,78(18):6491-6498.
[30] Wunderlich A,Torggler C,Elsasser D,Luck C,Niessner R,Seidel M.Anal.Bioanal.Chem.,2016,408(9):2203-2213.
[31] Ugelstad J,Kaggerud K H,Hansen F K,Berge A.MacromolChem.,1979,180(3):737-744.
[32] Niu M,Du M H,Deng Y,Gao M Y.Chem.J.Chin.Univ.(牛牧,杜美紅,鄧奕,高明遠.高等學校化學學報),2011,32(2):322-326.
[33] Dai F Y,Zhang M,Hu B B,Sun Y J,Tang Q W,Du M H,Zhang X.RscAdv.,2015,5(5):3574-3580.
[34] Dai F Y,Zhang M,Xu D X,Yang Y,Wang J X,Li M Z,Du M H.Biotechnol.Appl.Biochem.,2016,11(12).doi:10.1002/bab.1539.
[35] Yacoub-George E,Meixner L,Scheithauer W,Koppi A,Drost S,Wolf H,Danapel C,Feller K A.Anal.Chim.Acta,2002,457(1):3-12.
[36] Zhang Y,Tan C,Fei R H,Liu X X,Zhou Y,Chen J,Chen H C,Zhou R,Hu Y G.Anal.Chem.,2014,86(2):1115-1122.
[37] Park S,Min J,Kim Y K.Int.J.Environ.Anal.Chem.,2012,92(6):1-10.
[38] Dorst B V,Mehta J,Bekaert K,Rouah-Martina E,Coena D W,Dubruelc P,Blusta R,Robbens J.Biosens.Bioelectron.,2010,26(4):1178-1194.
[39] Kwun J,Yun S,Park L,Ji H L.Talanta,2014,119:262-267.
[40] Yue H,He Y,Fan E,Wang L,Lu S G,Fu Z F.Biosens.Bioelectron.,2017,94:429-432.
[42] Mun S,Choi S J.BioChipJ.,2015,9(1):10-15.
[43] Wang Z P,Duan N,Li J Q,Ye J,Ma S F,Le G W.Luminescence,2011,26(2):136-141.
[44] Yang M,Peng Z H,Neng Y,Chen Y Z,Zhou Q,Deng L.Sensors,2013,13(5):6865-6881.
Application of Chemiluminescence Immunoassay in Microbiological Detection
LI Jing-wen1,LIU Qing-jun1,DU Mei-hong1*,ZHAO Rui-xue1,WAN Yu-ping2,WU Xiao-sheng2,FENG Yue-jun2
(1.Beijing Engineering Research Center of Food Safety Analysis,Beijing Center for Physical and Chemical Analysis,Beijing 100089,China;2.Beijing Engineering Research Centre of Food Safety Immune Rapid Detection,Beijing Kwinbon Biotechnology Co.,Ltd.,Beijing 102206,China)
Chemiluminescence immunoassay is widely used in the rapid detection of microbes because of its high sensitivity of chemiluminescence and high specificity of immune response.In the paper,the advance of the coresystems of chemiluminescence immunoassay in microbiological detection is emphatically illustrated.The related sample pretreatments and the new detection methods are reviewed.Although Chemiluminescence immunoassay in the microbiological detection has the advantages of rapidness and low consumption,its specific recognition and sensitivity could be further improved.The innovative luminescence systems,the luminescence amplification methods,the alternative recognition elements and the related pretreatment techniques are the focuses in future research.
chemiluminescence immunoassay;microbiological detection;pretreatment;luminescence amplification;recognition element
2017-05-12;
2017-07-09
國家重大科學儀器設備開發專項(2013YQ140371);國家重點研發計劃資助(2016YFF0203802);北京市科技計劃項目(Z161100000916001);北京市自然科學基金項目(2162018)
*
杜美紅,博士,副研究員,研究方向:食品安全微生物快速檢測,Tel:010-58717271,E-mail:dumeihong@beijinglab.com.cn
10.3969/j.issn.1004-4957.2017.11.020
O657;O734
A
1004-4957(2017)11-1409-08

