生物油模型物糠醛催化加氫試驗研究
蔣恩臣,史冬冬,王明峰,許細微, 李世博,張世軍
(華南農業大學 材料與能源學院,廣州 510642)
?
生物油模型物糠醛催化加氫試驗研究
蔣恩臣,史冬冬,王明峰,許細微, 李世博,張世軍
(華南農業大學 材料與能源學院,廣州 510642)
選取糠醛作為生物油催化提質的模型物,以Al2O3分子篩為催化劑載體,制備的活性物質分別為Ni-Fe、Ni-Cu和Ni-Ce3種雙金屬催化劑,研究了活性組分負載量、反應溫度和氫醛摩爾比對糠醛常壓下催化加氫效果的影響。結果表明:當催化劑為7.5%Ni-7.5%Cu/ Al2O3、反應溫度為200℃、氫醛摩爾比為5.0時,能達到最佳效果,糠醛的轉化率為 69.95%,糠醇的選擇性達到了96.26%。催化劑表征結果表明:活性物質在載體上分散效果較好,用后催化劑表面積炭主要為未降解的有機物或者其聚合物。
生物油; 糠醛; 雙金屬催化劑; 催化加氫
0 引言
生物質能是新能源和可再生能源的重要組成部分[1]。生物質具有可再生、低污染、分布廣泛等特點,生物質能轉化與利用是國內外的熱點研究領域。
生物油是由生物質熱解得到的棕黑色油狀液體,可作為傳統液體燃料的替代品。生物質油組成成分復雜,其中的醛類、酸類和酚類等物質是影響生物油不穩定并決定其燃燒性能的主要成分,是生物油提質過程中優先重整的對象。Stefan Czernik等[2]認為生物油熱解過程中物理化學變化和液體內部的化學反應決定了生物油的穩定性,這些過程導致了大分子化合物的形成,而這些大分子化合物在生物油作為燃料使用時是不利于燃燒反應的。由于生物質油組分復雜,通過簡單組分的催化反應來研究復雜組分的反應特性是試驗研究中普遍應用的方法[3-5]。
本文選用糠醛(分子式C5H4O2)作為生物油催化提質的模型物,開展了催化加氫試驗研究。糠醛分子結構中呋喃環上的環醚鍵和兩個雙鍵,可以發生氫化、氧化、縮合、硝化和氯化等反應;而糠醛分子中醛基中心的羰基是活潑基團,所以糠醛是制備大量衍生產品必不可少的原料[6]。目前,工業上常用的Cu-Cr催化劑具對糠醛催化制糠醇的反應有活性好、選擇性高等優點[7-8];但該催化劑中Cr為毒性物質,易對環境造成嚴重污染,因此研發新型的無Cr催化劑成為必然趨勢。
1 材料與方法
1.1 試驗材料
試驗所用糠醛、硝酸鎳來自天津市大茂化學試劑廠,糠醛純度≥99%,硝酸鎳純度≥98.0%;硝酸鐵、硝酸銅、硝酸鈰均購自天津市福晨化學試劑廠,硝酸鐵純度≥98.5%,硝酸銅、硝酸鈰純度≥99%。
1.2 試驗方法
1.2.1 催化劑制備
催化劑的制備采用浸漬法,按照活性組分的負載量,配置不同濃度的活性組分硝酸鹽溶液,然后將Al2O3分子篩浸漬于硝酸鹽溶液中。在功率為27kW的超聲波清洗裝置中進行超聲波處理1h,然后攪拌2h,隨后放置于室溫下浸漬干燥12h。試驗制備等含量的雙金屬催化劑,控制活性物質Ni-Fe、Ni-Cu和Ni-Ce在催化劑中的質量分數分別為2.5%、5%、7.5%、10%、12.5%,并以單一組分的負載量作為催化劑命名的標準。
1.2.2 催化劑表征
催化劑的SEM表征在荷蘭FEI公司的XL-30-ESEM型掃描電子顯微鏡上進行,工作電壓為20kV,放大倍數為1 500~10 000。
傅里葉紅外FT-IR表征實驗儀器為布魯克VERTEX70紅外光譜儀,表征條件為:選取1~2mg的樣品與干燥的溴化鉀(A.R.級)粉末(約100 mg,粒度200目)混合均勻,在瑪瑙研缽中研磨成細粉末,然后將細粉末裝入模具內,在壓片機上壓制成片測試。
1.2.3 試驗儀器及步驟
生物油模型物糠醛的加氫試驗裝置如圖1所示。試驗方法如下:糠醛經保溫套預熱后,通過蠕動泵輸送到預熱管進行氣化,氣態糠醛與輸入的氫氮氣體(氫氣濃度為10%)混合后進入催化加氫石英反應管中,石英反應管外徑26mm、內徑22mm。用石英棉將催化劑固定在石英管中間部位,在催化劑上端部分,加入松散的纖維石英棉,保證氣流均勻通過催化劑床層。石英管處在外端的部分用伴熱帶進行加熱保溫,防止生成物冷凝發生縮聚反應;生成物利用含乙醇的冰水混合物在蛇形冷凝管中冷卻收集;液體產物利用GC-MS分析產物組分。
1.2.4 轉化率和選擇性計算方法
糠醛轉化率利用公式為
(1)
式中M(reactant)in—反應物入口端的摩爾含量(mol/L);
M(reactant)out—反應物出口端的摩爾含量(mol/L)。
糠醇的選擇性公式為
(2)
式中Ci—產物i的選擇性;
MCi—產品i的摩爾含量;
ΣMCi—所用產物的摩爾含量。
2 試驗結果與分析
2.1 活性組分對糠醛催化加氫反應的影響
糠醛催化加氫試驗在常壓下進行,催化劑用量15g,載氣流速0.27L/min,進料速率0.1g/min,氫氣與糠醛的摩爾比為5,反應溫度為200℃。試驗所用催化劑為Ni-Cu/Al2O3、Ni-Fe/Al2O3和Ni-Ce/Al2O33種雙金屬催化劑,活性組分的質量分數分別為 2.5%、5%、7.5%、10%和12.5%時,考察催化劑金屬活性組分含量對其活性的影響。3種類型催化劑的活性組分負載量對糠醛催化加氫的影響如圖2所示。

(a) Ni/Cu催化劑

(b) Ni/Fe催化劑

(c) Ni/Ce催化劑
從圖2(a)中可以看出:隨著Ni-Cu的負載量的增加,糠醛的轉化率逐漸增加,當Ni-Cu負載量由2.5%增加到7.5%時,糠醛轉化率增長效果顯著;但Ni-Cu負載量超過 7.5%時,糠醛轉化率增加緩慢。這是由于Ni負載量在2.5%~7.5%范圍內時,Ni高度分散于載體γ- Al2O3表面,但隨著Ni負載量進一步提高,則會聚集成為微晶分散在載體表面[9]。在糠醛加氫反應中,載體Ni表現出一定的活性和較高的選擇性。而對另一載體Cu,當銅含量較低時,單位表面載體的活性中心數少,導致催化劑的活性不高。所以,當銅的負載量增加時,糠醛的轉化率逐漸增大;但當銅含量超過一定值時,雖然單位表面的活性中心數增加,但過量的銅使部分活性中心被覆蓋,導致催化劑的活性提高緩慢。因此,確定活性組分Ni- Cu 的負載量分別為 7.5%。糠醇的選擇性隨著Ni/Cu的負載量的增加,變化并不顯著。當Ni-Cu負載量由2.5%增加到7.5%時,糠醇的選擇性緩慢增加;當Ni-Cu負載量超過 7.5%時,糠醇的選擇性呈下降趨勢。這是因為載體Ni為良好的加氫催化劑,隨著Ni的負載量增加,Ni2+與糠醛的極性基團C=O存在較強的吸附作用,從而更有利糠醇的生成;但當Ni的負載量繼續增加時,糠醛的完全加氫產物四氫糠醇的選擇性略有增加。
從圖2(b)中可以看出:Ni- Fe / Al2O3催化劑對糠醛的催化轉化率較低,在5%~20%之間。隨著Ni- Fe負載量的增加,糠醛的轉化率緩慢增加,當Ni- Fe的負載量分別為7.5%時達到最大;之后,隨著負載量的增加轉化率又呈下降趨勢。隨著Ni負載量的增加,催化劑的活性亦相應地增加,在7.5%Ni-7.5%Fe/Al2O3催化劑上表現出最高的糠醇選擇性,活性物質Ni含量過高或過低均不利于糠醇的生成。這是由于催化劑表面活性物質負載量增加,催化劑表面上活性中心增多,致使糠醇發生進一步加氫反應,生成四氫糠醇,從而導致糠醇的選擇性有所下降。Fe 的負載量提高催化劑活性是因為催化劑比表面積增加,有了更多不飽和的 Ni 活性中心;Fe 的加入,使催化劑對糠醛的 C=O 鍵的吸附能力有所增強,有利于加氫反應的進行;金屬 Fe 對金屬 Ni 供給電子,使得Ni得到電子,進而利于 C=O 鍵的氫化作用[10]。
在糠醛氣相加氫反應中, Ni-Ce /Al2O3催化劑對糠醛轉化率偏低。從圖2(c)中可以看出:在Ni- Ce的負載量分別為5%時,糠醛的轉化率32%為最大值;隨著Ni- Ce的負載量的增加,糠醛的轉化率呈下降的趨勢。隨著催化劑活性物質負載含量的增加,催化劑的活性先上升后降低;而Ni- Ce催化劑對糠醇的選擇性較好,均在80%以上。當Ni- Ce的負載量分別為7.5%時,表現出對糠醇的最佳選擇性。隨著 Ce 含量的增加,催化劑活性先升高后降低,Ce2O3被當作 Lewis 酸,使得對糠醛中 C=O 有較好的極化作用,對催化劑有較強的吸附作用,因而Ce 的負載量提高了催化劑的活性;但當 Ce 的負載量增加到一定量后催化劑活性開始下降,是由于過量的 Ce2O3覆蓋了 Ni 的活性中心。同時發現,隨著反應的進行催化劑活性也有所下降,則是由于非晶結構向晶態結構的轉變以及催化劑比表面積的減少所致[11-12]。
圖3為糠醛加氫反應示意圖。糠醛首先進行醛基中的碳-氧雙鍵加氫,生成糠醇,這是因為糠醛分子中醛基的碳-氧雙鍵比呋喃環的碳-碳雙鍵鍵長短,因而更為活潑,所以在反應時容易實現加氫。糠醛的活性中心是羰基,與羰基碳原子直接相連的3個原子處于同一平面,試劑對平面構型進攻的阻礙較小,這是羰基具有較高反應活性的原因之一。當采用銅系催化劑時,由于催化劑加氫能力較弱,加氫反應主要發生呋喃環側鏈的羰基上,低溫環境生成糠醇,高溫環境生成 2-甲基呋喃。若采用鎳系催化劑,則同時在C=C 雙鍵和 C=O 雙鍵發生加氫反應,低溫環境生成的產物四氫糠醛,高溫環境生成 1, 5-戊二醇。由此可以看出,若想實現糠醛的選擇性加氫,選擇合適的催化劑和控制反應條件是十分重要的[9]。綜合上述試驗結果:催化加氫效果由大到小依次為7.5%Ni-Cu/Al2O3、7.5%Ni-Ce/Al2O3、7.5%Ni-Fe /Al2O3。

圖3 糠醛加氫反應示意圖
2.2 溫度對糠醛催化加氫反應的影響
試驗選用催化效果最好的7.5%Ni-7.5%Cu/Al2O3催化劑用于糠醛加氫制糠醇反應,反應溫度為150、175、200、225℃,氫氣與糠醛的摩爾比為5,其它條件固定不變,考察溫度對糠醛催化加氫的影響。試驗結果如圖4所示。
結果表明:糠醛轉化率隨反應溫度的升高逐漸增大,在反應溫度為 200℃時轉化率達到最大,繼續升高反應溫度,糠醛轉化率的增加效果并不明顯;糠醇選擇性隨反應溫度的升高先增大后減小,在反應溫度為 200℃時,糠醇選擇性達到最大值。由此可知,低溫時不利于糠醛加氫反應的充分進行,糠醛轉化率和糠醇選擇性均較低。這是因為在低溫條件下,糠醛和氫分子不能充分第被催化劑活性中心活化,不利于反應向正方向進行,而反應溫度高于200℃時,糠醛轉化率略有上升,而糠醇選擇性比200℃時下降了4.02%。糠醛加氫制糠醇的反應是放熱反應,且高溫會促使糠醛的進一步加氫,進而降低糠醇選擇性,因此反應溫度過高不利于反應的進行。綜上所述,糠醛催化加氫制糠醇的最佳反應溫度為200℃。
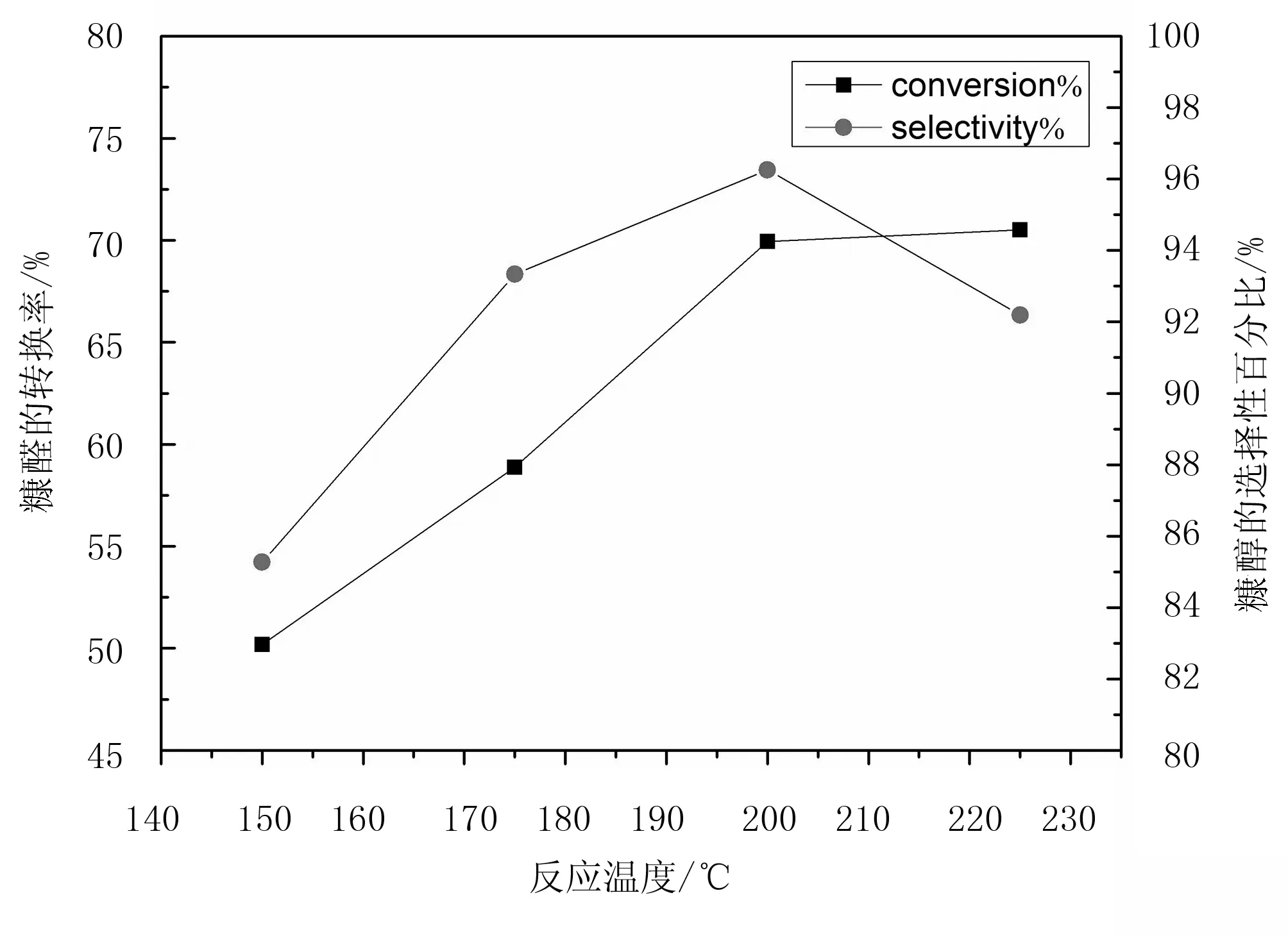
圖4 溫度對糠醛催化加氫反應的影響
2.3 氫醛摩爾比對糠醛催化加氫反應的影響
試驗所用催化劑為7.5%Ni-7.5%Cu/Al2O3,反應溫度為200℃,氫醛摩爾比為3、4、5、6、7,其它條件固定不變,考察氫醛摩爾比對糠醛催化加氫的影響。實驗結果如圖5所示。

圖5 氫醛摩爾比對糠醛催化加氫反應的影響
結果表明:隨著氫醛摩爾比的增加,糠醛的轉化率和選擇性迅速增大,在氫醛摩爾比為 5.0 時,糠醛的轉化率和糠醇的選擇性達到最優值;繼續增大氫醛摩爾比,糠醛的轉化率增加,但糠醇的選擇性呈下降趨勢。這是因為氫醛摩爾比過低或過高時,糠醛加氫的副反應增多導致糠醇選擇性較低,使得糠醇收率降低。實驗在固定床反應器上進行對催化劑活性的評價,在氫醛比小的情況下,由于氫氮混合氣攜帶糠醛的流速較低,導致氫氣與糠醛在催化劑表面的反應劇烈,放出大量的熱聚集在催化劑表面活性位,導致催化劑局部溫度升高燒結,使催化劑的活性逐漸減弱,甚至出現失活現象。當氫醛摩爾比為5.0時,溫度波動較小,反應條件溫和,糠醛與氫氣有充分的接觸時間進行反應,進而糠醛轉化率較高。隨著氫醛摩爾比的繼續增加,氫氮混合氣流量的增加,會帶走反應過程中產生的熱量,同時,氫氣、糠醛與催化劑的接觸時間縮短,反應不能充分進行,從而導致糠醇選擇性降低。
2.4 催化劑表征
糠醛催化加氫反應中,催化劑的催化加氫效果: Ni-Cu/Al2O3>Ni-Ce/ Al2O3>Ni-Fe / Al2O3。因此,本文選擇7.5%Ni-7.5%Cu/ Al2O3進行表征。
2.4.1 催化劑的掃描電鏡分析
7.5%Ni-7.5%Cu/ Al2O3催化劑的掃描電鏡譜圖如圖6所示。對比反應前催化劑表面形態結構及反應后催化劑表面積碳形貌可以看出:反應前,新鮮催化劑散亂的分布著微孔;凹凸不平,表面存在清晰可見的孔道。使用后催化劑表面形成了少量的松散、不規則的積碳,對孔道造成了一定堵塞,但仍留有部分空隙,反應物仍可進入催化劑內部。
2.4.2 催化劑的紅外分析
有機分子的紅外吸收光譜與其結構密切相關。催化劑的紅外分析圖譜如圖7所示。由圖7可知:波數在3 429.73處為-OH或分子間氫鍵的伸縮振動吸收峰;2 927、2 855、2 723cm-1處為烴類-CH2、-CH3結構中碳氫鍵的伸縮振動吸收峰; C=C伸縮振動的吸收峰在1 633cm-1處出現;1 483和1 384cm-1分別為-CH2、-CH3基團碳氫單鍵的彎曲振動吸收峰;仲醇中C-O的伸縮振動吸收峰在1 086cm-1處出現。Al2O3的特征峰在569cm-1處。Ni的特征吸收峰在582cm-1和789cm-1處。由此可見:使用后催化劑表面積炭主要為未降解的有機物或者其聚合物,該反應的焦炭前驅物中存在飽和烴類、醇、酮和烯烴等物質,產物中未檢測到芳香化合物。

(a) 7.5%Ni-7.5%Cu/Al2O3催化劑(新鮮)

(b) 7.5%Ni-7.5%Cu/Al2O3催化劑(用后)

(a) 7.5%Ni-7.5%Cu/ Al2O3催化劑(新鮮)

(b) 7.5%Ni-7.5%Cu/ Al2O3催化劑(用后)
3 結論
1)實驗結果表明:催化劑的催化加氫效果由大到小依次為:7.5%Ni-Cu/Al2O3、7.5%Ni-Ce/Al2O3、7.5%Ni-Fe /Al2O3。
2)考察溫度對糠醛催化加氫的影響。糠醛轉化率和糠醇選擇性在反應溫為200℃時達到最優值,分別為69.95%和 96.26%。
3)氫醛摩爾比對糠醛催化加氫的影響表明:隨著氫醛摩爾比的增加,糠醛的轉化率和選擇性迅速增大,在氫醛摩爾比為 5.0 時,糠醛的轉化率和糠醇的選擇性達到最優值;繼續增大氫醛摩爾比,糠醛的轉化率增加,但糠醇的選擇性有所下降。
4) 使用前后分子篩催化劑的FT-IR和SEM表征顯示:催化劑表面積炭主要為未降解的有機物或者其聚合物,該反應的焦炭前驅物中存在飽和烴類、醇、酮和烯烴等物質,產物中未檢測到芳香化合物。
[1] 劉榮厚.生物質能工程[M].北京:化學工業出版社, 2009:1-35.
[2] Marquevich M, Czernik S, Chornet E, et al.Hydrogen from biomass: steam reforming of model compounds of fast-pyrolysis oil[J].Energy & Fuels,1999,13(6):1160-1166.
[3] Mahfud F H, Ghijsen F, Heeres H J.Hydrogenation of fast pyrolyis oil and model compounds in a two-phaseaqueous organic system using homogeneous ruthenium catalysts[J].Journal of Molecular Catalysis A:Chemical,2007, 264(1-2):227-236.
[4] Sepulveda C, Leiva K, Garcia R. Hydrodeoxygenation of 2-methoxyphenol over MO2N catalysts supported on activated carbons[J].Catalysis Today, 2011, 172: 232-239.
[5] 魁彥萍,曹晶,周赫,等.生物油的成分分析及物性測定[J].化工生產與技術,2010(5): 52-54.
[6] 李憑力, 肖文平, 常賀英, 等.糠醛生產工藝的發展[J].林產工業,2006,33(2):13-16.
[7] Rao R, Dandekar A, Baker R T K, et al. Properties of Copper chromite catalysts in Hydrogenation Reactions[J].J Catal, 1997,171(2): 406-419.
[8] 趙修波, 蔣新, 周紅軍. 糠醛液相加氫催化劑的研制及工業應用[J].工業催化,2005,13(10): 47-50.
[9] Li H, Luo H, Zhuang L, et al.Liquid phase hydrogenation of furfural to furfuryl alcohol over the Fe-promoted Ni-B amorphous alloy catalysts[J].Journal of Molecular Catalysis a: Chemical, 2003,203(1):267-275.
[10] 劉琪英, 李勇, 蔡偉杰, 等.鎳基催化劑上糠醛選擇性加氫合成糠醇[J].分子催化, 2007,21(4):294-299.
[11] Li H, Zhang S, Luo H.A Ce-promoted Ni-B amorphous alloy catalyst (Ni-Ce-B) for liquid-phase furfural hydrogenation to furfural alcohol[J].Materials Letters, 2004,58(22): 2741-2746.
[12] Li Y, Xu X, Zhang P, et al.Highly selective Pd@ mpg-C 3 N 4 catalyst for phenol hydrogenation in aqueous phase[J].RSC Advances, 2013, 27 (3):10973-10982.
Experimental Research on Catalytic Hydrogenation of Bio-oil Model Compounds Furfural
Jiang Enchen, Shi Dongdong, Wang Mingfeng, Xu Xiwei, Li Shibo,Zhang Shijun
(Materials and Energy Engineering, South China Agricultural University, Guangzhou 510642,China)
Furfural was selected for bio-oil catalytic qualitative modelin this paper, used Al2O3molecular sieve as catalyst carrier, preparation of active substances were Ni-Fe, Ni-Cu and Ni-Ce three kinds of double metal catalyst, to study the effects of active component loading, reaction temperature and hydrogen ratio on catalytic hydrogenation of furfural aldehyde effect. The results showed that the best results can be achieved when the Al2O3was the carrier and the capacity of the active material of Ni-Cu was7.5%, and the reaction temperature was 200℃ and hydrogen aldehyde molar ratio was5. The yield of the target product furfuryl alcohol was 67.33% and the conversion rate was 69.95% and the selectivity is 96.26%. The results showed that: the active materials of the carrier were dispersed effectively . The main material of carbon deposit on the surface of catalysts are not degradation of organic matter or the polymer after reaction.
bio-oil; furfural ; bimetallic catalyst; catalytic hydrogenation
2016-05-23
科技部農業科技成果轉化資金項目(2014GB2E000048);土壤植物機器系統技術國家重點實驗室開放課題(2014-SKL-07)
蔣恩臣(1960-),男,黑龍江佳木斯人,教授,博士生導師,( E-mail)ecjiang@scau.edu.cn。
王明峰(1982-),男,遼寧鞍山人,講師,(E-mail)wangmingfeng@scau.edu.cn。
S216
A
1003-188X(2017)07-0218-06

