鞘氨醇激酶1對人骨肉瘤U2OS細胞增殖、凋亡的影響及機制
張萬賀,寶琪,杜春陽,郭義超
(1保定市蓮池區婦幼保健院,河北保定071000;2保定市骨科醫院;3河北醫科大學)
·基礎研究·
鞘氨醇激酶1對人骨肉瘤U2OS細胞增殖、凋亡的影響及機制
張萬賀1,寶琪2,杜春陽3,郭義超2
(1保定市蓮池區婦幼保健院,河北保定071000;2保定市骨科醫院;3河北醫科大學)
目的探討鞘氨醇激酶1(SphK1)對人骨肉瘤U2OS細胞增殖和凋亡的影響及機制。方法將體外培養的人骨肉瘤U2OS細胞隨機分為四組,轉染組、Vector組分別轉染SphK1 siRNA及對照siRNA,PF-543組在培養液中加入1 μmol/L SphK1特異性抑制劑PF-543,對照組常規培養。干預48 h時,采用Western blotting法檢測SphK1蛋白表達,明確siRNA轉染可在蛋白水平抑制骨肉瘤U2OS細胞SphK1高表達,且效果與其抑制劑PF-543相當。采用MTT法檢測各組細胞存活率,采用TUNEL法和流式細胞術檢測細胞凋亡率,采用Western blotting法檢測增殖細胞核抗原(PCNA)、細胞周期蛋白D1(Cyclin D1)、Bax、Bcl-2、Caspase-3及活化的Caspase-3(cleaved Caspase-3)蛋白表達。結果與對照組、Vector組比較,轉染組、PF-543組細胞存活率均下降,細胞凋亡率均增加,PCNA、Cyclin D1、Bcl-2蛋白表達均減低,Bax、Caspase-3及cleaved Caspase-3蛋白表達均增加,組間比較P均<0.05。結論SphK1基因可促進骨肉瘤細胞增殖、抑制細胞凋亡,調節凋亡及增殖相關因子表達可能是其作用機制。
骨肉瘤;鞘氨醇激酶1;細胞增殖;細胞凋亡;鞘氨醇激酶1特異性抑制劑
骨肉瘤是兒童及青少年常見的高度惡性骨組織原發腫瘤,年發病率為2/100萬~5/100萬,好發于血運豐富的長骨干骺端,具有早期肺轉移、復發率高等特點,患者預后較差[1~3]。鞘氨醇激酶1(SphK1)可將具有促細胞凋亡功能的鞘氨醇(Sph)磷酸化為具有促細胞存活功能的鞘氨醇1-磷酸(S1P),進而調控細胞的生長發育[4]。Zhou等[5]研究發現,microRNA-124(miRNA-124)可通過下調人骨肉瘤細胞SphK1表達抑制細胞增殖及侵襲;苯妥帝爾和阿霉素聯合應用能夠抑制骨肉瘤組織SphK1高表達,同時抑制骨肉瘤U2OS細胞生長發育[6]。上述研究結果提示,SphK1可能參與骨肉瘤的發病及其病理生理過程,但其作用機制尚不明確。2016年3月~2017年3月我們進行本研究,探討SphK1對人骨肉瘤U2OS細胞增殖、凋亡的影響及其機制。
1 材料與方法
1.1 材料 人骨肉瘤U2OS細胞購自南京凱基生物科技發展有限公司。SphK1 siRNA購自美國Santa Cruz公司。SphK1特異性抑制劑PF-543購自美國Selleck Chemicals公司。兔抗SphK1、Bcl-2、Caspase-3、活化的Caspase-3(cleaved Caspase-3)、增殖細胞核抗原(PCNA)、細胞周期蛋白D1(Cyclin D1)多克隆抗體及小鼠抗Bcl-2相關X蛋白(Bax)單克隆抗體均購自美國Promega公司。MTT購自Sigma公司。脂質體2000購自美國Invitrogen公司。辣根過氧化物酶標記羊抗兔IgG購自北京中杉金橋生物技術有限公司。聚偏二氟乙烯膜(PVDF)購自美國Milipore公司。TUNEL試劑盒購自美國Promega公司。
1.2 細胞培養 將U2OS細胞在DMEM完全培養基中37 ℃常規培養,當細胞融合75%~85%時,用無血清培養基培養24 h,進行以下研究。
1.3 細胞分組處理 將細胞隨機分為四組,其中轉染組、Vector組分別采用脂質體2000轉染SphK1 siRNA及對照siRNA,PF-543組在培養液中加入1 μmol/L SphK1特異性抑制劑PF-543,對照組常規培養。
1.4 相關指標觀察
1.4.1 細胞SphK1蛋白表達 采用Western blotting法檢測。將四組轉染48 h的細胞用冰冷PBS洗2遍,加入細胞裂解液200 μL,冰上放置1 h,4 ℃、12 000 r/min離心25 min,取上清液置于一干凈的EP管中,Lowry法測定總蛋白濃度。取細胞裂解蛋白50 μg,行SDS-PAGE電泳,將產物電轉移至PVDF膜;5%脫脂奶粉封閉PVDF膜2 h,加入SphK1抗體,4 ℃冰箱過夜;TBST液洗膜3次,加入辣根過氧化物酶標記的羊抗小鼠或兔抗體,37 ℃孵育1.5 h;TBST液洗膜后加ECL試劑,ODYSSEY遠紅外雙色熒光成像系統顯影(LLCOR Gene Company,USA)。LabWorks4.5軟件(UVP Company,USA)對蛋白條帶進行定量分析。
1.4.2 細胞增殖情況 采用MTT法檢測。將細胞(5×103個/mL)接種于96孔板,每孔定容為200 μL,分別加入200 μL(5 g/L)MTT,37 ℃培養箱中繼續培養4 h;棄培養液,每孔分別加入150 μL DMSO,待結晶完全溶解;采用酶標儀檢測各孔在490 nm波長處的吸光度(A)值,計算細胞存活率。細胞存活率=(處理組A值/對照組A值)×100%。
1.4.3 細胞凋亡率 ①采用TUNEL法檢測。將細胞(6×103個/mL)接種于8孔Leb-Tak腔室波片(美國Nalge Nunc公司)采用TUNEL法檢測陽性細胞。步驟嚴格按試劑盒說明書操作。陽性細胞核呈棕黃色。每孔至少計數500個細胞,計算細胞凋亡率。細胞凋亡率=(凋亡細胞數/總細胞數)×100%。②采用流式細胞術檢測。收集細胞培養液中的懸浮細胞及貼壁細胞,預冷PBS沖洗兩次,采用體積分數為70%的冰冷乙醇固定24 h,置于4 ℃冰箱;取出后PBS沖洗兩次,碘化丙啶4 ℃避光染色30 min,采用流式細胞儀檢測凋亡細胞數,計算細胞凋亡率。
1.4.4 PCNA、Cyclin D1、Bax、Bcl-2、Caspase-3及cleaved Caspase-3蛋白表達 采用Western blotting法檢測。具體步驟參照1.4.1。
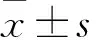
2 結果
2.1 各組SphK1蛋白表達比較 轉染組、Vector組、PF-543組、對照組SphK1蛋白相對表達量分別為0.16±0.03、0.91±0.02、0.32±0.01、0.98±0.02。轉染組、PF-543組SphK1蛋白相對表達量較對照組及Vector組明顯降低(P均<0.05),其余組間比較差異均無統計學意義(P均>0.05)。
2.2 各組細胞存活率比較 轉染組、Vector組、PF-543組、對照組細胞存活率分別為(45.17±0.21)%、(92.00±0.02)%、(53.05±0.26)%、(98.04±0.01)%。與對照組、Vector組比較,轉染組、PF-543組細胞存活率均下降(P均<0.01);其余組間比較差異均無統計學意義(P均>0.05)。
2.3 各組細胞凋亡率比較 流式細胞結果顯示,轉染組、Vector組、PF-543組、對照組細胞凋亡率分別為(54.81±0.15)%、(8.20±0.03)%、(47.31±0.16)%、(2.57±0.02)%。與對照組及Vector組比較,轉染組、PF-543組細胞凋亡率均升高(P均<0.01);其余組間比較差異均無統計學意義(P均>0.05)。
TUNEL結果顯示,轉染組、Vector組、PF-543組、對照組細胞凋亡率分別為(47.32±0.16)%、(4.35±0.05)%、(41.13±0.41)%、(4.82±0.06)%。與對照組和Vector組比較,轉染組、PF-543組細胞凋亡率均升高(P均<0.01);其余組間比較差異均無統計學意義(P均>0.05)。
2.4 各組PCNA、Cyclin D1、Bax、Bcl-2、Caspase-3及cleaved Caspase-3蛋白表達比較 與對照組和Vector組比較,轉染組、PF-543組PCNA、Cyclin D1、Bcl-2蛋白相對表達量均降低,Bax、Caspase-3及cleaved Caspase-3蛋白相對表達量均升高,組間比較P均<0.05。見表1。
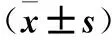
表1 各組細胞PCNA、Cyclin D1、Bax、Bcl-2、Caspase-3及 cleaved Caspase-3蛋白相對表達量比較
注:與對照組比較,*P<0.01;與Vector組比較,*P<0.01。
3 討論
80%的骨肉瘤患者在確診時已經發生轉移,手術及新輔助化療后5年生存率僅20%~30%[7,8]。骨肉瘤臨床治療效果不佳的重要原因是缺少特異性的分子治療靶點[9]。SphK1是維持細胞內鞘脂平衡的重要調節酶,具有SphK1和SphK2兩個亞型,雖然二者在結構域上高度保守,但在亞細胞定位、酶催化特性和組織表達譜等方面均顯著不同。SphK1是1-磷酸鞘氨醇(S1P)生成的限速酶,通過降低組織內神經酰胺和鞘氨醇含量,促進細胞增殖、抑制細胞凋亡[3]。研究發現,SphK1在腫瘤組織中表達明顯高于正常組織,如結腸癌、乳腺癌、前列腺癌、頭頸部鱗癌及甲狀腺癌等[10,11]。Bonhoure等[12]報道,特異性敲除人類白血病細胞系SphK1基因能夠抑制線粒體細胞色素C的釋放,進而促進細胞凋亡。Heffernan-Stroud等[13]報道,敲除SphK1基因可以抑制p53基因敲除小鼠特征性胸腺淋巴瘤的發生、發展。SphK1表達水平與腫瘤惡性程度和患者預后等臨床病理特征相關,因此SphK1被認為是生物體內重要的致癌因子。新近有報道稱,SphK1參與骨肉瘤的發病及其病理生理過程。彭晶等[4]研究發現,mi-124通過下調人骨肉瘤細胞SphK1表達抑制細胞的增殖及侵襲。苯妥帝爾和阿霉素聯合應用同樣能夠抑制骨肉瘤組織SphK1高表達,進而抑制骨肉瘤U2OS細胞的生長發育[5]。本研究采用短鏈microRNA和特異性抑制劑兩種手段敲低人骨肉瘤U2OS細胞SphK1表達,結果顯示,SphK1表達被抑制后U2OS細胞增殖受到明顯抑制,提示SphK1基因可能是骨肉瘤的靶基因。
腫瘤防治的關鍵是抑制腫瘤細胞增殖、促進腫瘤細胞凋亡。細胞凋亡是細胞接受內外源死亡信號刺激后發生的自殺性死亡,在調節生物生長發育和自身穩定方面發揮重要作用。目前臨床上大多數抗腫瘤藥物的作用機制是誘導腫瘤細胞凋亡。研究發現,SphK1在許多哺乳動物腫瘤細胞中發揮抗細胞凋亡作用[14]。有研究以病毒為載體,將野生型和突變型SphK1基因導入人胃癌細胞,結果顯示,過表達SphK1可抑制5-FU誘導的胃癌細胞凋亡[14];干擾乳腺癌MCF-7細胞SphK1基因表達可以抑制腫瘤細胞增殖和遷移能力,同時誘導細胞發生凋亡[15,16]。本研究發現,SphK1表達被抑制后骨肉瘤U2OS細胞凋亡率升高,凋亡細胞數明顯增加;同時細胞內重要的凋亡抑制基因Bcl-2蛋白表達明顯降低,促凋亡發生基因Caspase-3、cleaved Caspase-3、Bax蛋白表達明顯升高。提示在骨肉瘤發病過程中,SphK1基因通過調節凋亡相關因子表達抑制腫瘤細胞凋亡。PCAN及Cyclin D1是細胞增殖狀態的重要評價指標,其在腫瘤組織中的表達變化對疾病的發生、發展及患者預后具有關鍵性評估價值。本研究中SphK1表達被抑制后骨肉瘤U2OS細胞PCNA及Cyclin D1表達均受到明顯抑制,提示SphK1基因可能通過調控細胞增殖因子表達促進骨肉瘤細胞增殖。
綜上所述,SphK1基因具有促進骨肉瘤細胞增殖、抑制細胞凋亡的作用;調節凋亡及增殖相關因子表達可能是其作用機制。SphK1基因可能成為骨肉瘤的治療靶點。
[1] 閆抗,夏斯龍,王業華.丙戊酸鈉與順鉑聯合應用對人骨肉瘤細胞株U-2OS 增殖、凋亡的影響及其作用機制[J].山東醫藥,2016,56(3):11-13.
[2] Ren X, Shen Y, Zheng S, et al. miR-21 predicts poor prognosis in patients with osteosarcoma[J]. Br J Biomed Sci, 2016,73(4):158-162.
[3] Brown HK, Tellez-Gabriel M, Heymann D. Cancer stem cells in osteosarcoma[J]. Cancer Lett, 2017(386):189-195.
[4] 彭晶,蘭天,黃凱鵬,等.黃連素調節鞘氨醇激酶-1-磷酸鞘氨醇信號通路抗糖尿病小鼠腎損傷的研究[J].中國藥理學通報,2011,27(11):1544-1549.
[5] Zhou Y, Han Y, Zhang Z, et al. MicroRNA-124 upregulation inhibits proliferation and invasion of osteosarcoma cells by targeting sphingosine kinase 1[J]. Hum Cell, 2017,30(1):30-40.
[6] Yao C, Wu S, Li D, et al. Co-administration phenoxodiol with doxorubicin synergistically inhibit the activity of sphingosine kinase-1(SphK1), a potential oncogene of osteosarcoma, to suppress osteosarcoma cell growth both in vivo and in vitro[J]. Mol Oncol, 2012,6(4):392-404.
[7] Zhang N, Xie T, Xian M, et al. SIRT1 promotes metastasis of human osteosarcoma cells[J]. Oncotarget, 2016,7(48):79654-79669.
[8] Heymann MF, Brown HK, Heymann D. Drugs in early clinical development for the treatment of osteosarcoma[J]. Expert Opin Investig Drugs, 2016,25(11):1265-1280.
[9] Lettieri CK, Appel N, Labban N, et al. Progress and opportunities for immune therapeutics in osteosarcoma[J]. Immunotherapy, 2016,8(10):1233-1244.
[10] Shida D, Inoue S, Yoshida Y, et al. Sphingosine kinase 1 is upregulated with lysophosphatidic acid receptor 2 in human colorectal cancer[J]. World J Gastroenterol, 2016,22(8):2503-2511.
[11] Li J, Song Z, Wang Y, et al. Overexpression of SphK1 enhances cell proliferation and invasion in triple-negative breast cancer via the PI3K/AKT signaling pathway[J]. Tumour Biol, 2016,37(8):10587-10593.
[12] Bonhoure E, Lauret A, Barnes DJ, et al. Sphingosine kinase-1 is a downstream regulator of imatinib-induced apoptosis in chronic myeloid leukemia cells[J]. Leukemia, 2008,22(5):971-979.
[13] Heffernan-Stroud LA, Helke KL, Jenkins RW, et al. Defining a role for sphingosine kinase 1 in p53-dependent tumors[J]. Oncogene, 2012,31(9):1166-1175.
[14] Li PH, Wu JX, Zheng JN, et al. A sphingosine kinase-1 inhibitor, SKI-Ⅱ, induces growth inhibition and apoptosis in human gastric cancer cells[J]. Asian Pac J Cancer Prev, 2014,15(23):10381-10385.
[15] Sarkar S, Maceyka M, Hait NC, et al. Sphingosine kinase 1 is required for migration, proliferation and survival of MCF-7 human breast cancer cells[J]. Asian Pac FEBS Lett, 2005,579(24):5313-5317.
[16] Mahajan-Thakur S, Bien-M?ller S, Marx S, et al. Sphingosine 1-phosphate (S1P) signaling in glioblastoma multiforme-A systematic review[J]. Int J Mol Sci, 2017,18(11):pii: E2448.
河北省教育廳青年基金項目(QN2016018)。
寶琪(E-mail: 13731697766@163.com)
10.3969/j.issn.1002-266X.2017.48.008
R738.1
A
1002-266X(2017)48-0028-03
2017-06-26)

