低溫生物除鐵除錳工藝快速恢復試驗
王玉林,李 冬*,楊 航,曾輝平,張 杰, (.北京工業(yè)大學水質科學與水環(huán)境恢復工程北京市重點實驗室,北京 004;.哈爾濱工業(yè)大學城市水資源與水環(huán)境國家重點實驗室,黑龍江 哈爾濱 50090)
生物除錳固錳工藝因其高效、成本低、無需添加藥劑等優(yōu)勢在許多國家均有工程實踐應用的報道[1-6],蘭西縣水廠、哈爾濱松北水廠、沈陽開發(fā)區(qū)水廠、佳木斯江北水廠等的投產運行則是生物除鐵除錳技術在中國應用實踐的典型代表[7-9].然而生物除鐵除錳工藝運行過程中難免遭到破壞或停運,例如進水水質的變化,長期高濃度進水錳的巨大沖擊負荷導致生物濾層錳中毒,其除錳能力急劇下降甚至喪失[10-14];日常運行或反沖不當,亞鐵離子會溶解錳的生物氧化生成物,長此以往會破壞已成熟的生物除錳濾層結構[15-16];水廠日常運行中的濾池檢修、管道維護、設備保養(yǎng)、換井等意外情況的發(fā)生導致濾池停運時間較長等[9,15],生物除鐵除錳濾層一旦破壞后很難恢復[17],因此對于破壞失穩(wěn)后的生物除鐵除錳濾層“如何使其高效地恢復”是生物除鐵除錳技術工程應用上必須要解決的難題.然而,目前文獻中提到的對低溫生物除鐵除錳工藝進行恢復的研究還很少.濾層恢復與啟動的最大區(qū)別在于濾層結構的不同,啟動時的濾層為全新的濾料,而恢復時的濾層為包含鐵錳氧化物及失活的鐵錳氧化菌等失穩(wěn)的微生物系統(tǒng),其濾料粒徑等也發(fā)生了很大變化.所以如果采用與啟動相似的提升溫度[9]、接種高濃度菌液[18-20]、采取低反沖洗強度[21-22]的方式進行恢復,對于寒冷地區(qū)且鐵錳濃度較高的地下水及條件有限地區(qū)不切實際或很難達到.溫度是限制鐵錳氧化菌非常重要的指標[23].目前國外文獻報道水溫相對較高,大約 12~16.5℃[24],國內文獻報道中應用生物技術凈化含鐵錳水體的最低溫度一般8℃[25],其中黑龍江佳木斯市主要以含高鐵錳地下水作為供水水源冬季水溫低至 3~5℃,低溫會抑制微生物的活性[23],增加了生物濾層培養(yǎng)的難度,部分地區(qū)光培養(yǎng)時間就長達 4~9個月[9].顯然,對于凈化 3~5℃低溫地下水生物濾層破壞后的快速恢復將會是極大的挑戰(zhàn).
本文采用3根由于之前錳極限濃度探求試驗導致濾層錳中毒及長時間停運導致濾層除錳性能失效的生物濾柱(1#、2#、3#),1#采用不同流向恢復方式,2#采用不同鐵錳濃度常規(guī)恢復方式,3#采用添加無機碳恢復方式,并對恢復時間和恢復后穩(wěn)定性進行比較,以期得出最佳恢復方式,為低溫生物除鐵除錳工藝的工程應用提供技術支持.,
1 材料與方法
1.1 試驗裝置與方法
試驗在佳木斯市某地下水廠進行,試驗裝置采用 3根濾層除錳性能失效的有機玻璃濾柱,直徑為250mm,高為3000mm.濾柱內填充雙層濾料,上層為 300mm 厚顆粒無煙煤濾料,粒徑 1.5~2.5mm;下層為 1200mm 厚錳砂濾料,粒徑 0.8~1.0mm;以1~3mm的卵石作墊層,墊層厚300mm;沿濾柱高度每隔100mm設一個取樣口.試驗裝置如圖1所示.
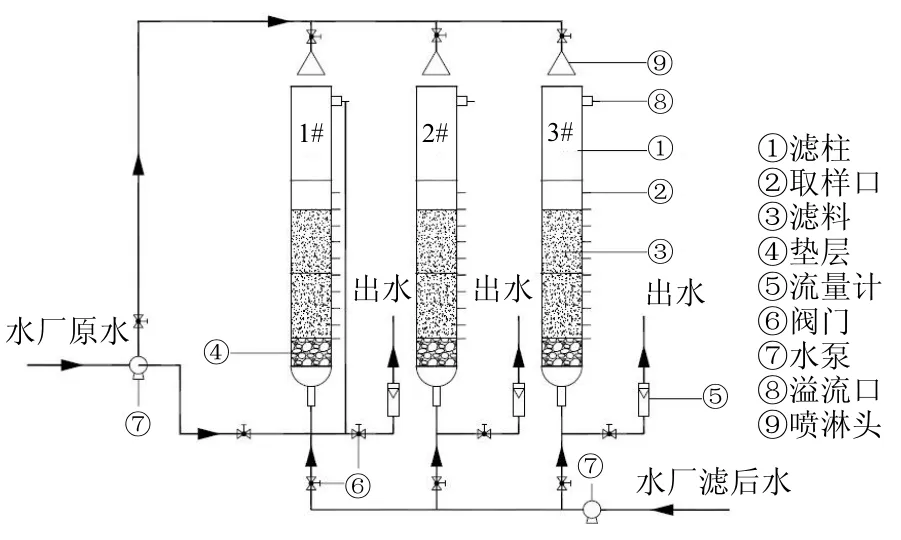
圖1 試驗裝置示意Fig.1 Schematic diagram of experimental equipment
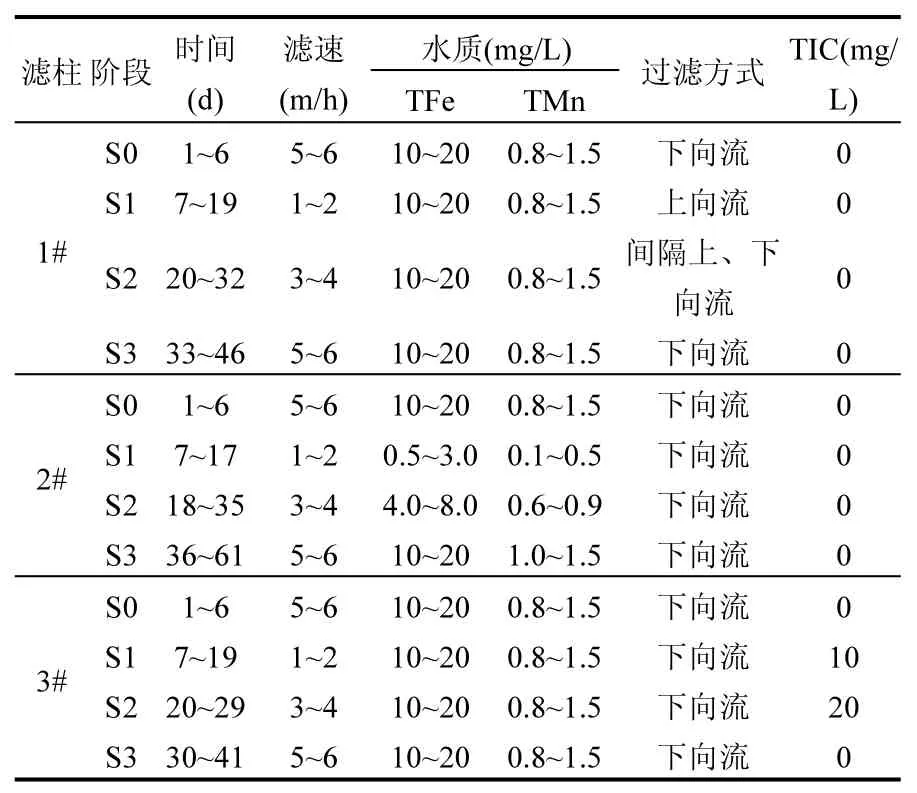
表1 各階段反應器參數變化Table 1 The parameter variations of each stage
試驗在水廠濾池間進行,室溫8~10℃.如表1所示,試驗分為S0、S1、S2、S3 4個階段.S0階段3根濾柱以正常濾速5~6m/h、原高濃度鐵錳水質、下向流方式運行1周左右.3根濾柱恢復開始都采用0.5~1m/h慢濾速運行,各濾柱濾速2m/h之前為 S1階段,濾速 2~4m/h為 S2階段,濾速4~6m/h為 S3階段.1#濾柱進水始終為原高濃度鐵錳水質,2#濾柱始終為下向流過濾,3#濾柱始終為下向流、原高濃度鐵錳水質過濾.S1階段1#濾柱采用上向流過濾,2#濾柱采用低濃度鐵錳水質過濾,3#濾柱采用添加10mg/L無機碳過濾;S2階段1#濾柱采用間隔上、下向流過濾,2#濾柱采用中濃度鐵錳水質過濾,3#濾柱采用添加 20mg/L無機碳過濾;S3階段 1#濾柱采用下向流過濾,2#濾柱采用原高鐵錳水質過濾,3#濾柱采用無添加無機碳過濾.各級濾速下待出水鐵、錳合格并穩(wěn)定 7~8d再逐級提升濾速,每次提升幅度不超過1m/h,同時隨時調整相應的反沖洗周期、強度、時間.每周測2次沿程總鐵、總錳的濃度,及時分析鐵、錳的沿程去除情況,通過沿程錳去除量和除錳性能分析以此反映錳氧化菌(MnOB)的活性和濾柱除錳穩(wěn)定性.各濾柱運行工況見表1.
1.2 試驗水質
試驗所用原低溫高濃度鐵錳地下水為佳木斯某水廠跌水曝氣后的水,試驗各階段水質及運行參數見表1.
1.3 檢測項目和方法
總鐵(TFe):二氮雜菲分光光度法;亞鐵(Fe2+):二氮雜菲分光光度法;總錳(TMn):原子吸收分光光度法;DO、pH:便攜式測定儀(WTW);TIC:非色散紅外吸收TOC測定儀[26].
為了加深對英語詞匯的理解,必須了解其所對應的文化背景,而許多單詞正是經由希臘羅馬神話才進入英語詞匯庫。神話所引申出來的詞匯可分為普通詞匯與專業(yè)術語,前者多與神、英雄、鬼怪等名稱有關,可利用其隱喻特征引申并拓展詞義。例如含義為長期艱辛的旅途odessay,這一單詞就是由神話中的著名英雄奧德修斯Oldysseus衍生而來,并且1月(January)和3月(March)也來自于神話故事中的兩面神janus和戰(zhàn)神mars。專業(yè)術語與自然科學有關,例如在天文學中許多星體的名稱都是由神話故事而來,故事中的戰(zhàn)神和愛與美之神分別對應的是火星Mars和金Venus。
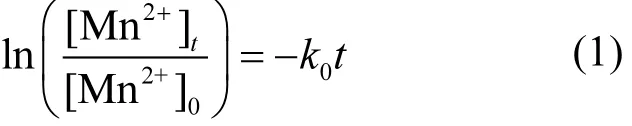
生物錳氧化動力方程為:式中:進水在生物濾層中的接觸氧化時間與公式左側成線性關系,k0為生物濾層的除錳能力,通過線性擬合可得知其值,其值越大,表明生物濾層的除錳能力越強.
2 結果與討論
2.1 濾柱恢復期TFe的去除效果
研究表明,因錳中毒及長時間停運造成失效的生物除錳濾柱,濾層內含有大量鐵錳氧化物及死去的鐵錳氧化菌(FeOB、MnOB),濾層堵塞嚴重[9,18,24],所以相對啟動新濾柱采用較弱的反沖洗強度而言[14,22,27],本試驗恢復初期宜采取較大的反沖洗強度和時間,從而徹底清潔濾層,為殘存FeOB、MnOB的生長創(chuàng)造良好條件.
各濾柱恢復前和恢復期對 TFe的去除效果如圖2所示,前5d為下向流、原水過濾,各濾柱恢復前出水 TFe濃度均較高,平均達 2.92mg/L.S1階段1#、3#濾柱開始出水TFe濃度較高,最高達到3.5mg/L左右,但分別僅經過5d和4d出水TFe濃度降至 0.3mg/L以下;2#濾柱由低鐵濃度開始恢復,出水TFe濃度低于0.3mg/L.S2、S3階段出水TFe濃度均合格.濾柱出水TFe僅幾天就合格,表明破壞濾層對TFe的去除影響較小.研究表明濾層因錳中毒及長時間停運造成失效的生物除錳濾柱濾料表面的鐵質活性濾膜遭受損壞[7,14],且FeOB數量很少,故而起始幾天出水TFe不合格;在pH中性域條件下, Fe2+很容易被空氣氧化生成新的FeOOH觸酶而將TFe去除[9,14,28],圖2中進水 TFe與 Fe2+濃度的差異表明原水中大部分 Fe2+離子在進入濾層之前已被氧化,剩余的Fe2+離子繼續(xù)在濾層內部被氧化去除.
2.2 濾柱恢復期TMn的去除效果
各濾柱恢復前和恢復期對TMn的去除效果如圖3所示,崩潰階段濾柱出水 TMn濃度很高,甚至高于進水錳濃度,濾層除錳性能很差.
由圖3可知,1#、3#濾柱S1階段都較長,均持續(xù)2周左右.1#濾柱第7~13d出水TMn濃度很高,甚至高于進水TMn濃度,分析認為一方面MnOB數量很少、活性較低;另一方面濾層長時間被高濃度鐵錳水浸泡,高濃度 Fe2+與高價錳離子發(fā)生氧化還原反應,置換出部分Mn2+[9,16],加上上向流的作用,與濾層中夾雜的鐵錳氧化物一起被帶出濾層.研究表明上向流過濾方式時三價鐵氧化物能夠到達濾層上部,反沖洗期間水頭損失較小,鐵泥可以輕易的被粉碎從而與反沖洗水一起排出濾層,增大了濾層的滲透空間和間隙,有助于細菌的廣泛分布并增加與過濾介質接觸的機會[29].所以第15d出水TMn已合格,在1~2m/h的低濾速下出水TMn濃度穩(wěn)定達標.3#濾柱恢復開始出水TMn一直呈下降趨勢,僅經過6d出水TMn合格,且濾速穩(wěn)步提升至2m/h.因為3#濾柱S1階段添加10mg/L無機碳,濾層殘存的MnOB處于饑餓狀態(tài),快速攝取碳源并除錳.
[10,17].而2#濾柱S1階段相對較短,在10d以內.因為其進水TMn僅為0.4~0.5mg/L,低濾速加上弱反沖強度,出水TMn濃度5d后合格且濾速穩(wěn)步提升.
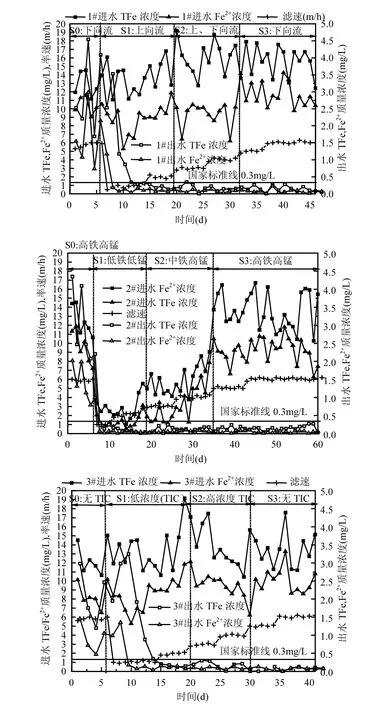
圖2 各濾柱進出水TFe/Fe2+濃度及濾速變化Fig.2 Variation of iron concentration and filtration rate of the biological filter
S2階段 1#、3#濾柱逐漸顯示出優(yōu)勢,其時間已略短于2#濾柱.經過S1階段的運行,各濾柱濾層已恢復為良好的除錳環(huán)境.所以 S2階段主要是MnOB增長和富集.由圖3可知,各濾柱出水 TMn基本合格.1#濾柱此階段既不失上向流的優(yōu)勢,又能為過渡到下向流做準備,出水 TMn濃度偶爾出現波動,但整體低于0.1mg/L.研究表明頻繁和高強度的反沖洗不利于MnOB的生長繁殖[7,9],而間隔上、下向流過濾方式一定程度上減弱了反沖洗強度,既為 MnOB增殖創(chuàng)造最大空間,又減少了其數量的流失.此階段用時不到2周.3#濾柱此階段 TMn去除較穩(wěn)定,基本低于0.1mg/L,分析認為至 S2階段,3#濾柱此階段無機碳濃度的進一步增加,為 MnOB提供了充足的碳源,極大地刺激了其活性和數量的增殖,此階段用時 10d左右.2#濾柱此階段進水 TMn濃度提升為 0.8mg/L左右.此階段開始出水 TMn濃度出現波動,達到 0.2mg/L,主要原因還是MnOB數量較少,對于進水 TMn負荷的提升一時難以適應,經過 4~5d的低濾速的運行,出水TMn濃度才逐漸合格.此階段用時 18d,約是 S1階段的2倍左右,比1#、3#濾柱長36%左右.
S3階段3個濾柱已都為下向流、原低溫高濃度鐵錳水質過濾.由圖3可知3#濾柱S3階段用時最短,其次是1#和2#濾柱.3#濾柱S3階段之所以用時最短,主要因為3#濾柱S2階段MnOB數量得以快速增值,MnOB為貧營養(yǎng)性細菌,在本地下水中的碳源微乎其微的水質下,營養(yǎng)的缺乏勢必會成為鐵錳氧化菌生長的限制因子[14,27],因此在無機碳的強化和刺激下,MnOB快速生長.但由圖3可知,1#、3#濾柱進入 S3階段后出水TMn濃度合格后又出現波動現象,除錳并不穩(wěn)定,分析認為這兩個濾柱進入S3階段后失去上向流和無機碳的作用,濾層重新進入下向流過濾模式、貧營養(yǎng)環(huán)境,MnOB生存空間被壓縮,此外1#、3#濾柱此時的濾層并沒有形成良好的生物除鐵錳體系,從而導致出水TMn濃度波動.2#濾柱S3階段進水 TMn濃度提升至 1.0~1.3mg/L,因為隨著濾速的緩慢提升,進水負荷的提高會導致濾層上部鐵泥的積累,反洗不當會導致濾層內部形成過濾水短路或水流通道,甚至會使濾層內部出現負壓導致氣體阻塞,最終破壞濾層的處理能力[7-9],所以本階段將反沖強度提升至 10~12L/(s·m2),較高的反沖強度能夠清洗掉濾層中細菌代謝積累的產物,有利于細菌在濾料表面的牢固附著,從而增強濾層的抗負荷沖擊能力[14].由圖3可知2#濾柱此階段只是初始幾天出水TMn不合格,但很快穩(wěn)定低于0.1mg/L.相比于1#、3#濾柱波動較小,主要因為 2#濾柱經過 S1、S2階段長達 35d的培養(yǎng),MnOB數量有了很大積累,活性上適應低溫水質,生物濾層形成了良好的除鐵錳體系,且隨著鐵錳含量的逐漸提升,生物濾層越來越穩(wěn)固.2#濾柱S3階段長達多于 20d,為前 2個階段總用時的80%左右.
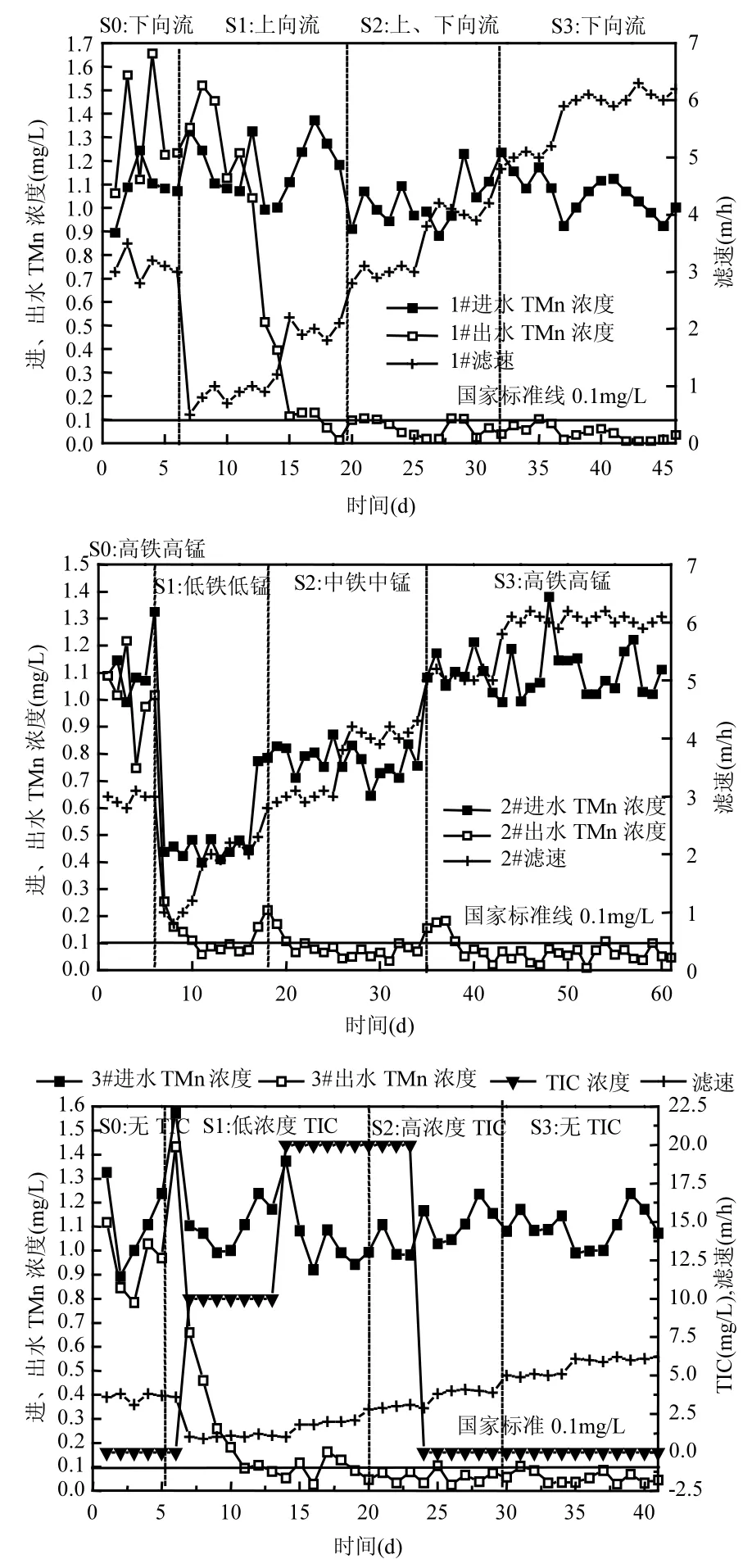
圖3 各濾柱進出水TMn濃度及濾速變化Fig.3 Variation of manganese concentration and filtration rate of the biological filter
綜上可知,以上 3種恢復方式都有較好的效果,以達到設計濾速6m/h且出水鐵錳穩(wěn)定合格視為濾柱恢復成功,1#、2#、3#濾柱分別僅經過40、54、35d恢復成功.
2.3 鐵錳沿程變化及除錳性能分析

圖4 濾層TMn、TFe沿程變化分析Fig.4 Analysis along filter bed of TMn、TFe
濾柱恢復期TFe沿程變化如圖4所示,3根濾柱進水TFe在濾層40cm深處去除率達80%以上,并且濾速在3m/h之前40cm處TFe濃度已降至 0.3mg/L以下.S1階段 1#濾柱上向流過濾,其TFe去除效果相較于 2#、3#濾柱較差.2#濾柱為低鐵恢復,其TFe去除效果非常好,3#濾柱起始恢復時TFe去除效果不好,但去除率也達到85%以上.這主要跟濾柱剛恢復運行濾層的結構、溫度、水質條件等有關.1#濾柱起始恢復時濾層中 TFe濃度出現先升高后降低的現象,歸因于上向流使得濾料顆粒之間的空隙較大,水流沖刷掉一部分濾料表面鐵氧化物的同時,削弱了濾層對鐵氧化物的截留能力[7,9];S2、S3階段各濾柱TFe去除效果較好,在濾層50cm處TFe去除率幾乎達到了100%.
濾柱恢復期TMn沿程變化如圖4所示,各濾柱各階段 TMn沿程去除差別較大.S1階段初始(3d、1m/h)各濾柱TMn沿程去除呈現同一現象:隨濾層深度的增加TMn濃度先升高后降低,濾層0.4m處TMn濃度高于進水TMn濃度0.2mg/L左右,盡管2#濾柱初始TMn只有0.4mg/L左右,但同樣表現出此現象,因為破壞的濾層 Fe2+與高價錳離子發(fā)生還原反應而溶出Mn2+,以及濾料表面錳氧化物的釋放[9],尤其1#濾柱S1階段上向流更甚.2#、3#濾柱S1階段初始運行TMn濃度隨濾層升高后再降低,出水盡管還不合格,但也只有0.2~0.3mg/L,而 1#濾柱初始運行 TMn濃度沿程逐漸升高,出水甚至高于進水0.4mg/L左右,可見上向流對去除錳的影響遠大于對去除鐵的影響.S1階段各濾柱單位時間單位濾層的錳去除量都很低,出水錳不合格.由圖4可知,2#、3#濾柱S1階段除錳帶主要在 0.4~0.8m 之間,1#濾柱在0.4~1.0m之間,3個濾柱S1階段0.4~0.8m的錳平均去除量分別為 0.517,0.248,0.832mg/L,可見 1#濾柱 S1階段除錳帶范圍略寬于 2#、3#濾柱,3#濾柱錳去除量略大于1#濾柱,因為2#濾柱錳濃度較低,3#濾柱無機碳強化了 MnOB氧化錳能力,而1#濾柱上向流過濾,雖然增大了MnOB與介質的接觸空間,但MnOB數量和活性有限,微生物作用微弱. S2階段各濾柱已重新適應低溫水質條件,MnOB在恢復活性的同時數量開始急劇增長.由圖4可知, 1#、2#濾柱S2階段在濾層1.0m處錳濃度均不合格,3#濾柱S2階段在濾層0.8m處也不合格,表明隨著濾速的提升 3個濾柱的除錳帶均下移.此時各濾柱除錳帶分別處于0.4~1.2m、0.4~ 1.1m、0.5~1.0m,S2 階段各濾柱0.6~1.0m的錳平均去除量分別為0.832、0.528、0.933mg/L. 1#濾柱除錳帶最寬,主要由于1#濾柱S2階段采取間隔上下向流過濾方式,水流流向的改變使得MnOB最大程度分布于全部濾料表面和間隙;3#濾柱除錳帶最窄,錳平均去除量最高,表明此階段 3#濾柱 MnOB的除錳能力最強.S2階段錳平均去除量明顯高于S1階段,表明盡管濾速提升,但各濾柱MnOB活性和數量都得到很大程度的提升.S3階段各濾柱的運行狀態(tài)、水質條件相同,由圖4可知,除錳帶進一步下移,在 6m/h濾速、低溫高濃度鐵錳進水水質下,各濾柱除錳帶基本都處于 0.6~1.3m 之間,甚至在濾層 1.3m處出水錳還不合格,只能依靠剩余的濾層進一步去除. 各濾柱S3階段0.8~1.2m濾層的錳平均去除量分別為 0.425、0.558、0.664mg/L,由此可知1#、3#濾柱錳平均去除量由于濾速的提升而降低,2#濾柱錳平均去除量則相對穩(wěn)定.
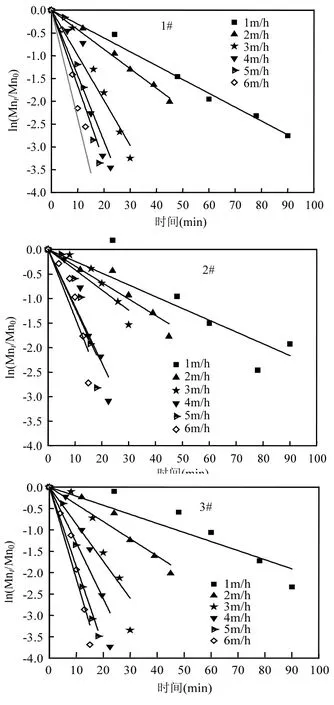
圖5 濾柱不同濾速下氧化除錳線性擬合Fig.5 Linear fitting of manganese oxidation under different filtration rates
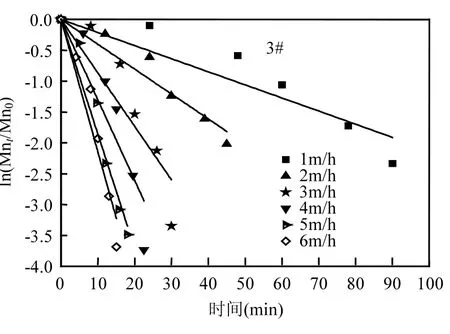
圖5 濾柱不同濾速下氧化除錳線性擬合Fig.5 Linear fitting of manganese oxidation under different filtration rates
對濾層進行沿程除錳動力學分析,將圖4中各濾速梯度下濾層的沿程錳去除量利用公式(1)進行擬合,其結果如圖5所示.圖4中濾層沿程錳濃度變化數據經擬合后,呈現良好的線性關系,表2中各R2值均大于0.9,表明式1能夠表征濾層的除錳性能.低溫條件下,1#、2#、3#濾柱在恢復過程中分別在1~6m/h濾速下穩(wěn)定合格時的k0值分別為:0.021、0.041、0.087、0.133、0.185、0.215;0.024、0.030、0.041、0.115、0.119、0.138; 0.030、0.042、0.098、0.140、0.166、0.238.由此可知 1#、3#濾柱隨著濾速的提升,k0逐漸增大,3m/h后的k0均值分別為0.178、0.181,除錳性能逐漸快速增強;而2#濾柱隨著濾速的提升k0變化出現拐點,3m/h之前k0變化不大,均值只有0.032,而3m/h之后k0同樣變化不大且逐漸趨于恒定,均值為 0.124,雖遠小于 1#、3#濾柱3m/h后的k0值,但除錳性能得以顯著提高.
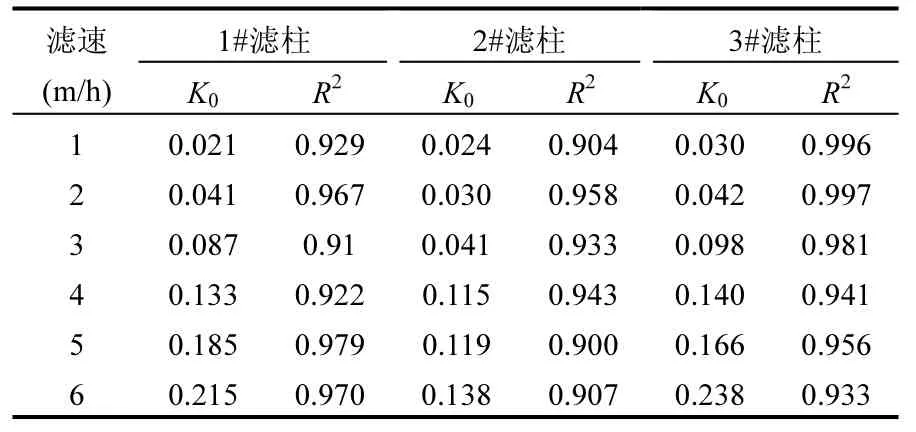
表2 各濾柱線性擬合參數值統(tǒng)計Table 2 The numerical simulation of the linear fitting parameters of each filter column
試驗表明 1#、3#濾柱的恢復方式能夠最大限度的縮短恢復時間和提高除錳性能,可能針對本地下水質除錳性能還有富余;而2#濾柱的恢復時間雖長于1#、3#濾柱,但2#濾柱升至3m/h后除錳性能較穩(wěn)定.
3 結論
3.1 采用不同流向過濾方式、改變進水鐵錳濃度、添加無機碳 3種方式均能夠有效縮短低溫(3~5℃)生物濾柱的恢復時間,其分別為 40、54和35d,相比2#濾柱常規(guī)恢復方式,1#、3#濾柱恢復時間分別縮短了26%、35%.
3.2 S1、S2階段表明上向流、適量無機碳能夠快速富集 MnOB,并提高除錳性能;S3階段表明不同流向過濾方式和添加無機碳的方式恢復的濾柱除錳性能較高,但除錳穩(wěn)定性不如采取改變進水鐵錳濃度的方式.
3.3 從恢復效果和經濟合理性綜合考量,最佳恢復方式建議為鐵錳濃度由低升高并在濾速提升至2~3m/h時添加無機碳的方式.
[1] Pacini V A, María Ingallinella A, Sanguinetti G. Removal of iron and manganese using biological roughing up flow filtration technology [J]. Water Research, 2005,39(18):4463-4475.
[2] Katsoyiannis I A, Zouboulis A I. Biological treatment of Mn(II)and Fe(II) containing groundwater: kinetic considerations and product characterization [J]. Water Research, 2004,38(7):1922-1932.
[3] Burger M S, Krentz C A, Mercer S S, et al. Manganese removal and occurrence of manganese oxidizing bacteria in full-scale biofilters [J]. Journal of Water Supply Research and Technology,2008,57(5):351-359.
[4] ?tembal T, Marki? M, Bri?ki F, et al. Rapid start-up of biofilters for removal of ammonium, iron and manganese from ground water. [J]. Journal of Water Supply Research and Technology,2004,53(7):509-518.
[5] Thapa C R, Suzuki I, Takezaki J, et al. Bacterial Diversity in Biological Filtration Plant for the Removal of Iron and Manganese from Groundwater [J]. Journal of Water and Environment Technology, 2013,11(1):33-47.
[6] Abu Hasan H, Sheikh Abdullah S R, Tan Kofli N, et al. Effective microbes for simultaneous bio-oxidation of ammonia andmanganese in biological aerated filter system [J]. Bioresource Technology, 2012,124(1):355-363.
[7] 張 杰,李 冬,楊 宏,等.生物固錳除錳機理與工程技術 [M].北京:中國建筑工業(yè)出版社, 2005:1-27.
[8] 李 冬,張 杰,陳立學,等.生物除鐵除錳在地下水處理廠的應用 [J]. 中國給水排水, 2004,20(12):85-88.
[9] 李 冬,曾輝平.高鐵錳地下水生物凈化技術 [M]. 北京:中國建筑工業(yè)出版社, 2015.
[10] Tang Y, Wu W, He Y, et al. Low-temperature domestication of an iron and manganese oxidizing bacteria [J]. Advanced Materials Research, 2012,374—377:826—830.
[11] D A Ratkowsky, R K Lowry, T A, et al. McMeekin, A. N. Stokes,R. E. Chandler, Model for bacterial culturegrowth rate throughout the entire biokinetic temperaturerange, [J]. Bacteriol, 1983,154:1222—1226.
[12] Ratkowsky D A, Olley J, T. A, et al. McMeekin, A. Ball,Relationship between temperature and growth rate ofbacterial cultures, [J]. Bacteriol, 1982,149:1—5.
[13] Cai Y A, Li D, Liang Y, et al. Operational parameters required for the start-up process of a biofilter to remove Fe, Mn, and NH3-N from low-temperature groundwater [J]. Desalination and Water Treatment, 2016,(57):3588-3596.
[14] 李 冬.生物除鐵除錳理論與工程應用技術研究 [D]. 北京:北京工業(yè)大學, 2004.
[15] 曾輝平.生物除鐵除錳濾池長期運行后除錳能力下降原因的探究 [D]. 哈爾濱:哈爾濱工業(yè)大學, 2007.
[16] 張 杰.生物濾層中Fe2+的作用及對除錳的影響 [J]. 中國給水排水, 2001,(9):14-16.
[17] Atta S Kh, Mojammed S A, Van Cleemput O, et al.Transformations of iron and manganese under controlled Eh,Eh-pH conditions and addition of organic matter r [J]. Soil Technology, 1996,9:223-237.
[18] 曾輝平.含高濃度鐵錳及氨氮的地下水生物凈化效能與工程應用研究 [D]. 哈爾濱:哈爾濱工業(yè)大學, 2010.
[19] Cahyani V R, Murase J, Ishibashi E, et al. Bacterialcommunities in manganese nodules in rice field subsoils: estimation using PCRDGGE and sequencing analyses [J]. Soil Sci. Plant Nutr,2007,53(5):575—584.
[20] Carmichael M J, Carmichael S K, Santelli C M, et al. Mn(II)-oxidizing bacteria are abundant and environmentally relevant members of ferromanganese deposits in caves of the upper Tennessee River Basin.Geomicrobiol [J]. Geomicrobiology Journal, 2013,30(9):779-800.
[21] Cai Y A, Li D, Liang Y, et al. Effective start-up biofiltration method for Fe, Mn, and ammonia removal and bacterial community analysis [J]. Bioresource Technology, 2015,176:149-155.
[22] 李 冬,路 健,等.低溫生物除鐵除錳工藝快速啟動與濾速的探求 [J]. 中國環(huán)境科學, 2016,36(1):82-86.
[23] Tekerlekopoulou A G, Pavlou S, Vayenas D V. Removal of ammonium, iron and manganese from potable water in biofiltration units: a review [J]. Journal of Chemical Technology and Biotechnology, 2013,88(5):751-773.
[24] 程慶峰.高鐵錳氨氮地下水凈化工藝優(yōu)化及菌群結構研究 [D].哈爾濱:哈爾濱工業(yè)大學, 2014.
[25] Hoyland V W, Knocke W R, Falkinham J O, et al. Effect of drinking water treatment process parameters on biological removal of manganese from surface water [J]. Water Research,2014,66:31-39.
[26] GB/T5750-2006 生活飲用水標準檢驗方法 [S].
[27] 蔡言安.含鐵錳氨氮地下水生物凈化試驗研究 [D]. 北京:北京工業(yè)大學, 2015.
[28] Huang S Q F M, et al. Fe (II) and Mn (II) removal from drilled well water: A case study from a biological treatment unit in Harbin [J]. Desalination, 2009,245(1-3):183-193.
[29] Yang H, Li D, Zhang J, et al. Design of biological filter for iron and manganese removal from water [J]. Journal of Environmental Science & Health Part A Toxic/hazardous Substances &Environmental Engineering, 2006,39(6):1447.

