鐵錳復合氧化膜同步去除地表水中氨氮和錳
白筱莉,黃廷林,張瑞峰,文 剛 (西安建筑科技大學環境與市政工程學院,陜西 西安 710055)
氨氮和錳的同步去除是飲用水處理中的重要課題,目前國內外關于飲用水中氨氮和錳同步去除的研究很多,但相關研究多在地下水條件下進行[1-3],針對地表水的研究開展較少.我國地表水中氨氮和錳污染超標的情況時有發生[4-5],因而探究地表水水源中氨氮和錳的同步去除具有重要意義.
地表水中現行的除錳方法多為強氧化劑預氧化,再通過混凝沉淀過濾去除,然而其藥劑投加量大,控制難度大[6],且過量的氧化劑會導致消毒副產物的增加[7],并對后續的生物法除氨氮產生不利影響[8];其次地表水錳污染的季節性、突發性[9]使得錳和氨氮的同步去除變得更加困難.
近年來在處理含鐵錳氨氮地下水的研究中發現,通過進水中投加高錳酸鉀,可在石英砂濾料表面形成一層鐵錳復合氧化膜(以下簡稱活性氧化膜),該活性氧化膜的活性成份為具有低結晶度和微細晶粒的水鈉錳礦,其培養成熟后,無需投加高錳酸鉀,對水中氨氮和錳具有高效、持續的催化氧化作用[10-12].
本研究利用表面已成功附著活性氧化膜的活性濾料,對地表水中氨氮和錳進行同步催化氧化去除.研究了地表水條件下該方法對水中氨氮和錳同步去除的效能及動力學過程,以探索地表水中氨氮和錳同步去除的新方法.
1 材料與方法
1.1 實驗裝置
實驗裝置如圖1所示,濾柱為內徑100mm的有機玻璃柱,內填表面附著活性氧化膜的濾料,濾料表面呈黑褐色,濾層厚度90cm,底部有20cm厚卵石承托層.

圖1 中試過濾系統Fig.1 Schematic of the pilot-scale filter system
1.2 實驗方法
1.2.1 氨氮和錳的去除效果及其影響因素 以地表水水廠沉淀池出水作為中試濾柱進水,向水中投加氯化銨和氯化錳調節進水氨氮和錳濃度,設定濾速為 7.0m/h,進水氨氮濃度為 0.6~2.5mg/L,錳濃度為 0.5~2.0mg/L,對濃度負荷的影響進行考察.
調節進水氨氮和錳濃度分別為1.6,0.8mg/L,控制濾速為4.0~16.0m/h,考察濾速對氨氮和錳去除效果的影響.
溫度影響實驗在冬季低溫條件下進行.濾柱進水首先進入反應盤管,盤管放置于水浴裝置內以調節進水溫度.設定濾速為 7m/h,溫度控制范圍為 7.3~21.3℃,調節進水氨氮濃度為 2.0mg/L,錳濃度為 0.8mg/L,考察溫度對氨氮和錳去除效果的影響.
1.2.2 氨氮和錳的去除動力學 檢測不同進水濃度條件下濾層沿程氨氮和錳濃度,并對上層0~50cm濾層處的濃度變化按擬一級反應動力學公式進行擬合:

積分可得:

濾速與去除氨氮和錳所需的濾層厚度采用傳質限制反應模型[13]進行擬合:

式中:CA為對應濾層處氨氮或錳的濃度,mg/L;CA0為初始濃度,mg/L;CAt為接觸時間為t時的濃度 mg/L;L為濾層厚度,m;ka為反應速率系數,s-1;kb為處理能力系數,h-1;t為接觸時間,s;U為濾速,m/s;其中kb取決于濾速和濾料性質.
1.3 分析項目和方法
實驗中檢測方法均采用標準方法[14].氨氮:納氏試劑分光光度法;硝氮:紫外分光光度法;亞硝氮:N-(1-萘基)-乙二胺光度法;錳:高碘酸鉀氧化光度法;溫度:水銀溫度計;溶解氧:雷磁 JPB-60TA便攜式溶解氧測定儀;pH值:雷磁PHS-3C pH計.
2 結果與討論
2.1 氨氮和錳的去除效果
與地下水相比,地表水存在低堿度、低 pH值以及冬季低溫的特點,這對氨氮和錳的去除是不利的,因此首先考察鐵錳復合氧化膜對地表水水質條件的適應性.實驗結果如圖2所示,當進水氨氮濃度為 1.3~1.7mg/L,錳濃度為 0.3~0.8mg/L,氨氮和錳的平均去除率分別為 94.6%和 90.5%,出水達標,說明鐵錳復合氧化膜濾料可以適應地表水水質特征,實現地表水中氨氮和錳的同步去除.
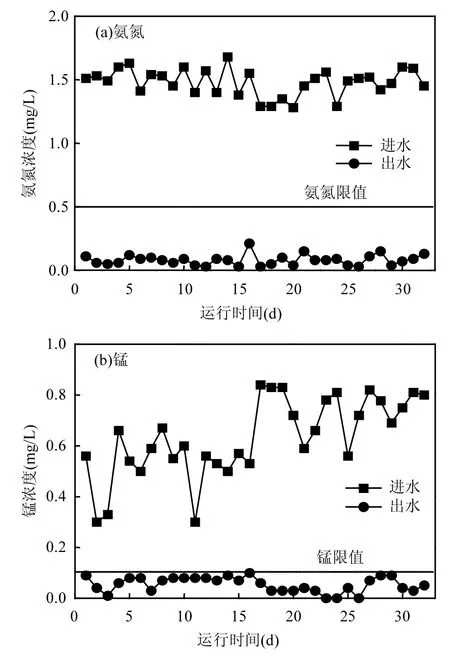
圖2 氨氮和錳的穩定去除效果Fig.2 Stable removal performance of ammonium and manganese
2.2 進水濃度的影響及動力學方程擬合
2.2.1 不同進水濃度下氨氮去除效果及動力學方程擬合 由圖3可看出,當進水氨氮濃度小于1.9mg/L時,出水氨氮濃度小于 0.2mg/L,且在上部濾層 50cm氨氮濃度均勻降至 0.6mg/L以下;當氨氮濃度升高至 2.3mg/L,出水氨氮迅速升高至接近 0.5mg/L,此時濾柱出水溶解氧濃度僅為0.9mg/L,出水氨氮濃度的迅速升高很可能是因為水中溶解氧不足所導致.

圖3 不同初始濃度下氨氮濃度隨濾層厚度的變化Fig.3 Ammonium concentration depth profiles at different influent concentrations
實驗中,氨氮主要在濾層上部 0~50cm 去除,因此對0~50cm濾層的氨氮濃度變化與接觸時間進行擬一級動力學擬合.結果如圖4所示,log(Ct/C0)與接觸時間 t呈很好的線性關系,其速率系數 ka因進水氨氮濃度的不同而分為明顯的高、中、低 3個層次.當進水氨氮濃度為 2.3~2.5mg/L,速率常數 ka1=1.3×10-3s-1,R2=0.974;當進水氨氮濃度為 1.0~1.3mg/L,速率常數 ka2=2.2×10-3s-1,R2=0.983;當進水氨氮濃度為0.6~0.7mg/L,速率常數ka3=4.5×10-3s-1,R2=0.982.隨著進水濃度升高,反應速率系數ka減小,可能原因是氨氮濃度過高時水中溶解氧濃度不足,對氨氮的去除產生了限制.氨氮氧化過程符合如下關系:
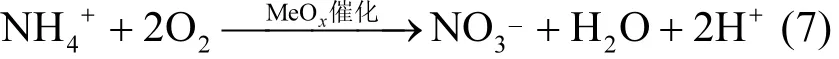
式中:MeOx表示活性氧化膜.理論上每氧化 1mg的氨氮消耗溶解氧4.57mg,氨氮與溶解氧之比為1:4.57.實驗期間進水溶解氧濃度約為 6.5mg/L,當進水氨氮濃度為 2.3~2.6mg/L時,其氨氮濃度與溶解氧之比為 1:2.65;當進水氨氮濃度為1.0~1.3mg/L時,該比值為1:5.65;當進水氨氮濃度為 0.6~0.7mg/L 時,該比值為 1:10.由此可知,在氨氮濃度較低(0.6~0.7mg/L)時,溶解氧濃度與氨氮濃度之比遠大于4.57,溶解氧處于過飽和態,氨氮氧化速率系數 ka3較大;在氨氮濃度較高 (2.3~2.6mg/L)時,溶解氧與氨氮濃度之比遠小于 4.57,水中溶解氧濃度不足,氨氮氧化受到限制,因而速率系數 k1較小.GUO等[11]在對地下水中氨氮去除過程的研究中也觀察到速率常數的分級現象,當氨氮濃度超過 2.4mg/L,其速率常數 ka較濃度0.5~1.5mg/L時明顯降低.
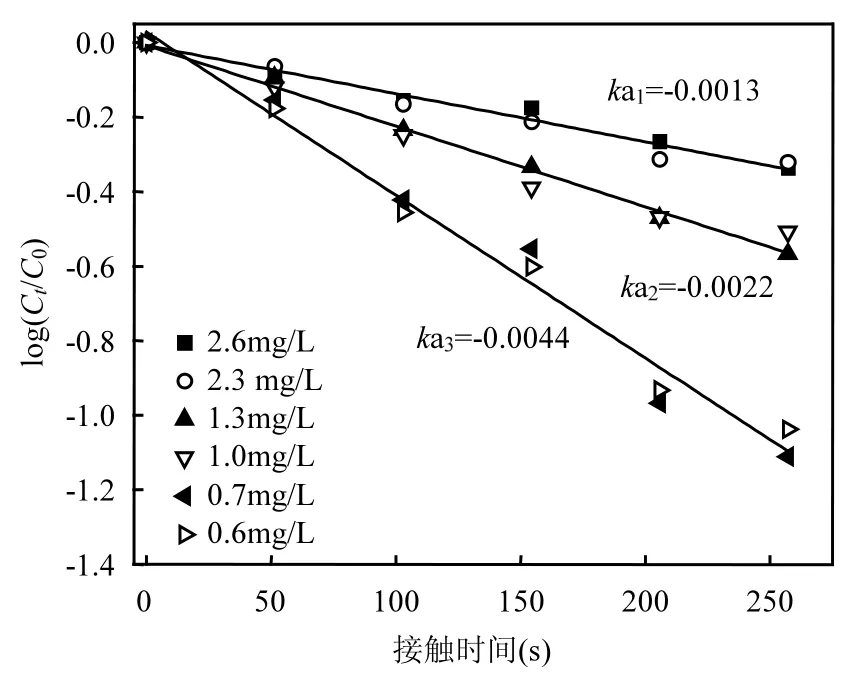
圖4 不同初始濃度下氨氮去除的擬一級動力學擬合曲線Fig.4 Fitting equations of first order kinetic model for ammonium oxidation at different influent concentrations
2.2.2 不同濃度下錳去除效果及其動力學方程擬合 實驗結果表明(圖5),當進水錳濃度從0.5mg/L逐步增加到1.6mg/L,濾池出水錳仍可達標.對上層 50cm 濾料去除效果進行擬合分析,如圖6所示,錳的去除過程符合擬一級動力學關系,其速率系數ka也隨進水濃度范圍的不同而變化.當進水錳濃度在 0.8~1.6mg/L范圍內時,速率系數 ka5=3.3×10-3s-1,R2=0.978.當進水錳濃度為0.5mg/L,其速率系數明顯減小,ka4=1.7×10-3s-1,R2=0.992;與氨氮的氧化過程不同,進水錳濃度較高時,錳反應速率系數 ka較大.這是因為,相比于氨氮的氧化過程相比,錳去除過程中消耗溶解氧較少,理論上氧化1mgMn2+僅消耗0.29mg的溶解氧,因而錳的氧化過程幾乎不受水中溶解氧濃度的限制.當進水錳濃度低至0.5mg/L時,反應速率系數 ka減小,原因可能是,濃度較低時,水中 Mn2+向濾料表面的擴散速率較慢,傳質過程限制了錳在低濃度條件下的去除速率.陰影部分 4個數據點未在擬合范圍內,這4個數據點處,反應速率系數ka有明顯減小的趨勢,其原因也可能是在此處錳濃度已經降低到比較小的值,傳質過程開始對錳等去除產生明顯的不利影響.?tembal等[13]認為氨氮和錳的去除過程均受到傳質過程的影響,傳質過程與濾速和污染物濃度有關,錳和氨氮去除動力學的差異在于它們對各影響因素的敏感度不同.

圖5 不同初始錳濃度下錳濃度隨濾層厚度的變化Fig.5 Manganese concentration depth profiles at different influent concentrations
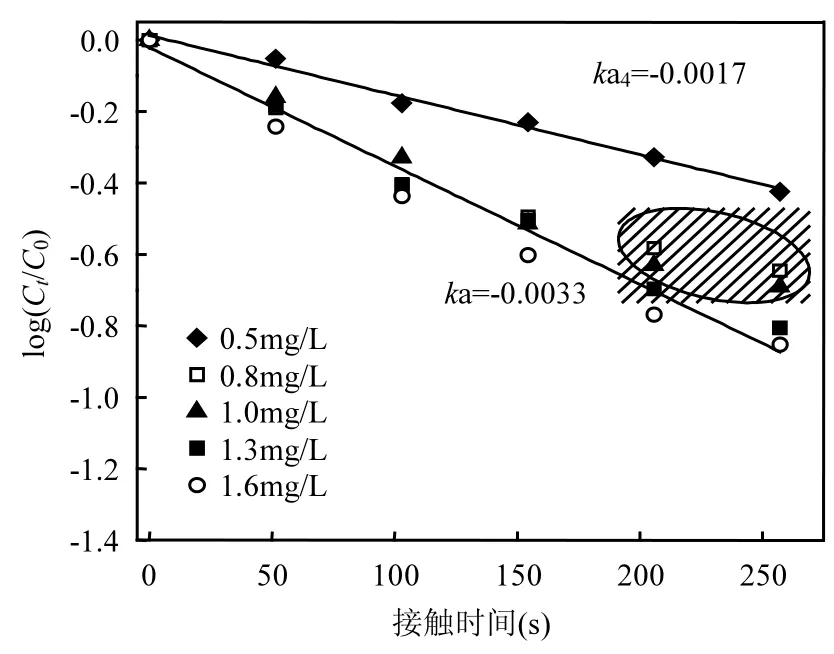
圖6 不同初始錳濃度下錳去除的擬動力學擬合曲線Fig.6 Fitting equations of first order kinetic model for manganese oxidation at different influent concentrations
2.3 濾速的影響
由圖7可見,隨著濾速的升高,氨氮和錳沿程變化曲線逐漸上移,濾池出水污染物達標所需濾層厚度不斷增加.濾速在 4.0~13.0m/h時,出水氨氮濃度均小于 0.5mg/L,出水錳濃度均小于0.1mg/L;當濾速達到 16.0m/h時,出水錳濃度為0.13mg/L,超過國家水質標準.

圖7 不同濾速下氨氮和錳的去除效果Fig.7 Removal performance of ammonium and manganese at different filtration rates
對濾料上層50cm氨氮和錳的體積氧化速率(單位時間單位體積濾料對氨氮和錳的去除量)進行計算,結果如表1所示.可以得出,濾速提高,單位時間單位體積濾料對氨氮和錳的去除量增加,這表明濾料對氨氮和錳的氧化為傳質限制型反應,其去除過程符合公式(5)和(6)所述模型[13].由公式(5)算出不同濾速所對應的 kb/Un值,并根據公式(6)對lg(kb/Un)和lgU進行擬合,得出n和kb值,其結果如表2所示.現假設進水氨氮濃度為1.5mg/L,錳濃度為0.8mg/L,錳和氨氮的去除率均為90%,由kb、n和公式(5)可得到濾速與去除相應污染物所需濾料厚度的關系,擬合結果如圖8所示,由圖可知,要使氨氮和錳的去除率達到90%,去除氨氮所需濾層厚度將大于去除錳所需的濾層厚度,其結果可以為活性氧化膜去除地表水中氨氮和錳工藝設計中濾層厚度的選擇提供理論依據.

表1 不同濾速下氨氮和錳的體積氧化速率Table 1 Volumetric oxidation rates of ammonium and manganese at different filtration rates
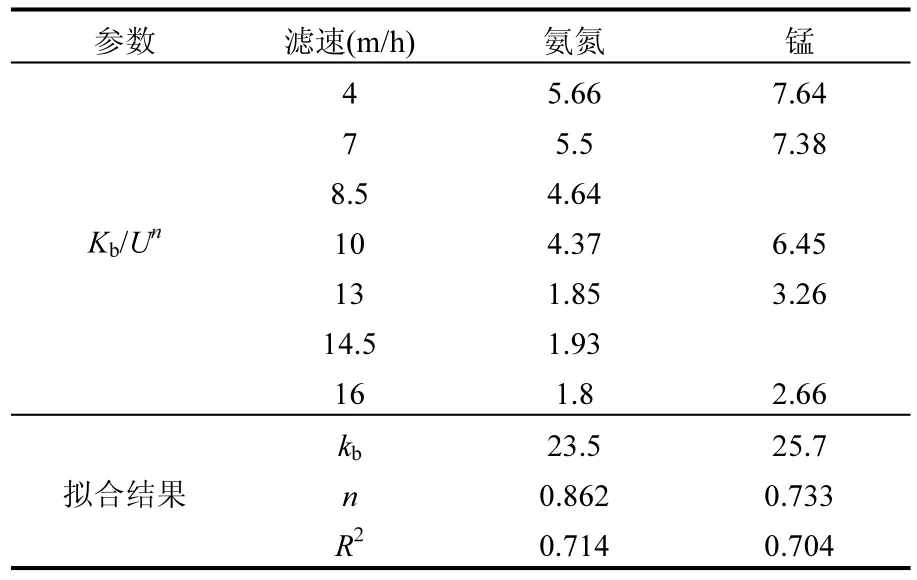
表2 不同濾速下kb/Un的實驗值以及kb,n擬合值Table 2 Review of the experimental data (kb/Un) and values of kb and n evaluated
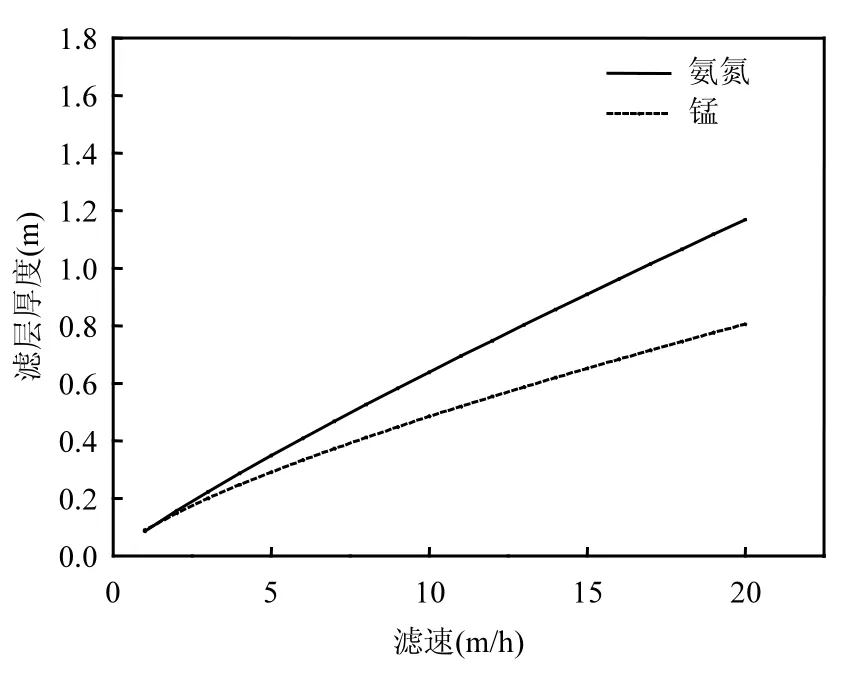
圖8 濾速與去除氨氮和錳所需濾層厚度的關系Fig.8 Required filter depth for the removal of ammonium and manganese at different filtration rates
2.4 溫度對氨氮和錳去除效果影響
由圖9(a)可知,溫度為 10.0~19.0℃時,進水氨氮平均濃度 2.0mg/L,出水氨氮小于 0.5mg/L;溫度降低至7.3℃時,出水氨氮濃度升高至0.7mg/L,濃度超標.對于普通生物濾池,Andersson 等[15]的研究表明,溫度為4~10℃時,氨氮去除率為10%~40%;Verstraete等[16]的研究也表明,生物濾池中硝化反應的速率在溫度低于 15℃時急劇下降,12℃時驟降至50%;Qin等[17]報道了通過培養馴化耐低溫優勢菌種構建生物活性炭濾池,溫度為8℃時對氨氮的去除量為(0.44±0.05) mg/L;Lee等[18]的研究表明生物砂濾池在溫度為9.1℃時最大氨氮去除負荷為 3.4g/(m3·h).本實驗中,溫度為7.3℃時,氨氮去除量為 1.3mg/L,去除負荷為10.0g/(m3·h),去除率為65%.這表明活性氧化膜對水中氨氮和錳的去除相對于普通生物法而言對低溫具有更好的適應性.
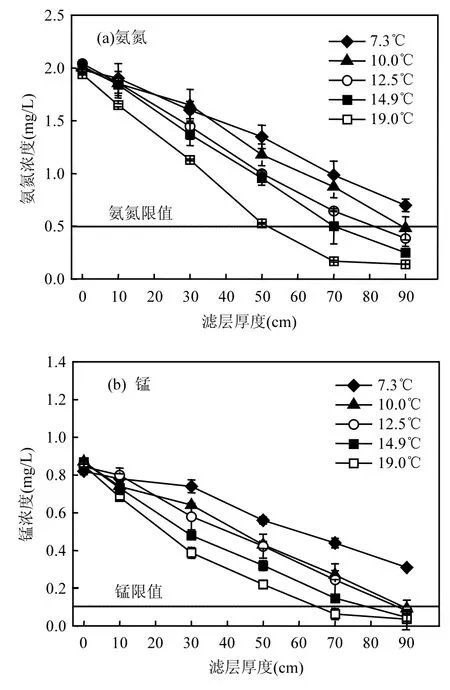
圖9 不同溫度下氨氮和錳的去除效果Fig.9 Removal performance of ammonium and manganese at different temperature
由圖9(b)可知,溫度為 10.0~19.0℃時,進水平均錳濃度為0.8mg/L,出水錳濃度小于0.1mg/L,溫度為 7.3℃時,出水錳濃度超標.鑒于地表水中錳污染多出現在夏秋季節[19],此時水溫相對較高,因而低溫并不是影響地表水錳去除的關鍵因素.同時,對于傳統的生物法而言,因為地表水中的錳超標具有季節性,在非超標季節水中錳含量低,難以在濾池中保持充足的生物量和生物活性以應對高錳季節的到來[19-20],而以鐵錳復合氧化膜濾料為基礎的催化氧化法可以很好的解決這一難題.
3 結論
3.1 鐵錳復合氧化膜可以有效地同步去除地表水中氨氮和錳,其污染物去除率可達90%以上.
3.2 濾柱上層 50cm濾層對氨氮和錳的去除均符合擬一級動力學關系,其動力學常數ka隨進水濃度的不同而分級,其中氨氮去除的反應動力學常數受進水氨氮濃度和溶解氧濃度之比影響較大,錳去除的動力學常數受其傳質過程影響較大.
3.3 去除氨氮和錳所需濾層厚度與濾速符合冪函數關系,要使進水氨氮和錳的去除率達到 90%以上,去除氨氮所需要的濾層厚度大于去除錳所需濾層厚度.
3.4 鐵錳復合氧化膜對地表水低溫條件具有較好的適應性,溫度為10℃時,進水氨氮2.0mg/L,錳0.9mg/L,濾速7.0m/h,出水可達標.
[1] 蔡言安,李 冬,曾輝平.生物濾池凈化含鐵錳高氨氮地下水試驗研究 [J]. 中國環境科學, 2014,34(8):1993-1997.
[2] Abu Hasan H, Sheikh Abdullah S R, Kamarudin S K, et al.Simultaneous NH4+-N and Mn2+removal from drinking water using a biological aerated filter system: Effects of different aeration rates [J]. Separation and Purification Technology, 2013,118(118):547-556.
[3] 布 浩,黃廷林,郭英明,等.石英砂表面活性濾膜去除地下水中氨氮的試驗研究 [J]. 中國環境科學, 2016,36(4):1045-1051.
[4] 劉樹元,鄭 晨,袁 琪.臺州長潭水庫鐵錳質量濃度變化特征及其成因分析 [J]. 環境科學, 2014,35(10):3702-3708.
[5] 黃 波,劉家春.長江經濟帶的錳"暴露"——長江干流錳污染狀況分析 [M]. 水利水電快報, 2015,36(10):33-35.
[6] 張和扳.淺談水庫水的錳砂除錳技術 [M]. 西南給排水, 2011,33(5):12-13.
[7] 劉 靜,郭海蓮,史 勇.受錳污染的地表水應急處理生產實踐[J]. 給水排水, 2007,33(1):23-24.
[8] 余 健,曾光明,何元春,等.湘江微污染飲用水源生物過濾試驗研究 [J]. 湖南大學學報(自科版), 2003,30(2):73-77.
[9] 陶岳云,倪木子,夏圣驥.地表水錳污染在水處理中去除研究進展 [J]. 水科學與工程技術, 2013,(5):62-65.
[10] 武俊檳,黃廷林,程 亞,等.催化氧化除鐵錳氨氮濾池快速啟動的影響因素 [J]. 中國環境科學, 2017,37(3):1003-1008.
[11] Guo Y, Huang T, Wen G, et al. The simultaneous removal of ammonium and manganese from groundwater by iron-manganese co-oxide filter film: The role of chemical catalytic oxidation for ammonium removal [J]. Chemical Engineering Journal, 2016,308:322-329.
[12] Cheng Y, Huang T, Sun Y, et al. Catalytic oxidation removal of ammonium from groundwater by manganese oxides filter:Performance and mechanisms [J]. Chemical Engineering Journal,2017,322:82-89.
[13] ?tembal T, Marki? M, Ribi?i? N, et al. Removal of ammonia, iron and manganese from groundwaters of northern Croatia—pilot plant studies [J]. Process Biochemistry, 2005,40(1):327-335.
[14] 國家環境保護總局.水和廢水監測分析方法.(第4版) [M]. 中國環境科學出版社, 2002.
[15] Andersson A, Laurent P, Kihn A, et al. Impact of temperature on nitrification in biological activated carbon (BAC) filters used for drinking water treatment [J]. Water Research, 2001,35(12):2923-2934.
[16] Verstraete W, Focht D D. Biochemical Ecology of Nitrification and Denitrification [J]. Advances in Microbial Ecology, 1977,1(6):135-214.
[17] Qin W, Li W G, Zhang D Y, et al. Ammonium removal of drinking water at low temperature by activated carbon filter biologically enhanced with heterotrophic nitrifying bacteria [J].Environmental Science and Pollution Research, 2016,23(5):4650-4659.
[18] Lee C O, Boe-Hansen R, Musovic S, et al. Effects of dynamic operating conditions on nitrification in biological rapid sand filters for drinking water treatment [J]. Water Research, 2014,64(7):226-236.
[19] Hoyland V W, Knoche W R, Pruden A, et al. Effect of drinking water treatment process parameters on biological removal of manganese from surface water [J]. Water Research, 2014,66(66):31-39.
[20] Katsoyiannis I A, Zouboulis A I. Biological treatment of Mn(II)and Fe(II) containing groundwater: kinetic considerations and product characterization [J]. Water Research, 2004,38(7):1922-1932.

