不同解磷菌群對復墾土壤磷素形態及油菜產量的影響
劉玲利,衛 迎,劉 洋,洪堅平
(山西農業大學 資源環境學院,山西 太谷 030801)
礦山開采活動對礦區土壤造成了嚴重破壞。礦區復墾土壤貧瘠,養分含量低,微生物數量少,活性低[1],而有益微生物可通過多方面的作用加速復墾進程,促進植物的生長發育[2]。磷是植物生長發育的必需營養元素,參與許多植物生理代謝過程,然而,缺磷是我國及世界農業生產中限制作物產量的一個重要因子,其原因主要為磷肥施入土壤后易被土壤固定,導致磷肥利用率低[3]。解磷微生物可以將土壤中難溶態磷轉換為有效磷[4-5],有研究表明,解磷微生物能夠提高磷肥利用率、土壤磷素的含量以及增加作物增產量[6-7]。梁利寶[8]研究表明,解磷細菌能夠促進石灰性土壤中磷素形態向易被作物吸收利用態轉化,同時可減緩其向緩效態、難溶態的轉化。目前,關于不同濃度解磷菌群對復墾土壤磷形態影響的研究較少。
本研究從石灰性土壤中篩選分離出不同種類解磷細菌和解磷真菌,進行油菜盆栽試驗,研究不同濃度下單施解磷細菌群、解磷真菌群以及混施解磷細菌群和真菌群對油菜土壤磷素形態、油菜產量和吸磷量的影響,以期為提高復墾土壤的磷素作物有效性、合理培肥復墾土壤、減少浪費與污染、提高磷肥利用率及有效指導農業生產提供理論依據。
1 材料和方法
1.1 試驗材料
1.1.1 供試土壤 試驗采用土壤為山西省長治市襄垣縣采煤塌陷區復墾1年的土壤,屬石灰性褐土,質地為中壤土。其有機質含量為2.19 g/kg,全氮含量為0.05 g/kg,全磷含量為0.37 g/kg,堿解氮含量為20.18 mg/kg,有效磷含量為0.85 g/kg,速效鉀含量為72.50 g/kg。
1.1.2 供試作物 供試油菜(Blassikakapestris)品種為四月蔓。
1.1.3 供試肥料 尿素:含氮460 g/kg;磷礦粉:含P2O5190 g/kg;硫酸鉀:含K2O 540 g/kg;有機肥:含有機質389 g/kg,含N2 15 %,含P2O510.6 g/kg,K2O 13.1 g/kg。
菌群:解磷細菌(假單胞細菌1、假單胞細菌2和拉恩氏菌,經驗證它們無拮抗反應,將這3株解磷細菌混合培養后經高密度發酵后制成液體菌劑),解磷真菌(黑曲霉和青霉,經驗證它們無拮抗反應,將這2株解磷細菌混合培養后經高密度發酵后制成液體菌劑)。
1.2 試驗方法
以解磷細菌、解磷真菌以及2種解磷菌群混施對復墾土壤進行處理,每一菌液設置C1(1 mL/盆)、C2(4 mL/盆)、C3(7 mL/盆)3個濃度,其中,混合菌液按1∶1進行配置,另外設置不施解磷菌群處理C0和不施肥對照處理CK,共11個處理,每個處理重復3次,共裝33盆。盆栽試驗用盆缽為15 cm×10 cm的塑料盆,土壤過2 mm篩后,裝盆,每盆裝風干土1.2 kg。除不施肥處理外,其余每盆都施入相同的基肥(尿素0.33 g,磷礦粉0.83 g,硫酸鉀0.14 g,有機肥10.00 g)。
1.3 測定項目及方法
采集土壤樣品自然風干,研磨后過1 mm篩,進行指標測定。其中,土壤有效磷含量、全磷含量參照鮑士旦[9]的方法進行測定,堿性磷酸酶活性、植物吸磷量參照李娜等[10]的方法進行測定,葉綠素含量的測定參照李合生等[11]的方法進行測定,油菜產量用電子秤直接稱量。
Hedley無機磷形態的測定方法:稱0.5 g過0.15 mm篩的細土于50 mL的離心管中,加蒸餾水30 mL,振蕩16 h;將取下的離心管在離心機上以轉速為10 000 r/min的速度離心10 min(溫度要設置在0 ℃下),在離心管中,分別吸取5,10 mL的上清液,置于2個比色管,編號待測,倒掉離心管中的剩余溶液后加入0.5 mol/L重碳酸鈉溶液30 mL,振蕩16 h;將取下的離心管在離心機上離心10 min,轉速為10 000 r/min(溫度要設置在0 ℃下)。在離心管中,分別吸取5,10 mL的上清液,置于2個比色管,編號待測,倒掉離心管中的剩余溶液后加入0.1 mol/L氫氧化鈉溶液30 mL,振蕩16 h;將取下的離心管在離心機上離心10 min,轉速為10 000 r/min(溫度要設置在0 ℃下),在離心管中,分別吸取5,10 mL的上清液,置于2個比色管,編號待測,倒掉離心管中的剩余溶液后加入1 mol/L的鹽酸溶液30 mL,振蕩16 h;將取下的離心管在離心機上離心10 min,轉速為10 000 r/min(溫度要設置在0 ℃下),在離心管中,分別吸取5,10 mL的上清液,置于2個比色管,編號待測,倒掉離心管中的剩余溶液,將其內土壤轉移至消煮管過夜;在消煮管中加入濃硫酸5 mL,120 °C消煮0.5 h后每20 min升溫20 ℃,直到300 ℃,取下試管,冷卻后搖勻,再次進行消煮,達到360 ℃取下試管,冷卻后加入0.5 mol/L的雙氧水繼續消煮0.5 h,重復直到消煮管中的土樣呈白色,液體清澈無色),結束消煮冷卻后,定容于100 mL容量瓶,搖勻過夜;吸取容量瓶中的上清液于比色管中,加3~5滴水和1滴0.5%磷硝基酚指示劑,用4 mol/L的氫氧化鈉和0.25 mol/L硫酸調節pH值,定容搖勻比色,測定殘渣態-P;吸取提取液10 mL轉移到50 mL比色管中,加入 0.9 mol/L硫酸3.6 mL,調節pH值,定容比色,分別測定H2O-Pi、NaHCO3-Pi、NaOH-Pi、HCl-Pi的含量。
1.4 數據分析
利用Excel、SPSS 18等軟件對試驗數據進行處理與統計分析。
2 結果與分析
2.1 不同解磷菌群處理對土壤有效磷含量、堿性磷酸酶活性及土壤全磷含量的影響
從表1可以看出,各處理土壤有效磷含量均高于CK,與不施解磷菌群處理相比,加入解磷菌群的土壤有效磷的含量均顯著增加,其中,增加最顯著的是解磷細菌群,增加了21.69%~50.42%;其次為解磷真菌群,增加了6.9%~16.19%;混合解磷菌群增加效果不明顯。當菌液濃度為4 mL/盆時,解磷細菌群與解磷真菌群處理下土壤有效磷含量最大,與不施解磷菌群處理相比差異顯著,且解磷細菌群與解磷真菌群之間差異顯著。
各施肥處理下,土壤堿性磷酸酶的活性均顯著高于CK,與不施解磷菌群處理相比,施入解磷細菌群土壤堿性磷酸酶活性增加了7.17%~25.45%,解磷真菌群增加了1.82%~20.00%,混合解磷菌群增加效果不明顯。當菌液濃度為4 mL/盆時解磷細菌群、解磷真菌群與混合解磷菌群處理下,堿性磷酸酶的活性含量最大,與不施解磷菌群處理之間差異均達顯著水平。各菌群處理在同一濃度下差異不顯著。
施入解磷細菌群和解磷真菌群能夠提高土壤全磷的含量,解磷細菌增加效果最好,與不施解磷菌群相比,解磷細菌處理提高了2.38%~9.52%;解磷真菌處理提高了2.38%。當菌液濃度為4 mL/盆時,解磷細菌群處理下土壤全磷的含量顯著高于低濃度和高濃度處理;解磷真菌群在各濃度處理下差異不顯著;混合菌群處理在1 mL/盆濃度下,土壤全磷的含量顯著高于其他處理。
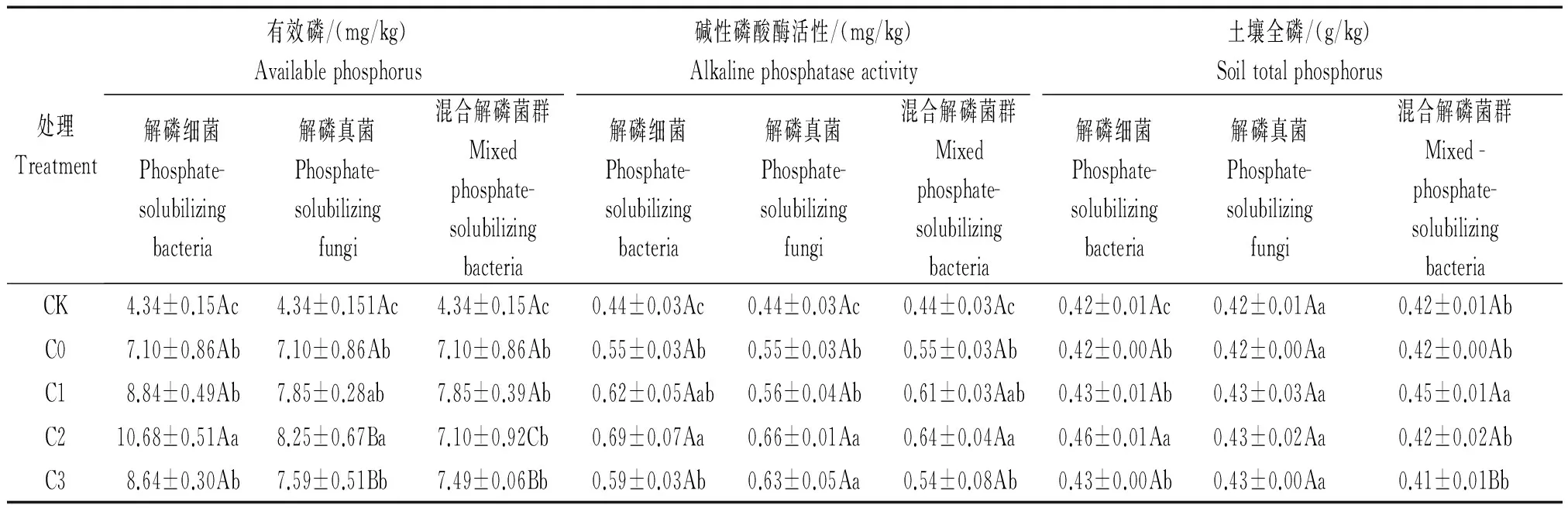
表1 不同解磷菌群處理對土壤有效磷含量、堿性磷酸酶活性以及土壤全磷含量的影響Tab.1 Effect of different phosphate-solubilizing bacteria on soil available phosphorus content,alkaline phosphatase activity and soil total phosphorus
注:表中不同小寫字母表示同一解磷菌群不同施肥濃度間差異顯著(P<0.05);不同大寫字母表示不同解磷菌群處理間差異顯著(P<0.05)。表2、圖1-5同。
Note: The lowercase letters in the table indicate that the difference of different fertilization rates was significant difference(P<0.05); Different capital letters indicate different solubilizing bacteria treatments were significant difference(P<0.05). The same as Tab.2,Fig.1-5.
2.2 不同解磷菌群處理對油菜產量、吸磷量和葉綠素的影響
從表2可以看出,施入解磷菌群能夠提高油菜的產量,作用效果最好的是解磷細菌群,比不施解磷菌群增加了4.13%~41.76%,在菌液濃度為4 mL/盆時,油菜產量達到最大,與不施解磷菌群處理間差異顯著;當菌液濃度為4 mL/盆時,解磷細菌群處理下油菜的產量顯著高于解磷真菌群處理,與混合解磷菌群處理差異不顯著;在7 mL/盆濃度處理下,解磷細菌群處理顯著高于解磷真菌群處理,與混合解磷菌群處理間差異不顯著。
不同處理與CK相比,油菜吸磷量均有所增加,與不施解磷菌群處理相比,增加效果最好的是解磷細菌群,增加了11.76%~44.12%;其次是解磷真菌群,增加了2.94%~29.41%;混合解磷菌群增加了11.76%~20.59%。當菌液濃度為4 mL/盆時,各種菌群處理下油菜吸磷量達到最大,解磷細菌群處理在該濃度下顯著高于1,7 mL/盆濃度處理。不同解磷菌群處理在同一菌液濃度下差異不顯著。李娜等[10]研究結果也表明,施入解磷細菌肥能夠提高油菜的吸磷量。
植物葉片中葉綠素含量與植物的產量密切相關,而磷元素的缺乏會影響植物葉綠素的合成,進而影響光合作用[12]。本研究中,不同菌群處理對油菜葉綠素含量的影響也不盡相同,其大小順序為解磷細菌群>解磷真菌群>混合菌群>不施解磷菌群處理>CK,與不施解磷菌群處理相比,解磷細菌群增加了3.60%~17.90%。在菌液濃度為4 mL/盆處理下時,油菜葉綠素含量達到最大,與CK、1 mL/盆之間差異顯著,與7 mL/盆之間差異不顯著。各菌群處理在同一濃度下差異不顯著。

表2 不同解磷菌群處理對油菜產量、吸磷量和葉綠素含量的影響Tab.2 Effect of different phosphate-solubilizing bacteria on rape yield, uptake of phosphorus and chlorophyll
2.3 不同解磷菌群處理對Hedley無機磷形態的影響
2.3.1 不同解磷菌群處理對土壤H2O-Pi的影響 從圖1可以看出,施入解磷細菌群能夠提高土壤H2O-Pi的含量,比不施解磷菌群處理提高1.35%~33.69%;且在4 mL/盆菌液濃度處理下達到最大,比CK增加9.85 mg/kg,比不施解磷菌群處理增加9.46 mg/kg,與其他處理差異顯著;解磷真菌群處理在4 mL/盆菌液濃度下與其他處理差異不顯著,混合菌群處理對提高土壤H2O-Pi的含量作用效果不明顯。不同菌群處理在同一濃度下差異不顯著。施入解磷菌群能夠提高土壤H2O-Pi的含量,可能是由于解磷菌能夠產生有機酸和磷酸酶,加速土壤難溶態磷的轉化[13]。陳芬等[14]研究也表明,施用菌肥可以增加復墾3年土壤的H2O-Pi含量。
2.3.2 不同解磷菌群處理對土壤NaHCO3-Pi含量的影響 從圖2可以看出,施入解磷菌群能夠提高土壤NaHCO3-Pi的含量,與不施解磷菌群處理相比,解磷細菌群增加了12.37%~52.43%,解磷真菌增加了8.6%~18.91%,混合解磷菌群增加了10.67%~17.42%。各菌群處理土壤NaHCO3-Pi含量均在菌液濃度為4 mL/盆時達到最大,解磷細菌群處理在該濃度下土壤NaHCO3-Pi含量較不施解磷菌群提高了15.79 mg/kg,與其他濃度處理間差異顯著,且與解磷真菌群、混合解磷菌群處理間差異顯著。土壤NaHCO3-Pi的含量多少依次為解磷細菌群>解磷真菌群>混合菌群>不施解磷菌群處理>CK。吳文麗等[15]研究也表明,施用解磷菌肥能夠提高復墾土壤中NaHCO3-Pi的含量。
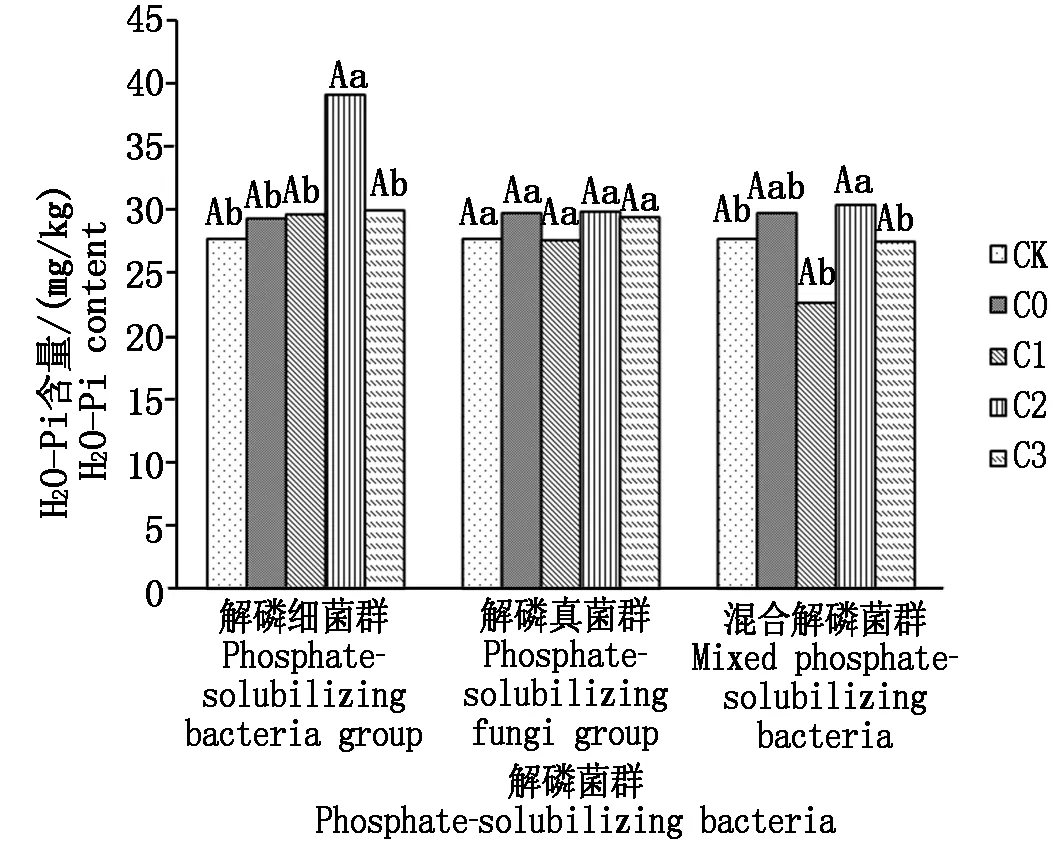
圖1 不同解磷菌群處理對土壤H2O-Pi含量的影響Fig.1 Effect of different phosphate-solubilizing bacteria on content of soil H2O-Pi
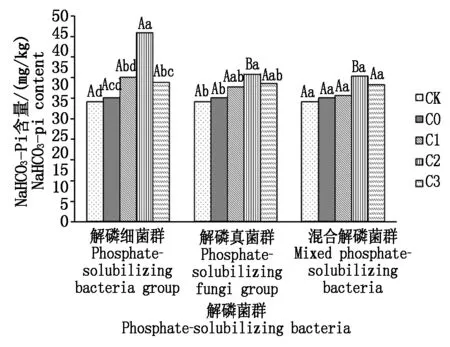
圖2 不同解磷菌群處理對NaHCO3-Pi含量的影響Fig.2 Effect of different phosphate-solubilizing bacteria on content of soil NaHCO3-Pi
2.3.3 不同解磷菌群處理對土壤NaOH-Pi的影響 從圖3可以看出,土壤NaOH-Pi的含量大小順序依次為解磷細菌群>解磷真菌群>不施解磷菌群處理>混合菌群>CK,解磷細菌群與解磷真菌群處理土壤NaOH-Pi的含量均在4 mL/盆濃度時達到最大,解磷細菌群處理土壤NaOH-Pi在該濃度下較不施解磷菌群處理提高7.83 mg/kg,且二者間差異顯著;解磷真菌群處理與不施解磷菌群處理間差異不顯著。解磷細菌群處理與解磷真菌群處理在各菌液濃度處理下均與混合解磷菌群處理間差異顯著,解磷細菌群處理與解磷真菌群處理間差異不顯著。
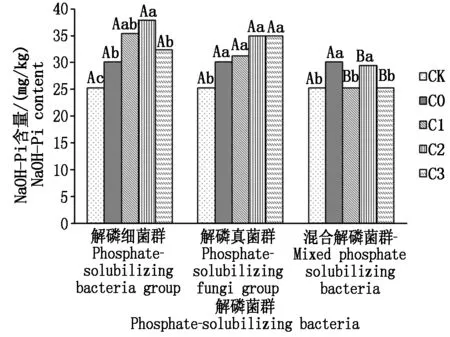
圖3 不同解磷菌群處理對土壤NaOH-Pi含量的影響Fig.3 Effect of different phosphate-solubilizing bacteria on content of soil NaOH-Pi
2.3.4 不同解磷菌群處理對土壤HCl-Pi含量的影響 從圖4可以看出,不同施肥處理下土壤HCl-Pi含量均低于CK,其大小依次為CK>解磷真菌群>不施解磷菌群處理>解磷細菌群。在菌液濃度為4 mL/盆時,解磷細菌群處理下土壤HCl-Pi含量最低,比CK降低了35.37 mg/kg,比不施解磷菌群處理降低了23.26 mg/kg,各菌群處理在同一濃度下差異不顯著。
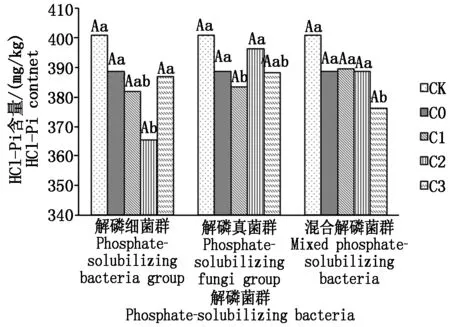
圖4 不同解磷菌群處理對土壤HCl-Pi含量的影響Fig.4 Effect of different phosphate-solubilizing bacteria on content of soil HCl-Pi
2.4 不同解磷菌群處理對土壤殘渣態-P的影響
從圖5可以看出,施入解磷菌群降低了土壤殘渣態磷的含量,其中,解磷細菌群殘渣態-P的含量最低,較不施解磷菌群處理降低了4.57%~16.19%,在菌液濃度為4 mL/盆時土壤殘渣態-P含量最低,較不施解磷菌群處理降低了47.02 mg/kg,且與其他濃度處理間差異顯著;在4 mL/盆濃度下,解磷細菌群處理土壤殘渣態-P含量顯著低于混合解磷菌群與解磷真菌群處理。各菌群處理在其他濃度下差異不顯著。

圖5 不同解磷菌群處理對土壤殘渣態-P含量的影響Fig.5 Effect of different phosphate-solubilizing bacteria on content of soil residual-P
3 結論與討論
相關研究表明,解磷微生物能夠將難溶態磷轉化為能夠被植物吸收利用的可溶性磷,其原因是解磷微生物產生的有機酸能夠溶解難溶態的無機磷酸鹽,一些解磷細菌在土壤缺磷條件下可分泌植酸、核酸以及磷脂酶類物質,通過酶解作用使有機磷轉化成可供植物吸收利用的有效磷[16-18]。郜春花等[19]研究表明,施入解磷菌,土壤磷酸酶含量與不接種相比增加了19.9%~50.3%,與空白處理相比,組合溶磷細菌肥處理土壤中磷酸酶含量增加了34.7%~41.9%,且差異顯著。白文娟等[20]研究表明,解磷細菌能夠提高苗期玉米葉綠素含量以及植株和根系中全磷的含量。李玉娥等[21]在苜蓿上接種解磷菌后,植株的株高、莖粗、干質量、干鮮比和葉莖比都比對照明顯增加。
本研究結果表明,施入解磷菌群能夠提高土壤有效磷含量、堿性磷酸酶活性以及土壤全磷的含量,改善土壤的營養環境,促進作物的吸收利用,從而提高作物的產量、吸磷量和葉綠素含量。其中,作用效果最好的是解磷細菌群,與不施解磷菌群處理相比,土壤有效磷、堿性磷酸酶活性、油菜的產量、吸磷量和葉綠素含量增加了21.69%~50.42%,7.17%~25.45%,4.13%~41.76%,11.76%~44.12%,3.6%~17.90%,且在菌液濃度為4 mL/盆處理下作用效果最顯著。
NaHCO3-Pi、NaOH-Pi是吸附在土壤粒子表面的活性磷和無機磷,易于被植物吸收和利用[14,22],而HCl-Pi、土壤殘渣態-P是難溶態磷,不易被作物吸收利用[23]。唐勇等[24]研究表明,微生物腐解植物殘體而產生的胡敏酸和富里酸能夠與復合磷酸鹽中的Ca2+、Fe3+和Al3+產生酸螯合,釋放出磷酸鹽。吳文麗等[15]研究發現,施用含有解磷菌的肥料,能夠提高復墾土壤H2O-Pi、NaHCO3-Pi、NaOH-Pi的含量,從而提高土壤磷的有效性。
本研究在油菜土壤中施入解磷菌群,與CK相比,施入解磷菌群能夠提高土壤中易被作物吸收和利用的H2O-Pi、NaHCO3-Pi、NaOH-Pi含量,降低土壤中HCl-Pi、殘渣態-P的含量。其中,作用效果最好的是中濃度4 mL/盆處理下的解磷細菌群,與不施解磷菌群處理相比,土壤中H2O-Pi、NaHCO3-Pi、NaOH-Pi含量分別提高了9.85,15.79,7.83 mg/kg;土壤中HCl-Pi、殘渣態-P的含量分別降低了23.26,47.02 mg/kg。施入解磷菌群能夠改善土壤的磷素營養狀況,提高磷素利用率。
[1] 錢奎梅,王麗萍,李 江.礦區復墾土壤的微生物活性變化[J].生態與農村環境學報, 2011,27(6):59-63.
[2] 杜慧平,劉利軍,閆雙堆.微生物對礦山復墾地土壤基質的改良作用[J].山西農業科學, 2011,39(1):43-46.
[3] 任海紅,劉學義,李貴全.大豆耐低磷脅迫研究進展[J].分子植物育種, 2008,6(2):316-322.
[4] 陳 謙,張維新,趙 海,等.生物有機肥中幾種功能微生物的研究及應用概況[J].應用與環境生物學報, 2010,16(2):294-303.
[5] 喬志偉,洪堅平,謝英荷,等.一株石灰性土壤強溶磷真菌的分離鑒定及溶磷特性[J].應用與環境生物學報, 2013,19(5):873-877.
[6] 蔣欣梅,夏秀華,于錫宏,等.微生物解磷茵肥對大棚茄子生長及土壤有效磷利用的影響[J].浙江大學學報:理學版, 2012,39(6):685-688.
[7] 郝 晶,洪堅平,劉 冰,等.不同解磷菌群對豌豆生長和產量影響的研究[J].作物雜志,2006,22(1):73-76.
[8] 梁利寶.解磷細菌對石灰性土壤磷形態的影響[J].山西農業大學學報:自然科學版,2008,28(4):454-457.
[9] 鮑士旦.土壤農化分析[M]. 3版.北京:中國農業出版社, 2000.
[10] 李 娜,喬志偉,洪堅平,等.溶磷混合菌肥對石灰性褐土磷素養分及解析特性的影響[J].應用與環境生物學報, 2014,20(4): 662-668.
[11] 李合生,孫 群,趙世杰,等.植物生理生化實驗原理和技術[M].北京:高等教育出版社,2000:167-169.
[12] 曹翠玲,毛圓輝,曹朋濤,等.低磷脅迫對豇豆幼苗葉片光合特性及根系生理特性的影響[J].植物營養與肥料學報,2010,16(6): 1373-1378.
[13] 胡曉峰,何元勝,岳 寧.不同溶磷菌生物有機肥對玉米苗期生長和土壤磷養分的影響[J].湖南農業科學,2012,42(11):74-77.
[14] 陳 芬,洪堅平,郝鮮俊,等.不同培肥處理對采煤塌陷地復墾土壤Hedley P形態的影響[J].山西農業科學,2012,40(3):243-245.
[15] 吳文麗,洪堅平,孟會生,等.連續施用解磷菌肥對復墾土壤磷酸酶和Hedley磷形態的影響[J].中國土壤與肥料,2016(4):59-64.
[16] 郝 晶,洪堅平,劉 冰,等.石灰性土壤中高效解磷細菌菌株的分離、篩選及組合[J].應用與環境生物學報,2006,12(3):404-408.
[17] Singh M, Bhui K, Singh R, et al. Tea polyphenols enhance cisplatin chemosensitivity in cervical cancer cells via induction of apoptosis[J]. Life Sciences,2013,93(1): 7-16.
[18] Rashid M, Khalil S, Ayub N. Organic acids production and phosphate solubilization by phosphate solubilizing microorganisms(PSM)underinvitroconditions[J]. Pakistan Journal of Biological Sciences,2004,7(2):187-196.
[19] 郜春花,盧朝東,張 強.解磷菌劑對作物生長和土壤磷素的影響[J].水土保持學報, 2006, 20(4): 54-56, 109.
[20] 白文娟,胡蓉蓉,章家恩,等.溶磷菌對玉米苗期生長和磷素吸收的影響[J].生態科學, 2014,33(3): 401-407.
[21] 李玉娥,姚 拓,榮良燕.溶磷菌溶磷和分泌IAA特性及對苜蓿生長的影響[J].草地學報, 2010, 18(1): 84-88.
[22] 賀麗娜,梁銀麗,熊亞梅,等.不同前茬對設施黃瓜產量和品質及土壤酶活性的影響[J].中國生態農業學報, 2009, 17(1): 24-28.
[23] 鐘傳青,黃為一.不同種類解磷微生物的溶磷效果及其磷酸酶活性的變化[J].土壤學報, 2005, 42(2): 286-294.
[24] 唐 勇,陸 玲,楊啟銀,等.解磷微生物及其應用的研究進展[J].天津農業科學, 2001, 7(2): 1-5.

