大孔樹脂純化酸漿果實多酚及其生物活性研究
王艷麗,許惠芳,郭瑜,王曉聞
(山西農業大學食品科學與工程學院,山西太谷030801)
酸漿 [Physalis alkekengi L.var.franchetii(Mast)Makino)]為一種茄科酸漿屬,野生性強且營養價值較豐富的水果蔬菜[1]。其中含有豐富的生物活性成分,有研究證明酸漿具有降血糖[2]、降血脂[3]、抗氧化[4]、抗癌[5]、抗炎[6]、抑菌[7]等生物活性,具有藥食兩用的價值。
酚類物質是植物的主要次生代謝產物之一,已被研究證實多酚類化合物具有抗氧化、抗腫瘤[8]、抗炎[9]、抗病毒、抗血栓形成和抗動脈硬化[10]等重要作用。
目前對酸漿的研究主要集中在苦素類[11]、多糖類[12-13]、皂苷類[6-7]、黃酮類[1]、生物堿類[14]等生物活性的分析。從現已發表的文章資料來看,國內外對酸漿果實中酚類化合物的研究較少,以及其在體外的抗氧化活性和酶抑制活性尚未見報道。
因此本實驗以乙醇為溶劑提取酸漿果實多酚,針對酸漿果實多酚的性質特點選擇合適的大孔樹脂進行初步純化,來探討酸漿果實多酚在體外的抗氧化活性以及對酶活性的抑制作用,為進一步研究酸漿果實多酚在體內對糖、脂代謝的影響提供一定的科學依據。
1 材料與方法
1.1 材料與儀器
1.1.1 材料
酸漿:原料采自山西省大同市陽高縣。
樹脂:ADS-17、AB-8、D101、NKA、NKA-9、NKAII、HP-20、XAD-16和HPD-826均購自滄州寶恩吸附材料科技有限公司,各樹脂的物理特性見表1。

表1 9種大孔吸附樹脂的物理特性Table 1 Physical characteristics of nine macroporous resins
1.1.2 試劑
Folin-Ciocalteu、沒食子酸(索萊寶試劑有限公司)、DPPH、Trolox、2,4,6-三吡啶基三嗪(2,4,6-Tris(2-pyridyl)-s-triazine,TPTZ)、Tris-HCI緩沖液、二甲基亞砜(Dimethyl sulfoxide,DMSO)、4-硝基苯基-β-D-吡喃葡萄糖苷(4-Nitrophenyl β-D-glucopyranoside,PNPG)、4-硝基苯基棕櫚酸酯(4-Nitrophenyl palmitate,PNPP)、胰脂肪酶、α-淀粉酶、α-葡萄糖苷酶均購自sigma公司。
1.1.3 儀器
JYZ-D51榨汁機:九陽股份有限公司;ST3100 pH計:奧豪斯儀器有限公司;ELx800酶標儀:美國寶特BIo-TeK公司;UV-1200紫外可見分光光度計:上海美譜達儀器有限公司;LD5-10低速離心機:北京雷勃爾離心機有限公司。
1.2 實驗方法
1.2.1 樣品的制備
將酸漿果實洗凈,去梗,用榨汁機破碎,根據實驗室前期的研究,按照一定條件對酸漿果實多酚進行提取。
1.2.2 總多酚含量的測定
采用Folin-Ciocalteu法測定[15]。得到吸光度值Y與沒食子酸標準溶液濃度X(μg/mL)之間的回歸方程為:Y=0.045 8X+0.012 1;R2=0.992 9。
1.2.3 大孔樹脂對酸漿果實多酚的初步純化
參考王若蘭[16]、馮進[17]和甘芝霖等[18]的方法。
1.2.3.1 大孔吸附樹脂對酸漿果實多酚的靜態吸附、解析實驗
稱取已處理好的各樹脂2.0 g于三角瓶中,加入30 mL一定濃度的酸漿果實多酚提取液,于恒溫振蕩器中(室溫,180 r/min)靜態吸附24 h,每間隔一定時間檢測上清液多酚含量,由公式(1)、(2)計算吸附量和吸附率。將靜態吸附24 h后的各樹脂進行過濾,用一定量的蒸餾水清洗樹脂,再過濾,將其轉入三角瓶中,加入40 mL 70%的乙醇溶液,于恒溫振蕩器中(室溫,180 r/min)靜態解析24 h,每間隔一定時間檢測上清液多酚含量,由公式(3)計算解析率。

式中:Q1為吸附量,mg/g;Q2為吸附率,%;P 為解析率,%;C0為吸附前酸漿果實多酚起始質量濃度,mg/mL;Cr為平衡質量濃度,mg/mL;V1為吸附溶液體積,mL;m為樹脂質量,g;C為解析后溶液中總酸漿果實多酚質量濃度,mg/mL;V2為解析液體積,mL。
酸漿果實多酚提取液濃度對吸附率的影響:選用處理好的理想型樹脂對不同濃度的樣液于恒溫振蕩器中(室溫,180 r/min)靜態吸附,24 h后檢測上清液多酚含量,由公式(2)計算吸附率。
酸漿果實多酚提取液pH值對吸附率的影響:選用處理好的理想型樹脂對不同pH值的樣液于恒溫振蕩器中(室溫,180 r/min)靜態吸附,24 h后檢測上清液多酚含量,由公式(2)計算吸附率 。
不同體積分數的乙醇對解析率的影響:將靜態吸附24 h后的樹脂進行過濾,用一定量的蒸餾水清洗樹脂至無提取液殘留,將其轉入三角瓶中,加入70%乙醇溶液40 mL,置于恒溫振蕩器中(室溫,180 r/min)靜態解析,24 h后檢測上清液多酚含量,由公式(3)計算解析率。
1.2.3.2 大孔吸附樹脂對酸漿果實多酚的動態吸附、解析實驗
將用預處理好的理想型大孔樹脂濕法裝柱,用去離子水平衡2 h,將適當濃度的酸漿果實多酚提取物用不同的流速上柱,每10 mL收集一管,檢測每管流出液的多酚濃度,當流出液的吸光值達到上樣液吸光值的1/10時,吸附達到飽和,停止上樣,用2 BV去離子水洗去雜質,再用80%的乙醇溶液以一定流速洗脫,以每10 mL收集一管,檢測每管流出液的多酚濃度。
1.2.4 酸漿果實多酚的抗氧化活性測定
1.2.4.1 酸漿果實多酚對DPPH·清除能力的測定
參考張瑞妮等[19]的方法稍作改進。各組溶液反應如下:
實驗組:40 μL 不同濃度的樣品液+160 μL 0.1 mmol/L DPPH 工作液(A1);空白組:40 μL 80%甲醇溶液+160 μL 0.1 mmol/L DPPH 工作液(A0);對照組:40 μL 不同濃度的樣品液+160 μL 80%甲醇溶液(A2)。
將以上3組溶液使用96孔板置于暗處反應30 min,于517 nm下測其吸光值,根據公式(4)計算出各待測樣品的清除率:

1.2.4.2 酸漿果實多酚對·OH基清除能力的測定
參考邢佳等[20]的方法稍作改進。各組溶液反應如下:
實驗組:50 μL不同濃度的樣品液+50 μL 6 mmol/L FeSO4溶液+50 μL 6 mmol/L H2O2溶液+50 μL 6 mmol/L水楊酸溶液(A1);空白組:50 μL 6 mmol/L FeSO4溶液+50 μL 6 mmol/L H2O2溶液+50 μL 6 mmol/L 水楊酸溶液+50 μL 80%甲醇溶液(A0);對照組:50 μL 不同濃度的樣品液+50 μL 6 mmol/L FeSO4溶液+50 μL 6 mmol/L水楊酸溶液+50 μL 80%甲醇溶液(A2)。
將以上3組溶液置于96孔板中,37℃水浴加熱30 min,于510 nm下測其吸光值,根據公式(5)計算出各待測樣品的清除率:

1.2.4.3 酸漿果實多酚對Fe2+還原能力的測定
參考王畢妮等[21]的方法稍作修改。
溶液配制:FRAP試劑為0.3 mol/L醋酸緩沖溶液(pH=3.6)∶10mol/LTPTZ(溶于 40mmol/L 鹽酸)∶20mmol/L三氯化鐵=10∶1∶1(體積比),現配現用。
標樣配制:用80%甲醇將1mmol/LTrolox標準溶液稀釋,濃度為 0.025、0.100、0.150、0.200、0.500、1 mmol/L,得到以吸光值與Trolox質量濃度之間的回歸方程為:Y=0.000 6X-0.012 3;R2=0.996 4。
實驗組:50 μL 不同濃度的樣品液+245 μLFRAP工作液。
對照組:50 μL不同濃度的各樣品液+245 μL80%甲醇溶液。
將以上兩組溶液置于96孔板中,37℃反應10min,于593 nm下測其吸光值。樣品對Fe2+還原能力以達到同樣吸光度所需的Trolox的量表示。
1.2.5 酸漿果實多酚的酶抑制活性測定
1.2.5.1 酸漿果實多酚對胰脂肪酶活性抑制率的測定
參考張麗娜[22]和Paulina Worsztynowicz等[23]的方法稍作改進。各組溶液反應如下:
實驗組:100μL不同濃度的樣品液+50μL1.2mg/mL PPL+50 μL PNPP(A1);空白組:50 μL 1.2 mg/mL PPL+50 μL PNPP+100 μL 50 mmol/L 緩沖液(A0);對照組:100μL不同濃度的樣品液+50μLPNPP+50μL50mmol/L緩沖液(A2)。
將溶液置于96孔板中,混勻后37℃反應5 min,于405 nm處測定其吸光值。根據公式(6)計算出各待測樣品的抑制率:

1.2.5.2 酸漿果實多酚對α-淀粉酶活性抑制率的測定
參考袁娟等[24]的方法稍作改進。各組溶液反應如下:
實驗組:50 μL 不同濃度的樣品液+25 μL 5 mg/mL α-淀粉酶溶液+50 μL 1% 底物+100 μLDNS 溶液(A1)。
空白組:25 μL 5 mg/mL α-淀粉酶溶液+50 μL 1%底物+100 μLDNS 溶液+50 μL 0.02 mol/L 緩沖液(A0)。
對照組:50 μL不同濃度的各樣品液+50 μL1%底物+100 μLDNS 溶液+50 μL 0.02 mol/L 緩沖液(A2)。
將不同濃度的各樣品液與α-淀粉酶溶液置于96孔板中,混勻后37℃反應20 min,隨后加入淀粉溶液,37℃再反應8 min,最后將DNS溶液加入其中,且立即沸水浴5 min以終止反應試驗。于540 nm處測定其吸光值。根據公式(7)計算出各待測樣品的抑制率:

1.2.5.3 酸漿果實多酚對α-葡萄糖苷酶活性抑制率的測定
參考李波等[25]的方法稍作改進。各組溶液反應如下:
實驗組:30μL不同濃度的樣品液+50μL0.1mg/mL α-葡萄糖苷酶溶液+50 μL 3 mmol/L PNPG 溶液+100 μL 0.1 mol/L Na2CO3溶液(A1);空白組:30 μL 0.1 mol/L 緩沖液+50 μL 0.1 mg/mL α-葡萄糖苷酶溶液+50 μL 3 mmol/L PNPG 溶液+100 μL 0.1 mol/L Na2CO3溶液(A0);對照組:30 μL 不同濃度的樣品液+50 μL 0.1 mol/L緩沖液+50 μL 3 mmol/L PNPG 溶液+100 μL 0.1 mol/L Na2CO3溶液(A2)。
將以上3組溶液的前3種試劑置于96孔板中,37℃水浴加熱10 min,最后加入Na2CO3溶液,于540 nm下測其吸光值,根據公式(8)計算出各待測樣品的抑制率:

2 結果與討論
2.1 大孔樹脂對酸漿果實多酚的初步純化
2.1.1 不同大孔樹脂對酸漿果實多酚的靜態吸附、解析性能
9種大孔樹脂對酸漿果實多酚的靜態吸附、解析結果見表2、圖1。

表2 9種大孔樹脂對酸漿果實多酚的靜態吸附與解析結果Table 2 Results of static adsorption and desorption rates of nine macroporous resins on Physalis fruit polyphenols
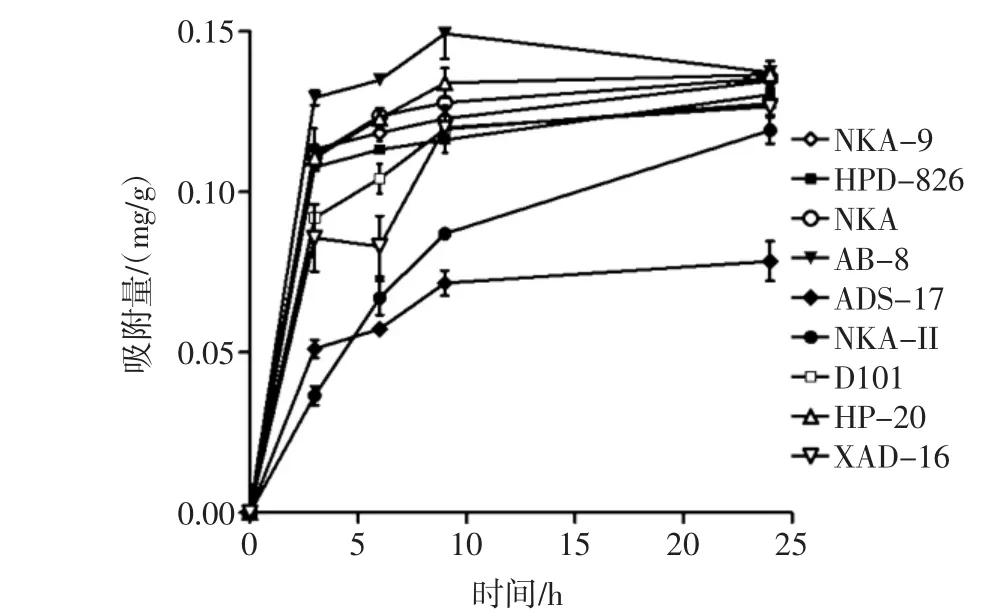
圖1 各樹脂對酸漿果實多酚的靜態吸附曲線Fig.1 Static adsorptive dynamics curves of different types of resins on Physalis fruit polyphenols
從表2可以看出,不同型號的大孔吸附樹脂對酸漿果實多酚的吸附和解析效果不同。9種樹脂中NKA-9、HPD-826、NKA、AB-8 和 HP-20 的吸附量較大,吸附量可達0.130 0 mg/mL以上,D101樹脂和XAD-16樹脂的吸附量次之,ADS-17樹脂和NKA-II樹脂的吸附量最小;吸附率最高的是HP-20樹脂,AB-8樹脂次之,二者都達到了75%以上,但是AB-8樹脂的解析率遠遠大于HP-20樹脂。
從圖1的靜態吸附曲線中可以看出,9種樹脂對酸漿果實多酚的吸附呈先快速上升后平穩型,隨著時間的增加各樹脂的吸附速率降低,各樹脂漸漸達到飽和。
綜上考慮,AB-8樹脂的吸附量、吸附率和解析率都較高,所以選用AB-8樹脂作為純化酸漿果實多酚的最優樹脂。
2.1.1.1 酸漿果實多酚提取液濃度、pH值對AB-8樹脂吸附率的影響
AB-8樹脂對不同濃度、pH值酸漿果實多酚提取液的吸附性能結果見圖2、圖3。

圖2 酸漿果實多酚濃度對AB-8樹脂吸附率的影響Fig.2 Effects of Physalis fruit polyphenols concentration on adsorption capacity of AB-8 resin

圖3 樣品液pH值對AB-8樹脂吸附率的影響Fig.3 Effects of pH value on adsorption capacity of AB-8 resin
從圖2可以看出,隨著樣品液質量濃度的增大,AB-8樹脂對樣品液的吸附率呈先上升后下降趨勢,當樣品液的濃度為0.3 mg/mL時,AB-8樹脂的吸附率達到最大,吸附飽和,而樣品液濃度在0.3 mg/mL~0.4 mg/mL范圍時,AB-8樹脂的吸附率逐漸下降,因為隨著樣品液質量濃度的增大,樣品液中雜質的量也增加,使得樹脂與樣品液中多酚物質的有效接觸面積下降,因此,選用樣品液質量濃度在0.3 mg/mL左右時較為適合。
AB-8樹脂對相同濃度不同pH值的樣品液進行吸附,從圖3中看出,不同樣品液pH值對AB-8樹脂的吸附率不同。當樣品液的pH值為4時,AB-8樹脂的吸附率達到最大,而pH值為3和7時,AB-8樹脂的吸附效果都較差。因此得出,酸漿果實多酚在中性和強酸性條件下不易被吸附,可能原因是在強酸和中性條件下酸漿果實多酚的性質發生了改變,從而導致樣液的吸附率下降。經試驗測得,原樣品液的pH值約為4.7,所以在進行后續實驗中選用樣品原液本身的pH值即可。
2.1.1.2 不同體積分數乙醇對AB-8樹脂解吸率的影響
將濃度大約為0.3 mg/mL的樣品液加入AB-8樹脂中進行吸附,待樹脂吸附飽和后,用適量的蒸餾水洗去未吸附的樣液和雜質,抽濾后向吸附飽和的AB-8樹脂中加入相同體積不同體積分數的乙醇溶液進行解析,解析效果見圖4。
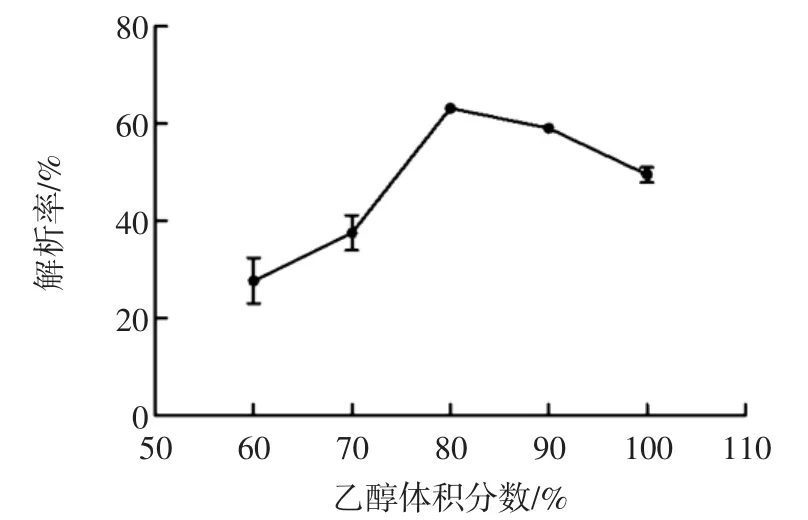
圖4 不同體積分數乙醇對AB-8樹脂解析率的影響Fig.4 Influence of ethanol concentration on static desorption percentage of AB-8 resin
從圖4可以看出,不同體積分數的乙醇對AB-8樹脂的解析率不同。乙醇體積分數為80%時,解析率最大,可達70%以上。乙醇體積分數在60%~80%之間時,解析率的增幅較快,乙醇體積分數在80%以上時,解析率逐漸減小。可能是酸漿果實中的多酚有一小部分為水溶性物質,當乙醇體積分數過高時,水溶性的酸漿果實多酚較難溶出;乙醇體積分數過低時,有機溶劑的含量較少,溶于有機溶劑中的酸漿果實多酚較難溶出,二者都會影響解析效果。所以選用80%乙醇作為最佳的解析溶劑。
2.1.2 AB-8樹脂對酸漿果實多酚類物質的動態吸附
2.1.2.1 動態吸附性能曲線
以1mg/mL上樣速度為例,將濃度大約在0.3mg/mL的樣品液加入裝有AB-8樹脂的層析柱中,直到流出液的吸光值是原上樣液吸光值的1/10時,則停止上樣,檢測樹脂的動態吸附性能,其結果見圖5。

圖5 AB-8型樹脂對酸漿果實多酚的動態吸附曲線Fig.5 Dynamic adsorption curve of AB-8 resin on Physalis fruit polyphenols
從圖5可以看出,隨著樣品液的不斷加入,流出液的酸漿果實多酚含量逐漸增大,動態吸附曲線接近理想的S形,并且當上樣體積達200 mL時,流出液的質量濃度接近原上樣液的質量濃度的1/10,此時AB-8樹脂已吸附飽和。
2.1.2.2 上柱流速對吸附效果的影響
將pH值約為4.7、濃度約為0.3 mg/mL的樣品液以上柱流速分別為1、2、3、4 mL/min通過AB-8層析柱,流出液每10 mL為單位收集一管,檢測上柱流速對AB-8樹脂吸附酸漿果實多酚的影響,結果見圖6。

圖6 上樣流速對動態吸附的影響Fig.6 Effect of loading flow rate on dynamic adsorption
從圖6可以看出,上樣流速為1、2、3、4 mL/min時,隨著上樣量的增加,AB-8樹脂對其吸附的動態效果呈平穩增長型,收集液體積分別在190、170、140 mL和130 mL左右時出現了泄漏點,出現泄漏點最晚的是1 mL/min的上樣流速,因為上樣流速較慢時,AB-8樹脂對酸漿果實多酚的吸附時間較為充分,能夠發揮樹脂的最大吸附效果,所以選用流速為1 mL/min的上樣速度較為合適。
2.1.2.3 洗脫劑流速對洗脫效果的影響
以 80%的乙醇作為洗脫劑,選用 1、2、3、4 mL/min的洗脫速度分別對吸附飽和的AB-8樹脂進行洗脫,其洗脫效果見圖7。

圖7 洗脫劑流速對洗脫效果的影響Fig.7 Desorption curve of Physalis fruit polyphenols from AB-8
從圖7可以看出,洗脫速度為3mL/min和4mL/min時,峰形較寬,有明顯的拖尾現象,因為洗脫速度過快,洗脫性能不充分,會有拖尾現象;洗脫速度為1 mL/min和2 mL/min時,峰形集中,無拖尾現象,但是二者相比之下,洗脫速度為1 mL/min時,洗脫效果更好。因此,洗脫流速選擇1 mL/min較為合適。
2.2 酸漿果實多酚的抗氧化活性測定
2.2.1 酸漿果實多酚對DPPH·清除能力的測定
不同濃度酸漿果實多酚溶液及其對應的DPPH·的清除率,結果見圖8。

圖8 酸漿果實多酚對DPPH自由基的清除作用Fig.8 Scavenging effects of Physalis fruit polyphenols on DPPH radical
從圖8可以看出,隨著酸漿果實多酚溶液濃度的增加,對DPPH自由基的清除能力也增強。當酸漿果實多酚溶液濃度在 0.25 mg/mL~4 mg/mL范圍時,對DPPH自由基的清除能力呈上升趨勢,在4 mg/mL時,酸漿果實多酚對DPPH自由基的清除率達到了60%以上;當清除率達到50%時所對應的酸漿果實多酚濃度為2.262 mg/mL。表明酸漿果實多酚對DPPH自由基有一定的清除作用。
2.2.2 酸漿果實多酚對羥自由基清除能力的測定
不同濃度酸漿果實多酚溶液及其對應的羥自由基清除率,結果見圖9。

圖9 酸漿果實多酚對羥自由基的清除作用Fig.9 Scavenging effects of Physalis fruit polyphenols on hydroxyl radical
從圖9可以看出,隨著酸漿果實多酚溶液濃度的增加,對羥自由基的清除能力也增加。當酸漿果實多酚溶液濃度在0.25 mg/mL~2 mg/mL范圍時,對DPPH自由基的清除能力呈直線上升趨勢;在8 mg/mL時,酸漿果實多酚對DPPH自由基的清除率達到了80%以上;當清除率達到50%時所對應的酸漿果實多酚濃度為0.604 4 mg/mL。表明酸漿果實多酚對羥自由基有一定的清除作用。
2.2.3 酸漿果實多酚對Fe2+還原能力的測定
測定不同濃度的酸漿果實多酚溶液對Fe2+的還原能力,結果見圖10。

圖10 酸漿果實多酚對Fe2+的還原能力Fig.10 The reduction ability of Physalis fruit polyphenols on Fe2+
酸漿果實多酚的還原能力通過Trolox來表示。從圖10可以看出,酸漿果實多酚濃度與其還原亞鐵離子的能力呈良好的依賴關系。隨著酸漿果實多酚濃度的增加,還原能力也在不斷增強。在試驗范圍內,其還原力在最高濃度時相當于Trolox的量為544.39 μmol/L。表明酸漿果實多酚有一定的還原能力。
2.3 酸漿果實多酚的酶抑制活性測定
2.3.1 酸漿果實多酚對胰脂肪酶活性抑制率的測定
不同濃度酸漿果實多酚溶液及其對應的胰脂肪酶的抑制率,結果見圖11。

圖11 酸漿果實多酚對胰脂肪酶的抑制作用Fig.11 Inhibitory effect of Physalis fruit polyphenols on pancreatic lipase
在體內脂肪水解過程中胰脂肪酶起到了關鍵作用,若抑制胰脂肪酶的活性,即可抑制機體對脂肪的水解和消化吸收,減少肥胖的發生[26]。從圖11可以看出,隨著酸漿果實多酚溶液濃度的增加,對胰脂肪酶的抑制作用也在增強。在試驗范圍內,對胰脂肪酶的抑制率在最大濃度時為90%,對胰脂肪酶的半數抑制濃度為0.826 2 mg/mL。表明酸漿果實多酚對胰脂肪酶有一定的抑制效果。
2.3.2 酸漿果實多酚對α-葡萄糖苷酶活性抑制率的測定
不同濃度酸漿果實多酚溶液及其對應的α-葡萄糖苷酶的抑制率,結果見圖12。

圖12 酸漿果實多酚對α-葡萄糖苷酶的抑制作用Fig.12 Inhibitory effect of Physalis fruit polyphenols on αglucosidase
α-葡萄糖苷酶是引起餐后血糖水平提高的關鍵酶,也是引起Ⅱ型糖尿病發生的關鍵酶[27]。從圖12可以看出,隨著酸漿果實多酚溶液濃度的成倍增加,對α-葡萄糖苷酶的抑制作用也在逐漸增強。在試驗范圍內,對α-葡萄糖苷酶的抑制率在最大濃度時為80%,對α-葡萄糖苷酶的半數抑制濃度為1.011 mg/mL。表明酸漿果實多酚對α-葡萄糖苷酶有一定的抑制效果。
2.3.3 酸漿果實多酚對α-淀粉酶活性抑制率的測定
不同濃度酸漿果實多酚溶液及其對應的α-淀粉酶的抑制率,結果見圖13。

圖13 酸漿果實多酚對α-淀粉酶的抑制作用Fig.13 Inhibitory effect of Physalis fruit polyphenols on αamylase
α-淀粉酶也是引起餐后血糖水平提高的關鍵酶,同時也是引起Ⅱ型糖尿病發生的關鍵酶[26]。從圖13可以看出,隨著酸漿果實多酚溶液濃度的成倍增加,對α-淀粉酶的抑制作用也在逐漸增強。當酸漿果實多酚溶液濃度在0.25 mg/mL~4 mg/mL范圍時,對α-淀粉酶的抑制作用呈直線上升趨勢,在4 mg/mL時,酸漿果實多酚對α-淀粉酶的抑制作用達到了90%以上,其對α-淀粉酶抑制率達到一半時的濃度為0.817 8 mg/mL。表明酸漿果實多酚對α-淀粉酶有很好的抑制效果。
3 結論
通過靜態、動態的吸附和解析試驗,從9種大孔樹脂中篩選出的純化酸漿果實多酚的最適大孔吸附樹脂為AB-8樹脂,該樹脂對酸漿果實多酚有較好的吸附和解析性能,并且進一步研究了AB-8樹脂吸附和解析酸漿果實多酚的最佳條件:以樣液濃度為0.3 mg/mL、pH為樣品本身的pH值、流速為1mL/min上樣200mL;用300 mL體積分數為80%的乙醇,以1 mL/min的流速進行洗脫。
在此條件下,研究酸漿果實多酚的抗氧化作用和酶活性抑制作用。得出酸漿果實多酚具有一定還原能力,對羥自由基和DPPH自由基有清除作用,其IC50值分別為0.604 4 mg/mL和2.262 mg/mL,并對胰脂肪酶、α-淀粉酶和α-葡萄糖苷酶有抑制作用,半抑制濃度(IC50)分別為0.826 2、0.8178 mg/mL 和 1.011 mg/mL。因此,酸漿果實多酚具有抗氧化作用,對胰脂肪酶、α-淀粉酶和α-葡萄糖苷酶的活性有抑制作用,這為進一步研究酸漿果實多酚在體內對糖、脂代謝的影響提供了科學依據。
[1]王家東,王曉聞.酸漿營養成分的分析[J].山西農業大學學報(自然科學版),2005,25(4):376-379
[2]劉雅麗,韓書影,趙后,等.錦燈籠宿萼皂苷降血糖作用研究[J].東北師大學報(自然科學版),2010,42(2):105-109
[3]劉敏,徐斌,杜鵑,等.酸漿水提物對高脂模型大鼠血脂水平的影響[J].江蘇農業科學,2014,42(10):310-313
[4]張嵐,葛紅娟,溫武略,等.酸漿宿萼總黃酮體外對羥基自由基的抑制作用[J].時珍國醫國藥,2011,22(8):1936-1937
[5]孔靜.酸漿醇提物抑制食管癌EC-1.71細胞增殖和誘導其凋亡的實驗研究[D].鎮江:江蘇大學,2011:20-27
[6]孟慶然.酸漿宿萼總皂苷對巨噬細胞炎癥反應的調控作用[D].晉中:山西農業大學,2014:50-51
[7]孟慶然,李立博,王曉聞.酸漿宿萼總皂苷體外抑菌效果研究[J].食品科學,2013,34(19):84-87
[8]何雪梅,孫健,李麗,等.蔗梢多酚類化合物抗氧化與抗腫瘤活性的研究[J].食品工業科技,2015,36(23):343-346
[9]金星玉.植物多酚類化合物在巨噬細胞中抗炎作用機制的研究[D].延吉:延邊大學,2006:7-10
[10]金亞倩,馬雪豪,白元生,等.葡多酚生物學功能研究進展[J].中國草食動物科學,2015,35(3):44-47
[11]Ji L,Yuan Y,Luo L,et al.Physalins with anti-inflammatory activity are present in Physalis alkekengi var.franchetii and can function as Michael reaction acceptors[J].Steroids,2012,77(5):441-447
[12]Tong H,Liang Z,Wang G.Structural characterization and hypoglycemic activity of a polysaccharide isolated from the fruit of Physalis alkekengi L.[J].Carbohydrate Polymers,2008,71(2):316-323
[13]Yu G,Duan Y F,Fang G Z,et al.Polysaccharides from fruit calyx of Physalis alkekengi var.francheti:Isolation,purification,structural features and antioxidant activities[J].Carbohydrate Polymers,2009,77(2):188-193
[14]郭穎,劉靜,聶黎行,等.錦燈籠的研究進展[J].中藥材,2012,35(12):2039-2045
[15]田樹革,魏玉龍,劉宏炳.Folin-Ciocalteu比色法測定石榴不同部位總多酚的含量[J].光譜實驗室,2009,26(2):341-343
[16]王若蘭,田志琴,孔祥剛,等.大孔吸附樹脂純化小米酚類化合物的工藝條件研究[J].中國糧油學報,2011,26(10):35-39
[17]馮進,李敏,曾曉雄,等.大孔樹脂純化藍莓葉多酚及其組成分析[J].食品科學,2013,34(10):86-91
[18]甘芝霖,倪元穎,郭悅,等.大孔樹脂分離純化玫瑰果多酚及其抗氧化性[J].農業工程學報,2015,31(24):298-304
[19]張瑞妮.紅棗多酚的提取分離及體外抗氧化活性研究[D].西安:陜西師范大學,2013:37-38
[20]邢佳,陸文娟,趙云霞,等.石榴葉多酚的純化及抗氧化活性研究[J].南京師大學報(自然科學版),2015,38(3):84-90
[21]王畢妮,黃慶瑗,高慧,等.不同極性紅棗多酚的抗氧化活性比較[J].食品與發酵工業,2014,40(10):142-145
[22]張麗娜.水翁花對胰脂肪酶和α-淀粉酶抑制活性及作用機制初步探討[D].上海:華東理工大學,2012:22-23
[23]Worsztynowicz P,Napierala M,Bialas W,et al.Pancreatic α-amylase and lipase inhibitory activity of polyphenolic compounds present in the extract of black chokeberry(Aronia melanocarpa L.)[J].Process Biochemistry,2014,49(9):1457-1463
[24]袁娟,衛娜,徐勇,等.白豆提取物對α-淀粉酶和α-葡萄糖苷酶活性研究[J].食品與發酵科技,2014,50(3):12-15
[25]李波,包怡紅,高峰,等.紅松松球鱗片多酚對α-淀粉酶和α-葡萄糖苷酶的抑制作用[J].食品工業科技,2015,36(1):63-69
[26]張忠.茶多酚對胰脂肪酶活性的抑制作用[J].食品工業,2013,34(8):168-170
[27]彭冰潔,宋卓,劉云龍,等.多酚類化合物對糖脂代謝影響的研究進展[J].食品科學,2015,36(17):270-273

