溫度對黃顙魚無水保活工藝的影響
王立紅,李韜,劉悅,李含笑,張甜甜,張長峰,聶小寶,*
(1.山東省農產品貯運保鮮技術重點實驗室,山東濟南250103;2.山東師范大學,山東濟南250014;3.國家農產品現代物流工程技術研究中心,山東濟南250103;4.山東商業職業技術學院,山東濟南250103)
黃顙魚屬鯰形目,鲿科的黃顙魚屬,俗稱昂刺、黃姑、黃蠟丁、黃鰭魚等[1]。黃顙魚具有高蛋白、低脂肪,肉質細嫩,味道鮮美,營養豐富等特點,且無肌間刺,養殖簡單,此外,黃顙魚還有滋補作用,具有一定的藥用價值,是出口創匯的優良品種,主要出口日本、韓國、東南亞等國家[2-3]。目前,黃顙魚的運輸方式主要為有水保活運輸,但其存在運輸距離短、載水量大、運輸量小、成活率低等諸多劣勢[4-5]。因此,研究溫度對黃顙魚無水保活工藝的影響,對提高黃顙魚的經濟價值和成活率具有重要的意義,為黃顙魚無水保活技術的實施提供理論依據。
低溫無水保活運輸是一種低成本、高存活率、長時間、高品質,且優于其它相關技術的綠色保活方法[6]。近年來,國內學者對水產品無水保活運輸技術進行了廣泛的研究和探索。上世紀九十年代末,劉淇等[10]選用2齡人工養殖牙鲆,采用生態冰溫學原理,研究了溫度對牙鲆無水保活的影響。認為采用低溫法,牙鲆無水保活52 h,成活率100%,60 h,成活率90%,低溫法明顯優于TMS麻醉法。直至2008年以后,國內學者在該領域的研究逐漸展開。徐若等[11]將泥蚶放在冷藏溫度為4、8℃和冰塊堆積條件下進行無水低溫保活效果研究,結果顯示無水冰溫保藏效果最好,4℃保活效果較好。韓利英等[9]研究認為鯽魚無水保活條件下臨界溫度為6℃~7℃,同時,梯度降溫速率也是影響鯽魚無水保活時間的主要因子。劉偉東等[7]研究了低溫條件下大菱鲆有水和無水保活過程中生理生化變化情況,結果表明:有水保活的大菱鲆血液中1BUN、CR、UA和GLU顯著低于無水保活。張觀科等[12]以毛蚶為研究對象進行饑餓無水保活實驗,探索了不同溫度條件下ATP的變化情況,結果表明:在不同保活溫度下毛蚶ATP含量差異顯著。聶小寶等[8]探索了泥鰍在0、5、10℃下無水保活成活率以及機體生化指標變化情況,表明5℃為泥鰍最佳無水保活溫度。上述研究均表明在無水保活過程中其環境溫度是至關重要的影響因素之一。因此,本文以黃顙魚為研究對象,探索了0、3、6℃無水保活條件下其存活率、O2消耗量、CO2含量、肌糖原含量、ATP含量和乳酸含量等指標的變化,旨在為黃顙魚無水保活運輸實踐提供理論參考。
1 材料與方法
1.1 材料與處理
1.1.1 材料
黃顙魚:從濟南海鮮大市場購買,挑選體格健壯,色澤光亮,新鮮而活躍,個體大小均勻,健康無疾病的黃顙魚用于試驗。每尾全長約(15±5)cm,體質量約(100±10)g。
1.1.2 主要儀器與設備
MAP-Q7200扎口氣調包裝機:蘇州森瑞保鮮設備有限公司;T6新世紀紫外可見分光光度計:北京普析通用儀器有限責任公司;OXYBABYM+O2/CO2氧氣分析儀:上海眾林機電設備有限公司;UPR-11-10T純凈水器:四川優普超純科技有限公司;電子萬用爐:北京市永光明醫療儀器廠;離心機:德國Hettich科學儀器有限公司;METTLER TOLEDO EL204-IC電子天平:梅特勒-托利多儀器(上海)有限公司。
1.1.3 處理方法
購買160尾黃顙魚放入水溫為25℃的暫養桶中進行暫養,對暫養桶連續充氧,停止投餌,暫養48 h后,調節溫度調控系統并以2℃/h降溫速率降至0℃時,留3尾黃顙魚在暫養桶中做空白,將其他魚打撈出桶,分別移至不同的塑料袋中,排除空氣,充入純氧,采用橡皮筋進行密封處理,以每40尾一組,分別移入0、3℃和6℃,3個不同溫度的冷庫中進行無水保活(分別記為0℃組,3℃組和6℃組),其中20尾黃顙魚用來測定黃顙魚在保活第12、24、36 h和48 h時的成活率和O2和CO2含量,同時,另外20尾黃顙魚在保活第 12、24、36、48 h,分別取出 3 尾,采集背部肌肉。
1.1.4 樣品的制備
肌肉樣品的制備:將黃顙魚取完血液后,用剪刀剪取其的背部肌肉,去除其表皮和脊柱,用蒸餾水沖洗干凈,再用濾紙吸干背部肌肉上的水分;放置-20℃低溫冰箱中暫存。用于肌糖原、乳酸和ATP含量的測定。
1.2 測定項目及方法
1.2.1 存活率的確定
每一個時間段統計一下每一組溫度下魚存活的數量,計算存活率。
存活率/%=(存活數/樣品總數)×100
1.2.2 O2和CO2含量的測定
采用OXYBABYM+O2/CO2氧氣分析儀進行分析,從一開始到結束一直使用相同的兩條進行測定,并做好標記。
1.2.3 肌糖原的測定
采用南京建成生物工程研究所肌糖原試劑盒法測定。
1.2.4 ATP含量的測定
采用南京建成生物工程研究所ATP含量測定試劑盒。
1.2.5 乳酸
采用南京建成生物工程研究所乳酸試劑盒。
1.3 數據處理
采用orignPro2016 64bit進行繪圖,利用SPSS 21.0進行相關性分析,顯著性水平設置為P<0.05。
2 結果與分析
2.1不同溫度對黃顙魚無水保活過程中存活率的影響
不同溫度對黃顙魚無水保活過程中存活率的影響見圖1。
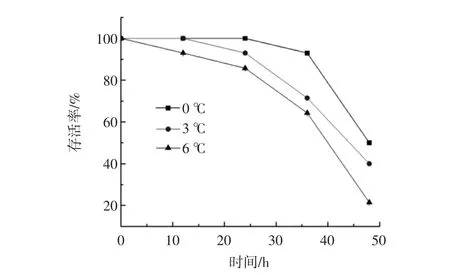
圖1 不同溫度對黃顙魚無水保活過程中存活率的影響Fig.1 Effect of different temperature on the survival rate of yellow catfish in the process of keeping alive without water
存活率是表明活魚保活效果的關鍵指標,其高低直接說明保活方法是否可行[13]。由圖1可知,隨著無水保活時間的延長,不同溫度無水保活下的黃顙魚存活率逐漸降低。其中,6℃組隨保活時間的增加其死亡速率最快。0℃組在保活的24 h內始終無死亡率,3℃組在保活24 h時,成活率仍能夠達到93%,而6℃在24 h時黃顙魚的存活率已達到85.71%。由圖中數據可以得出,在0℃下黃顙魚的無水保活效果最佳,能夠維持較長的保活時間。因此,在對魚類進行無水保活貯運時,溫度不易過高或過低,應該選擇適宜的低溫進行保活,環境溫度偏高或偏低均影響其存活時間及成活率。
2.2 不同溫度對黃顙魚無水保活過程中O2消耗量的影響
不同溫度對黃顙魚無水保活過程中O2消耗量的影響見圖2。

圖2 不同溫度對黃顙魚無水保活過程中O2消耗量的影響Fig.2 Different temperature preserving effect of O2consumption in the process of living on pelteobagrus fulvidraco anhydrous
魚類在有水環境中,則是通過鰓蓋的閉合使水流流過鰓絲,從而達到呼吸的目的,維持生命特征。當魚類在無水保活貯運過程下,只能通過鰓的閉合直接與空氣結合進行呼吸作用,但該方式的呼吸效率上不明確[14]。由圖2可得,保活袋內的初始O2含量并不是100%而是84%左右,這是由于在充氧時充入的氧氣不足導致的。從圖2可知在0、3、6℃3個不同溫度無水保活環境下的保活袋內O2的含量隨保活時間地延長均呈下降趨勢(P>0.05),且不同溫度無水保活環境下,黃顙魚呼吸消耗O2速率不同,其中,6℃無水保活環境下黃顙魚呼吸消耗O2速率最快,在保活12 h時O2消耗量達到64.6%,保活36 h時O2消耗量達到56.8%;0℃無水保活環境下黃顙魚呼吸消耗O2速率最慢,在保活12 h時O2消耗量達到71.9%,保活36 h時O2消耗量達到65.6%,且在相同時間內兩個不同溫度組均呈顯著性差異(P<0.05)。綜上可知,無水保活溫度越低,黃顙魚對O2的需求量就越少,則0℃相較于3℃和6℃更適合于黃顙魚的無水保活運輸。
2.3 不同溫度對黃顙魚無水保活過程中CO2含量的影響
不同溫度對黃顙魚無水保活過程中CO2含量的影響見圖3。
保活袋中CO2含量的增加是因為黃顙魚的呼吸作用產出的。由圖3可看出,3個保活溫度組CO2含量隨保活時間的延長逐漸增多(P>0.05),其變化趨勢與O2的消耗量呈現相反的變化趨勢。6℃時CO2含量增長最快且保活袋中的CO2含量最多,0℃時CO2含量增長緩慢,且在整個保活過程中CO2含量最少。由此可見,溫度越低黃顙魚呼吸產出的CO2越少。因此,0℃是無水保活的最適溫度。
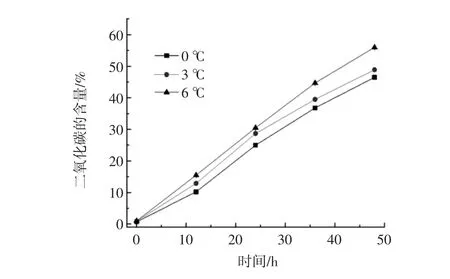
圖3 不同溫度對黃顙魚無水保活過程中CO2含量的影響Fig.3 Effects of different temperature and CO2content in the process of living on pelteobagrus fulvidraco anhydrous
2.4 不同溫度對黃顙魚無水保活過程中肌糖原含量的影響
不同溫度對黃顙魚無水保活過程中肌糖原含量的影響見圖4。
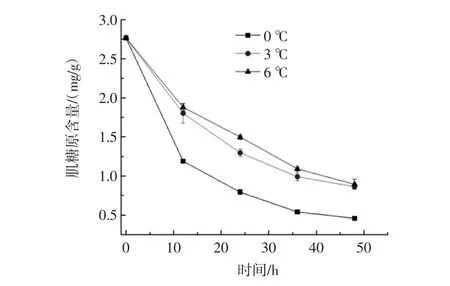
圖4 不同溫度對黃顙魚無水保活過程中肌糖原含量的影響Fig.4 Effects of different temperature and muscle glycogen content in the process of living on pelteobagrus fulvidraco anhydrous
肌糖原是反應動物對外界環境應激程度的重要指標,其變化規律能夠清晰的反應機體對環境的適應情況[15-17]。由圖4可知,在0、3、6℃下無水保活的黃顙魚隨保活時間的延長肌糖原逐漸降低,且差異性顯著(P<0.05)。在 0 h時肌糖原的含量為 2.766 mg/g,在12 h時0、3℃和6℃下的肌糖原含量分別為1.189、1.802、1.879 mg/g,由此可看出0℃下肌糖原下降的速度最快,6℃下肌糖原含量下降的最慢,從而表明了溫度越低對黃顙魚機體的影響越大,應激強度越大。
2.5 不同溫度對黃顙魚無水保活過程中ATP含量的影響
不同溫度對黃顙魚無水保活過程中ATP含量的影響見圖5。
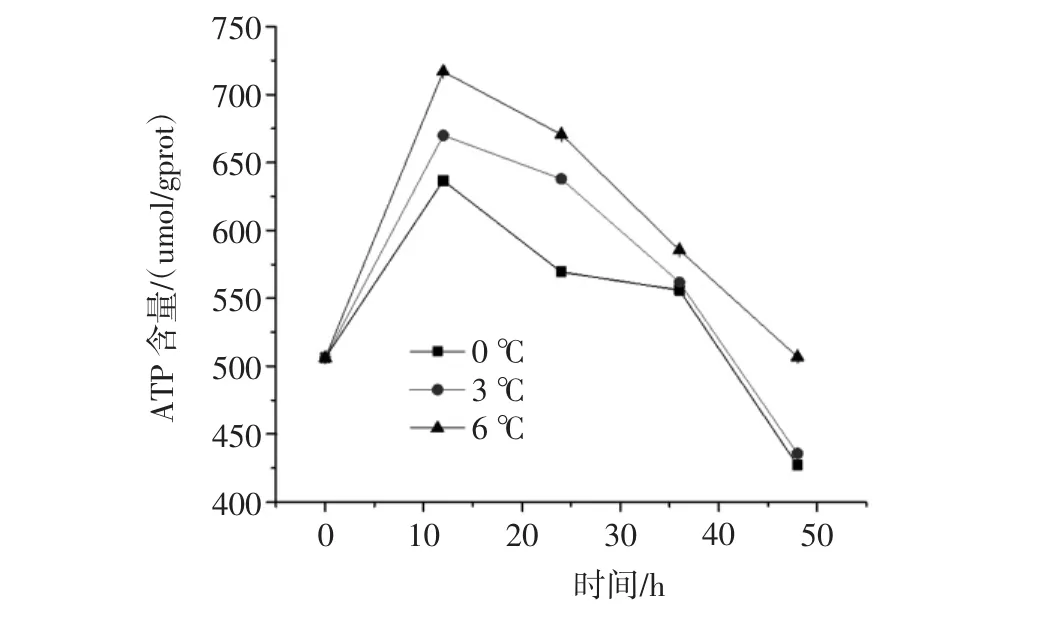
圖5 不同溫度對黃顙魚無水保活過程中ATP含量的影響Fig.5 Effects of different temperature and ATP content in the process of living on pelteobagrus fulvidraco anhydrous
由圖5可知,在0、3℃和6℃無水保活下黃顙魚的ATP含量隨保活時間的延長先增高后降低,且各組之間無明顯差異(P>0.05)。在保活12 h之前ATP含量是逐漸增加的,無水保活6℃的黃顙魚ATP含量上升速率最快,0℃下的ATP含量的上升速率最慢,且在相同的保活時間下兩組有明顯差異(P<0.05)。由此可說明在無水低溫環境中,黃顙魚的生命代謝受到影響,在無養分供給時,開始消耗ATP以供給生命的需要。12 h時ATP含量最高,說明其生命代謝比較旺盛,生命活動較強。在12 h后,ATP含量逐漸降低,黃顙魚的代謝速率降低,使得最終的存活率降低,這與戴志遠等[18]所做出的結論是一致的。由此可看出0℃下消耗的ATP最少,因此0℃是最佳的黃顙魚無水保活的溫度。
2.6 不同溫度對黃顙魚無水保活過程中乳酸含量的影響
不同溫度對黃顙魚無水保活過程中乳酸含量的影響見圖6。
由圖6可知,乳酸含量的變化趨勢和ATP含量的變化趨勢是相同的,乳酸含量隨黃顙魚保活時間的延長先上升后降低,且各組之間無明顯差異(P>0.05)。乳酸的初始含量為0.949 ug/g,之后逐漸上升,到第12天時達到最高值,無水保活溫度0、3℃和6℃下的乳酸含量分別為2.107、2.519、2.706 ug/g,在此時間點3個無水保活溫度下的乳酸含量呈顯著性差異(P<0.05),6℃乳酸含量最高,0℃乳酸含量最低。12 h后乳酸含量又逐漸下降,這是由于黃顙魚在低溫無水保活條件下,體內氧氣供應不足,排泄系統也受到影響,造成肌肉乳酸含量上升,而后由于生命活動減弱,乳酸含量也隨之下降[19]。因此,0℃是最適合黃顙魚無水保活的溫度。

圖6 不同溫度對黃顙魚無水保活過程中乳酸含量的影響Fig.6 Effects of different temperature and the content of lactic acid in the process of living on pelteobagrus fulvidraco anhydrous
3 結論
本文主要研究黃顙魚在0、3、6℃3個不同溫度下無水保活48 h過程中存活率、O2消耗量、CO2含量、肌糖原含量、ATP含量和乳酸含量等指標的變化,試驗結果表明:隨著無水保活時間的延長,各組黃顙魚存活率逐漸降低。其中,6℃組隨保活時間的增加其死亡速率最快,在保活24 h時,0℃組無死亡,3℃組成活率仍能夠達到93%,而6℃組存活率已達到85.71%。在保活48 h時,0℃組成活率仍最高。O2消耗量隨著保活時間的延長逐漸降低,6℃組消耗O2速率最快,在保活12 h時O2消耗量達到64.6%,保活36 h時O2消耗量達到56.8%;0℃組消耗O2速率最慢,在保活12 h時O2消耗量達到71.9%,保活36 h時O2消耗量達到65.6%,且在相同時間內兩個不同溫度組均呈顯著性差異(P<0.05)。由此可見,在整個無水保活過程中,環境溫度越低,黃顙魚對氧氣的消耗量就越少,體內新陳代謝越緩慢。CO2含量隨著保活時間的延長逐漸上升,因黃顙魚呼吸要不斷產生CO2。6℃組CO2含量增長最快,0℃組CO2含量增長緩慢。黃顙魚肌糖原的含量隨著保活時間的延長也逐漸降低,0℃組下降的速度最快,6℃組下下降的最慢。黃顙魚在無水保活的過程中ATP含量和乳酸含量的變化趨勢是一致的。在保活12 h之前ATP含量是逐漸增加的,無水保活6℃組的黃顙魚ATP含量上升速率最快,0℃組的ATP含量的上升速率最慢,且在相同的保活時間下兩組有明顯差異(P<0.05),由此可說明,在無水低溫環境中,黃顙魚的生命代謝受到影響,在無養分供給時,開始消耗ATP以供給生命的需要。乳酸的初始含量為0.949 ug/g,之后逐漸上升,到第12天時達到最高值,在此時間點3個無水保活溫度下的乳酸含量呈顯著性差異(P<0.05),6℃組乳酸含量最高,0℃組乳酸含量最低。12 h后乳酸含量又逐漸下降。這是由于黃顙魚在低溫無水保活條件下,體內氧氣供應不足,排泄系統也受到影響,造成肌肉乳酸含量上升,而后由于生命活動減弱,乳酸含量也隨之下降。綜上所述,黃顙魚的最適保活溫度是0℃。
[1]白艷龍,譚昭儀,邸向乾,等.黃顙魚無水保活技術研究[J].食品工業科技,2013,34(1):334-337
[2]劉行彪,付熊,吳晗冰,等.黃顙魚營養學的研究進展[J].水產學雜志,2011,24(1):55-59
[3]黃峰,嚴安生,熊傳喜,等.黃顙魚的含肉率及魚肉營養評價[J].淡水漁業,1999(10):3-6
[4]何蓉,謝晶.水產品保活技術研究現狀和進展[J].食品與機械,2012,28(5):243-246
[5]聶小寶,章艷,張長峰.水產品低溫保活運輸研究進展[J].食品研究與開發,2012,33(12):218-223
[6]汪之和.張飲江,李勇軍.水產品保活運輸技術[J].漁業現代化,2001(2):31-34
[7]劉偉東,薛長湖,殷邦忠,等.低溫下大菱鲆有水和無水保活過程中生理生化變化的研究[J].漁業科學進展,2009(5):69-74
[8]聶小寶,劉淇,張長峰,等.泥鰍低溫無水保活技術研究[J].湖南農業科學,2013(5):80-83
[9]韓利英,張慜.鯽魚保活條件對存活率的影響[J].食品與生物技術學報,2009(5):642-646
[10]劉淇,殷邦忠,姚健,等.牙鲆無水保活技術[J].中國水產科學,1999(2):101-103
[11]徐若,曹井志,包建強.泥蚶無水低溫保活技術研究[J].食品工業科技,2008,29(5):256-258
[12]張觀科,劉紅英,齊鳳生,等.毛蚶保活過程中ATP含量的變化[J].食品科技,2011,36(1):120-123
[13]何蓉,謝晶,蘇輝,等.不同溫度對無水保活條件下的中華鱉肌肉營養成分及血液生化指標影響[J].食品科學,2014(6):194-199
[14]吳云輝,陳慧斌,葉福財,等.溫度對半滑舌鰨無水保活的影響[J].食品工業,2016(1):177-180
[15]洪磊,張秀梅.環境脅迫對魚類生理機能的影響[J].海洋科學進展,2004,22(1):114-121
[16]WENDELAAR BONGA S E.The stress response in fish[J].Physiological Reviews,1997(77):591-625
[17]周玉,郭文場,楊振國,等.魚類血液指標研究進展[J].上海水產大學學報,2001,10(2):163-165
[18]戴志遠,張燕平,張虹,等.紫貽貝低溫無水保活過程中的生化變化[J].中國食品學報,2004,4(3):16-19
[19]Donaldson M R,Cooke S J,Patterson D A,et al.Cold shock and fish[J].Journal of Fish Biology,2008,73(7):1491-1530

