乳酸菌降解草酸鹽活性及機制研究進展
國立東,王麗群,于純淼,*,劉曉艷,焦月華,韓 華,*
原發性草酸鈣腎結石的形成通常與高鈣尿癥、高草酸尿癥和低枸櫞酸尿癥有關[1],其中高草酸尿癥是草酸鈣腎結石形成的主要因素[2],其主要由草酸鹽在體內的產生、吸收與分泌失衡導致。機體內的草酸鹽主要有兩方面的來源,即內源和外源。內源是通過哺乳動物肝臟代謝產生;外源則是通過胃腸道對食源草酸鹽的吸收獲取,而草酸鹽是大多數食源性植物產生的次生代謝產物。哺乳動物體內缺乏分解利用草酸鹽的酶類,草酸鹽主要是通過尿液排出體外[3]。健康機體每天通過尿分泌的草酸為10~40 mg,如果超過40~45 mg,臨床診斷即為高草酸尿癥[4]。隨著組學技術的發展,腸道微生物的功能逐漸被揭示,例如腸道微生物菌群失衡可導致腎臟疾病,腎臟疾病患者腸道微生物組成也在發生改變,二者是相互的[5]。腸道菌群是影響腸道草酸鹽分解的一個重要因素,其中食草酸桿菌為研究最廣泛、最深入的草酸鹽降解菌[6],并已有相應商業化產品上市[7]。食草酸桿菌在腸道內的定植與尿草酸濃度的降低存在直接相關性[8-11],然而,這種細菌作為益生菌應用時往往受到在腸道定植不穩定和對抗生素敏感的限制[7,12]。近年來一系列體外實驗、動物模型實驗、人體臨床實驗均發現,乳酸菌有一定的潛在降解草酸鹽的能力,可降解草酸鹽的乳酸菌主要包括乳桿菌屬、雙歧桿菌屬和腸球菌屬菌株[13-19]。其中,乳桿菌屬和雙歧桿菌屬為人體腸道內固有的有益菌群,通常認為其應用于人體是安全的,因此被廣泛作為益生菌應用。本文主要對可降解草酸鹽的乳酸菌種類、乳酸菌降解草酸鹽的能力以及乳酸菌降解草酸鹽的機理進行綜述,為降解草酸鹽乳酸菌的篩選及其作用機理研究提供指導,也為預防和治療高草酸尿癥益生菌產品的開發提供理論參考。
1 具有降解草酸鹽功能的乳酸菌
乳酸菌在自然界中分布廣泛,傳統發酵食品、動物和人的口腔、腸道及陰道中均棲居著大量乳酸菌。國內外研究人員已從自然環境中分離篩選到大量可降解草酸鹽的乳酸菌菌株,這些乳酸菌分離株主要來源于傳統發酵食品(如酸奶)、人體糞便以及動物糞便樣品等[20-24]。目前,已表現出可降解草酸鹽活性的乳酸菌主要包括乳桿菌屬、雙歧桿菌屬、腸球菌屬、明串珠菌屬以及乳球菌屬等,其中已明確具有降解草酸鹽能力的乳桿菌屬中主要有嗜酸乳桿菌[21,25-27]、格氏乳桿菌[26]、植物乳桿菌[21,26]、干酪乳桿菌[26,28]、鼠李糖乳桿菌[26]、副干酪乳桿菌[29]、羅伊氏乳桿菌[24,29]、發酵乳桿菌[23]等,雙歧桿菌屬主要有動物雙歧桿菌乳亞種[20,30]、短雙歧桿菌[14]、腸球菌屬中的糞腸球菌[13]和屎腸球菌[31]、明串珠菌屬中的乳明串珠菌[21]和腸膜明串珠菌[31],以及乳球菌屬中的乳酸乳球菌[31-32]和格氏乳球菌[31],具體見表1。除此之外,嗜熱鏈球菌、德氏乳桿菌保加利亞亞種、短乳桿菌、嬰兒雙歧桿菌、長雙歧桿菌的個別菌株可能也具有降解草酸鹽的活性,主要是因為這些菌一般與其他乳酸菌聯合制成益生菌制劑應用,如Oxadrop?和VSL#3?產品[33-34]。另外,魏斯氏菌屬內的一些菌株也展現出了一定的草酸鹽降解活性[23]。乳酸菌降解草酸鹽的活性具有菌種特異性和菌株特異性。例如,Federici等[20]研究了雙歧桿菌屬內某些菌株的草酸鹽降解活性,發現動物雙歧桿菌乳亞種DSM 10140的草酸鹽降解活性最高,能降解培養基中61%的草酸鹽;而長雙歧桿菌MB 282和青春雙歧桿菌MB 238的草酸鹽降解率分別為35%和57%,同為短雙歧桿菌的MB 283菌株可降解38%的草酸鹽,而MB 151菌株的草酸鹽降解率僅為1%;此外,供試的5 株長雙歧桿菌中僅有4 株能降解草酸鹽。
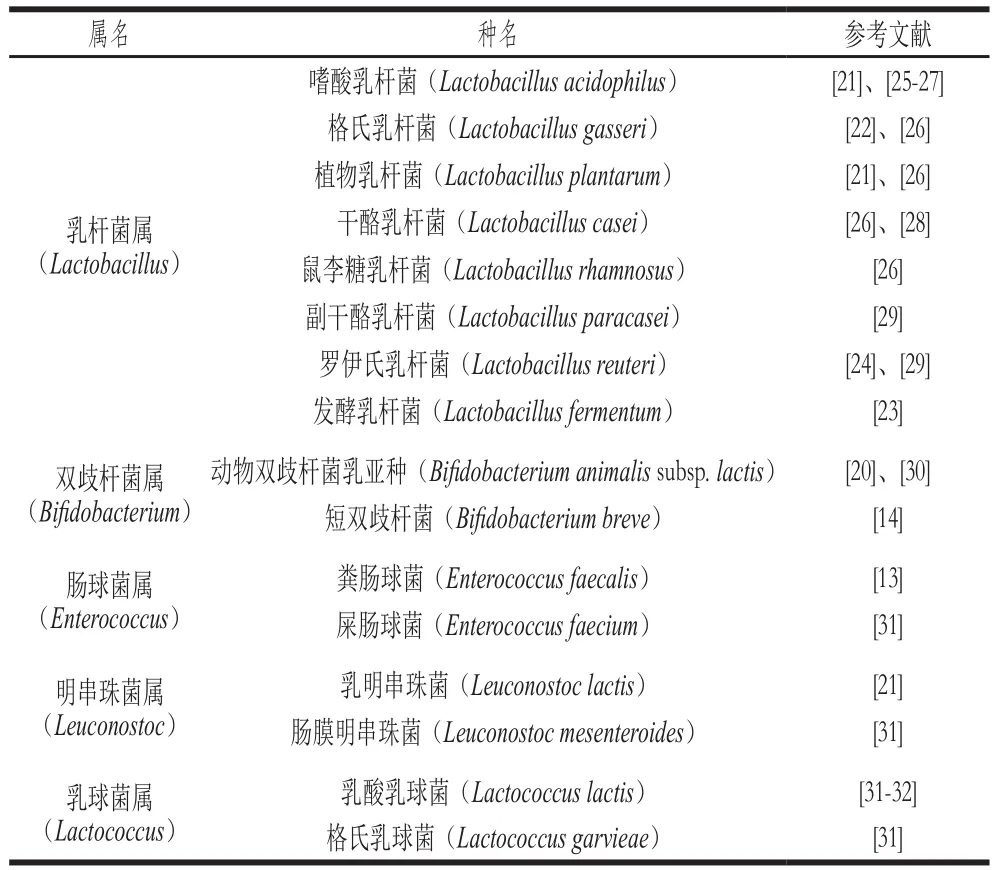
表1 具有降解草酸鹽活性乳酸菌的主要種屬Table 1 Major genera and species of lactic acid bacteria with oxalate-degrading activity
2 乳酸菌降解草酸鹽的特性
2.1 體外實驗
體外實驗通常作為篩選具有益生功能乳酸菌的首要步驟。研究乳酸菌草酸鹽降解活性的實驗是將供試乳酸菌菌株培養在含草酸鹽的培養基中,通過培養前后培養基中草酸鹽含量變化計算降解率進而評價其草酸鹽降解活性。2000年,Hokama等[13]首次報道了乳酸菌具有降解草酸鹽的能力,分離到11 株可降解草酸鹽的糞腸球菌,其中有4 株菌培養2 d后,其培養基中草酸鹽(2.0 g/L)全部被降解,同時發現糞腸球菌需要一種貧瘠的營養生境且重復傳代培養才能維持其降解草酸鹽的活性。隨后,研究人員通過體外實驗篩選到許多其他種屬的乳酸菌也具有草酸鹽降解活性,如廣泛用于乳制品和藥品的12 株雙歧桿菌在含有5 mmol/L草酸鈉的培養基中培養5 d,供試菌株中動物雙歧桿菌乳亞種DSM 10140菌株草酸鹽降解活性最強,可降解培養基中61%的草酸鈉[20]。Weese等[21]對來自犬糞便樣品的37 株乳酸菌進行體外降解草酸鹽活性研究,發現降解率為0%~65%,其中4 株菌無草酸鹽降解活性。同樣來源于犬糞便的47 株乳酸菌中,49%菌株無草酸鹽降解活性,34%菌株對草酸鹽的降解率低于5%[31]。13 株乳桿菌和5 株雙歧桿菌在含10 mmol/L草酸銨的培養基中培養24 h后,發現供試乳桿菌的草酸鹽降解活性高于雙歧桿菌[29]。由此說明,乳酸菌降解草酸鹽的能力具有菌株特異性。同時有研究發現,乳酸菌降解草酸鹽的能力明顯低于食草酸桿菌,食草酸桿菌幾乎可100%降解培養基中的草酸鹽[20,29]。為了更接近人體內真實情況,研究人員通過模擬人體結腸微生態條件評價了格氏乳桿菌Gasser AM63T的草酸鹽降解活性,發現其在構建的三階段連續培養系統的第一個階段(即近端結腸)就出現了草酸鹽降解活性[22]。此外,甲酰輔酶A轉移酶(formyl-CoA transferase,Frc)和草酰輔酶A脫羧酶(oxalyl-CoA decarboxylase,Oxc)作為人體內草酸鹽降解的2 個關鍵酶,其編碼基因和功能在乳酸菌中已得以鑒定[13,20,25,35]。因此,具有Frc基因frc和Oxc基因oxc一度成為體外分離篩選可降解草酸鹽乳酸菌菌株的依據之一[26]。
2.2 體內實驗
動物模型數據尤其是人體臨床實驗結果能最直接證明乳酸菌益生功能在體內能否真正發揮作用。目前已有大量研究證實了乳酸菌在體內具有抑制腸道草酸鹽吸收的作用。
高草酸尿癥及相關腎臟疾病實驗的模型動物通常以大鼠、小鼠以及犬最為常見。Kwak等[28]研究了乳桿菌對大鼠尿路結石形成的預防作用,與對照組相比,體外具有降解草酸鹽活性的干酪乳桿菌HY2743和HY7201菌株可明顯降低大鼠尿草酸的分泌,并且可使模型大鼠腎臟內晶體形成量明顯減少。Klimesova等[36]研究了一株雙歧桿菌對原發性高草酸尿癥小鼠模型尿草酸分泌的影響,發現動物雙歧桿菌乳亞種DSM 10140可降低模型小鼠尿草酸分泌,不同于食草酸桿菌通過促進腸道草酸分泌來降低尿草酸的分泌量[37],這種作用是該菌株通過降解飲食草酸鹽從而限制腸道對草酸鹽的吸收來完成的。Gomathi等[16]以富含草酸鉀的飲食誘導大鼠構建高草酸尿和草酸鈣結石模型,以體外具有降解草酸鹽活性的乳酸菌為受試對象,發現5×108CFU/mL劑量的供試發酵乳桿菌AB1、TY5菌株和唾液乳桿菌AB11菌株組成的三聯菌(活菌數之比為1∶1∶1)灌胃給予模型大鼠21 d后,模型大鼠的尿草酸水平明顯降低。鐘文婷[32]研究了一株乳酸乳球菌對食源性草酸過多導致的犬尿石癥的預防作用,發現在乳酸乳球菌處理第15天時模型犬尿草酸分泌量降低了21%,但差異不顯著,而在處理第30天時模型犬尿草酸分泌量下降了33%,且差異顯著(P<0.05),同時發現處理30 d后,犬尿鈣含量降低了10%,且差異顯著(P<0.05);說明該菌株具有潛在的降低尿草酸和尿鈣分泌的能力。
乳酸菌的草酸鹽降解活性在人體臨床實驗上也取得了較好的效果,尤以商業化的可降解草酸鹽的乳酸菌產品Oxadrop?和VSL#3?研究報道最多[33-34,38-39]。Campieri等[38]以原發性草酸尿路結石癥或弱高草酸尿癥患者為研究對象,每次給予活菌數為8×1011個的凍干乳酸菌混合物Oxadrop?(嗜酸乳桿菌、植物乳桿菌、短乳桿菌、嗜熱鏈球菌和嬰兒雙歧桿菌的活菌數之比為1∶1∶1∶1∶1),每天2 次,重懸于冷水中,飯前服用,連續服用4 周后,患者24 h的尿草酸分泌量從55.5 mg降到33.5 mg,下降了40%,實驗結束1 個月后,尿草酸分泌量繼續下降到28.3 mg,下降了49%。隨后,Lieske等[33]同樣以Oxadrop?為研究對象,考察了其對腸源性高草酸尿癥人群的影響,但使用的Oxadrop?產品菌種組成及比例(嗜酸乳桿菌、短乳桿菌、嗜熱鏈球菌和嬰兒雙歧桿菌活菌數之比為1∶1∶4∶4)與Campieri等[38]所使用的略有不同,受試人群每天服用1 次該產品(活菌數8×1011個),服用1 個月后尿草酸分泌量下降了19%,第2個月改為每天服用2次,尿草酸分泌量下降了24%,第3個月改為每天服用3 次,尿草酸分泌量相比于初始值僅下降了2%,而且停藥1 個月后,尿草酸分泌量仍下降了20%,這說明乳酸菌在人體腸道內發生定植并繼續發揮作用。Okombo等[39]研究了VSL#3?產品對健康人體消化道草酸鹽吸收的影響,VSL#3?產品由嗜熱鏈球菌、短雙歧桿菌、長雙歧桿菌、嬰兒雙歧桿菌、嗜酸乳桿菌、植物乳桿菌、副干酪乳桿菌、德氏乳桿菌保加利亞亞種8 種活性乳酸菌組成,受試個體每天攝取含相同量的低草酸鹽的食物,并口服80 mg草酸鹽,同時給予VSL#3?產品(8×1011個活菌),發現服用產品4 周后,總草酸鹽在22 h內的吸收率從30.8%降到11.6%,并且停用產品4 周后,22 h內的吸收率仍能維持在11.5%水平,但對于6 h內的吸收率,與服用4 周后、服用前均無顯著差異;由此推測,VSL#3?產品對草酸鹽的降解作用可能發生在結腸部位。Al-Wahsh等[34]考察了VSL#3?產品對人體消化道對草酸鹽吸收的影響,以11 名健康個體為研究對象,對照組口服草酸鈉,低劑量組和高劑量組除口服草酸鈉外分別口服1 粒和2 粒VSL#3?膠囊,每粒VSL#3?膠囊中含有4.5×1011個活菌,結果發現,該產品可明顯降低受試個體尿草酸水平,但高低兩個劑量組在草酸鹽吸收上沒有明顯差異。然而,Goldfarb等[40]在一項隨機控制臨床實驗中,考察了Oxadrop?產品對原發性高草酸尿癥人群的影響,與Lieske等[33]研究中使用Oxadrop?產品相比,該臨床實驗所用的Oxadrop?產品的菌種組成和比例不變,患者每天服用劑量(活菌數1.08×1012個)略高但無實質性差異,服用該產品4 周后,患者在24 h內的尿草酸分泌量雖然降低了6%,但與服用前的差異并不顯著,與此類似的結果也出現在Siener等[41]的研究報道中。由此說明,Oxadrop?產品在人體臨床實驗報道中并不都是積極的結果,這可能是源于人體臨床實驗相比動物實驗,在飲食上往往難于控制,同時受試個體數量有限且個體之間差異較大。
3 乳酸菌降解草酸鹽的機理
目前,草酸鹽降解菌研究最為清楚的是食草酸桿菌,草酸鹽是其生長代謝的唯一或主要碳源,因此被稱為“專性草酸營養型”[42],其對草酸鹽的降解首先是利用草酸鹽-甲酸鹽反向轉運體OxlT(oxlT基因編碼)將胞外草酸鹽吸收到細胞內,然后再利用Frc(frc基因編碼)將胞內草酸鹽轉化成草酰輔酶A,草酰輔酶A再通過Oxc(oxc基因編碼)的作用脫羧形成甲酸鹽和CO2,最后再利用OxlT將胞內甲酸鹽運輸到胞外,從而完成對草酸鹽的降解作用[43]。
與食草酸桿菌不同,乳酸菌屬于兼性草酸營養型微生物,即不以草酸鹽作為其生長的主要碳源,僅能利用草酸鹽作為碳源[38]。乳酸菌對草酸鹽的降解機理與食草酸桿菌類似,最早是在一株糞腸球菌中被闡述[13]。研究人員通過蛋白質免疫印跡技術檢測到可降解草酸鹽的糞腸球菌中存在2 種蛋白,可以同抗食草酸桿菌源的Frc和Oxc蛋白的抗體發生免疫反應;由此說明,糞腸球菌中降解草酸鹽的酶類與食草酸桿菌中的酶相似[13],但并沒有發現草酸鹽轉運蛋白的存在,糞腸球菌降解草酸鹽的確切機制尚未完全明確。Federici等[20]以已公布的食草酸桿菌oxc基因為模板設計引物,在一株具有草酸鹽降解活性的動物雙歧桿菌乳亞種中通過PCR反應成功擴增出同源體,其氨基酸序列與食草酸桿菌Oxc的氨基酸序列同源性為47%,在大腸桿菌中過表達的蛋白能夠與抗食草酸桿菌的Oxc抗體發生雜交,并通過酶活性分析證實了動物雙歧桿菌乳亞種源oxc基因的Oxc功能活性。隨后,Turroni等[30]在動物雙歧桿菌乳亞種中鑒定出了oxc和frc基因,細胞預適應于亞抑制濃度草酸鹽條件后,將其暴露于pH 4.5條件下,發現其草酸鹽降解率顯著提高,證實了酸性條件是動物雙歧桿菌乳亞種產生較高草酸鹽降解率的前提。乳桿菌屬的草酸鹽降解機制同樣是圍繞Frc和Oxc提出,Azcarate-Peril等[25]在嗜酸乳桿菌NCFM中鑒定了編碼降解草酸鹽的Frc和Oxc的基因,發現這兩個基因只有在細菌細胞適應亞抑制濃度草酸鹽并且在弱酸性條件下(pH 5.5)才能發揮功能。在格氏乳桿菌Gasser AM63T中,同樣檢測到了frc和oxc基因,也需要在弱酸性、同時有草酸鹽存在的條件下才能夠被誘導表達[22]。Turroni等[26]發現草酸鹽降解率超過50%的所有供試嗜酸乳桿菌和格氏乳桿菌中均存在oxc和frc基因。Kullin等[44]對一株羅伊氏乳桿菌100-23C進行全基因組分析,發現其基因組中存在緊鄰的oxc和frc基因,預測的Oxc和Frc產物分別與格氏乳桿菌、嗜酸乳桿菌和動物雙歧桿菌乳亞種中的Oxc和Frc具有高度的同源性,但該菌株野生型并不能降解培養基中的草酸鹽,這可能是由于其缺少草酸鹽轉運體。由此說明,細菌的基因組中含有oxc和frc基因并不足以證明其一定具有降解草酸鹽的能力。除了Oxc和Frc之外,還需草酸鹽轉運體將草酸鹽由胞外轉移到胞內,而Turroni等[30]在動物雙歧桿菌乳亞種中發現了一個可能與草酸鹽轉運有關的編碼透性酶的開放閱讀框,并且存在于已公布的全基因組序列中,這種透性酶基因也存在于許多可降解草酸鹽的乳桿菌屬菌株中;然而,在羅伊氏乳桿菌100-23C全基因組中并不存在該透性酶基因,這可能是該菌株不能降解草酸鹽的主要原因。
綜上所述,乳酸菌通過透性酶將胞外草酸鹽轉運到胞內,通過Frc將草酸鹽轉化為草酰輔酶A,再通過Oxc脫羧產生甲酸鹽和CO2完成對草酸鹽的降解。
4 結 語
不論是體外實驗還是體內實驗結果均表明,乳酸菌的草酸鹽降解活性無法與食草酸桿菌相媲美。食草酸桿菌的生長需要以草酸鹽作為其生長代謝的唯一或主要碳源,因此,食草酸桿菌對治療高草酸尿癥非常有效。此外,腸道內草酸鹽濃度的高低受飲食組成影響較大,這也是食草酸桿菌在腸道內定植不穩定的根本原因。相比之下,乳酸菌能夠利用草酸鹽但不以其作為主要碳源,在腸道內的定植不受腸道草酸鹽水平的限制,可穩定定植于腸道內。因此,乳酸菌在預防高草酸尿癥方面具有獨特的優勢。可降解草酸鹽的乳酸菌主要分布于乳桿菌屬、雙歧桿菌屬以及腸球菌屬,且具有菌種和菌株特異性,其降解草酸鹽的作用受3個基因調控,即oxc、frc及編碼透性酶的基因,但關于透性酶的遺傳信息及發揮功能的確切機制仍需更深入的研究加以證實。總之,乳酸菌的草酸鹽降解活性是明確的,在預防與治療草酸鹽相關的腎臟疾病上具有較好的應用前景。
[1] COCHAT P, RUMSBY G. Primary hyperoxaluria[J]. The New England Journal of Medicine, 2013, 369: 649-658. DOI:10.1056/NEJMra1301564.
[2] BHASIN B, üREKLI H M, ATTA M G. Primary and secondary hyperoxaluria: understanding the enigma[J]. World Journal of Nephrology, 2015, 4(2): 235-244. DOI:10.5527/wjn.v4.i2.235.
[3] WEINMAN E J, FRANKFURT S J, INCE A, et al. Renal tubular transport of organic acids. Studies with oxalate and para-aminohippurate in the rat[J]. The Journal of Clinical Investigation, 1978, 61(3): 801-806.DOI:10.1172/JCI108994.
[4] STEF R, BERND H, BENJAMIN A V, et al. Hyperoxaluria: a gut-kidney axis?[J]. Kidney International, 2011, 80(11): 1146-1158.DOI:10.1038/ki.2011.287.
[5] KHODOR S A, SHATAT I F. Gut microbiome and kidney disease:a bidirectional relationship[J]. Pediatric Nephrology, 2016, 32(6): 921-931.DOI:10.1007/s00467-016-3392-7.
[6] JAIRATH A, PAREKH N, OTANO N, et al. Oxalobacter formigenes: opening the door to probiotic therapy for the treatment of hyperoxaluria[J]. Scandinavian Journal of Urology and Nephrology, 2015,49(4): 334-337. DOI:10.3109/21681805.2014.996251.
[7] ELLIS M L, SHAW K J, JACKSON S B, et al. Analysis of commercial kidney stone probiotic supplements[J]. Urology, 2015, 85(3): 517-521.DOI:10.1016/j.urology.2014.11.013.
[8] ALLISON M J, DAWSON K A, MAYBERRY W R, et al. Oxalobacter formigenes gen. nov., sp. nov.: oxalate-degrading anaerobes that inhabit the gastrointestinal tract[J]. Archives of Microbiology, 1985, 141(1): 1-7.DOI:10.1007/BF00446731.
[9] JIANG J, KNIGHT J, EASTER L H, et al. Impact of dietary calcium and oxalate, and Oxalobacter formigenes colonization on urinary oxalate excretion[J]. Journal of Urology, 2011, 186(1): 135-139. DOI:10.1016/j.juro.2011.03.006.
[10] LI X S, ELLIS M L, KNIGHT J. Oxalobacter formigenes colonization and oxalate dynamics in a mouse model[J]. Applied and Environmental Microbiology, 2015, 81(15): 5048-5054. DOI:10.1128/AEM.01313-15.
[11] BARNETT C, NAZZAL L, GOLDFARB D S, et al. The presence of Oxalobacter formigenes in the microbiome of healthy young adults[J]. Journal of Urology, 2016, 195(2): 499-506. DOI:10.1016/j.juro.2015.08.070.
[12] LANGE J N, WOOD K D, WONG H, et al. Sensitivity of human strains of Oxalobacter formigenes to commonly prescribed antibiotics[J]. Urology,2012, 79(6): 1286-1289. DOI:10.1016/j.urology.2011.11.017.
[13] HOKAMA S, HONMA Y, TOMA C, et al. Oxalate-degrading Enterococcus faecalis[J]. Microbiology and Immunology, 2000, 44(4):235-240. DOI:10.1111/j.1348-0421.2000.tb02489.x.
[14] FERRAZ R R, MARQUES N C, FROEDER L, et al. Effects of Lactobacillus casei and Bifidobacterium breve on urinary oxalate excretion in nephrolithiasis patients[J]. Urological Research, 2009, 37(2):95-100. DOI:10.1007/s00240-009-0177-5.
[15] GIARDINA S, SCILIRONI C, MICHELOTTI A, et al. In vitro antiinflammatory activity of selected oxalate-degrading probiotic bacteria:potential applications in the prevention and treatment of hyperoxaluria[J].Journal of Food Science, 2014, 79(3): M384-M390. DOI:10.1111/1750-3841.12344.
[16] GOMATHI S, SASIKUMAR P, ANBAZHAGAN K, et al. Oral administration of indigenous oxalate degrading lactic acid bacteria and quercetin prevents calcium oxalate stone formation in rats fed with oxalate rich diet[J]. Journal of Functional Foods, 2015, 17: 43-54.DOI:10.1016/j.jff.2015.05.011.
[17] PECK A B, CANALES B K, NGUYEN C Q. Oxalate-degrading microorganisms or oxalate-degrading enzymes: which is the future therapy for enzymatic dissolution of calcium-oxalate uroliths in recurrent stone disease?[J] Urolithiasis, 2016, 44(1): 45-50. DOI:10.1007/s00240-015-0845-6.
[18] DI CERBO A, PEZZUTO F, PALMIERI L, et al. Clinical and experimental use of probiotic formulations for management of end-stage renal disease: an update[J]. International Urology and Nephrology, 2013,45(6): 1569-1576. DOI:10.1007/s11255-012-0335-5.
[19] 任志華. 草酸降解菌的分離鑒定及其對犬草酸鈣尿結石的預防作用與機理研究[D]. 南京: 南京農業大學, 2011: 115-123.
[20] FEDERICI F, VITALI B, GOTTI R, et al. Characterization and heterologous expression of the oxalyl coenzyme A decarboxylase gene from Bifidobacterium lactis[J]. Applied and Environmental Microbiology, 2004, 70(9): 5066-5073. DOI:10.1128/AEM.70.9.5066-5073.2004.
[21] WEESE J S, WEESE H E, YURICEK L, et al. Oxalate degradation by intestinal lactic acid bacteria in dogs and cats[J]. Veterinary Microbiology,2004, 101(3): 161-166. DOI:10.1016/j.vetmic.2004.03.017.
[22] LEWANIKA T R, REID S J, ABRATT V R, et al. Lactobacillus gasseri Gasser AM63Tdegrades oxalate in a multistage continuous culture simulator of thehuman colonic microbiota[J]. FEMS Microbiology Ecology, 2007, 61(1): 110-120. DOI:10.1111/j.1574-6941.2007.00327.x.
[23] GOMATHI S, SASIKUMAR P, ANBAZHAGAN K, et al. Screening of indigenous oxalate degrading lactic acid bacteria from human faeces and South Indian fermented foods: assessment of probiotic potential[J]. The Scientiベc World Journal, 2014, 2014: 648059. DOI:10.1155/2014/648059.
[24] 董婷婷. 降解草酸益生菌的篩選及其對實驗動物的功效研究[D]. 大連: 大連醫科大學, 2012: 6-28.
[25] AZCARATE-PERIL M A, BRUNO-BáRCENA J M, HASSAN H M,et al. Transcriptional and functional analysis of oxalyl-coenzyme A (CoA)decarboxylase and formyl-CoA transferase genes from Lactobacillus acidophilus[J]. Applied and Environmental Microbiology, 2006, 72(3):1891-1899. DOI:10.1128/AEM.72.3.1891-1899.2006.
[26] TURRONI S, VITALI B, BENDAZZOLI C, et al. Oxalate consumption by lactobacilli evaluation of oxalyl-CoA decarboxylase and formyl-CoA transferase activity in Lactobacillus acidophilus[J]. Journal of Applied Microbiology, 2007, 103(5): 1600-1609. DOI:10.1111/j.1365-2672.2007.03388.x.
[27] CHO J G, GEBHART C J, FURROW E, et al. Assessment of in vitro oxalate degradation by Lactobacillus species cultured from veterinary probiotics[J]. American Journal of Veterinary Research, 2015, 76(9): 801-806. DOI:10.2460/ajvr.76.9.801.
[28] KWAK C, JEONG B C, KU J H, et al. Prevention of nephrolithiasis by Lactobacillus in stone-forming rats: a preliminary study[J]. Urological Research, 2006, 34(4): 265-270. DOI:10.1007/s00240-006-0054-4.
[29] MOGNA L, PANE M, NICOLA S, et al. Screening of different probiotic strains for their in vitro ability to metabolise oxalates: any prospective use in humans?[J] Journal of Clinical Gastroenterology, 2014, 48: S91-S95.DOI:10.1097/MCG.0000000000000228.
[30] TURRONI S, BENDAZZOLI C, DIPALO S C F, et al. Oxalatedegrading activity in Biベdobacterium animalis subsp. lactis: impact of acidic conditions on the transcriptional levels of the oxalyl coenzyme A(CoA) decarboxylase and formyl-CoA transferase genes[J]. Applied and Environmental Microbiology, 2010, 76(16): 5609-5620. DOI:10.1128/AEM.00844-10.
[31] REN Z, PAN C, JIANG L, et al. Oxalate-degrading capacities of lactic acid bacteria in canine feces[J]. Veterinary Microbiology, 2011, 152(3/4):368-373. DOI:10.1016/j.vetmic.2011.05.003.
[32] 鐘文婷. 富硒乳酸菌對食源性草酸過多犬尿石癥的預防作用[D]. 南京: 南京農業大學, 2013: 31-43.
[33] LIESKE J C, GOLDFARB D S, DE SIMONE C, et al. Use of a probiotic to decrease enteric hyperoxaluria[J]. Kidney International, 2005,68(3): 1244-1249. DOI:10.1111/j.1523-1755.2005.00520.x.
[34] AL-WAHSH I, WU Y, LIEBMAN M. Acute probiotic ingestion reduces gastrointestinal oxalate absorption in healthy subjects[J]. Urological Research, 2012, 40(3): 191-196. DOI:10.1007/s00240-011-0421-7.
[35] ALTERMANN E, RUSSELL W M, AZCARATE-PERIL M A, et al. Complete genome sequence of the probiotic lactic acid bacterium Lactobacillus acidophilus NCFM[J]. Proceedings of the National Academy of Sciences of the United States of Aemrica, 2005, 102(11):3906-3912. DOI:10.1073/pnas.0409188102.
[36] KLIMESOVA K, WHITTAMORE J M, HATCH M. Biベdobacterium animalis subsp. lactis decreases urinary oxalate excretion in a mouse model of primary hyperoxaluria[J]. Urolithiasis, 2015, 43(2): 107-117.DOI:10.1007/s00240-014-0728-2.
[37] HATCH M, CORNELIUS J, ALLISON M, et al. Oxalobacter sp. reduces urinary oxalate excretion by promoting enteric oxalate secretion[J]. Kidney International, 2006, 69(4): 691-698. DOI:10.1038/sj.ki.5000162.
[38] CAMPIERI C, CAMPIERI M, BERTUZZI V, et al. Reduction of oxaluria after an oral course of lactic acid bacteria at high concentration[J].Kidney International, 2001, 60(3): 1097-1105. DOI:10.1046/j.1523-1755.2001.0600031097.x.
[39] OKOMBO J, LIEBMAN M. Probiotic-induced reduction of gastrointestinal oxalate absorption in healthy subjects[J]. Urological Research, 2010, 38(3): 169-178. DOI:10.1007/s00240-010-0262-9.
[40] GOLDFARB D S, MODERSITZKI F, ASPLIN J R. A randomized,controlled trial of lactic acid bacteria for idiopathic hyperoxaluria[J].Clinical Journal of the American Society of Nephrology, 2007, 2(4): 745-749. DOI:10.2215/CJN.00600207.
[41] SIENER R, BADE D J, HESSE A, et al. Dietary hyperoxaluria is not reduced by treatment with lactic acid bacteria[J]. Journal of Translational Medicine, 2013, 11: 306. DOI:10.1186/1479-5876-11-306.
[42] SAHIN N. Oxalotrophic bacteria[J]. Research in Microbiology, 2003,154(6): 399-407. DOI:10.1016/S0923-2508(03)00112-8.
[43] ABRATT V R, REID S J. Oxalate-degrading bacteria of the human gut as probiotics in the management of kidney stone disease[J]. Advances in Applied Microbiology, 2010, 72: 63-87. DOI:10.1016/S0065-2164(10)72003-7.
[44] KULLIN B, TANNOCK G W, LOACH D M, et al. A functional analysis of the formyl-coenzyme A (frc) gene from Lactobacillus reuteri 100-23C[J]. Journal of Applied Microbiology, 2014, 116(6): 1657-1667.DOI:10.1111/jam.12500.

