高砷高硫難處理金精礦生物預氧化—氰化炭浸提金試驗研究
趙思佳,劉宇利
(1.長沙華時捷環保科技發展股份有限公司,湖南 長沙 410013;2.湖南水利水電職業技術學院,湖南 長沙 410100)
目前,世界上1/3左右的黃金產量來源于難處理金礦石[1-3]。在高砷高硫難處理金礦石中,金以微細粒形式存在,且被黃鐵礦、砷黃鐵礦、毒砂等硫化礦物包裹,與浸出劑不能有效接觸[4-5],再加上部分已氰化浸出的金被碳等有機物吸附,導致金浸出率很低[6]。
高砷高硫難處理金礦石在氰化浸出之前需要進行預處理,使其中的硫化物、碳酸鹽等分解釋放出被包裹的金。難處理金礦石的處理方法主要有浮選—焙燒—氰化浸出法,一段焙燒—氰化浸出法[4],兩段焙燒—氰化浸出法[4],循環流態化焙燒—氰化浸出法[7],催化氧化—氰化浸出法[4],常壓化學氧化—氰化浸出法[4],酸性加壓預氧化—氰化浸出法[4,8],堿性加壓預氧化—氰化浸出法[4],生物預氧化—氰化浸出法[4,9]及焙燒預氧化—硫代硫酸鹽浸出法[10]等。難處理金礦石焙燒預處理過程中會產生大量含砷煙塵,對環境危害較大;加壓預氧化法目前只有酸性加壓預氧化法在工程上有應用[4];生物預氧化法因操作環境友好、安全性高、投資少、工藝過程簡單等優點,已在國內外有較多工程應用[11-14]。
試驗研究了采用生物預氧化—氰化炭浸工藝處理廣西某高砷高硫難處理金精礦,采用的細菌為氧化亞鐵硫桿菌、氧化硫硫桿菌及氧化亞鐵鉤端螺旋菌的混合菌,考察了礦漿濃度、生物預氧化溶液pH、氧化時間及溶氧量對生物預氧化效果的影響,以期為高砷高硫金礦資源的合理開發提供可供借鑒的方法。
1 礦石性質
廣西某高砷高硫難處理金精礦中,金屬礦物以硫化物為主,氧化物較少。硫化物主要是黃鐵礦,其次是毒砂,另有少量或微量黃銅礦、黝銅礦、閃鋅礦等。黃鐵礦和毒砂為金的主要載體礦物。鈦質氧化物多為重礦物鈦鐵礦、金紅石,或鈦鐵礦風化分解的產物白鈦礦及分散質點狀氧化鈦質物等。鐵質氧化物為褐鐵礦。偶見單質礦物自然銅。精礦化學多元素分析結果見表1,物相分析結果見表2。

表1 難處理金精礦化學多元素分析結果 %
*.單位為g/t。
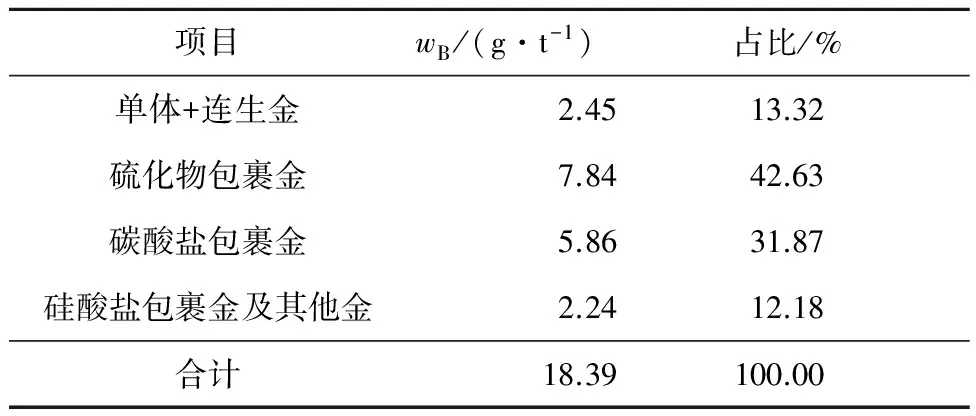
表2 難處理金精礦中金化學物相分析結果
由表1看出:金精礦中的主要有價金屬是金,砷、硫、碳等為有害雜質,影響金的提取,應考慮分離脫除。
由表2看出:金精礦中,金主要以硫化物包裹形式存在,約占42.63%;其次以碳酸鹽包裹形式存在,約占31.87%;有單體及連生金,約占13.32%;而硅酸鹽包裹及其他形式的金質量分數僅占12.18%。這表明直接氰化浸出時金浸出率只能達14%,因此,需對包裹金的硫化物載體進行氧化預處理,對包裹金的碳酸鹽載體進行預處理,使它們釋放出包裹的金。
2 試驗原理與方法
生物預氧化是將包裹金的黃鐵礦、毒砂等礦物氧化溶解,使金從中解離出來。酸性條件下,金可以從碳酸鹽包裹物中解離出來。
氧化黃鐵礦、毒砂等硫化物常用的菌種為氧化亞鐵硫桿菌、氧化硫硫桿菌、氧化亞鐵鉤端螺旋菌等。氧化亞鐵鉤端螺旋菌是一種重要的浸礦微生物,可以將Fe(Ⅱ)氧化成Fe(Ⅲ)。氧化亞鐵硫桿菌可以將Fe(Ⅱ)氧化成Fe(Ⅲ),也可以將還原態硫氧化。氧化硫硫桿菌可以快速氧化單質硫及還原態硫化物。這些菌種組成的混合菌隨氧化電位、溶液pH的變化,各菌種的相對優勢也發生變化。
細菌對礦物的生物氧化作用分直接作用、間接作用及復合作用[15]。直接作用是微生物直接氧化硫化礦。間接作用是微生物代謝產生的化學氧化劑及硫酸與礦物反應。復合作用是指細菌浸礦過程中,既有細菌直接作用又有通過Fe3+氧化的間接作用。
黃鐵礦和毒砂在細菌作用下會發生如下反應[15-16]:

(1)
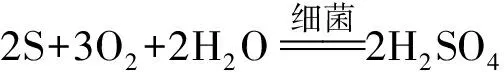
(2)

(3)
(4)
一般認為,金在氰化物溶液中的化學反應[17]為

(5)
氰化炭浸過程中,氰化物浸出金與活性炭吸附金同時進行。礦漿液相中的金始終維持在最低水平有利于加速金的氰化浸出過程[4]。
試驗工藝流程如圖1所示。
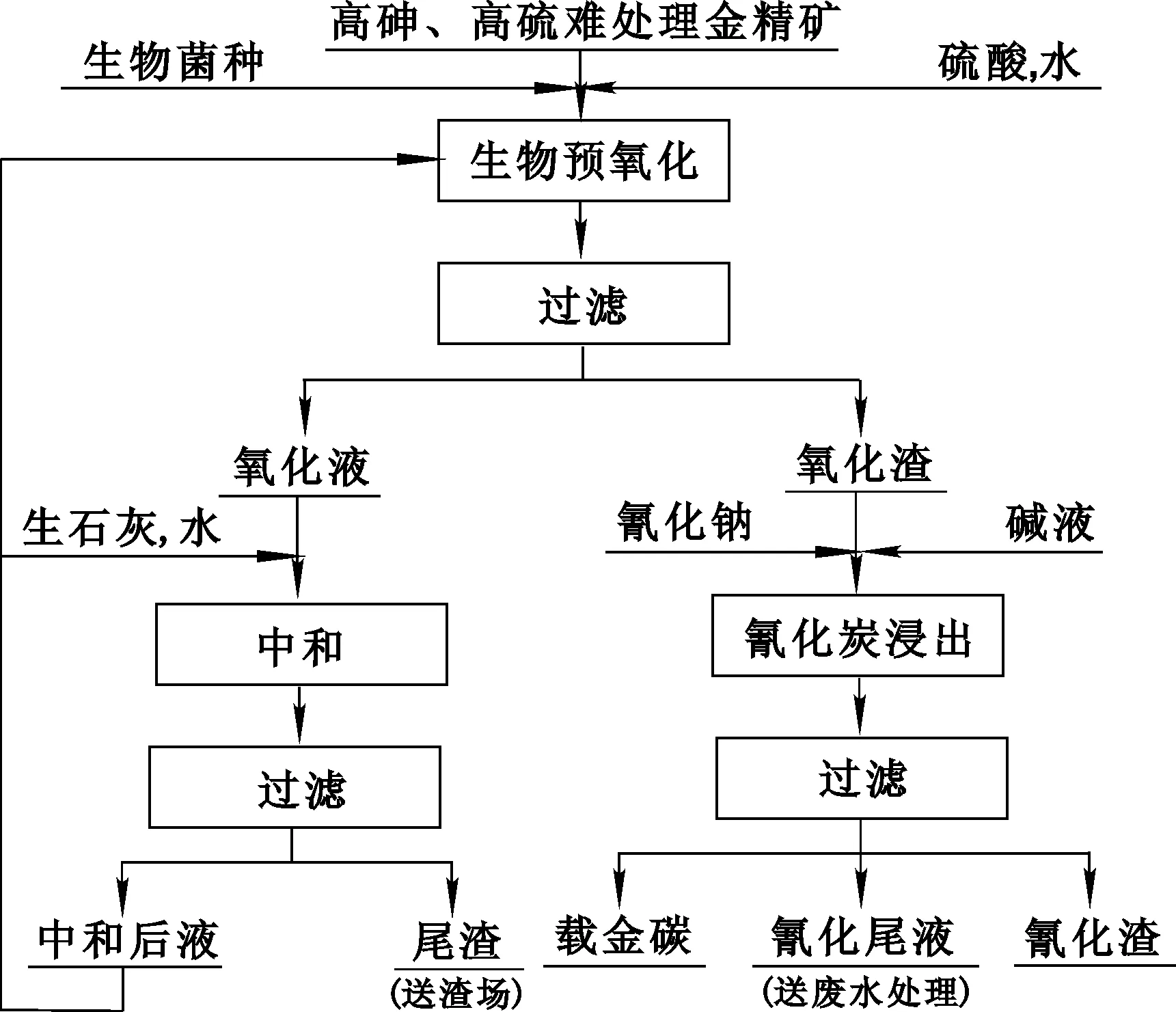
圖1 金精礦生物預氧化—氰化炭浸試驗工藝流程
2.1 生物預氧化
生物預氧化試驗在1 000 mL氧化槽中進行。金精礦粒度-200目占92%以上。菌種取自廣西某礦區礦坑水中,經過一段時間的富集、培養、馴化。菌液每次轉接量為10%,生物預氧化溶液初始pH=2.0。試驗過程中,需要測量溶液pH、氧化完成后溶液體積及砷、銅、鐵、鉛、錳、鎳、鎘等質量濃度。氧化渣烘干后,分析其中S2-質量分數、硫化物氧化率及金質量分數。
2.2 氰化炭浸
氰化炭浸試驗在燒杯中進行。將生物預氧化渣與堿液、氰化鈉溶液及活性炭混合在燒杯中,攪拌,用氫氧化鈉溶液調節溶液pH。
氰化炭浸條件:氰化鈉質量濃度維持在3 g/L左右,溶液pH為10~11,用堿液處理1~2 h,活性炭用量14 g/L,液固體積質量比4∶1,浸出時間24 h,氫氧化鈉用量12.5 kg/t金精礦。氰化炭浸后,過濾,得到氰化浸出渣和氰化浸出液。氰化浸出渣烘干,分析其中金質量分數。氰化浸出液量取體積并分析氰化鈉質量濃度。
2.3 氧化液中和
用生石灰乳中和氧化液。中和后溶液pH達到一定值后,靜置2~4 h,然后過濾,取濾液分析其中金屬離子及非金屬離子質量濃度。
3 試驗結果與討論
3.1 礦漿濃度對生物預氧化效果的影響
試驗條件:反應溫度43 ℃,溶液初始pH=2.0,攪拌速度300 r/min,菌種轉接量10%,氧化時間7 d,氧化過程中不控制生物預氧化溶液pH,溶氧量為6×10-6。礦漿濃度對金精礦生物預氧化效果的影響試驗結果如圖2所示。可以看出:礦漿濃度在12%~16%范圍內,隨礦漿濃度增大,金精礦中硫化物氧化率降低,氧化渣中S2-質量分數增大,金浸出率提高,這說明包裹金的硫化礦物發生溶解,金發生部分解離;礦漿濃度為16%時,金浸出率達80.23%;進一步增大礦漿濃度,金浸出率反而有所下降,這可能是隨礦漿濃度增大,菌種吸收的營養物質減少,使細菌生長、繁殖受到影響,黃鐵礦、毒砂的解離效果變差,致使金浸出率有所降低。綜合考慮,確定高砷高硫難處理金精礦生物預氧化的礦漿濃度以16%為宜。
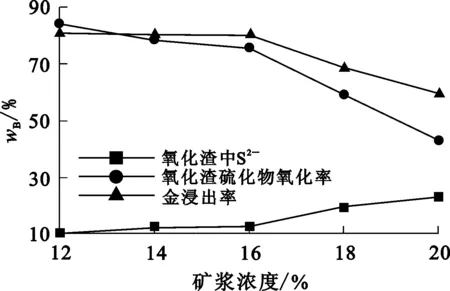
圖2 礦漿濃度對金精礦生物預氧化效果的影響
3.2 溶液pH對生物預氧化效果的影響
試驗條件:溫度43 ℃,礦漿濃度16%,溶液初始pH=2.0,攪拌速度300 r/min,菌種轉接量10%,氧化時間7 d,生物預氧化溶液pH用200 g/L氫氧化鈉溶液調節,溶氧量為6×10-6。溶液pH對金精礦生物預氧化效果的影響試驗結果見表3。

表3 溶液pH對金精礦生物預氧化效果的影響
由表3看出:生物預氧化過程中,不控制溶液pH,金浸出率較高,可達80.21%;隨溶液pH升高,金浸出率降低。這可能是因為菌種在較低pH條件下的生長、繁殖狀況良好,黃鐵礦、毒砂的解離速度較快,有利于金的浸出。由于調節溶液pH所需的氫氧化鈉耗量較大,綜合考慮,生物預氧化過程中可以不控制溶液pH。
3.3 生物預氧化時間對生物預氧化效果的影響
試驗條件:溫度43 ℃,礦漿濃度16%,攪拌速度300 r/min,菌種轉接量10%,溶液初始pH=2.0,氧化過程中不控制溶液pH,溶氧量為6×10-6。生物預氧化時間對金精礦生物預氧化效果的影響試驗結果如圖3所示。

圖3 生物預氧化時間對金精礦生物預氧化效果的影響
由圖3看出:隨生物預氧化時間延長,硫化物氧化率提高,金浸出率提高;生物預氧化7 d時,金浸出率達最大80.13%;進一步延長生物預氧化時間,金浸出率變化不大。綜合考慮,確定生物預氧化時間以7 d為宜。
3.4 溶氧量對生物預氧化效果的影響
試驗條件:溫度43 ℃,礦漿濃度16%,攪拌速度300 r/min,菌種轉接量10%,氧化時間7 d,溶液初始pH=2.0,氧化過程中不控制生物預氧化溶液pH。溶氧量對金精礦生物預氧化效果的影響試驗結果如圖4所示。
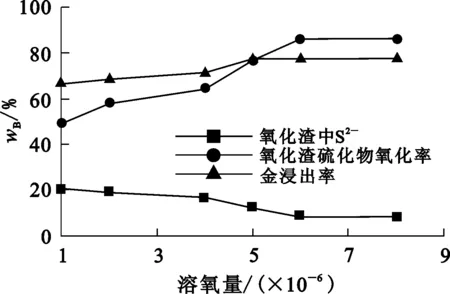
圖4 溶氧量對金精礦生物預氧化效果的影響
由圖4看出:隨溶液中溶氧量增加,硫化物氧化率增大,金浸出率提高;溶液中溶氧量達5×10-6時,金浸出率達77.34%;進一步增大溶氧量,金浸出率基本保持不變,硫化物氧化率也無明顯變化。這說明,當溶氧量為5×10-6時,能夠滿足生物預氧化反應的需氧量,因此,溶氧量以控制在5×10-6為宜。
4 綜合試驗
根據上述試驗結果,確定生物預氧化最佳試驗條件為:溫度43 ℃,礦漿濃度16%,攪拌速度300 r/min,溶氧量5×10-6,細菌轉接量10%,氧化時間7 d,溶液初始pH=2.0,氧化過程不控制溶液pH。最佳條件下的綜合試驗結果見表4,氧化渣氰化炭浸試驗結果見表5。
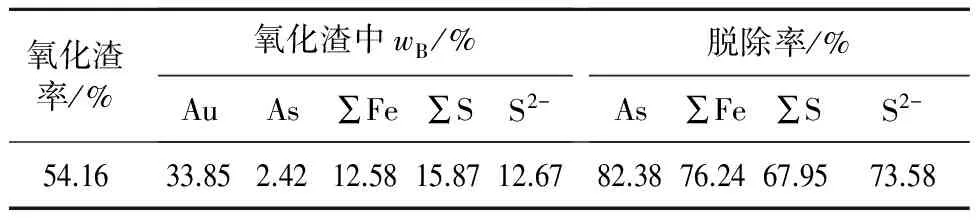
表4 生物預氧化綜合試驗結果
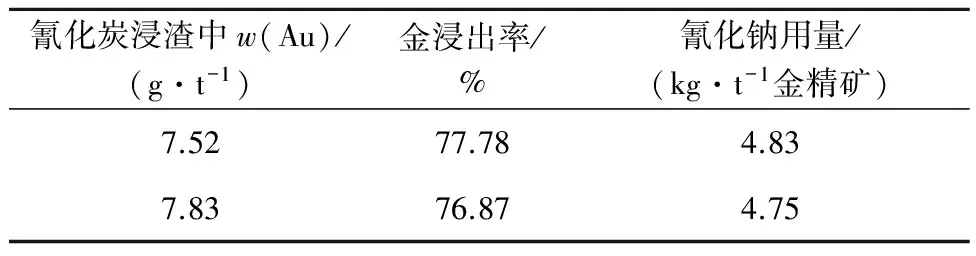
表5 氧化渣氰化炭浸試驗結果
由表4、5看出,高砷高硫難處理金精礦采用生物預氧化—氰化炭浸工藝處理:金浸出率達77.78%,砷、鐵、硫脫除率分別達82.38%,76.24%,67.95%;氰化炭浸渣中金質量分數降至7.52 g/t,氰化鈉用量約為4.8 kg/t金精礦。
5 氧化液中和處理
高砷高硫難處理金精礦生物預氧化得到的氧化液用石灰乳中和處理,在pH=6.5條件下靜置3 h,過濾后得到中和后液,其成分見表6。
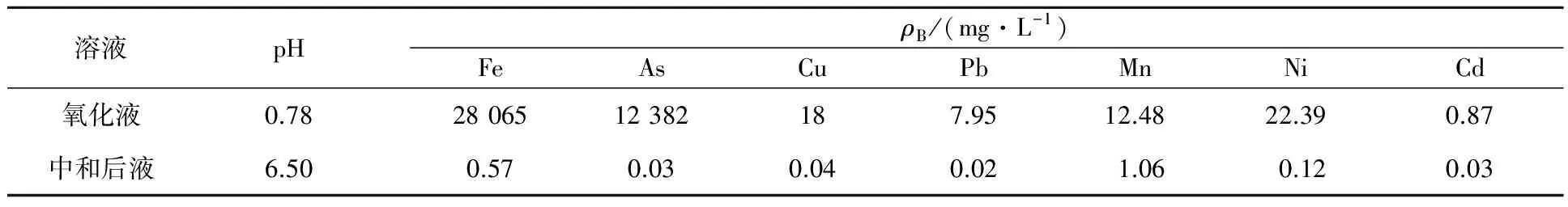
表6 氧化液及中和后液的pH及成分
由圖6看出,石灰乳中和后的氧化液中各有害金屬離子及非金屬離子質量濃度均符合《污水綜合排放標準》(GB 8978—1996)要求,可返回系統使用。
6 結論
廣西某高砷高硫難處理金精礦采用生物預氧化—氰化炭浸工藝提取金是可行的,適宜條件下,金浸出率達77.78%。生物預氧化得到的氧化液用生石灰乳中和處理,pH調至6.5后靜置3 h,過濾后得到的溶液中各種有害金屬離子及非金屬離子含量均符合《污水綜合排放標準》(GB 8978—1996)要求,可返回系統使用,工藝基本無廢水排放。
[1] 李廷梁.俄羅斯難浸金礦的生物冶金技術[J].貴金屬,1998,19(1):54-56.
[2] 許鵬秋.難浸金礦石采用Polycom高壓輥磨礦的進展[J].國外黃金參考,1997(3):8-13.
[3] 張永濤.中國黃金礦產資源開發及礦產品供需形勢分析[J].中國礦業,2009,18(2):8-11.
[4] 黃禮煌.金銀提取技術[M].北京:冶金工業出版社,2001:214-215,274-279,336-349.
[5] 楊顯萬,沈慶峰,郭玉霞,等.微生物濕法冶金[M].北京:冶金工業出版社,2003:165-170.
[6] 吳昊隼.金礦石中劫金碳的微生物鈍化[J].國外黃金參考,1995(8):18-22.
[7] 李云,王云,袁朝新,等.難處理復雜金礦循環流態化焙燒提金技術[J].有色金屬(冶煉部分),2011(3):31-33.
[8] 徐忠敏,翁占平,國洪柱.復雜難處理金精礦加壓氧化預處理工藝試驗研究[J].黃金,2017,38(2):54-57.
[9] 劉志樓,楊天足.難處理金礦的處理現狀[J].貴金屬,2014,35(1):79-89.
[10] 高鵬,唐道文,唐攢浪,等.用硫代硫酸鈉從某卡林型金礦石中浸出金試驗研究[J].濕法冶金,2017,36(1):12-15.
[11] 李奇偉,陳奕然,陳明軍,等.云南某高硫難處理金精礦堿性加壓預氧化—氰化浸金試驗研究[J].云南冶金,2015,44(4):22-25.
[12] BRIERLRY C.Biohydrometallurgical prospects[J].Hydr-ometallurgy,2010,104(3):324-328.
[13] 李俊萌.難處理金礦石預處理方法研究現狀及發展趨勢[J].稀有金屬,2003,27(4):478-481.
[14] 姚國成,阮仁滿,溫建康.難處理金礦的生物預氧化技術及工業應用[J].礦產綜合利用,2003(1):33-39.
[15] 《浸礦技術》編輯委員會.浸礦技術[M].北京:原子能出版社,1994:427-430.
[16] 訾建威,楊洪英,鞏恩普,等.細菌氧化預處理含砷難處理金礦的研究進展[J].貴金屬,2005,26(1):66-70.
[17] 孫戩.金銀冶金[M].北京:冶金工業出版社,1998:130-135.

