PiCCO指導下的液體復蘇對合并心肌損傷感染性休克患者預后的影響
錢志賢,宋 佳,周娟娣,龔仕金,明自強,劉丹平,葉 斌,宋飛珍
心肌損傷是嚴重膿毒癥和感染性休克最常見的并發癥之一[1]。合并心肌損傷感染性休克患者的液體復蘇更加復雜,更需要動態評估患者的血流動力學狀態、心功能及肺水的變化。脈搏指示劑連續心排血量(pulse indicator continuous cadiac output,PiCCO)是一種將熱稀釋技術和脈搏輪廓分析技術結合起來的微創血流動力學監測方法,能通過床旁監測獲得多項反映患者容量、肺水及心功能參數。已經有多項研究表明[2~4],PiCCO在重癥患者的液體復蘇、液體管理、利尿劑應用、治療效果的評價等方面具有重要作用。本研究應用PiCCO監測指導合并心肌損傷的感染性休克患者早期液體復蘇,探討其對患者預后的影響。
1 資料和方法
1.1 一般資料:選取2014年4月至2016年4月收治于本院ICU的感染性休克患者60例,其中男33例,女27例,年齡26~94歲,平均(69.43±13.84)歲。入選標準:年齡≥18歲;符合2012嚴重膿毒癥與感染性休克治療國際指南(SSC 2012)[5]中感染性休克的診斷標準;存在下列任何一項心肌損傷的證據:血清肌鈣蛋白I(troponin I,TnI)>0.1μg/L,血清B型腦鈉肽(brain natriuretic peptide,BNP)>100ng/L。排除標準:年齡<18歲、孕婦、惡性腫瘤等終末期疾病者、嚴重肝功能衰竭、慢性腎臟病、急性冠狀動脈綜合征、慢性心力衰竭等基礎心臟疾病。本研究符合醫學倫理標準,并通過醫院倫理委員會批準,所有治療及監測獲得簽署知情同意書。
1.2 方法:
1.2.1 本研究為前瞻性隊列研究,入選后對所有患者進行抗休克治療(液體復蘇、血管活性藥物、抗菌藥物、機械通氣等),所有患者經頸內靜脈或鎖骨下靜脈置入上腔靜脈導管(ARROW導管,美國ARROW公司)進行中心靜脈壓(central venous pressure,CVP)測定,并抽取中心靜脈血標本進行血氣分析檢查(IL GEM3000,美國GEM公司)。PiCCO組經股動脈放置PiCCO導管,連接監護儀(德國PULSION公司)進行血流動力學監測。
1.2.2 干預方法:入選患者根據數字表法隨機分成兩組:PiCCO組和對照組各30例。PiCCO組根據胸腔內血容積指數(intrathoracic blood volume index,ITBVI)及心指數(cardiacindex,CI)指導液體復蘇,使ITBVI達到850~1000ml/m2且CI≥2.5L/min·m2;如ITBVI>1000ml/m2但CI仍<2.5L/min·m2或左心收縮指數(dPmax)降低,則使用多巴酚丁胺或米力農調節心功能;根據體循環阻力指數(systemic vascularresistance index,SVRI)調節去甲腎上腺素(NE)劑量以平穩維持平均動脈壓(mean arterial pressure,MAP)≥65mmHg;根據血管外肺水指數(extravascular lung water index,EVLWI)指導液體的選擇及利尿劑的應用;如中心靜脈血氧飽和度(central venous oxygen saturation,ScvO2)<70%且紅細胞壓積(hematocrit,HCT)<30%,則輸注紅細胞使HCT≥30%。
對照組按照SSC 2012給予早期目標導向治療(earlygoal_directed therapy,EDGT)集束化方案復蘇[5]。對存在低血壓或高乳酸血癥患者30分鐘內給予1000ml晶體液或者500ml膠體液,直到CVP≥8mmHg;如MAP<65mmHg,使用NE維持MAP≥65mmHg;如ScvO2<70%且HCT<30%,則輸注紅細胞使HCT≥30%。6h液體復蘇治療目標為:CVP:8~12mmHg;MAP≥65mmHg;ScvO2≥70%;尿量≥0.5ml/kg·h。
1.2.3 數據采集和記錄:所有入選患者在診斷為感染性休克時及復蘇后第6h、24h、48h、72h記錄以下數據:TnI、BNP、MAP、CVP、ScvO2、白細胞計數(WBC)、C反應蛋白(CRP)、動脈血乳酸;復蘇液體量、尿量、液體正平衡量。
本研究主要終點為28d病死率。次要終點為第3d序貫器官衰竭(sequential organ failure assessment,SOFA)評分,存活不滿3d者記錄死亡當天SOFA評分;機械通氣時間;住ICU時間。

2 結果
2.1 兩組患者一般臨床資料比較:兩組患者年齡、性別、急性生理學與慢性健康狀況Ⅱ(Acute Physiology and ChronicHealth Evaluation II,APACHEⅡ)評分等一般臨床資料差異均無統計學意義(P>0.05),見表1。
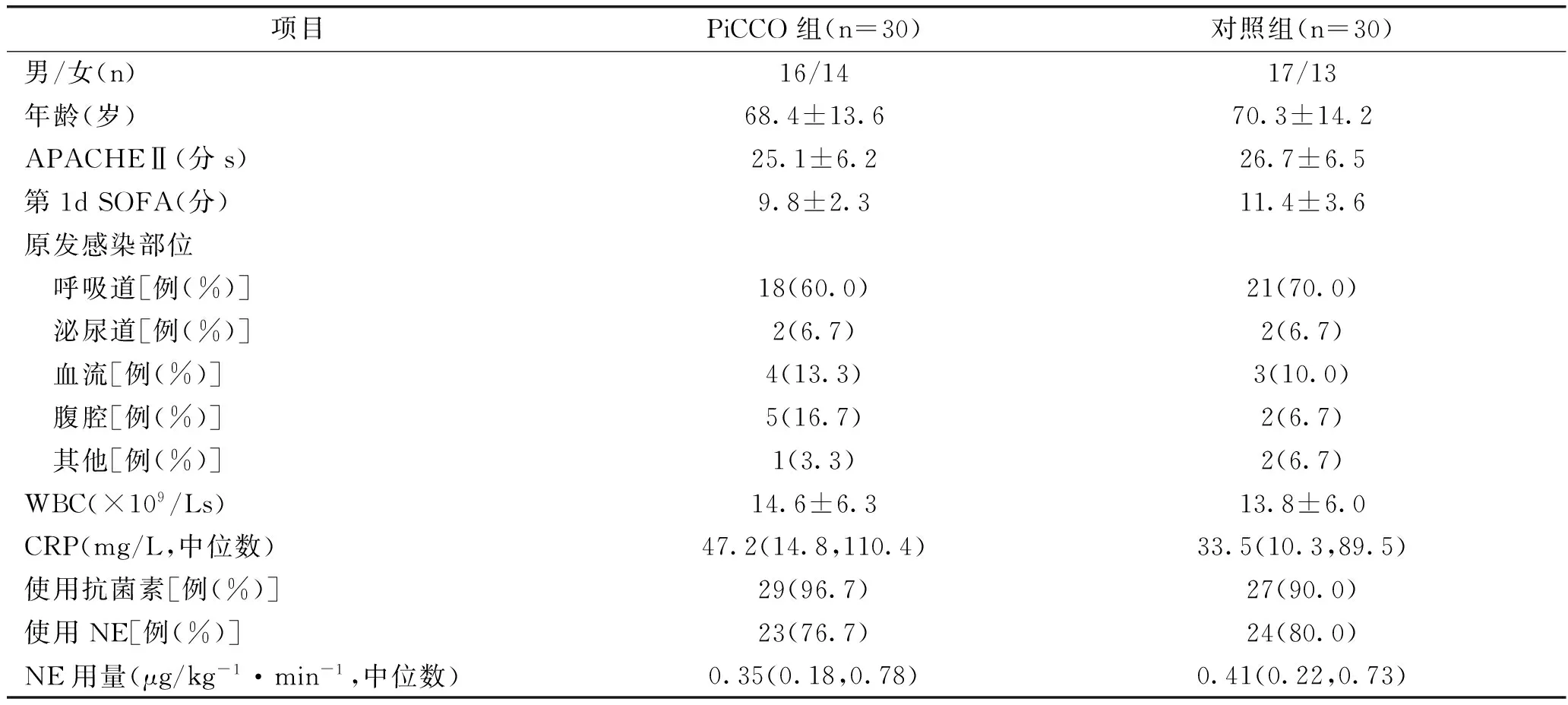
表1 兩組合并心肌損傷感染性休克患者的一般臨床資料比較
2.2 兩組患者液體復蘇前后血流動力學參數、氧代謝參數及心功能參數比較:PiCCO組在復蘇第24h、48h和72h的BNP均低于對照組,差異有統計學意義(均P<0.05)。PiCCO組在復蘇第48h及72h的CVP低于對照組,差異有統計學意義(均P<0.05)。

表2 兩組合并心肌損傷感染性休克患者復蘇前后各項指標比較
注:與PiCCO組同一時間點比較*P<0.05
2.3 兩組患者復蘇液體量、尿量及液體正平衡量比較:PiCCO組在復蘇第24h、48h及72h的復蘇液體量和液體正平衡量均少于對照組,差異具有統計學意義(均P<0.05),見表3。
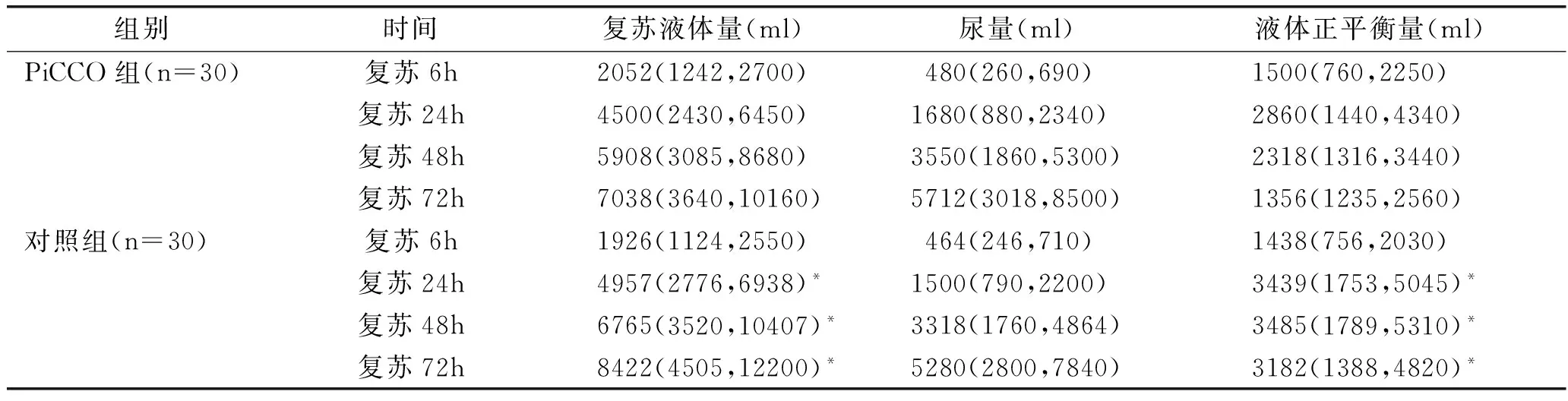
表3 兩組合并心肌損傷感染性休克患者復蘇前后液體量及尿量比較[M(P25,P75)]
注:與PiCCO組同一時間點比較*P<0.05
2.4 兩組患者的終點比較:PiCCO組第3d SOFA評分、機械通氣時間、住ICU時間均低于對照組,差異有統計學意義(均P<0.05)。兩組28d病死率差異無統計學意義(P>0.05),生存曲線比較差異無統計學意義(log_rank=0.67,P>0.05),見表4。

表4 兩組合并心肌損傷感染性休克患者終點比較
注:與對照組比較*P<0.05
3 討論
膿毒癥是由宿主對感染的反應失調引起的危及生命的器官功能障礙,感染性休克是膿毒癥的一種,伴隨著組織低灌注的發生,具有很高的發病率及死亡率[6]。心臟是感染性休克最常見的受累器官[7],有研究表明[8,9],無基礎心臟疾病的感染性休克患者左心收縮功能減退非常常見,且發生率隨時間增加而增加,感染性休克第1天發生率約40%,第3天約60%,而一旦合并心肌損傷可加重疾病的嚴重程度,多器官功能障礙綜合征(multiple organ dysfunction syndrome,MODS)的發生率及死亡風險也將大大增加。盡管目前缺乏統一的診斷標準,但多項研究[10~12]表明膿毒癥相關的心肌損傷有以下3個特點:左右心室的急性擴張、左室射血分數(left ventricular ejection fraction,LVEF)下降、心功能在7~10天后恢復正常。
早期識別膿毒癥相關的心肌損傷,對制定合適的治療方案是至關重要的。多項研究表明[13,14],TnI能反映膿毒癥心肌損傷程度,且其升高預示著更高的疾病嚴重程度以及不良的臨床預后。BNP作為一種具有利尿、擴血管、抑制腎素和醛固酮的釋放等作用的神經內分泌激素,最初被用于充血性心力衰竭的診斷和危險分層。在膿毒癥和感染性休克患者中的研究[15,16]也表明,BNP在膿毒癥和感染性休克患者中普遍升高,且升高水平與膿毒癥心肌損傷的發生密切相關。由于肌鈣蛋白和BNP水平變化與膿毒癥心肌損傷的程度有良好相關性,故本研究將其作為膿毒癥心肌損傷的診斷指標。
除了控制感染源和應用合適的抗生素以外,感染性休克治療的關鍵環節是及時充足的液體復蘇和血流動力學支持[17]。需要根據不同患者制定個體化的液體策略,此時連續動態的容量評估以及心血管功能的監測顯得非常重要。PiCCO技術能獲得一系列反映前負荷、心功能、后負荷及肺水的參數。熱稀釋技術測得的全心舒張末容積指數(global enddiastolic volume index,GEDVI)和ITBVI兩個容量指標被認為是敏感、可重復,且不受呼吸運動和心肌順應性影響的反映心臟前負荷的指標[18~20]。EVLWI作為定量評估肺水腫的指標,被認為與感染性休克患者臨床預后密切相關[21]。本研究中兩組患者復蘇6h后的乳酸水平均有明顯下降,且ScvO2均達標,說明兩組患者都接受了有效的早期液體復蘇,組織低灌注得到改善,此時兩組復蘇液體量無明顯差異。此外,本研究也發現PiCCO組24~72h的復蘇液體量及液體正平衡量明顯低于對照組。液體正平衡是感染性休克患者死亡的獨立危險因素,液體正平衡越多,持續時間越久,患者預后越差[22]。特別是初步液體復蘇后,判斷患者是否能從進一步的液體治療中獲益應基于詳細的臨床檢查以及更先進的血流動力學監測。PiCCO監測的容量、肺水等參數能指導“滴定式”的液體治療,SVV能動態評估容量反應性,用更少的液體達到改善組織灌注的目標,減少液體過負荷的風險。本研究中對照組復蘇后第24h~72h的BNP水平明顯高于PiCCO組也說明EGDT指導的液體復蘇可能導致更多容量過負荷。有研究[23]顯示,容量過負荷時隨著左室充盈壓的升高及右心功能障礙的加重,BNP水平也隨之升高。
先前有研究[24]報道,相比較傳統的EGDT集束化治療方案,PiCCO指導的改良集束化治療能減輕感染性休克患者的疾病嚴重程度,更準確地指導液體復蘇,減少肺水,縮短機械通氣和住ICU時間,本文與之相似。但是對于合并心肌損傷的感染性休克患者,PiCCO是否能改善患者臨床預后目前尚缺乏相關研究。已經有多項研究證明[25~27],CVP不是一個評估容量狀態的可靠指標,亦不能預測容量反應性程度。感染性休克早期,即使達到8~12mmHg的CVP目標,患者仍可能存在容量不足或過負荷,而這兩種情況都與更差的預后密切相關。
本研究也存在一些不足:首先,由于設備和技術的原因,本研究中沒有使用超聲心動圖評估心功能,其次,本研究為小樣本量研究,兩組患者的主要終點未發現統計學差異,仍需設計完善的大樣本量研究來證實PiCCO指導下的液體復蘇對合并膿毒癥心肌損傷的感染性休克患者病死率的影響。
綜上所述,本研究顯示,相比較傳統EGDT方案,PiCCO指導下的血流動力學管理能優化合并心肌損傷感染性休克患者的液體復蘇,減少液體過負荷的風險,并減輕器官功能障礙的程度,縮短機械通氣時間和住ICU時間。
[1]Antonucci E, Fiaccadori E, Donadello K, et al. Myocardial depression in sepsis: From pathogenesis to clinical manifestations and treatment[J]. J Crit Care,2014,29(4):500-511.
[2]唐坎凱,溫曉紅,董朝暉,等.感染性休克患者PiCCO指導早期液體復蘇的臨床研究[J].中華急診醫學雜志,2012,21(009):1039-1041.
[3]Liu X, Ji W, Wang J, et al. Application strategy of PiCCO in septic shock patients[J]. Experimental and therapeutic medicine,2016,11(4):1335-1339.
[4]伊敏,么改琦,郭向陽.脈搏指示連續心排血量監測下膿毒性休克患者心功能變化的前瞻性研究[J].中華危重病急救醫學,2015,27(1):22-27.
[5]Dellinger RP, Levy MM, Rhodes A, et al. Surviving sepsis campaign: international guidelines for management of severe sepsis and septic shock: 2012[J]. Crit CareMed,2013,41(2):580-637.
[6]Singer M, Deutschman CS, Seymour CW, et al. The third international consensus definitions for sepsis and septic shock (sepsis_3)[J]. JAMA,2016,315(8):801-810.
[7]Vieillard_Baron A, Cecconi M. Understanding cardiac failure in sepsis[J]. Intensive care Med,2014,40(10):1560.
[8]Vieillard_Baron A, Prin S, Chergui K, et al. Hemodynamic instability in sepsis: bedside assessment by Doppler echocardiography[J]. Am J Respir Crit Care Med,2003,168(11):1270-1276.
[9]Bouhemad B, Nicolas_Robin A, Arbelot C, et al. Isolated and reversible impairment of ventricular relaxation in patients with septic shock[J]. Critical care Med,2008,36(3):766-774.
[10]Parker MM, Shelhamer JH, Bacharach SL, et al. Profound but reversible myocardial depression in patients withseptic shock[J]. Ann Intern Med,1984,100(4):483-490.
[11]Kakihana Y, Ito T, Nakahara M, et al. Sepsis_induced myocardial dysfunction: pathophysiology andmanagement[J]. J Intensive Care,2016,4(1):22.
[12]Sato R, Nasu M. A review of sepsis_induced cardiomyopathy[J]. J Intensive Care,2015,3(1):48.
[13]Landesberg G, Jaffe AS, Gilon D, et al. Troponin elevation in severe sepsis and septic shock: the role of left ventricular diastolic dysfunction and right ventricular dilatation[J]. Critical care medicine,2014,42(4):790-800.
[14]Masson S, Caironi P, Fanizza C, et al. Sequential N_terminal pro_B_Type natriuretic peptide and high_sensitivity cardiac troponin measurements during albumin replacement in patients with severe sepsis or septic shock[J]. Crit Care Med,2016,44(4):707-716.
[15]Papanikolaou J, Makris D, Mpaka M, et al. New insights into the mechanisms involved in B_type natriuretic peptide elevation and its prognostic value in septic patients[J]. Crit Care,2014,18(3):R94.
[16]Post F, Weilemann LS, Messow CM, et al. B_type natriuretic peptide as a marker for sepsis_induced myocardial depression in intensive care patients[J]. Crit Care Med,2008,36(11):3030-3037.
[17]Vincent JL, De Backer D. Circulatory shock[J]. N Engl J Med,2013,369(18):1726-1734.
[18]Compton F, Vogel M, Zidek W, et al. Changes in volumetric hemodynamic parameters induced by fluid removal on hemodialysis in critically ill patients[J]. Ther Apher Dial,2015,19(1):23-29.
[19]Kapoor PM, Bhardwaj V, Sharma A, et al. Global end_diastolic volume an emerging preload marker vis_a_vis other markers_Have we reached our goal[J]? Ann Card Anaesth,2016,19(4):699.
[20]徐永昊,劉曉青,何為群,等.胸腔內血容量指數在感染性休克患者液體管理中的應用[J].中國危重病急救醫學,2011,23(8):462-466.
[21]Zhang Z, Lu B, Ni H. Prognostic value of extravascular lung water index in critically ill patients: a systematic review of the literature[J]. J Crit Care,2012,27(4):421-428.
[22]Garzotto F, Ostermann M, Martín_Langerwerf D, et al. The dose response multicentre investigation on fluid assessment (DoReMIFA) in critically ill patients[J]. Crit Care,2016,20(1):196.
[23]Celik G, Silinou E, Vo Van C, et al. PlasmaBNP, a useful marker of fluid overload in hospitalized hemodialysis patients[J]. Hemodial Int,2012,16(1):47-52.
[24]盧年芳,鄭瑞強,林華,等.PiCCO指導下集束化治療感染性休克的臨床研究[J].中華危重病急救醫學,2014,26(1):23-27.
[25]Marik PE, Monnet X, Teboul JL. Hemodynamic parameters to guide fluidtherapy[J]. Ann Intensive Care, 2011,1(1):1.
[26]Magder S. Understanding central venous pressure: not a preload index[J]. Curr Opin Crit Care,2015,21(5):369-375.
[27]Boyd J H, Forbes J, Nakada T, et al. Fluid resuscitation in septic shock: a positive fluid balance and elevated central venous pressure are associated with increased mortality[J]. Crit Care Med,2011,39(2):259-265.

