院前預通知流程改善急性缺血性卒中患者血管內治療的預后
張美霞,陳智才,張睿婷,史飛娜,樓敏
卒中已成為我國國民第一致死病因[1-2]。顱內大血管閉塞(large vessel occlusion,LVO)導致的急性缺血性卒中(acute ischemic stroke,AIS)再通率僅13%~18%,90 d死亡率和致殘率達21%和68%[3]。臨床指南推薦LVO患者行血管內治療[4],但其效益具有時間依賴性。研究表明,LVO患者的起病至再灌注時間每縮短1 min,壽命可增加4.2 d[5]。
既往靜脈溶栓研究表明,優化急救系統(emergency medical service,EMS)的院前預通知流程(prehospital notification procedure,PNP)不僅有助于AIS患者在更短時間內接受治療[6-8],并且可以改善臨床預后[9]。限于醫療衛生服務質量和院前基礎設施條件,PNP沒有廣泛開展。一項意大利的研究發現,仍有43%的患者通過EMS送至醫院急診室但未提前通知急診室[10]。在中國,僅有8.9%的AIS患者選擇通過EMS至醫院接受治療[11]。
目前,PNP是否可改善LVO患者血管內治療的預后尚不明確。本卒中中心自2015年3月開始與杭州市120急救系統合作,建立PNP,旨在快速評估、轉運和治療AIS患者。本研究旨在通過分析我院前瞻性收集的血管內治療患者的臨床和時間追蹤資料,來驗證優化的PNP是否可以縮短血管內治療的院內延誤時間,從而改善預后。
1 對象與方法
1.1 研究對象 納入于浙江大學醫學院附屬第二醫院連續收集的2015年3月-2017年3月的急性LVO并接受血管內治療,包括橋接取栓和單純取栓的患者。入組標準如下:①缺血性卒中起病8 h內。②基線電子計算機斷層掃描血管成像(computed tomography angiography,C TA)或磁共振血管成像(magnetic resonance angiography,MRA)見以下動脈閉塞:頸內動脈(internal carotid artery,ICA),大腦中動脈(middle cerebral artery,MCA)M1、M2段,基底動脈(basilar artery,BA),大腦后動脈(posterior cerebral artery,PCA)P1段以及大腦前動脈(arteria cerebral artery,ACA)A1段。③家屬簽訂知情同意書。排除3個月后失訪的患者。
記錄患者的基線資料,包括年齡、性別、溶栓前美國國立衛生研究院卒中量表(National Institutes of Health Stroke Scale,NIHSS)評分,卒中相關危險因素[高血壓、糖尿病、冠狀動脈粥樣硬化性心臟病、既往卒中或短暫性腦缺血發作(transient ischemic attack,TIA)病史],院內時間追蹤等。時間追蹤主要包括起病至入院時間、起病至再灌注時間、入院至影像時間、穿刺至再灌注時間和入院至再灌注時間(door to reperfusion time,DRT),同時記錄起病至溶栓時間(onset to needle time,ONT)、入院至溶栓時間、影像至溶栓時間、溶栓至穿刺時間。
1.2 研究方法
1.2.1 多模式影像學檢查 CT灌注掃描采用64排螺旋CT(德國西門子),檢查序列包括頭顱CT平掃,全腦容積灌注CT掃描。以6 ml/s的速度注射60 ml對比劑,后續以6 ml/s的速度推注20 ml生理鹽水。掃描參數:z軸100 mm,80 kV,120 mA,延遲4 s開始,掃描總時間為74.5 s,共采集26個時間點,層厚10 mm,準直32 mm×1.2 mm。
MRA檢查在配備八通道頭線圈的3.0T系統(Signa Excite HD,美國通用電氣公司)上進行掃描。參數:TR/TE=20/3.2 ms,翻轉角度=15°,視野=24 cm×24 cm,矩陣大小=320×224,層厚=1.4 mm,32×3層,掃描時間226 s。
1.2.2 治療方法 靜脈溶栓治療均選用德國勃林格英格翰國際公司生產的重組組織型纖溶酶原激活劑(recombinant tissue plasminogen activator,rt-PA),溶栓劑量按照指南規定的0.9 mg/kg,最大劑量90 mg,首劑為10%靜脈推注,剩余90%微泵注射。
血管內治療包括靜脈溶栓橋接取栓和單純取栓[12]。通過全腦血管造影檢查,如果造影中發現責任動脈未再通,則通過SolitaireTM血流重建裝置(美敦力公司,美國)取出取栓,取栓次數不超過5次。手術過程中根據臨床需要使用支架、球囊擴張、抗血小板藥物等。
1.2.3 院前流程EMS院前預通知流程(PNP):對120 EMS工作人員進行缺血性卒中疾病的培訓,指導其根據面、臂、言語、時間(Face Arm Speech Time,FAST)評分量表篩選可疑缺血性卒中患者,并在接到患者后轉運至我院的過程中,電話提前通知我院卒中小組。我院溶栓小組通過電話獲取患者身份信息,起病時間和簡要病史,提前在急診建立病歷檔案,開處檢驗單和檢查單,預約登記CT灌注成像(CT perfusion,CTP),聯系神經介入醫生和導管室做好準備。患者到達急診后留取血液標本,行CTP檢查,若為大血管閉塞,且無靜脈溶栓禁忌證,則行靜脈溶栓橋接動脈取栓;若有溶栓禁忌證,則直接送至導管室進行單純取栓。
EMS但無院前預通知流程(Non-PNP):通過120 EMS到達急診室,但未進行電話提前通知,由預檢臺分診、急診神經內科醫生評估后通知溶栓小組,并開處檢驗單和檢查單。隨后溶栓小組啟動血管內治療流程,并聯系神經介入醫生和導管室,同時急診護士留取血液標本,再行影像檢查等。非EMS(Non-EMS):通過其他途徑如私家車、出租車等自行到達急診室。本研究故此將患者分為PNP組、Non-PNP組和Non-EMS組。
1.3 結局的評估血管成功再通標準[13]:使用改良腦梗死溶栓評分(modified thrombolysis in cerebral infarction,mTICI)評定術后血管是否成功再通,mTICI達到2b和3級定義為血管再通。
出血轉化的評估:由再灌注治療后24 h內復查的磁共振或CT影像評估出血轉化。依據歐洲協作性急性卒中研究(European Cooperative Acute Stroke Study,ECASS)Ⅱ標準[14],將癥狀性出血定義為24 h內復查的磁共振或CT影像見出血,并且由出血引起的NIHSS評分增加超過4分。
治療后3個月門診或電話隨訪評定患者改良Rankin量表(modified Rankin Scale,mRS)評分,mRS評分≤2分定義為預后良好。
1.4 統計學處理 應用SPSS 17.0統計學軟件,計量資料符合正態分布,以()表示,兩組間的比較采用獨立樣本t檢驗,多組間的比較采用單因素方差分析;計量資料不符合正態分布則用四分位間距表示,兩組間和多組間的比較采用非參數分析。計數資料以(%)表示,兩組間比較采用χ2檢驗或Fisher精確檢驗,多組間比較采用χ2檢驗。3個月預后良好多元回歸分析采用二元Logistics回歸,P<0.10進入回歸方程。P<0.05為差異有統計學意義。
2 結果
2.1 基本資料 共112例患者符合納入標準,排除2例失訪患者,最終110例患者進入分析。其中,女性49例(44.5%),平均年齡(68±12)歲,單純取栓23例(20.9%),平均起病到再灌注時間為(364±133)min,DRT(174±64)min,基線NIHSS為16(12~19)分,預后良好38例(34.5%)。其中,Non-EMS組有19例(17.3%),PNP組有21例(19.1%),Non-PNP組有70例(63.6%)。
2.2 PNP組、Non-PNP組和Non-EMS組之間的單因素比較 對三組患者進行單因素方差分析發現,PNP組、Non-PNP組和Non-EMS組除入院至溶栓時間和入院至影像時間外,三組間其他因素比較差異無統計學意義(表1)。PNP組預后良好9例(42.9%),Non-PNP組22例(31.4%),Non-EMS組7例(36.8%),比較差異亦無統計學意義(P=0.611)(表1,圖1)。
進一步兩兩比較發現:與Non-EMS組相比,PNP組的入院至溶栓時間、入院至影像時間、影像至溶栓時間和溶栓至穿刺時間更短(P<0.05)。并且,與Non-EMS組相比,PNP組的起病至溶栓時間和DRT趨于更短(P<0.05),而穿刺至再灌注時間卻無統計學差異。Non-PNP組較Non-EMS組的入院至溶栓時間、入院至影像時間有較短的趨勢(P<0.05)。與Non-PNP組相比,PNP組的DRT、入院至溶栓時間、入院至影像時間較短(P<0.05),其余因素比較差異則無統計學意義(表1)。
2.3 3個月預后的單因素分析 與預后良好組相比,預后不良組基線NIHSS更高、高血壓比例較高、基線收縮壓較高,入院至影像時間、起病至再灌注時間和DRT均較長,比較差異有統計學意義(P<0.05)。而單因素分析時PNP在不同預后組之間差異無統計學意義(表2)。
2.4 3個月預后的多因素分析 以Non-PNP作為參照,校正基線NIHSS、高血壓和基線收縮壓,多因素分析結果顯示:PNP是急性LVO患者血管內治療3個月預后良好的獨立影響因素[優勢比(odds ratio,OR)3.653,95%可信區間(confidence interval,CI)1.085~12.301,P=0.037)。二元Logistic回歸模型中納入DRT后,DRT是3個月預后良好的獨立影響因素(OR0.981,95%CI0.968~0.994,P=0.005)(表3)。
3 討論
本研究共有82.7%的LVO患者通過EMS入院,但其中啟動PNP流程僅占23.1%。我們發現PNP可以縮短DRT,并且改善LVO患者血管內治療后的3個月臨床預后。
本研究發現PNP能縮短DRT,表明LVO患者通過PNP可獲得更加快速的治療,減少院內延誤。該結果與Sin Kyu Kim團隊[8]和Cheryl B. Lin團隊[15]關于PNP的回顧性分析結果一致,他們也發現,PNP可以縮短入院至溶栓時間,減少院內延誤。不過Ying Xian等[16]得到不一致的研究結果,他們發現EMS提前通知溶栓團隊并不能降低入院至溶栓時間。該陰性的結果可能是由于他們中心在接到EMS提前通知后,僅報告他們將如何處理,而沒有積極做好相關準備事項,如事先與相關科室進行溝通協調并做好準備。本中心PNP的有效性可能歸因于溶栓小組的積極行動,一旦他們提前收到EMS的通知,在獲取患者相關信息之后立刻行動,在患者到達之前已經開始準備工作。PNP的本質就在于提前進行院內外資源的整合和調配[17]。
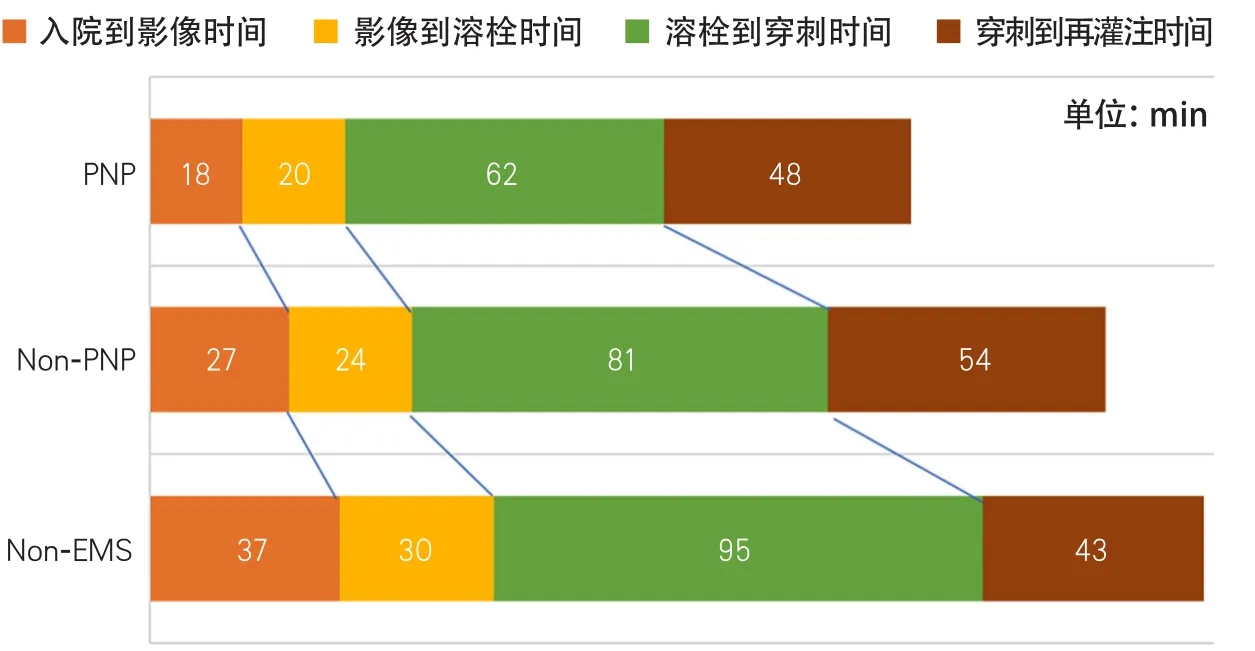
圖1 PNP組、Non-PNP組和Non-EMS組入院后時間對比圖
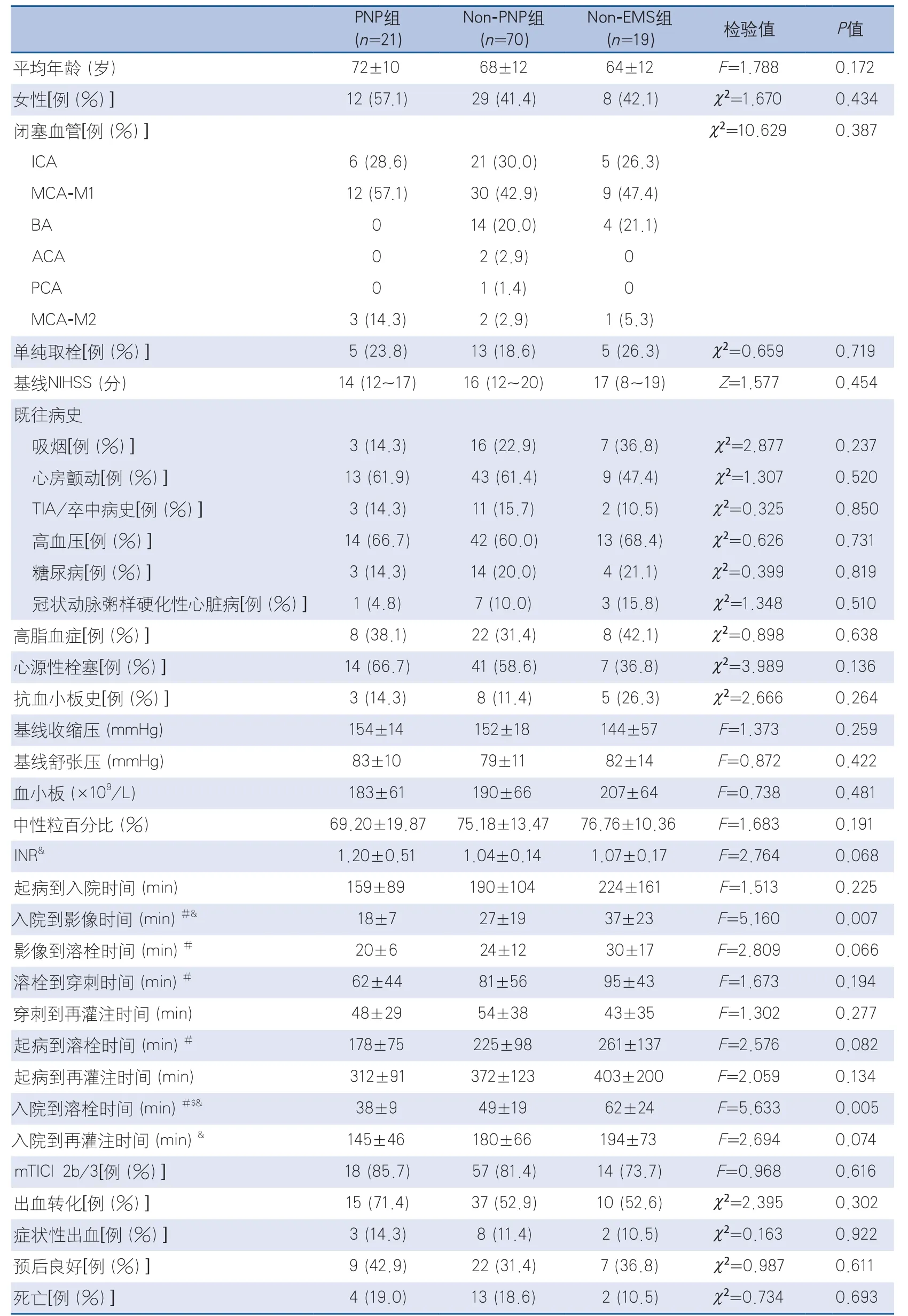
表1 PNP組、Non-PNP組和Non-EMS組患者基線資料和結局的單因素分析
隨著PNP組DRT的縮短,本研究發現PNP的應用與LVO患者血管內治療遠期神經功能結局良好有關。Gregg C. Fonarow等[9]研究發現,縮短院內治療延誤,及時靜脈溶栓治療與臨床結局的改善有關。最近一項關于院內延誤與預后關系的研究證實,院內延誤會增加住院患者的死亡率并加重患者出院時的神經功能障礙[18]。但是,Sin Kyu Kim等[8]研究中,雖然PNP縮短了入院至溶栓時間,但其并未改善90 d神經功能結局。這可能是由于該研究中PNP雖然縮短了入院至溶栓時間,但實際上兩組間的人群并不均質,PNP組距離醫院更遠,并且PNP組的患者中途轉運至非卒中中心,因而PNP組的患者平均ONT反而從74.7 min延長至121.5 min。而我們研究中,PNP組患者的起病到再灌注時間未比Non-PNP組更長。另一項來自西班牙的研究報告[19],巴塞羅那北部的“卒中規范”(Stroke Code)提到,PNP可以提高靜脈溶栓率和改善患者臨床結局。本研究首次明確,PNP是改善急性LVO患者血管內治療3個月結局的有效方法。
本研究發現有82.7%患者通過EMS入院,這個比例與國外研究的EMS利用率相當[20]。這可能由于本研究納入的都是LVO患者,基線的癥狀較重,患者及家屬更愿意選擇EMS。這也從側面反映出對于癥狀重的患者,EMS更容易被接受和利用。但遺憾的是,通過EMS入院患者中,PNP只占23.1%,這個比例明顯低于Sin Kyu Kim等[8]的研究。這提示,EMS管理水平有待進一步提高,建立區域化卒中的聯動管理刻不容緩。城市EMS系統應與醫院建立更加密切的合作關系,同時加強院前急救人員的培訓,不僅可以將疑似卒中患者優先轉運到最近有卒中診療資質的卒中中心,而且需要提前預通知相關的卒中中心,令其提前積極進行各項準備,以期縮短急診室滯留時間和檢查等的延誤。區域內不同級別的卒中中心也應建立雙向轉診協議,院前預通知流程可作為連接紐帶來分層轉運患者。
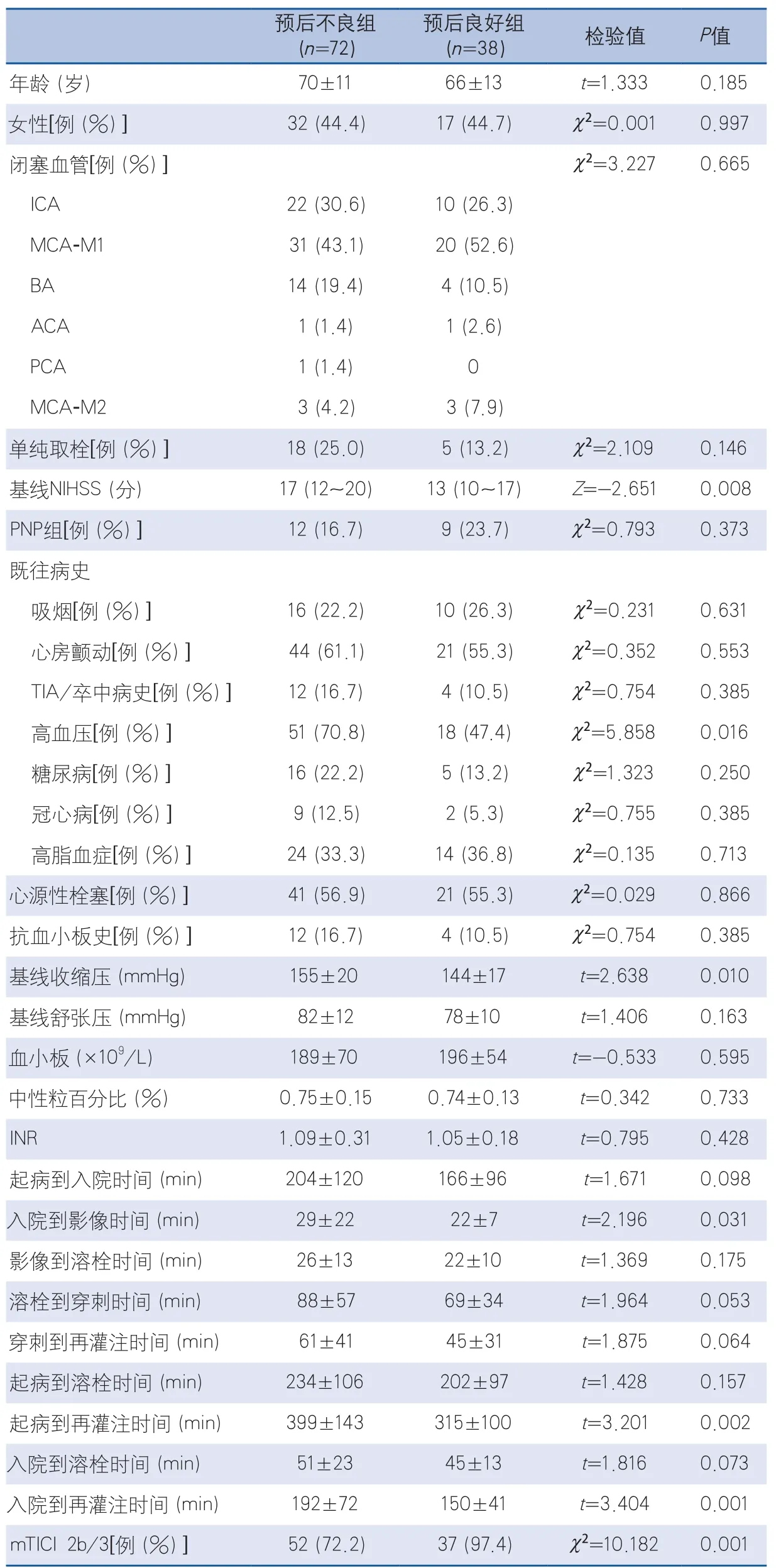
表2 血管內治療后3個月預后的單因素分析
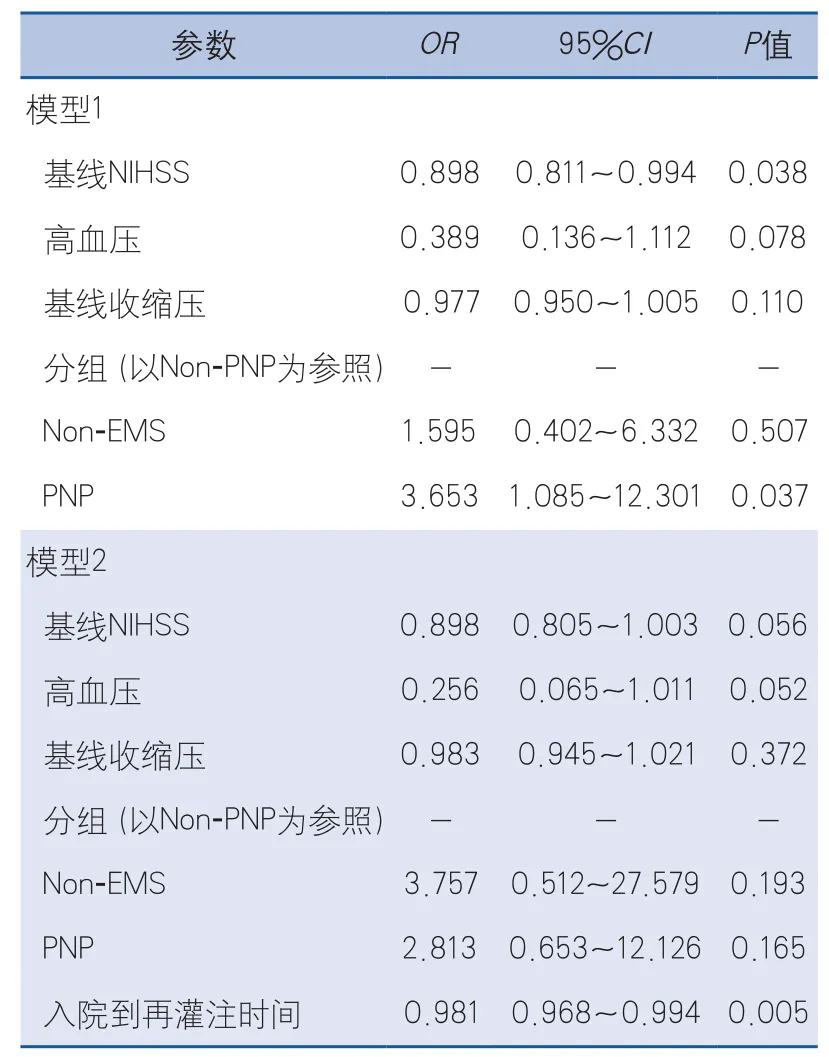
表3 血管內治療3個月預后的多因素分析
本研究尚存在一些不足。首先,這是個單中心小樣本的研究,研究結果有待長期觀察和進一步驗證;其次,本研究只納入了LVO取栓的患者,PNP對于LVO患者未進行動脈內取栓治療的預后有無影響仍未知。
總之,PNP可以縮短急性LVO患者血管內治療的DRT,并且改善其3個月預后。本研究結果支持目前的指南,主張通過EMS對缺血性卒中患者提前預通知卒中中心。PNP是訓練有素的EMS系統和卒中中心之間密切合作的有效策略。
[1] LI Z,WANG C,ZHAO X,et al. Substantial progress yet signi ficant opportunity for improvement in stroke care in China[J]. Stroke,2016,47(11):2843-2849.
[2] 王隴德. 中國腦卒中防治報告(2015)[M]. 北京:中國協和醫科大學出版社,2015.
[3] RHA J H,SAVER J L. The impact of recanalization on ischemic stroke outcome:a meta-analysis[J].Stroke,2007,38(3):967-973.
[4] GOYAL M,MENON B K,VAN ZWAM W H,et al. Endovascular thrombectomy after large-vessel ischaemic stroke:a meta-analysis of individual patient data from five randomised trials[J]. Lancet,2016,387(10029):1723-1731.
[5] MERETOJA A,KESHTKARAN M,TATLISUMAK T,et al. Endovascular therapy for ischemic stroke:Save a minute-save a week[J].Neurology,2017,88(22):2123-2127.
[6] GLADSTONE D J,RODAN L H,SAHLAS D J,et al. A citywide prehospital protocol increases access to stroke thrombolysis in Toronto[J]. Stroke,2009,40(12):3841-3844.
[7] CASOLLA B,BODENANT M,GIROT M,et al.Intra-hospital delays in stroke patients treated with rt-PA:impact of preadmission noti fication[J]. J Neurol,2013,260(2):635-639.
[8] KIM S K,LEE S Y,BAE H J,et al. Pre-hospital noti fication reduced the door-to-needle time for iv t-PA in acute ischaemic stroke[J]. Eur J Neurol,2009,16(12):1331-1335.
[9] FONAROW G C,ZHAO X,SMITH E E,et al. Door-to-needle times for tissue plasminogen activator administration and clinical outcomes in acute ischemic stroke before and after a quality improvement initiative[J]. JAMA,2014,311(16):1632-1640.
[10] VIDALE S,VERRENGIA E,GERARDI F,et al. Stroke management in northern Lombardy:organization of an emergency-urgency network and development of a connection between prehospital and in-hospital settings[J]. Int J Stroke,2012,7(6):527-533.
[11] YIN X,YANG T,GONG Y,et al. Determinants of emergency medical services utilization among acute ischemic stroke patients in hubei province in China[J]. Stroke,2016,47(3):891-894.
[12] CAMPBELL B C,MITCHELL P J,KLEINIG T J,et al. Endovascular therapy for ischemic stroke with perfusion-imaging selection[J]. N Engl J Med,2015,372(11):1009-1018.
[13] ZAIDAT O O,YOO A J,KHATRI P,et al.Recommendations on angiographic revascularization grading standards for acute ischemic stroke:a consensus statement[J]. Stroke,2013,44(9):2650-2663.
[14] LARRUE V,VON KUMMER R R,MüLLER A,et al. Risk factors for severe hemorrhagic transformation in ischemic stroke patients treated with recombinant tissue plasminogen activator:a secondary analysis of the European-Australasian Acute Stroke Study(ECASS Ⅱ)[J]. Stroke,2001,32(2):438-441.
[15] LIN C B,PETERSON E D,SMITH E E,et al.Emergency medical service hospital prenoti fication is associated with improved evaluation and treatment of acute ischemic stroke[J]. Circ Cardiovasc Qual Outcomes,2012,5(4):514-522.
[16] XIAN Y,SMITH E E,ZHAO X,et al. Strategies used by hospitals to improve speed of tissue-type plasminogen activator treatment in acute ischemic stroke[J]. Stroke,2014,45(5):1387-1395.
[17] MERETOJA A,STRBIAN D,MUSTANOJA S,et al. Reducing in-hospital delay to 20 minutes in stroke thrombolysis[J]. Neurology,2012,79(4):306-313.
[18] KAMAL N,SHENG S,XIAN Y,et al. Delays in door-to-needle times and their impact on treatment time and outcomes in get with the guidelinesstroke[J]. Stroke,2017,48(4):946-954.
[19] KIM D H,NAH H W,PARK H S,et al. Impact of prehospital intervention on delay time to thrombolytic therapy in a stroke center with a systemized stroke code program[J]. J Stroke Cerebrovasc Dis,2016,25(7):1665-1670.
[20] SONG D,TANAKA E,LEE K,et al. Factors associated with early hospital arrival in patients with acute ischemic stroke[J]. J Stroke,2015,17(2):159-167.

